改性骨架镍催化3-氯-4-甲基硝基苯加氢制备3-氯-4-甲基苯胺
郑飞跃,荣泽明,徐晓清,梁 琰,王 越,吕连海
(大连理工大学 化工与环境生命学部 精细化工国家重点实验室,辽宁 大连 116012)
改性骨架镍催化3-氯-4-甲基硝基苯加氢制备3-氯-4-甲基苯胺
郑飞跃,荣泽明,徐晓清,梁 琰,王 越,吕连海
(大连理工大学 化工与环境生命学部 精细化工国家重点实验室,辽宁 大连 116012)
考察了不同氯化物改性的骤冷骨架镍(QS-Ni)催化剂对3-氯-4-甲基硝基苯(CMNB)选择性加氢制备3-氯-4-甲基苯胺(CMAN)反应的影响。实验结果表明,采用SnCl4·5H2O或SnCl2·2H2O改性时,QS-Ni催化剂的活性提高,且在CMNB完全转化的条件下,CMAN的选择性可达100.0%。同时考察了反应条件的影响,当n(SnCl4·5H2O)∶n(QS-Ni)=1 ∶8时,在55 ℃、1.0 MPa、7.0 g CMNB、25 mL 甲醇、催化剂用量0.20 g的条件下反应100 min,CMNB 转化率和 CMAN 选择性均达到100.0%;且延长反应时间,仍能完全抑制脱氯副反应的发生,CMAN的选择性保持在100.0%。
骤冷骨架镍;催化加氢;3-氯-4-甲基硝基苯;3-氯-4-甲基苯胺
氯代苯胺是一类重要的有机中间体,广泛应用于医药、染料等精细化工产品的合成。其中,3-氯-4-甲基苯胺(CMAN)是合成2B酸和农药绿麦隆的重要中间体[1-2]。
工业上,CMAN一般由3-氯-4-甲基硝基苯(CMNB)还原制得,常用的还原剂为铁粉、硫化钠等。由于该法“三废”多,对环境污染严重正逐渐被淘汰,而催化加氢法因其环境友好而日益受到重视。针对氯代硝基苯催化加氢体系,研究较多的是骨架镍及 Pt,Pd,Ru 等负载型贵金属催化剂[3-6]。贺志真等[7]采用Pt/C催化剂,对CMNB加氢制备CMAN反应进行了研究,在Pt/C催化剂中引入助剂后,产品脱氯量可降至0.3%。通过向负载型Pd,Pt,Ru 催化体系中加入改性剂[8-10],可提高氯代苯胺的选择性,但会导致催化剂活性大幅降低且中间产物增多,产品选择性仅为 97.8%[11]。
本工作在已有研究[12-15]的基础上,将骤冷法制备的骨架镍(QS-Ni)催化剂应用于CMNB加氢制备CMAN反应中,研究了改性剂氯化物种类和用量、反应温度、H2压力、CMNB初始浓度以及催化剂用量等条件对CMNB加氢反应的影响。
1 实验部分
1.1 主要试剂
CMNB:工业级,铜陵广信化工厂;甲醇:分析纯,天津博迪化工有限公司;SnCl4·5H2O,SnCl2·2H2O:分析纯,西陇化工股份有限公司。
1.2 催化剂的制备
催化剂的制备参照文献[16]。将 Ni,Al,Mo(质量分数分别为 46.4%,49.3%,4.3%)在氩气保护下熔融,待形成均匀合金后,用氩气将其压到高速旋转的铜辊上以106℃/s的速率骤冷,得到前体合金薄条,研磨成200~300目的颗粒,然后加入到过量的NaOH(质量分数20%)水溶液中,在100℃下搅拌1 h,用去离子水洗涤至中性,得到QS-Ni催化剂,保存在去离子水中待用。
1.3 催化剂的改性
称取定量QS-Ni催化剂,用去离子水洗涤5次,甲醇洗涤2次,放入75 mL高压釜中,加入定量氯化物和甲醇,密闭反应釜,分别用N2和H2置换3次,在45℃水浴加热下搅拌30 min,冷却至室温,倒出上层清液,保存待用。
1.4 实验方法
向高压釜中加入定量的原料、催化剂和溶剂后,密闭高压釜,分别用N2和H2置换3次,升温至设定值后将H2压力调至设定值,开启搅拌进行反应。反应至预定时间后将高压釜冷却,放空,开釜取样分析。
1.5 分析方法
采用浙江福立分析仪器有限公司GC-9790型气相色谱仪对试样进行定量分析,SE-54型毛细管色谱柱(30 m ×0.32 mm ×0.5 μm),氢火焰离子化检测器。分析条件:柱温100℃,以10℃/min的速率程序升温至200℃,保持20 min;气化室温度280℃,检测器温度280℃,采用面积归一化法定量。采用美国安捷伦公司HP6890GC/5937MSD型气-质联用仪进行定性分析。
2 结果与讨论
2.1 不同氯化物改性的影响
考察了不同氯化物改性的QS-Ni催化剂对CMNB加氢反应的催化性能,实验结果见表1。由表1可见,在CMNB完全转化的条件下,与未改性的催化剂相比,除 SnCl2·2H2O和 SnCl4·5H2O外,其他氯化物改性的QS-Ni催化剂催化CMNB加氢,反应时间均有不同程度的延长;而采用SnCl2·2H2O和SnCl4·5H2O改性后,反应时间均有所缩短,催化活性提高,CMAN的选择性达100%,脱氯副反应被完全抑制。可能的原因是骨架镍与Sn2+和Sn4+发生了置换反应,在骨架镍表面形成了一种Ni-Sn合金结构,该合金结构影响了骨架镍活性中心上镍原子的电子分布状态,从而使得硝基加氢的活性提高,同时也能抑制脱氯副反应的发生[3-17]。采用SnCl4·5H2O改性时,反应时间最短,因此选择SnCl4·5H2O为QS-Ni催化剂的改性剂。
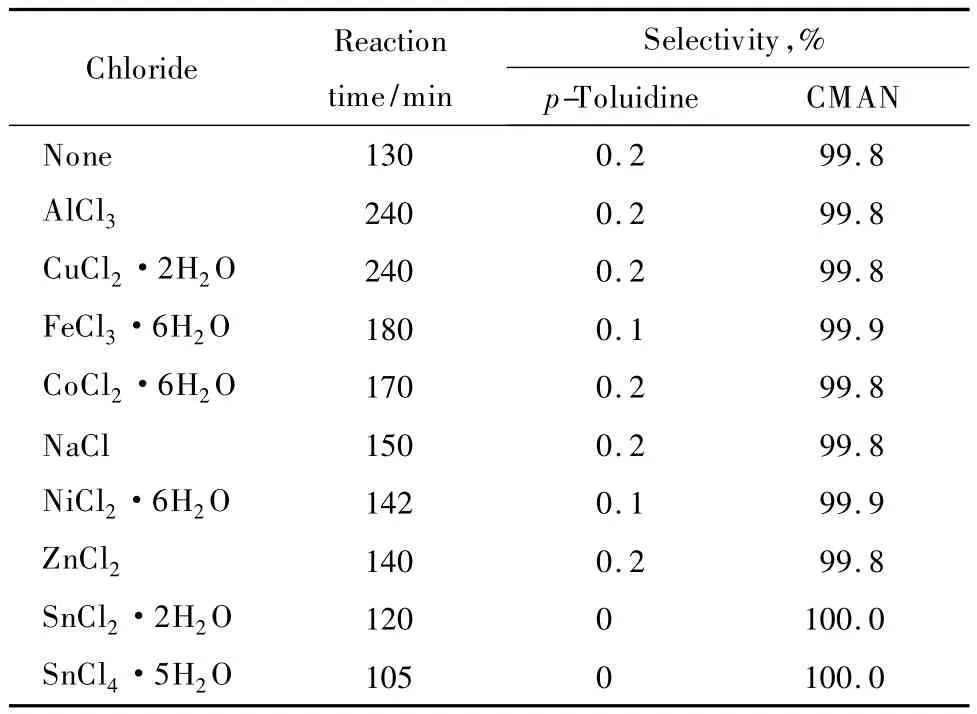
表1 不同氯化物改性的QS-Ni催化剂对CMNB加氢反应的催化性能Table 1 Catalytic activities of quenched skeletal Ni(QS-Ni)catalysts modified by different chlorides in 3-chloro-4-methylnitrobenzene(CMNB)hydrogenation
2.2 SnCl4·5H2O 用量的影响
考察了不同SnCl4·5H2O用量改性的QS-Ni催化剂对CMNB加氢反应的催化性能,实验结果见表2。由表2可见,当改性剂用量太少或太多时,都会导致催化剂活性降低,只有添加适当量的改性剂,才能最大程度地发挥其修饰作用[8-9]。当n(SnCl4·5H2O)∶n(Ni)为1∶8时,改性 QS-Ni催化剂呈现出较好的活性,同时产物CMAN的选择性达到100.0%。因此选择 n(SnCl4·5H2O)∶n(Ni)为1 ∶8。

表2 不同SnCl4·5H2O用量改性的QS-Ni催化剂对CMNB加氢反应的催化性能Table 2 Catalytic activities of QS-Ni catalysts modified by different amounts of SnCl4·5H2O in CMNB hydrogenation
2.3 反应条件的影响
2.3.1 反应温度的影响
采用SnCl4·5H2O改性的QS-Ni催化剂,考察了反应温度对CMNB加氢反应的影响,实验结果见表3。由表3可见,随反应温度的升高,CMNB加氢反应速率加快,当反应温度由35℃升至75℃时,反应时间由180 min缩短至30 min;而在65℃时开始有微量脱氯产物生成。综合考虑反应时间和CMAN的选择性,适宜的反应温度为55℃。

表3 反应温度对CMNB加氢反应的影响Table 3 Effect of reaction temperature on CMNB hydrogenation
2.3.2 反应压力的影响
采用SnCl4·5H2O改性的QS-Ni催化剂,考察了反应压力对CMNB加氢反应的影响,实验结果见表4。由亨利定律可知,随反应压力的升高,H2分压增大,反应速率加快。在一定温度下,升高反应压力,即增大了气相H2分压和H2在溶液中的浓度,H2分子在催化剂表面的吸附量增加,活化氢的数量也相应增加,因此反应速率加快。由表4可见,当反应压力由0.4 MPa升至0.8 MPa时,反应时间由140 min缩短为90 min;而反应压力由0.8 MPa升至1.6 MPa时,反应时间的变化相对不明显。同时,反应压力对CMAN选择性无影响。考虑到对设备的要求,选择反应压力为0.8~1.2 MPa较适宜。

表4 反应压力对CMNB加氢反应的影响Table 4 Effect of reaction pressure on CMNB hydrogenation
2.3.3 原料投入量的影响
采用SnCl4·5H2O改性的QS-Ni催化剂,考察了原料CMNB投入量对CMNB加氢反应的影响,实验结果见图1。由图1可见,在相同的反应时间内,随原料投入量的增加,CMNB转化率逐渐降低,平均吸氢速率先升高后降低;当原料投入量为7.0 g时,平均吸氢速率达到最大值。因此确定较佳的原料投入量为7.0 g。

图1 原料投入量对CMNB转化率和平均吸氢速率的影响Fig.1 Effects of CMNB dosage on its conversion and average H2uptake rate.
2.3.4 催化剂用量的影响
采用SnCl4·5H2O改性的QS-Ni催化剂,考察了催化剂用量对CMNB加氢反应的影响,实验结果见图2。由图2可见,随催化剂用量的增加,CMNB转化率增加,而CMAN选择性基本保持不变。综合考虑反应速率及经济成本,选择适宜的催化剂用量为0.20 g。

图2 催化剂用量对CMNB转化率和CMAN选择性的影响Fig.2 Effects of catalyst dosage on conversion of CMNB and selectivity to CMAN.
2.3.5 反应时间的影响
采用SnCl4·5H2O改性前后的QS-Ni催化剂,考察了反应时间对CMNB加氢反应的影响,实验结果见表5。由表5可见,采用未改性的QS-Ni催化剂,反应150 min时CMNB完全转化,CMAN选择性为99.6%;延长反应时间至175 min时,CMAN选择性降至87.8%,并生成大量的脱氯产物对甲基苯胺。而采用SnCl4·5H2O改性的QS-Ni催化剂,反应 100 min时 CMNB即完全转化,CMAN选择性为100.0%;延长反应时间至125 min时,CMAN选择性仍保持 100.0%。说明采用SnCl4·5H2O改性QS-Ni催化剂,催化剂活性明显提高,而且能完全抑制脱氯副反应。

表5 延长反应时间对CMNB加氢反应的影响Table 5 Effect of prolonging the reaction time on CMNB hydrogenation
3 结论
(1)采用改性QS-Ni催化剂催化CMNB加氢制备CMAN反应,适宜的改性剂为SnCl4·5H2O,适宜的改性剂用量为n(SnCl4·5H2O)∶n(Ni)=1∶8。改性后催化剂的活性提高,且能完全抑制脱氯副反应。
(2)采用 SnCl4·5H2O改性的 QS-Ni催化剂,优化的反应条件为:55 ℃、1.0 MPa、7.0 g CMNB、25 mL甲醇、0.20 g催化剂。在此条件下反应100 min,CMNB转化率和CMAN选择性均达到100.0%,延长反应时间仍能完全抑制脱氯副反应。
[1] 郭方,吕连海.氯代硝基苯催化加氢制备氯代苯胺的研究进展[J].化工进展,2007,26(1):1-6.
[2] 熊峻,陈吉祥,张继炎.氯代硝基苯催化加氢合成氯代苯胺的催化剂研究进展[J].化学试剂,2006,28(6):331-335.
[3] Yan Xinhuan,Sun Junqing,Wang Youwen,et al.A Fe-Promoted Ni-P Amorphous Alloy Catalyst(Ni-Fe-P)for Liquid Phase Hydrogenation of m-and p-Chloronitrobenzene[J].J Mol Catal A:Chem,2002,252(1-2):17-22.
[4] Xu Danqian,Hu Zhiyan,Li Weiwei,et al.Hydrogenation in Ionic Liquids:An Alternative Methodology Toward Highly Selective Catalysis of Halonitrobenzenes to Corresponding Haloanilines[J].J Mol Catal A:Chem,2005,235(1 -2):137 - 142.
[5] Tu Weixia,Liu Hanfan,Tang Yao.The Metal Complex Effect on the Selective Hydrogenation of m-and p-Chloronitrobenzene over PVP-Stabilized Platinum Colloidal Catalysts[J].J Mol Catal A:Chem,2000,159(1):115 -120.
[6] Han Xiaoxiang,Zhou Renxian,Lai Guohua,et al.Effect of Transition Metal(Cr,Mn,Fe,Co,Ni and Cu)on the Hydrogenation Properties of Chloronitrobenzene over Pt/TiO2Catalysts[J].J Mol Catal A:Chem,2004,209(1 -2):83 -87.
[7] 贺志真,朱国彪.3-氯-4-甲基苯胺合成研究[J].化工时刊,2008,22(8):29 -31.
[8] 赵松林,陈骏如,刘新梅,等.金属离子对Ru-Pt/γ-Al2O3催化剂上对氯硝基苯选择加氢反应的影响[J].催化学报,2004,25(11):850 -854.
[9] 刘新梅,樊光银,赵松林,等.Sn4+离子修饰的Pd/γ-Al2O3催化卤代芳香硝基化合物选择性加氢[J].分子催化,2005,19(6):430 -435.
[10] 许琼,王磊,陈骏如,等.有机胺修饰的Ru-Ir/γ-Al2O3催化剂上对氯硝基苯选择性加氢[J].催化学报,2007,28(7):579-581.
[11] 许丹倩,严新焕,徐振元.低压液相催化加氢合成3-氯-4-甲苯胺研究[J].染料化工,2001,38(1):16-18.
[12] 侯洁,郭方,王越,等.改性骨架钌催化加氢间二硝基苯制备间硝基苯胺[J].精细化工,2006,23(11):1064 -1067.
[13] 郭方,王越,吕连海.高分散Ru/C选择性催化对氯硝基苯加氢制备对氯苯胺[J].精细化工,2007,24(3):252 -256.
[14] 李玉涵,侯洁,马荣华,等.催化加氢制备3-氨基-4-甲氧基乙酰苯胺[J].石油化工,2008,37(2):132 -135.
[15] 胡少伟,荣泽明,刘益材,等.改性骨架镍催化加氢3,4-二甲基硝基苯制备3,4-二甲基苯胺[J].精细化工,2010,27(2):170-173.
[16] 张鹏,杜文强,荣泽明,等.温和条件下非晶态NiAl合金催化苯甲腈加氢制苄胺[J].石油化工,2008,37(10):1037-1041.
[17] Ayumu Onda,Takayuki Komatsu,Tatsuaki Yashima.Characterization and Catalytic Properties of Ni-Sn Intermetallic Compounds in Acetylene Hydrogenation[J].Phys Chem Chem Phys,2000,2(13):2999 -3005.
Catalytic Hydrogenation of 3-Chloro-4-Methylnitrobenzene to 3-Chloro-4-Methylaniline over Modified Skeletal Nickel
Zheng Feiyue,Rong Zeming,Xu Xiaoqing,Liang Yan,Wang Yue,Lü Lianhai
(State Key Laboratory of Fine Chemicals,Faculty of Chemical,Environmental and Biological Science and Technology,Dalian University of Technology,Dalian Liaoning 116012,China)
Hydrogenation of 3-chloro-4-methylnitrobenzene(CMNB)to 3-chloro-4-methylaniline(CMAN) over quenched skeletal nickel(QS-Ni) catalyst modified by various chlorides was investigated.The results showed that the catalytic activity of QS-Ni modified by SnCl4·5H2O or SnCl2·2H2O was enhanced and selectivity to CMAN could reach 100.0%in the case of complete conversion of CMNB.Under the optimized conditions of 0.20 g the modified QS-Ni catalyst with n(SnCl4·5H2O)∶n(QS-Ni)1 ∶8,55 ℃,1.0 MPa,CMNB 7.0 g and methanol 25 mL,both the conversion of CMNB and the selectivity to CMAN could reach 100%after reaction for 100 min.The side-reaction dechlorination had still not been observed even after another 25 min reaction.
quenching skeletal nickel;catalytic hydrogenation;3-chloro-4-methylnitrobenzene;3-chloro-4-methylaniline
1000-8144(2011)06-0630-05
TQ 426.61
A?
2010-12-28;[修改稿日期]2011-03-17。
郑飞跃(1984—),男,安徽省亳州市人,硕士生,电邮zhengfeiyuea@163.com。联系人:荣泽明,电话0411-84986242,电邮 zeming@dlut.edu.cn。。
国家高技术研究发展计划项目(2007AA03Z345);辽宁省教育厅2010年度高等学校科研项目(LT2010021);大连理工大学基本科研业务费专项资金资助项目(DUT10RC(3)107)。
(编辑 安 静)

