微波辅助合成硼酸钙
刘 霞,张丽芳,李建辉
(北京石油化工学院化工系,北京 102617)
微波辅助合成硼酸钙
刘 霞,张丽芳,李建辉
(北京石油化工学院化工系,北京 102617)
采用硼酸、氢氧化钙为原料,利用微波加热方式合成硼酸钙(xCaO·yB2O3·nH2O),以缩短反应时间、提高反应效率。实验中考察了反应温度、微波辐射时间、原料比等因素的影响;确定了合成硼酸钙 (CaO·2B2O3· 2H2O)的适宜反应条件:反应温度为 95~105℃、微波辐射时间为 40 min、氢氧化钙与水物质的量比为1∶39.6、氢氧化钙与硼酸物质的量比为 1∶4.5,在此条件下产品收率达 88%。产品的组成分析结果基本符合要求,CaO·2B2O3· 2H2O的粒径约为 10μm,失水温度为 190℃,微波加热条件下的反应速率约是常规加热法反应速率的 4倍。
氢氧化钙;硼酸钙;微波辐射
硼酸钙(xCaO·yB2O3·nH2O)是一类重要的新兴化工原料,广泛应用在玻璃、陶瓷、搪瓷、釉、光学材料、农业、阻燃剂、防腐剂以及医药等领域,尤其在无碱玻璃纤维中是唯一无氟、低镁、含铁甚微的化工原料。硼酸钙应用于无碱玻璃纤维行业,替代硼酸、硼砂和天然硼镁石,可大幅度降低氧化硼的挥发,使烧成温度降低、减少损耗、降低成本、提高产品质量,并且有效地解决了环境污染和设备腐蚀的问题,实现部分清洁生产,保护劳动者的身体健康。目前,中国硼酸钙的合成尚处于研发阶段,硼酸钙主要依赖进口,因此利用现有的硼资源来制备不同组成的硼酸钙具有重要的现实意义[1-3]。笔者拟采用氢氧化钙、硼酸为原料,利用微波加热合成硼酸钙(xCaO·yB2O3·nH2O),以缩短反应时间、提高反应效率。
1 实验部分
1.1 仪器与试剂
仪器:MAS-I型常压微波辅助合成/萃取反应器;SHZ-D型循环水式真空泵;HCT-1型微机差热天平;FA1004A型电子天平;QUANTA400F型场发射扫描电镜。
试剂:硼酸、氢氧化钙、氢氧化钠、乙二胺四乙酸(EDTA)、甘露醇、氯化铵、氨水等,均为分析纯。
1.2 实验方法
将 2.6 g氢氧化钙 (0.035 1 mol)、9.8 g硼酸(0.158 mol)及 25.0 mL去离子水加入微波专用的150 mL圆底烧瓶中,然后安装好冷凝回流管、搅拌器。设定:工步 1,100℃、5 min;工步 2,105℃、5 min;工步 3,110℃、30 min。启动反应器,运行设定程序,反应结束后,将反应液冷却至 90℃左右趁热抽滤,再用沸水洗涤 2~3次,将滤饼在 110~120℃下烘 8 h以上,即可得到白色粉末状固体的硼酸钙(CaO·2B2O3·2H2O)产品。
1.3 分析方法[4]
1.3.1 试样的准备
准确称取 1.0 g样品 (准确至 0.000 2 g)置于50 mL烧杯中,加 15 mL水及 10 mL、1 mol/L的HNO3溶液,搅拌溶解后,移入 250 mL容量瓶中,加水稀释至刻度,摇匀备用。
1.3.2 CaO的含量测定
按文献[4]的方法配制 EDTA溶液,并进行标定,浓度为 0.019 87 mol/L。
用移液管准确移取25.00 mL试样于250 mL锥形瓶中,加入pH=10的标准缓冲溶液(NH3·H2ONH4Cl)10.0 mL,再加入 1~2滴铬黑 T指示剂,用EDTA标准溶液滴定,溶液由酒红色变为蓝色即为终点,滴定 3次取平均值。
1.3.3 B2O3的含量测定
按文献[4]的方法配制 NaOH溶液,并进行标定,浓度为 0.095 26 mol/L。
用移液管准确移取25.00 mL试样于250 mL锥形瓶中,准确加入与测定氧化钙消耗的 EDTA同量的标准溶液,以甲基红为指示剂,逐滴加入1.0 mol/L的NaOH溶液至溶液变黄,然后逐滴加入0.5 mol/L的 HCl至溶液恰好变红,再加入0.1 mol/L的NaOH到溶液恰好变黄,加入 1.0 g甘露醇,溶解后溶液再次呈现红色,再加入 2滴酚酞指示剂,以配制好的NaOH标准溶液滴至红色消失又重现浅红色即为终点,滴定 3次取平均值。按上述方法测定空白值。
1.3.4 结晶水的测定
利用微机差热天平测出硼酸钙中的结晶水及失水温度。
2 结果与讨论
2.1 温度对反应的影响
固定反应条件:加入氢氧化钙 2.6 g,硼酸 9.8 g (氢氧化钙与硼酸物质的量比为 1∶4.5);微波辐射时间为 60 min;总溶剂量为 42.0 mL。
温度对硼酸钙的形成有较大的影响,通过设定微波反应器工步及在溶剂水中添加乙醇来调节反应体系的温度,实验结果见表 1。
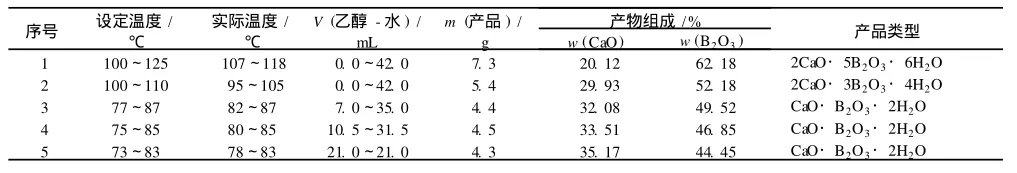
表1 温度对反应的影响
由表 1可见,通过添加一定量的无水乙醇,反应体系的温度可降至 100℃以下,且随反应体系温度的降低,所得产品中 CaO的含量升高,B2O3的含量降低;且不同温度下产物组成不同,说明温度对该反应的影响较大。综合考虑微波效率及溶剂的影响,选定反应的实际温度为 95~105℃(微波设定温度为100~110℃)。
2.2 氢氧化钙与水物质的量比对反应的影响
固定条件:加入氢氧化钙 2.6 g,硼酸 9.8 g(氢氧化钙与硼酸物质的量比为 1∶4.5);以水为溶剂,反应体系的实际温度控制在 95~105℃;微波辐射时间为 60 min。改变水的用量,以考察氢氧化钙与水物质的量比对反应的影响,实验结果见表 2。由表 2可见,随着溶剂水量的变化,产物的组成有变,但在一定范围内,组成基本不变。当溶剂水的用量为 35.0~48.0 mL时,得到的产品为 2CaO·3B2O3· 4H2O;而当溶剂水的用量为 21.0~30.0 mL时,所得到的产品是 CaO·2B2O3·nH2O(n为 2或 3)。因准备合成的目标产物为 CaO·2B2O3·nH2O,所以选择溶剂水的用量为 25.0 mL,即氢氧化钙与水的物质的量比为1∶39.6。
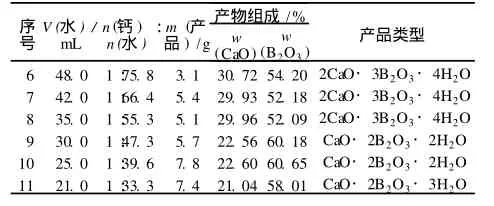
表 2 Ca(OH)2与 H2O物质的量比对反应的影响
2.3 氢氧化钙与硼酸物质的量比对反应的影响
固定条件:加入氢氧化钙 2.6 g,水 25.0 mL(氢氧化钙与水的物质的量比为 1∶39.6);微波辐射时间为 60 min;反应体系的实际温度控制在 95~105℃。改变硼酸的用量,以考察氢氧化钙与硼酸的物质的量比对反应的影响,实验结果见表 3。
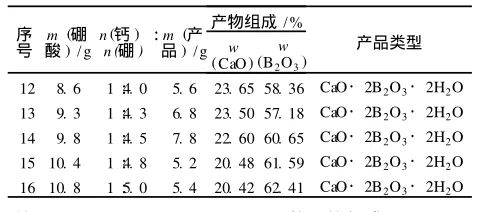
表3 Ca(OH)2与H3BO3物质的量之比对反应的影响
由表 3组成分析结果可见,所得产品为 CaO· 2B2O3·2H2O。其中当n[Ca(OH)2]∶n(H3BO3)= 1∶(4.0~5.0)时,产品组成变化不大,而当n[Ca(OH)2]∶n(H3BO3)=1∶4.5时产品收率较高,因此实验选择n[Ca(OH)2]∶n(H3BO3)=1∶4.5。
2.4 微波辐射时间对反应的影响
固定条件:加入氢氧化钙 2.6 g,硼酸 9.8 g,水25.0 mL(氢氧化钙与硼酸物质的量比为 1∶4.5,氧化钙与水的物质的量比为 1∶39.6;反应体系的实际温度控制在 95~105℃。改变微波辐射时间,考察微波辐射时间对反应的影响,实验结果见表 4。

表 4 微波辐射时间对反应的影响
由表 4可见,当微波辐射时间低于 40 min时,产品的产量降低,当微波辐射时间≥40 min时,产品的产量较高,故选择适宜的微波辐射时间为 40 min。
2.5 优化条件下的平行实验
综合以上实验结果得出微波辐射下,以硼酸和氢氧化钙为原料合成CaO·2B2O3·2H2O的适宜反应条件:加入氢氧化钙 2.6 g,硼酸 9.8 g,水25.0 mL (氢氧化钙与硼酸物质的量比为 1∶4.5,氢氧化钙与水的物质的量比为 1∶39.6),微波反应器条件设定为:工步 1,100℃、5min;工步 2,105℃、5 min;工步3,110℃、30 min,微波辐射总时间为 40 min。在此条件下重复进行实验得到 22号产品,产品质量为7.1 g,收率为 87.4%,其中w(CaO)=21.49%,w(B2O3)=63.89%,与 20号结果比较平行。
2.6 与传统加热法的比较
将 2.6 g氢氧化钙 (0.035 1 mol)与 9.8 g硼酸(0.158 mol)固体混合均匀后加入到 250 mL三口烧瓶中,加去离子水 25.0 mL。装上温度计、搅拌器和回流管,加热搅拌并回流 3 h。反应结束后,将反应液冷却至 90℃左右趁热抽滤,再用沸水洗涤 2~3次,将滤饼在 110~120℃下烘干 8 h以上,即可得到白色粉末状固体产物,质量为 7.2 g。对比表 4中的结果可以看出,微波加热比传统加热的反应时间大为减少,其反应速率约是常规加热法的 4倍。
3 xCaO·yB2O3·nH2O的表征
3.1xCaO·yB2O3·nH2O的热重分析
分别对 5号(CaO·B2O3·2H2O)、7号(2CaO· 3B2O3·4H2O)、9和 22号(CaO·2B2O3·2H2O)样品进行热重分析,结果表明:5号样品分段失水,失水温度为 189、454℃;7号样品的失水温度为167℃,9和 22号样品失水温度约为 190℃。
3.2 CaO·2B2O3·2H2O的电镜分析
图 1为22号样品的场发射扫描电镜 (FE-SEM)照片。由图 1可以看出,产品颗粒分布比较均匀,在1 600倍下,晶体团聚在一起形似小球 (图1a);在12 000倍下,可以看出每个小球是由众多的片状晶体团簇而成,粒径约为10μm(图 1b)。

图1 CaO·2B2O3·2H2O的 FE-SEM照片
4 结论
1)对微波辅助合成硼酸钙的条件进行了研究,系统考察了物料配比、反应温度、微波辐射时间对反应产物硼酸钙收率及组成的影响,得到合成CaO·2B2O3·2H2O的适宜工艺条件:m(氢氧化钙)=2.6 g,m(硼酸)=9.8 g,V(水)=25.0 mL [n(氢氧化钙)∶n(水)=1∶39.6,n(氢氧化钙)∶n(硼酸)=1∶4.5],反应温度为 95~105℃,微波辐射时间为 40 min。在此条件下,产品收率约为88%。CaO·2B2O3·2H2O的粒径约为 10μm,失水温度为 190℃。
2)CaO·B2O3·2H2O的热重分析结果显示,该物质为分段失水,第一次失水温度为 189℃,第2次失水温度为 454℃,有望用作阻燃剂。
3)利用微波加热方式辅助合成硼酸钙 (CaO· 2B2O3·2H2O),与传统加热方式相比,微波辐射法可使反应加快、时间缩短、效率提高,微波辐射法的反应速率约是常规加热法的 4倍。
[1] 曹春娥,曹惠峰,卢希龙,等.硼酸钙的研究现状及其应用[J].中国陶瓷,2007,43(1):12-15.
[2] 李治阳,廖梦霞,邓天龙.合成硼酸钙的研究进展[J].无机盐工业,2007,39(11):4-7.
[3] Cao Chune,Wang Yingjun,Zheng Naizhang,et al.Study on the synthetic process of calcium borate[J].Key Engineering Materials,2005,(280-283):605-608.
[4] 任晓红.阻燃剂硼酸锌的分析测定 [J].山西化工,2002, 22(4):33-34.
M icrowave-assisted synthesis of calcium borate
Liu Xia,ZhangLifang,Li Jianhui
(Departm ent of Chem ical Engineering,Beijing Institute of Petrochem ical Technology,Beijing102617,China)
Microwave heating method was adopted to synthesize calcium borate(xCaO·yB2O3·nH2O)so as to shorten reaction time and increase reaction efficiencywhen using boric acid and calcium hydroxide as raw materials.Effects of reaction factors,such as reaction temperature,microwave irradiation time,andmix ratio of raw materials,were investigated in the experiment.Suitable reaction conditions for synthesis of calcium borate(CaO·2B2O3·2H2O)were deter mined as follows:reaction temperaturewas 95~105℃,time ofmicrowave irradiationwas 40 min,amountof substance ratio-of-calcium hydroxide to waterwas 1∶39.6,amount-of-substance ratio of calcium hydroxide to boric acid was 1∶4.5.Under those conditions,the product′s yield reached 88%,the composition analysis of product was up to the standard,its diameter was about 10μm and its dehydration temperature was 190℃.Reaction was 4 times faster undermicrowave irradiation than that under conventional heating.
calcium hydroxide;calcium borate;microwave irradiation
TQ132.32
A
1006-4990(2011)05-0033-03
2010-11-22
刘霞(1962— ),女,硕士,副教授,主要从事基础化学教学和精细化学品的开发研究,已公开发表文章 30余篇。
联系方式:liuxia@bipt.edu.cn

