氢过氧化物裂解酶合成己烯醛反应的研究
陈 晨,华欲飞,孔祥珍,张彩猛
(江南大学食品科学与技术国家重点实验室,食品学院,江苏无锡214122)
氢过氧化物裂解酶合成己烯醛反应的研究
陈 晨,华欲飞*,孔祥珍,张彩猛
(江南大学食品科学与技术国家重点实验室,食品学院,江苏无锡214122)
以苋菜作为氢过氧化物裂解酶(HPL)的酶源,研究了氢过氧化物裂解酶合成己烯醛的反应,并通过顶空-气相联用法(HS-GC)对产物进行分析。该反应中HPL对产物具有较强的吸附作用,大大影响了产物测量的准确度。通过一个校正方法来减少误差,并在此基础上考察了该反应的反应时间、pH、温度、底物浓度、酶浓度、BHT浓度等因素对己烯醛产率的影响,其中当反应时间10min,pH7.5,温度20℃,40mmol/L底物,酶浓度为12U/mL,BHT浓度为1mmol/L时,己烯醛的产率达到985mg/L。
氢过氧化物裂解酶,己烯醛,吸附作用,酶催化
1 材料与方法
1.1 实验材料
亚麻酸 工业品(质量分数80%),河北欣奇典生物科技有限公司;硼酸、四硼酸钠、磷酸氢二钠、磷酸二氢钠、无水乙醚、无水硫酸镁、硫酸、硫酸铵、无水乙醇、tritonX-100等试剂 均为分析纯;二硫苏糖醇(DTT)、己烯醛(质量分数98%)Sigma;LOX本实验室制备;新鲜苋菜 购自当地市场。
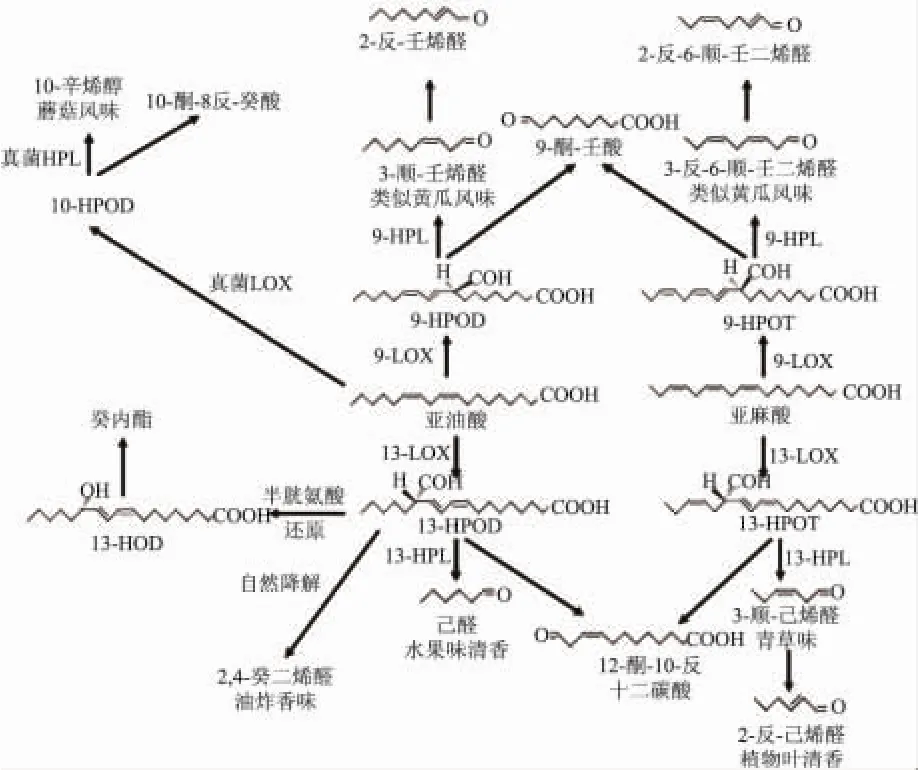
图1 LOX/HPL途径降解不饱和脂肪酸生成芳香物质
1.2 实验方法
1.2.1 亚麻酸氢过氧化物的制备[5]亚麻酸氢过氧化物通过LOX氧化亚麻酸制备。称取一定量的亚麻酸加入pH9.0硼酸盐缓冲液中,在4℃下搅拌充分后再加入LOX并通氧气进行反应。反应生成的氢过氧化物具有共轭双键,在234nm处有特征吸收峰,因此在反应过程中测234nm处的吸光度值,当吸光度不再随反应时间增加时,反应结束。置于4℃下冷藏待用。
1.2.2 HPL粗酶的提取 取苋菜叶(100g)加入300mL匀浆液(0.1mol/L Tris-HCl,0.5%PVP-K30,pH 8.5)组织捣碎后过滤,滤液冷冻离心后取沉淀,用含有 0.5%tritonX-100(w/v)的磷酸盐缓冲液(0.02mol/L,pH6.8,1mmol/LDTT)溶解1h,10000r/min冷冻离心30min。取上清液置4℃下待用。
1.2.3 HPL酶活的测定 亚麻酸氢过氧化物具有共轭双键,在234nm处有紫外特征吸收峰而己烯醛不具备此特征,随着底物的裂解,其共轭双键被破坏,在234nm的紫外吸光度也随之下降。摩尔吸光系数为:ε=25000cm-1M-1[6]。1U酶活定义为:在25℃,pH6.0条件下,在1min内转化1μmol底物的酶量。
1.2.4 氢过氧化物裂解反应 亚麻酸氢过氧化物在HPL的作用下生成己烯醛。反应在密封的顶空瓶中进行,反应后直接顶空气相法检测,以减少产物损失。底物除去溶剂后加入0.1mol/L磷酸盐缓冲液中,然后加入HPL于恒温振荡水浴锅中进行反应,反应终体积为5mL。反应结束后加H2SO4调酸终止反应。
1.2.5 HPL粗酶对产物吸附作用的研究 由于HPL粗酶的蛋白含量较高,对于己烯醛具有明显的吸附作用。将己烯醛标样与不同浓度HPL混合,搅拌一定时间达到吸附平衡后,进行HS-GC分析。
1.2.6 校正己烯醛含量方法 在相同条件下做两个

式中,X-吸附率;As-空白峰面积;Aa-样A峰面积;Ab-样B峰面积。
表观峰面积比吸附率即可得到实际峰面积,通过此法可基本排除吸附作用对反应的干扰,结果更加接近真实值。
1.2.7 产物的检测方法 样品通过HS-GC检测。将样品置于顶空进样器上,在70℃下保温10min,顶空进样至气相色谱仪GC-2010,PEG-20M毛细管色谱柱(30m×0.32mm,岛津,日本),程序升温:40℃保温5min,10℃/min升温至180℃,保温5min。载气为氮气,流速1.5mL/min,FID检测器,检测器温度为250℃。己烯醛的保留时间为14.6min附近。
样品浓度=(样品峰面积×标样浓度)/标样峰面积
产率=样品浓度×体积反应A和B,体积为3mL。A加入2mL缓冲液,B加入2mL己烯醛标样;C为空白样(2mL己烯醛标样加入3mL缓冲液)。分别进行HS-GC分析。通过公式可计算出吸附率,即产物被HPL粗酶吸附的百分比。
2 结果与讨论
2.1 粗酶的吸附作用
由于所使用的HPL是粗酶,具有较高的蛋白含量,这些蛋白对于产物己烯醛具有较强的吸附作用。图2为不同酶浓度对于产物(106mg/L己烯醛)的吸附状况。从图2可以看出,随着酶浓度的提高,酶对于产物的吸附呈线性上升,不过当酶浓度大于18U/mL时,吸附率增加速率逐渐趋于平缓。

图2 不同酶浓度对产物的吸附状况注:己烯醛浓度为106mg/L。
2.2 反应时间
在前10min内,亚麻酸氢过氧化物的转化率迅速升高,可以得出,这段时间内的反应是剧烈而快速的,裂解作用明显,当反应10min以后时,己烯醛产率会迅速下降,可能是被杂酶分解所引起的。因此,在反应进行到10min时,迅速加酸终止反应。
2.3 pH
pH是影响反应的关键因素。当pH在5.5~6.0之间时,HPL的酶活达到最高。但是在进行高底物浓度反应时,亚麻酸氢过氧化物在低pH下的溶解性较差,酶与底物之间传质不良,因此己烯醛产率较低;当pH达到7.5附近时,亚麻酸氢过氧化物基本溶解,此时己烯醛产率最高,为560mg/L。随着pH的进一步增加,酶活迅速下降,己烯醛产量迅速降低。

图3 反应时间对己烯醛产率的影响注:底物浓度30mmol/L,pH6.0,25℃,酶浓度为3U/mL。
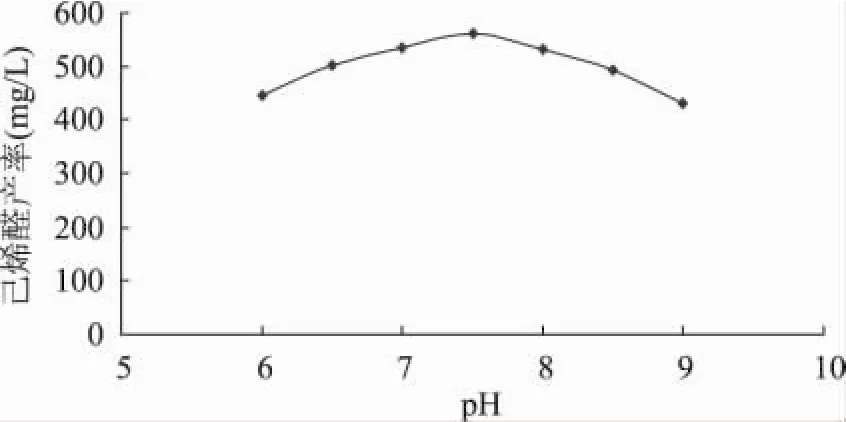
图4 pH对己烯醛产率的影响注:底物浓度30mmol/L,25℃,酶浓度为3U/mL,反应时间10min。
2.4 温度
温度对酶促反应的影响包括两个方面:一方面当温度升高时,与一般化学反应一样,反应速度加快;另一方面,随着温度的升高而使酶蛋白逐步变性,反应速度随之下降。因此,酶促反应的最适温度就是这两种过程平衡的结果。据报道,HPL酶活性的最适温度在室温附近。由图5可以看出,在20℃附近时,己烯醛产率最高,达到640mg/L,这与酶活的最适温度一致。
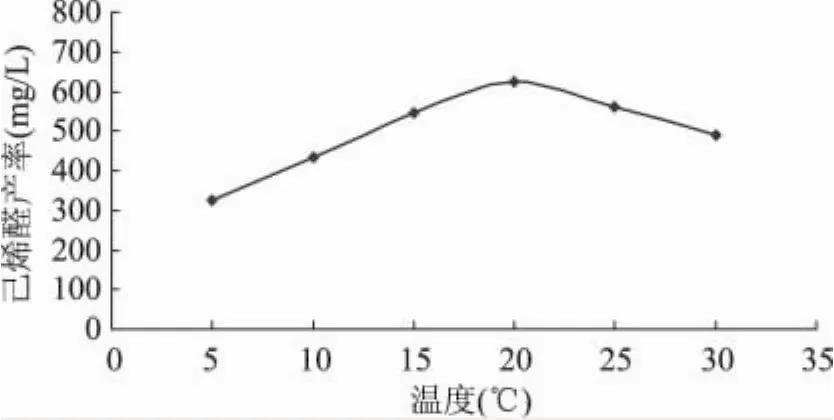
图5 温度对己烯醛产率的影响注:底物浓度30mmol/L,pH7.5,酶浓度为3U/mL,反应时间10min。
2.5 底物浓度
由图6可以看出,随着底物浓度的增加,己烯醛的产率不断增加,当底物浓度达到40mmol/L时,己烯醛产率达到最大值651mg/L。随后,随着底物浓度的增加,己烯醛产率逐渐下降。这表明底物可能对于HPL存在抑制作用。Matsui等人[7]提出,氢过氧化物与HPL的活性中心结合并被转化为自由基,自由基破坏了活性中心的巯基而使酶失活,该假设尚未完全被证实。
2.6 加酶量
由图7可以看出,随着反应液中酶浓度的提高,己烯醛产率提高,当酶浓度达到12U/mL时,己烯醛产率达到最高,为901mg/L左右,进一步增加酶浓度时,由于酶与底物结合已经达到饱和,高浓度的酶液的粘度偏大,影响酶与底物的充分结合,导致反应产率略有下降。

图6 底物浓度对己烯醛产率的影响注:pH7.5,20℃,加酶量分别为0.5、1、2、3、4、5、6、8U/mL,以确保酶底比一致,反应时间10min。
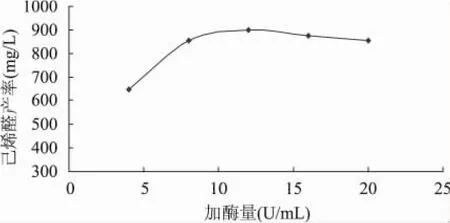
图7 加酶量对己烯醛产率的影响注:底物浓度40mmol,pH7.5,20℃,反应时间10min。
2.7 BHT浓度
如图8所示,最适的BHT浓度为1mmol/L,此时己烯醛产率为985mg/L。HPL反应过程中会产生大量的自由基,这些自由基攻击HPL的活性中心,进而抑制了HPL反应的继续进行,而BHT可能会对这些自由基具有清除作用,对于己烯醛产率的提高具有促进作用。
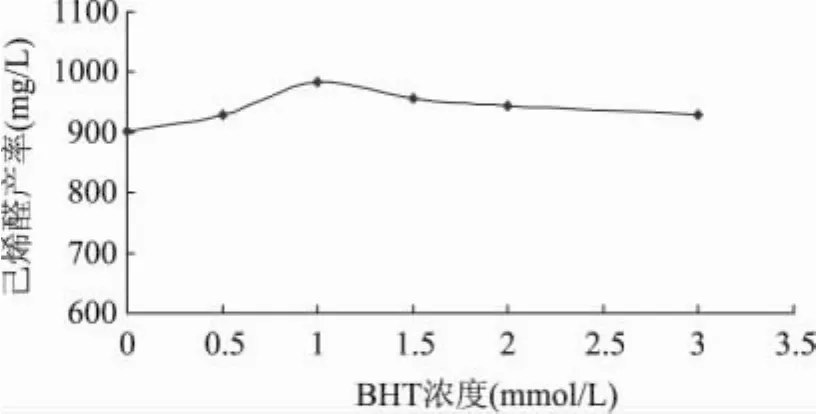
图8 BHT浓度对己烯醛产率的影响注:40mmol/L底物,pH7.5,20℃,加酶量12U/mL,反应时间10min。
3 结论
3.1 HPL对于合成的产物己烯醛具有较强的吸附作用,酶浓度越高,吸附作用越强,本文提出了一个校正产率的方法。
3.2 HPL合成己烯醛的最佳条件为:反应10min、pH 7.5、20℃、底物浓度40mmol/L、加酶量12U/mL、BHT 1mmol/L;在此条件下己烯醛的产率为985mg/L。
[1]Kishimoto K,Matsui K,Ozawa R,et al.Components of C6-aldehyde-induced resistance in Arabidopsis thaliana against a necrotrophic fungal pathogen,Botrytis cinerea[J].Plant Sci,2006,170:715-723.
[2]Matsui K.Green leaf volatiles:hydroperoxide lyase pathway of oxylipin metabolism[J].Curr Opin Plant Biol,2006(90):274 -280.
[3]Noordermeer M A,Goot W,Kooij A J,et al.Development of a Biocatalytic Process for the Production of C6-Aldehydes from Vegetable Oils by Soybean Lipoxygenase and Recombinant Hydroperoxide Lyase[J].J Agric Food Chem,2002,50:4270 -4274.
[4]Mohamed Gargouri,Philippe Drouet,Marie-Dominique Legoy.Hydroperoxide-lyase activity in mint leaves Volatile C6-aldehyde production from hydroperoxy-fatty acids[J].Journal of Biotechnology,2004,111(1):59-65.
[5]蔡琨,周建东,方云,等.大豆脂肪氧合酶酶促合成亚油酸氢过氧化物[J].精细化工,2005,22(1):74-77.
[6]Vick,B.A..A spectrophotometric assay for hydroperoxide lyase[J].Lipids,1991,26:315-320.
[7]Matsui K,Kajiwara T,Hatanaka A.Inactivation of tea leaf hydroperoxide lyase by fatty acid hydroperoxide[J].J Agric Food Chem,1992,40:175-178.
Study on the synthesis of hexenal catalyzed by hydroperoxide lyase
CHEN Chen,HUA Yu-fei*,KONG Xiang-zhen,ZHANG Cai-meng
(State Key Laborary of Food Science and Technology,School of Food Science and Technology,Jiangnan University,Wuxi 214122,China)
Amaranth was used as resource material of hydroperoxide lyase(HPL).Synthesis of hexenal with hydroperoxide(13-HPOT)catalyzed by hydroperoxide lyase was studied,the method of HS-GC was taken to analyze the product.The crude enzyme had a strong adsorption effect on the product influencing the accuracy of result.A method was found to revise the amount of product.On the basis of this analytical method’s improvement,the reaction was explored.The optimal condition was:10min reaction time,pH 7.5,20℃,40mmol/L concentration of substrate,12U/mL HPL concentration,1mmol/L BHT concentration.The yield of hexenal achieved 985mg/L.
hydroperoxide lyase;hexenal;adsorption effect;enzymatic catalysis
TS201.2
B
1002-0306(2011)11-0296-04
绿色植物所特有的清香香气的主要成分是C6醛类和酮类,如己醛、己烯醛等化合物。这些物质在植物组织受伤,或者受到昆虫和细菌侵害时产生[1-2]。它们在植物体内主要是通过脂肪氧合酶/氢过氧化物裂解酶(LOX/HPL)途径生成的(见图1)。多不饱和脂肪酸(PUFA)在脂肪氧合酶(lipoxygenase,LOX)的作用下与O2结合,形成氢过氧化脂肪酸;后者又作为氢过氧化物裂解酶(hydroperoxide lyase,HPL)的底物被裂解;随着LOX和HPL特异性的不同,将分别产生C6、C9或C10醛[3]。植物HPL属于细胞色素P450(CytP450)类蛋白家族,相对分子质量为40000~60000的血红素-铁硫蛋白。它可以分成两类,一种催化C18氢过氧化物生成两个C9片段,另一种催化C18氢过氧化物生成一个C6醛和一个C12过氧酸片段。具有第一种活性的HPL在梨的果实和叶片中发现,具有第二种活性的HPL在西瓜苗、茶叶、番茄果实、紫花苜蓿苗、大豆以及菠菜叶中被发现,而黄瓜HPL同时具有两种位置特异性[4]。将发生在植物组织内的LOX/HPL酶联催化过程应用到食品风味成分的商业化制备具有非常诱人的前景。该过程采用天然原料,在模拟植物代谢过程的条件下制备完成,根据欧洲和美国食品法规,产品是“天然的”。工艺过程不产生任何有毒、有害废料,因此是“绿色和清洁的”。目前国外采用该法制备香料化合物取得了一定成果,但国内尚未见报道。本文对HPL途径生成己烯醛的反应进行了初步探索,研究了该反应的影响因素并确定其最佳反应条件,为其工业化应用提供基础。
2010-10-21 *通讯联系人
陈晨(1986-),男,在读硕士,主要从事粮食油脂及植物蛋白方面研究工作。
国家863计划基金(2008AA10Z305);中央高校基本科研业务费专项资金(JUSRP10919)。

