巧克力起霜研究进展
王风艳,王兴国,陶冠军,周胜利,金青哲,刘元法,*
(1.江南大学食品学院,江苏 无锡 214122;2.江南大学 食品科学与技术国家重点实验室,江苏 无锡 214122;3.东海粮油工业张家港有限公司,江苏 张家港 215634)
巧克力起霜研究进展
王风艳1,王兴国1,陶冠军2,周胜利3,金青哲1,刘元法1,*
(1.江南大学食品学院,江苏 无锡 214122;2.江南大学 食品科学与技术国家重点实验室,江苏 无锡 214122;3.东海粮油工业张家港有限公司,江苏 张家港 215634)
巧克力起霜导致产品品质下降,成为困扰糖果工业的一个世界性难题。基料油种类不同,起霜的机理显著不同。从基料油性质出发,详细阐述基料油组成、加工条件以及储存条件对巧克力起霜的影响。在此基础上,对各类巧克力起霜的机理进行总结,为解决起霜问题提供理论支持。参考国内外文献报道,对巧克力起霜的研究方法进行总结,并详细阐述具有延缓起霜作用的措施,为巧克力生产提供参考。
巧克力;起霜;机理;研究方法;改善
巧克力按基料油性质和来源不同,可分为天然纯可可脂巧克力、类可可脂(CBE)巧克力、非月桂酸型代可可脂(CBR)巧克力及月桂酸型代可可脂(CBS)巧克力[1]。巧克力在贮存过程中极易出现起霜现象。起霜分两种:糖霜和脂霜。相对湿度较高时,巧克力表面湿气增加使砂糖晶体溶化,当相对湿度降低时,砂糖重新结晶形成“糖霜”。脂霜的形成与巧克力中所用的油脂密切相关[2]。引起脂霜(后简称起霜)的因素很多[3-4],并且起霜形式多样,使得对起霜的研究难度增加。人们提出了多种起霜机理,包括晶型转变、油脂迁移等,然而到目前为止还未达成一致[2]。不同种类巧克力的起霜机理是否一致也尚未明确。随着新型精密仪器不断出现,进一步明确起霜机理成为可能[5-7]。本文从不同类型的基料油出发,对基料油的性质及相应巧克力的起霜机理作一阐述,并对巧克力起霜因素、防控措施及研究手段进行总结,以期为研究和解决起霜问题提供理论和技术支持。
1 巧克力基料油
1.1 可可脂
可可脂是巧克力加工中的主要油脂,其甘三酯(TAG)类型主要为对称的单不饱和型,含量超过了总TAG含量的75%[2]。可可脂具有6种晶型[8],即Ⅰ~Ⅵ型晶型,热力学稳定性按顺序递增,晶型的转变方式如图1所示。Ⅴ型晶型是巧克力加工中期望的晶型,需由熔化后的巧克力以适当调温过程获得。

图1 可可脂同质多晶型的转化Fig.1 Polymorphism transition of cocoa butter
1.2 类可可脂
类可可脂(CBE)一般由富含2-油酸-1,3-二棕榈酸-sn-甘油酯(POP)、2-油酸-1,3-二硬脂酸甘油酯(SOS)及1-棕榈酸-2-油酸-3-硬脂酸(POS)的油脂调配而成,如棕榈油分提中间物(PMF,富含POP)、kokum酯(富含SOS)、Illipe酯(富含POS),也可通过酶法合成或酯交换手段来获得[9-10]。CBE具有与可可脂相似的TAG组成及同质多晶现象,可以任意比例与可可脂相容[11-12]。
1.3 非月桂酸型可可脂替代品
非月桂酸型可可脂替代品(CBR),主要由大豆油、棉籽油、卡诺拉油和棕榈油的部分氢化或部分氢化结合分提获得[1]。CBR中TAG主要含十六碳和十八碳脂肪酸,与可可脂的相容性低于CBE,但仍可达25%。大豆、棉籽油部分氢化后具有与可可脂相似的同质多晶型。氢化棕榈油可迅速结晶成β′晶型,但贮存期间将转化为β晶型。
1.4 月桂酸型可可脂替代品
月桂酸型可可脂替代品(CBS)一般由椰子油或棕榈仁油氢化或分提而获得[13]。CBS富含月桂酸(40%~50%),主要TAG为三月桂酸甘三酯(LaLaLa)。CBS具有与可可脂相似的熔化曲线,可完全取代可可脂用于巧克力产品的生产。CBS的同质多晶型以β′晶型为主,加工过程无需调温,可直接结晶成稳定的β′晶型。
2 巧克力起霜机理
2.1 可可脂巧克力
可可脂基巧克力的起霜问题最早被研究,常见的起霜机理包括晶型转变、油脂迁移、共晶作用、晶体分层等(图 2)。
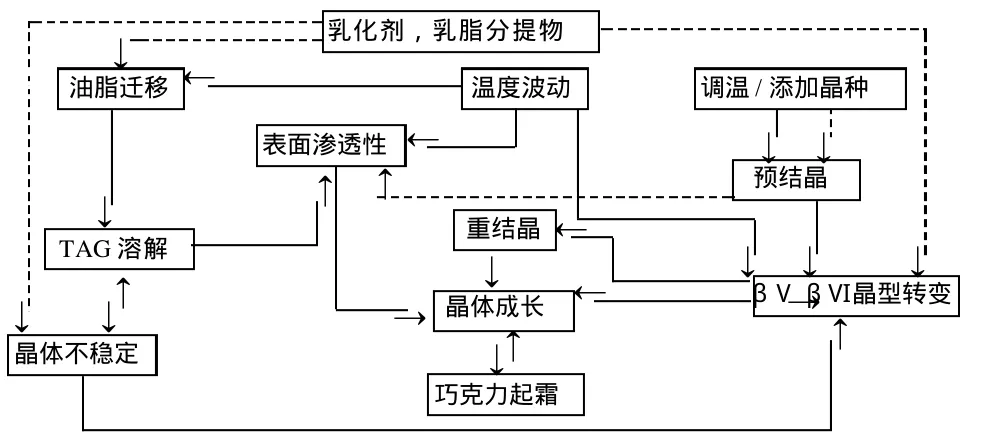
图2 可可脂基巧克力起霜的机理Fig.2 Mechanism of frost in chocolate at the condition of cocoa butter as the matrix oil
2.1.1 晶型转变
晶型转变理论认为起霜的过程总是伴随着βⅥ型晶体的出现,且随温度的升高和波动而加快,因此βⅤ型向βⅥ型的转变导致了巧克力的起霜[8,14]。调温较好的巧克力在贮存过程中存在βⅤ型晶体向βⅥ型晶体的转变,然而,并非存在βⅥ型晶体的巧克力都表现为起霜。Bricknell等[14]研究发现含有大量βⅥ型晶体的巧克力并未起霜,因此认为晶型的转变是起霜的结果而不是原因。
2.1.2 油脂迁移
常温下呈固态的脂肪并非完全以固态存在,而是含有相当数量的、束缚在脂肪晶体基质中的液态TAG组分。Lonchampt等[2]认为油脂迁移(高熔点TAG融于液态油脂中)至巧克力表面发生重结晶并伸出巧克力表面散射光线导致起霜。Kinta等[15]认为晶体成长过程中周围的脂肪向巧克力内部迁移造成起霜。
2.1.3 共晶作用
共晶作用可发生在单一油脂中,也可发生在两种不相容的油脂混合体系中。如可可脂初始结晶过程出现高低熔点组分分离,晶体中SOS浓度显著升高,而POP和POS浓度明显降低[16-18]。但脂霜中并未发现SOS含量显著提高[15,19-20],因此,该理论未得到进一步的证实。
2.2 CBS巧克力
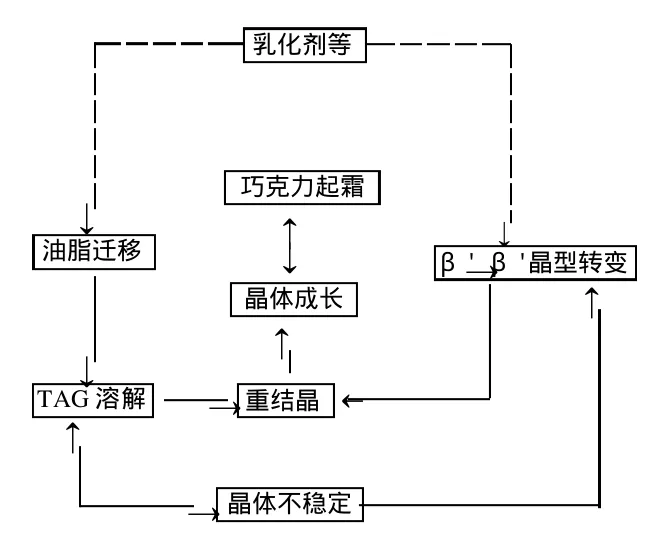
图3 CBS巧克力起霜的机理Fig.3 Mechanism of CBS-based chocolate
目前关于CBS巧克力起霜的理论主要有共晶作用、油脂迁移以及晶型衍变等,如图3所示。
2.2.1 共晶作用
CBS对可可脂非常敏感,可可脂含量很低时也会出现严重的共晶现象。但是共晶现象是否是CBS巧克力起霜的机制还存在疑问。Williams等[21]在比较不同种类的CBS和可可脂的混合物时发现共晶现象明显的样品起霜却相对较慢。这一现象还有待于进一步研究。
2.2.2 油脂迁移
Ali等[22]对不同储存条件下的夹心棕榈仁硬脂黑巧克力的油脂迁移进行了分析,发现18℃时油脂迁移的速度很慢且未起霜;而30℃时油脂迁移速度很快并迅速起霜。Smith等[23]研究发现不同温度下发生迁移的油脂组分不同。
2.2.3 晶型转变
LaLaLa本身可由β′晶型向β晶型转变并向表面迁移,其含量增加将会诱发CBS巧克力很快起霜[23]。Williams等[21]发现可可脂含量低于40%的可可脂-氢化棕榈仁油混合物在18周的储存期内并未出现β′向β晶型转变。因此,晶型转变是否是引发起霜的关键还有待于进一步研究。
2.3 CBE巧克力
由于法律法规的束缚以及生产成本较高,CBE用于巧克力的生产还受很大限制,因此关于CBE巧克力起霜机理的研究还未见报道。不过可以推测,由于CBE与可可脂类似的TAG组成,其起霜的机理应该相同或相似。
2.4 CBR巧克力
CBR巧克力在储存过程中起霜现象不明显,样品在室温下放置几个月仍未起霜[12,24]。已有CBR巧克力起霜的报道主要倾向于油脂不相容导致起霜,而非储存过程中的起霜。
3 巧克力起霜因素及防控
3.1 巧克力组分
3.1.1 基料油脂
两种不相容的油脂共用将导致组分相互分离及共晶现象,并加速巧克力起霜。夹心巧克力油脂含量很高,比块状巧克力更易起霜。夹心量越大,巧克力层越薄,越易起霜。这与巧克力夹心中高不饱和油脂组分从内部向表面的迁移有关[25-26]。
3.1.2 乳脂及其熔点分提物
乳脂具有延缓巧克力起霜的作用,特别是高熔点乳脂分提物[27-31]。乳脂中的微量脂质成分(甘二酯、单甘酯等)也可显著影响脂肪结晶及巧克力起霜[29]。不过,乳脂用于CBS巧克力中不仅不能延缓起霜,反而会诱发霜的形成[21,32-33]。
3.1.3 乳化剂
乳化剂可影响脂肪的结晶,作为抗起霜剂及调节油脂的同质多晶型转变。卵磷脂、人工合成的磷脂(YN)、聚甘油多聚蓖麻酸酯(PGPR)可有效改善巧克力的黏度和屈服应力,山梨醇酯、单甘酯、甘二酯主要影响油脂的结晶过程[34]。
3.2 加工条件
3.2.1 调温工艺
调温过程直接影响巧克力的品质。合理调温的巧克力中含有最大量有正确晶型的小晶体,脱模性好、表面光亮并可有效预防起霜。若调温不足,油脂冷却过程中将形成不稳定晶型,将发生重结晶导致巧克力迅速起霜[19,35-37]。若调温过度,脱模面光泽度消失,非脱模面很快变为沉闷的灰色[19]。
3.2.2 冷却速率
冷却速率太快会使可可脂基和CBE基巧克力形成不稳定晶型,同时可能出现孔隙和裂缝,从而促发起霜。恰当的冷却速率有利于油脂潜热的均匀释放,有效减少巧克力表面张力,延缓起霜。但对CBS和CBR巧克力而言,冷却速率需足够快以保证油脂充分结晶,温度越低、结晶速率越快越有利于抑制起霜。
3.3 储存条件
3.3.1 储存温度
温度升高会导致巧克力中低熔点TAG流动性增加,引发起霜或品质下降[7,25]。温度在18~30℃之间时,随着温度的升高起霜速率加快。而当温度大于32~34℃时,巧克力部分熔化,当温度降低时油脂结晶形成不稳定晶型导致起霜。然而有报道称对于CBS巧克力而言,15℃时比20℃和25℃时更易起霜[23]。
3.3.2 温度波动
温度波动将降低起霜的诱导时间,从而促使可可脂基巧克力快速起霜[14,38-39]。不过,CBS基巧克力对温度波动不敏感[21,23]。
因此,应保持巧克力在较低的温度下储存并严格控制温度波动。此外,还可通过建立网络结构来固定液态油从而延缓和(或)减少油脂迁移以预防起霜[21,40]。
4 研究方法
4.1 扫描电镜
扫描电镜(SEM)、环境扫描电镜(ESEM)和冷冻扫描电镜(cryo-SEM)可对样品的表面形态和结构进行全面分析。Cryo-SEM检测精度高,可提供高分辨率的图像。ESEM检测复杂,但可对巧克力样品在储存中的变化进行监测。两者结合为研究巧克力起霜提供有力手段[6]。然而,SEM技术也存在缺陷,如操作环境必须为高真空,样品不能进行无损检测等。
4.2 立体显微镜
立体显微镜可观察不同类型的巧克力产品体系组分分布情况、结晶网络结构以及脂肪晶体的变化[36]。该方法不损坏巧克力的结构,能反映巧克力的真实结构。但放大倍数小、分辨率不高,仅能提供巧克力宏观形态变化,无法精确观察巧克力中的颗粒形态。
4.3 原子力显微镜
原子力显微镜(AFM)为食品研究提供了纳米精度的检测方法。样品无需预处理且扫描过程不会对样品造成损坏,因此优于传统的显微镜技术[41]。原子力显微镜具有强大的形貌分析功能,可提供巧克力表面的三维形貌图,分析巧克力表面的凸起和凹陷区域,从而为分析起霜过程提供依据[5,39]。
4.4 核磁共振光谱及核磁共振成像
核磁共振(NMR)光谱及成像技术(MRI)是一种基于特殊核(比如质子)的磁特性的无创无损技术,通过自旋-自旋(T1)和自旋-晶格(T2)弛豫时间分别给出核的流动性信息及自旋发生环境的物理结构信息[42-44]。
4.5 X射线衍射
巧克力在储存过程中油脂晶型的转变可通过X射线衍射(XRD)来分析。糖晶体的存在会影响油脂晶型的观察,因此需另行去除。可采用基质谱图减去加热后样品(50℃)谱图[15],也可先将糖组分溶解再进行扫描[45]。
4.6 质构仪
硬度、脆度是影响巧克力可接受性的重要指标[21],采用质构仪可对这些性质进行全面检测。Emmanuel等[35,46]发现巧克力硬度和表面颜色高度相关,可用于预测巧克力起霜。
研究起霜的各种手段各有优势,彼此之间互相印证又互相补充,结合各种手段对起霜的过程及结果进行全面分析,对于明确巧克力起霜的机理大有裨益。
5 结 语
巧克力种类不同其起霜机理也存在差异,因此需对症解决起霜问题。调温工艺是可可脂基巧克力起霜的主要影响原因,不相容油脂共用导致的起霜也很常见。晶型转变出现在可可脂巧克力和CBE巧克力起霜过程中,有时也会影响其他类型巧克力。CBS巧克力起霜的主要原因在于两种不相容油脂的共用,但这与以可可脂基巧克力起霜明显不同,其机理有待于进一步研究。对巧克力起霜的研究从整个巧克力体系入手,将宏观检测与微观研究相结合,有利于深入了解起霜的机理。与此同时,多种延缓起霜的措施被用于指导生产。但巧克力种类及形态多样,针对性地解决各种起霜问题仍需大量的深入研究。
[2] LONCHAMPT P, HARTEL R W. Fat bloom in chocolate and compound coatings[J]. Eur J Lipid Sci Technol, 2004, 106(4): 241-274.
[3] 华聘聘. 巧克力制品起霜的主要原因[J]. 食品科学, 1994, 15(6): 20-23.
[4] 任雁, 张惟广. 巧克力起霜问题探讨[J]. 粮食与油脂, 2005(11): 36-39.
[5] SMITH P R, DAHLMAN A. The use of atomic force microscopy to measure the formation and development of chocolate bloom in pralines[J]. JAOCS, 2005, 82(3): 165-168.
[6] JAMES B J, SMITH B G. Surface structure and composition of fresh and bloomed chocolate analysed using X-ray photoelectron spectroscopy,cryo-scanning electron microscopy and environmental scanning electron microscopy[J]. LWT, 2009, 42(5): 929-937.
[7] CHOI Y J, MCCARTHY K L, MCCARTHY M J. Oil migration in a chocolate confectionery system evaluated by magnetic resonance imaging[J]. Journal of Food Science, 2005, 70(5): 312-317.
[8] WILLE R L, LUTTON E S. Polymorphism of cocoa butter[J]. JAOCS,1966, 43(8): 491-496.
[9] KHUMALO L W, MAJOKO L, READ J S, et al. Characterisation of some underutilised vegetable oils and their evaluation as starting materials for lipase-catalysed production of cocoa butter equivalents[J]. Industrial Crops and Products, 2002, 16(3): 237-244.
[10] UNDURRAGA D, MARKOVITS A S, ERAZO S. Cocoa butter equivalent through enzymic interesterification of palm oil midfraction[J]. Process Biochemistry, 2001, 36(10): 933-939.
[11] TORBICA A, JOVANOVIC O, PAJIN B. The advantages of solid fat content determination in cocoa butter and cocoa butter equivalents by the Karlshamns method[J]. Eur Food Res Technol, 2006, 222(3/4): 385-391.
[12] PEASE J J. Confectionery fats from palm oil and lauric oil[J]. JAOCS,1985, 62(2): 426-430.
[13] ROSSELL J B. Fractionation of lauric oils[J]. JAOCS, 1985, 62(2):385-390.
[14] BRICKNELL J, HARTEL R W. Relation of fat bloom in chocolate to polymorphic transition of cocoa butter[J]. JAOCS, 1998, 75(11): 1609-1615.
[15] KINTA Y, HATTA T. Composition and structure of fat bloom in untempered chocolate[J]. Journal of Food Science, 2005, 70(7): 450-452.
[16] DAVIS T R, DIMICK P S. Lipid composition of high-melting seed crystals formed during cocoa butter solidification[J]. JAOCS, 1989, 66(10): 1494-1498.
[17] ARRUDA D H, DIMICK P S. Phospholipid composition of lipid seed crystal isolates from ivory coast cocoa butter[J]. JAOCS, 1991, 68(6):385-390.
[18] DAVIS T R, DIMICK P S. Isolation and thermal characterization of high-melting seed crystals formed during cocoa butter solidification[J].JAOCS, 1989, 66(10): 1488-1493.
[19] LONCHAMPT P, HARTEL R W. Surface bloom on improperly tempered chocolate[J]. Eurm J Lipid Sci Technol, 2006, 108(2): 159-168.
[20] KINTA Y, HATTA T. Composition, structure, and color of fat bloomdue to the partial liquefaction of fat in dark chocolate[J]. JAOCS, 2007,84(2): 107-115.
[21] WILLIAMS S D, RANSOM-PAINTER K L, HARTEL R W. Mixtures of palm kernel oil with cocoa butter and milk fat in compound coatings[J]. JAOCS, 1997, 74(4): 357-366.
[22] ALI A, SELAMAT J, MAN Y B, et al. Characterization and fat migration of palm kernel stearin as affected by addition of desiccated coconut used as base filling centre in dark chocolate[J]. Int J Food Sci Nutr,2001, 52(3): 251-261.
[23] SMITH K W, CAIN F W, TALBOT G. Nature and composition of fat bloom from palm kernel stearin and hydrogenated palm kernel stearin compound chocolates[J]. J Agric Food Chem, 2004, 52(17): 5539-5544.
[24] LOVEGREN N V, GAJEE B B, GREY M S, et al. Cocoa butter-like fats from fractionated cottonseed oil: II. Properties[J]. JAOCS, 1973, 50(2): 53-57.
[25] DEPYPERE F, CLERCQ N, SEGERS M, et al. Triacylglycerol migration and bloom in filled chocolates: effects of low-temperature storage[J].Eur J Lipid Sci Technol, 2009, 111(3): 280-289.
[27] CAMPBELL L B, ANDERSEN D A, KEENEY P G. Hydrogenated milk fat as an inhibitor of the fat bloom defect in dark chocolate[J].Journal of Dairy Science, 1969, 52(7): 976-979.
[28] SABARIAH S, ALI A R M, CHONG C L. Chemical and physical characteristics of cocoa butter substitutes, milk fat and malaysian cocoa butter blends[J]. JAOCS, 1998, 75(8): 905-910.
[29] TIETZ R A, HARTEL R W. Effects of minor lipids on crystallization of milk fat-cocoa butter blends and bloom formation in chocolate[J]. JAOCS,2002, 77(7): 763-771.
[30] PAJIN B, JOVANOVIC O. Influence of high-melting milk fat fraction on quality and fat bloom stability of chocolate[J]. European Food Research Technology, 2005, 220(3/4): 389-395.
[31] FULL N A, REDDY S Y, DIMICK P S, et al. Physical and sensory properties of milk chocolate formulated with anhydrous milk fat fractions[J]. Journal of Food Science, 1996, 61(5): 1068-1073.
[32] RANSOM-PAINTER K L, WILLIAMS S D, HARTEL R W. Incorporation of milk fat and milk fat fractions into compound coatings made from palm kernel oil[J]. J Dairy Sci, 1997, 80(10): 2237-2248.
[33] SCHMELZER J M, HARTEL R W. Interactions of milk fat and milk fat fractions with confectionery fats[J]. J Dairy Sci, 2001, 84(2): 332-344.
[34] SCHANTZ B, LINKE L, ROHM H. Effects of different emulsifiers on rheological and physical properties of chocolate[C]// Proceeding of 3rd International Symposium on Food Rheology and Structure. Zurich,Switzerland, February 9-13, 2003: 329-333.
[35] AFOAKWA E O, PATERSON A, FOELER M, et al. Fat bloom development and structure- appearance relationships during storage of undertempered dark chocolates[J]. Journal of Food Engineering, 2009, 91(4):571-581.
[36] AFOAKWA E O, PATERSON A, FOWLER M, et al. Effects of tempering and fat crystallisation behaviour on microstructure, mechanical properties and appearance in dark chocolate systems[J]. Journal of Food Engineering, 2008, 89(2): 128-136.
[37] AFOAKWA E O, PATERSON A, FOWLER M, et al. Influence of tempering and fat crystallization behaviours on microstructural and melting properties in dark chocolate systems[J]. Food Research International,2009, 42(1): 200-209.
[38] HODGE S M, ROUSSEAU D. Fat bloom formation and characterization in milk chocolate observed by atomic force microscopy[J]. JAOCS,2002, 79(11): 1115-1121.
[39] ROUSSEAU D. On the porous mesostructure of milk chocolate viewed with atomic force microscopy[J]. LWT, 2006, 39(8): 852-860.
[40] AFOAKWA E O, PATERSON A, FOWLER M, et al. Modelling tempering behaviour of dark chocolates from varying particle size distribution and fat content using response surface methodology[J]. Innovative Food Science and Emerging Technologies, 2008, 9(4): 527-533.
[41] YANG Hongshun, WANG Yifen, LAI Shaojuan, et al. Application of atomic force microscopy as a aanotechnology tool in food science[J].Journal of Food Science, 2007, 72(4): R65-R75.
[42] WALTER P, CORNILLON P. Lipid migration in two-phase chocolate systems investigated by NMR and DSC[J]. Food Research International,2002, 35(8): 761-767.
[43] WALTER P, CORNILLON P. Influence of thermal conditions and presence of additives on fat bloom in chocolate[J]. JAOCS, 2001, 78(9):927-932.
[44] GUIHENEUF T M, COUZENS P, WILLE H, et al. Visualisation of liquid triacylglycerol migration in chocolate by magnetic resonance imaging[J]. J Sci Food Agric, 1997, 73(3): 265-273.
[45] CEBULA D J, ZIEGLEDER G. Studies of bloom formation using X-ray diffraction from chocolates after long-term storage[J]. Fat Sci Technol,1993, 95(9): 340-343.
[46] AFOAKWA E O, PATERSON A, FOWLER M, et al. Particle size distribution and compositional effects on textural properties and appearance of dark chocolates[J]. Journal of Food Engineering, 2008, 87(2):181-190.
Research Progress of Frost in Chocolate
WANG Feng-yan1,WANG Xing-guo1,TAO Guan-jun2,ZHOU Sheng-li3,JIN Qing-zhe1,LIU Yuan-fa1,*
(1. School of Food Science and Technology, Jiangnan University, Wuxi 214122, China;2. State Key Laboratory of Food Science and Technology, Jiangnan University, Wuxi 214122, China;3. Eastocean Oils and Grains Industries Co. Ltd., Zhangjiagang 215634, China)
Frost in chocolate can result in the decrease of product quality, which is a worldwide problem in the confectionery industry. The mechanisms of frost in chocolate are varied as the change of matrix oil types. In this article, the effects of matrix oil compositions, processing conditions and storage conditions on frost in chocolate have been discussed. Meanwhile, the possible mechanisms of frost in chocolate have been summarized. Moreover, the corresponding strategies for attenuating the formation of frost in chocolate have also been proposed. All of these investigations will provide a theoretical guidance for chocolate production.
chocolate;frost;mechanism;research approach;improvement
TS225.6
A
1002-6630(2011)05-0301-05
2010-06-22
国家“863”计划重点项目(2010AA101506);江南大学博士研究生科学研究基金项目
王风艳(1985—),女,博士研究生,主要从事专用油脂的研究与开发。E-mail:wfs1013@126.com
*通信作者:刘元法(1974—),男,教授,博士,主要从事油脂深加工研究。E-mail:yuanfa.liu@gmail.com

