二氧化碳在金属-有机骨架材料中吸附的阶梯现象
安晓辉 刘大欢 仲崇立
(北京化工大学化学工程学院,计算化学研究室,北京100029)
二氧化碳在金属-有机骨架材料中吸附的阶梯现象
安晓辉 刘大欢*仲崇立
(北京化工大学化学工程学院,计算化学研究室,北京100029)
采用巨正则系综蒙特卡罗(GCMC)模拟方法,对二氧化碳在5种具有相同拓扑结构的金属-有机骨架材料(IRMOFs),即IRMOF-1,-8,-10,-14,-16中吸附产生的阶梯现象进行了详细的研究.结果表明:低温条件下,孔径越大的IRMOFs越容易发生阶梯现象;发生阶梯现象的转变压力与能够发生阶梯现象的转变温度都与孔径呈线性关系.此外,模拟结果进一步验证了二氧化碳分子之间的静电作用力是阶梯现象发生的关键因素.这些规律将为金属-有机骨架材料(MOFs)的设计和改性以及二氧化碳在混合气体中的吸附分离提供有用的信息.
吸附; 二氧化碳; 金属-有机骨架材料; 阶梯现象
Abstract: Grand canonical Monte Carlo(GCMC)simulations were performed to study the stepped behaviors of carbon dioxide adsorption in the following five isoreticular metal-organic frameworks(IRMOFs):IRMOF-1,-8,-10,-14,-16.The simulation results show that the stepped phenomenon occurs easily when the temperature is low and the pore size is large for these IRMOFs.The critical pressure and temperature where the stepped behavior occurs show a linear relationship with the pore size.The results also further indicate that the electrostatic interaction between CO2and CO2molecules plays a dominant role on the stepped behavior.All these findings may provide useful information for the design and modification of MOFs for the adsorption and separation of carbon dioxide in gas mixtures.
Key Words:Adsorption;Carbon dioxide;Metal-organic frameworks;Stepped behavior
1 引言
随着世界人口的激增和工业的快速发展,空气中大量排放的二氧化碳已经对地球环境造成了重大的危害,21世纪末地球平均气温将升高1.4-5.8°C,是一万年来升温最快的.1此外,二氧化碳还是一种重要的工业原料.因此,捕集回收二氧化碳不仅可以缓解减排压力,还能有效地降低工业成本.吸附法是目前常用的二氧化碳捕集技术,常见的吸附材料有沸石分子筛、2,3活性炭4等.
金属-有机骨架材料(MOFs)是除沸石之外又一类引人瞩目的材料,由含氧、氮等的多齿有机配体与金属离子自组装而成,5-8广泛应用于储气、分离、催化、生物化学、药物控制等领域.9-13MOF材料的出现为研究二氧化碳的存储提供了更为广阔的空间.随着对MOFs吸附性能的深入研究,Sunrr等14在考察IRMOF-1对二氧化碳的吸附特性时,发现了一种奇特的阶梯现象,即在特定温度和压力下,二氧化碳的吸附量会发生快速上升,他们认为阶梯现象的产生主要是由被吸附的二氧化碳分子之间的静电作用引起的.但目前对于这种阶梯现象的认识不够深入,如对转变温度、转变压力与材料结构之间的关系等尚不明确,故本工作拟利用分子模拟方法对此问题进行探讨.IRMOFs系列材料作为具有典型代表意义的MOFs之一,是由[Zn4O]6+无机基团与不同类型的有机配体桥联而形成的三维立方微孔骨架材料,15其结构具有相似性.因此,本文选择了五种孔径不同的 IRMOFs:IRMOF-1、IRMOF-8、IRMOF-10、IRMOF-14、IRMOF-16,对二氧化碳在其中的吸附行为进行研究,并讨论孔径、温度等对阶梯现象的影响,这些信息有助于更好地设计具有良好二氧化碳吸附分离性能的新型MOF材料.
2 模型及研究方法
2.1 模型
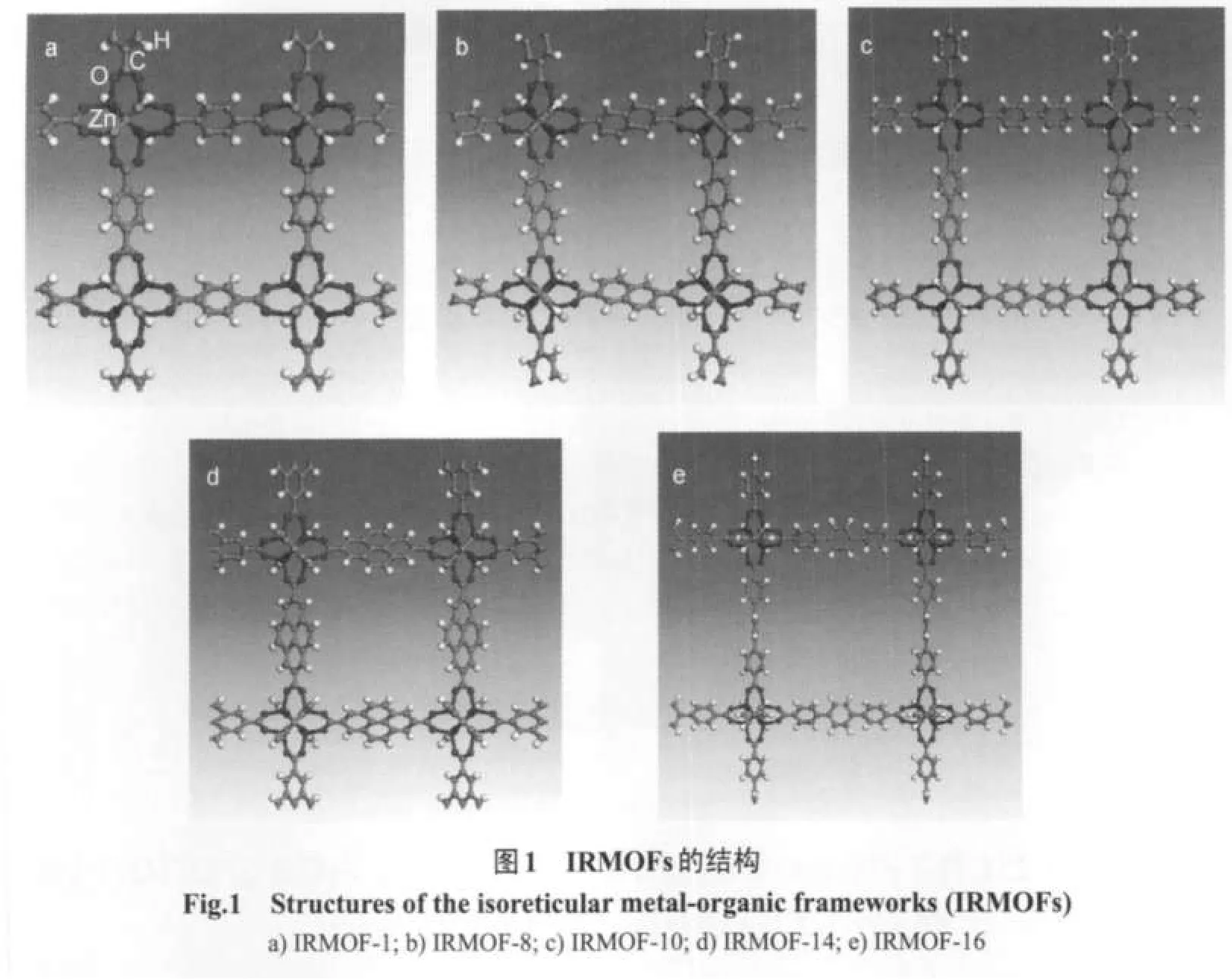
本工作中对材料的模拟均采用刚性结构模型.利用X射线衍射数据,16通过Materials Visualizer软件17构建.IRMOFs的骨架结构如图1所示.
IRMOFs是由[Zn4O]6+无机基团与一系列芳香羧酸配体以八面体形式桥联而成的微孔晶体材料,15每个Zn4O单元与6个羧酸配体相连,而每个羧酸配体与2个Zn4O单元连接,形成三维立方微孔.本文中使用的各种材料的结构性质详细列在表1中,其中dpore为孔径(如1.09/1.43是指材料中小孔和大孔的直径),ρcryst为晶体密度,Vfree为自由体积,Sacc为比表面积.
2.2 力场参数
TraPPE力场18已被广泛应用于研究二氧化碳在介孔材料中的吸附行为.14,15,19因此,二氧化碳分子由TraPPE力场描述,原子点电荷qO=-0.35e,qC=0.70e,C―O键长0.116 nm,键角180°.MOF材料的骨架原子采用Dreiding力场参数,20二氧化碳气体与材料之间的相互作用通过L-J势能模型来描述,L-J参数如表2所示.其中σ和εk分别表示分子间L-J势能的尺寸和能量参数.
2.3 模拟细节
利用本研究组开发的巨正则系综蒙特卡罗模拟(GCMC)程序,21-23研究IRMOFs对二氧化碳的吸附行为.对于IRMOF-1,-8,-10,-14等材料,模拟盒子选择1×1×1个单元晶胞;对于IRMOF-16,模拟盒子为2×2×2个单元晶胞.采用周期性边界条件,L-J势能截断半径为1.28 nm,长程静电作用力采用Ewald加和技术,模拟步数为1.20×108步,其中前6.00×107步用于使体系达到平衡,后6.00×107步用于抽样统计,用Peng-Robinson方程计算气体的逸度(计算过程见补充材料).
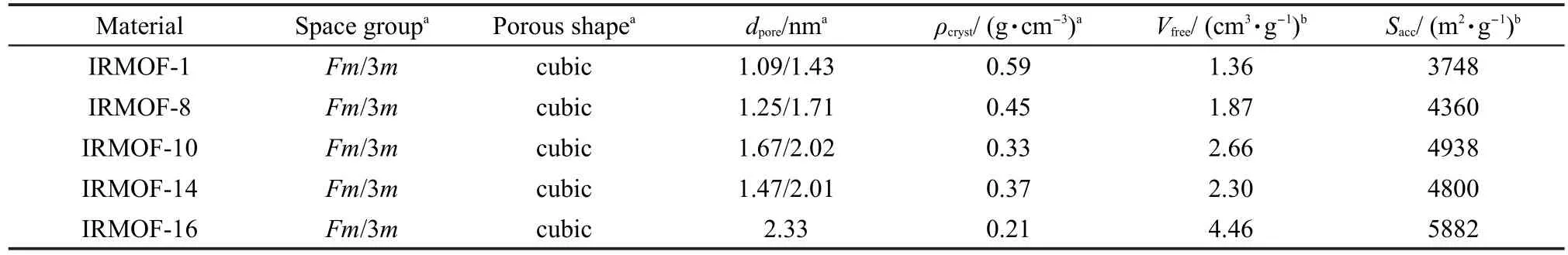
表1 本文使用的IRMOFs结构参数Table 1 Structural parameters of the IRMOFs used in this work

表2 本文中CO2和IRMOFs的L-J势能参数Table 2 L-J potential parameters for CO2and IRMOFs used in this work
3 结果与讨论
3.1 力场验证
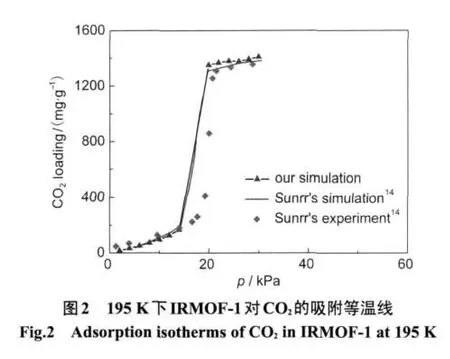
采用与Sunrr等14相同的模拟方法,首先模拟了195 K下IRMOF-1对CO2的吸附等温线,结果见图2.从图中可以看出,本文的模拟结果与文献14中得到的结果吻合.这说明我们采用的模拟方法以及选择的力场参数是合适的.
3.2 IRMOFs对CO2的吸附行为
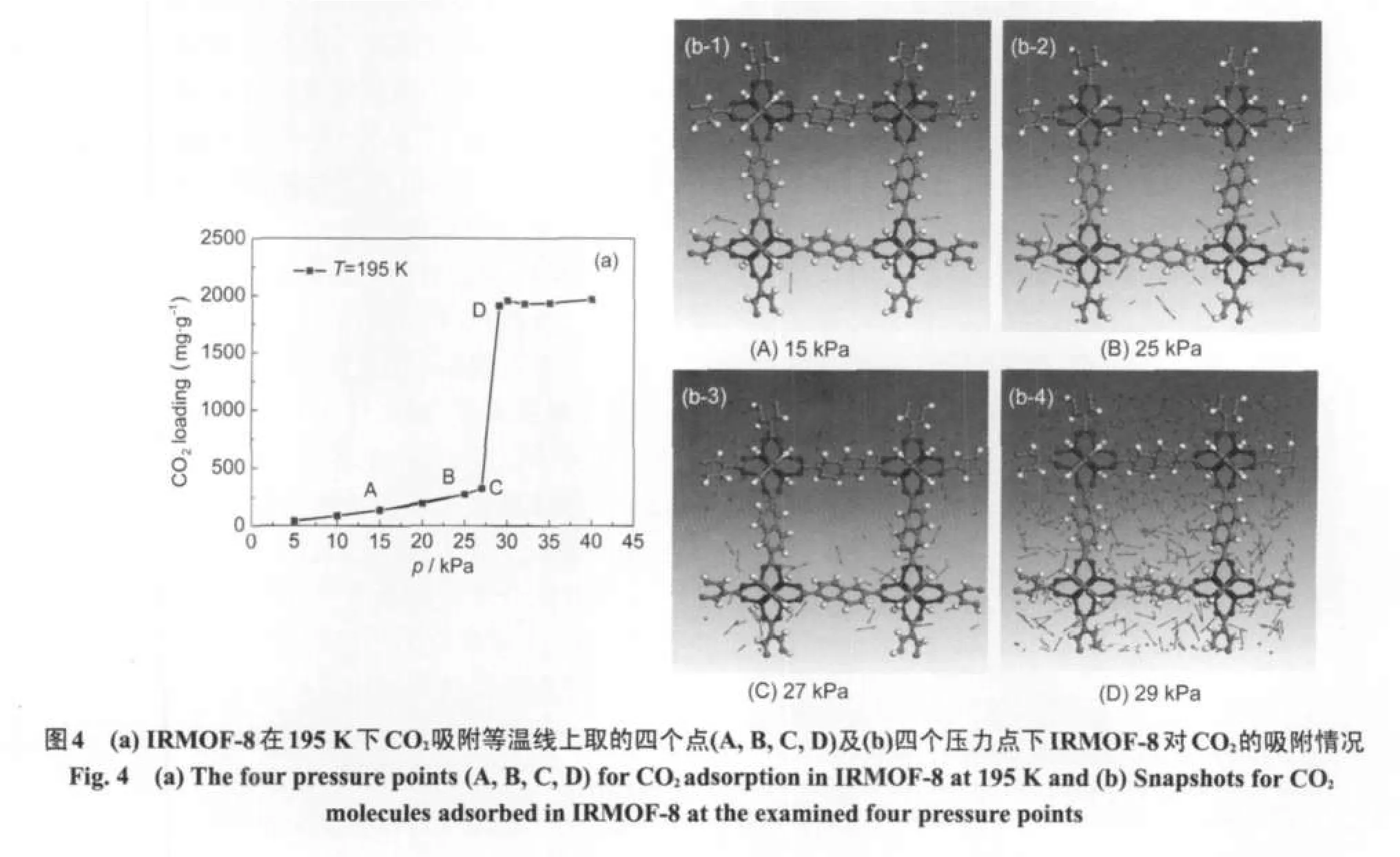
为研究二氧化碳分子间静电力、温度及材料孔径对二氧化碳阶梯现象的影响,本工作对同种材料在多个温度下的二氧化碳吸附等温线进行了模拟,选择温度的依据主要是为了寻找材料的临界转变温度,即材料能够发生阶梯现象的最高温度,为此我们采用插值法,在接近临界温度时将温度间隔控制在5 K左右,以确保得到的临界温度值是可靠的.结果如图3所示.结果显示,5种材料均有阶梯现象发生,但出现阶梯现象的压力和温度有所不同.我们以IRMOF-8为例,给出了195 K时发生阶梯现象前后四个压力点下的CO2吸附情况,见图4.在低于27 kPa时,只有少量的CO2分子吸附在微孔的壁面上,到29 kPa时,虽然压力变化极小,但CO2分子迅速填满微孔,吸附量陡然增加,出现阶梯现象.从图中可以看出,阶梯现象发生前分子的单层吸附并不规则,这与最近在二维共价有机骨架材料(COFs)中出现的阶梯现象19有所不同,二氧化碳分子先在孔壁上形成非常规则的单层吸附,随着压力的增加,二氧化碳分子填满微孔,形成多层吸附.这可能是由于IRMOFs中立方型孔道壁面的结构以及化学性质不如二维COFs孔道均匀.
3.2.1 二氧化碳分子间的静电力对阶梯现象的影响
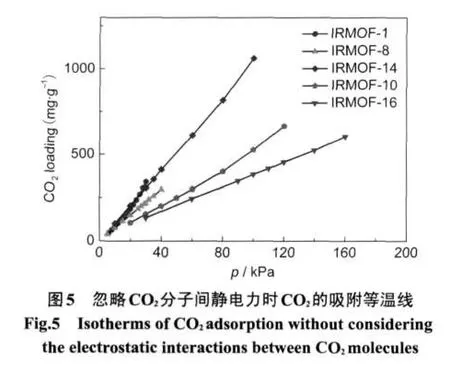
分子模拟发现,静电作用对具有偶极矩和/或四极矩的分子在MOFs中的吸附具有很大的贡献.24比较常见气体偶极矩和四极矩的值25可知,二氧化碳分子的四极矩较大.因此,我们以195 K为例,考察了二氧化碳分子间的静电力对阶梯现象的影响,如图5所示.关掉静电力后,5种材料在195 K下的二氧化碳吸附等温线均未出现阶梯现象,说明二氧化碳分子间的静电作用是产生阶梯现象的关键因素.这与Sunrr等14得到的结论一致.
3.2.2 孔径及温度对阶梯现象的影响
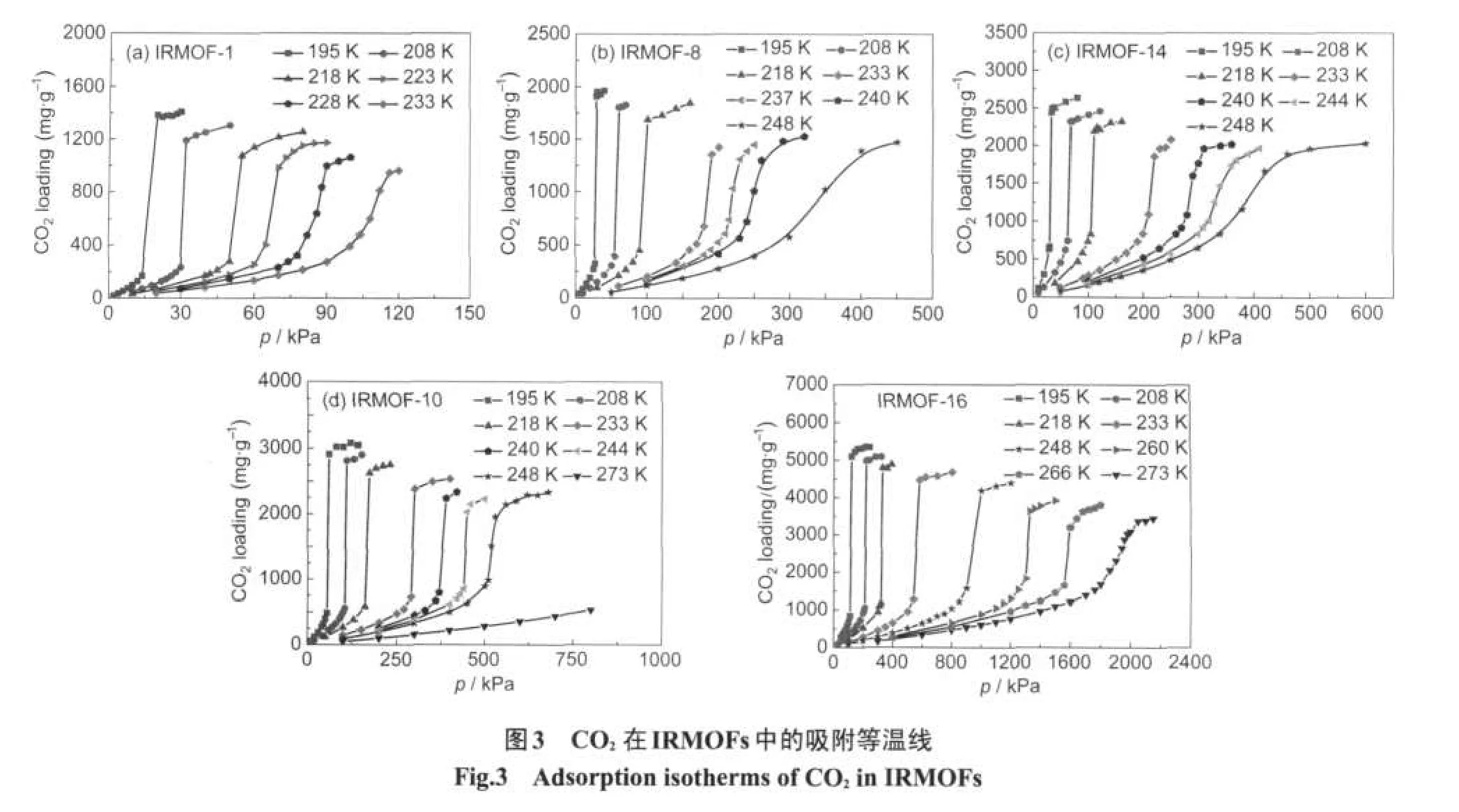
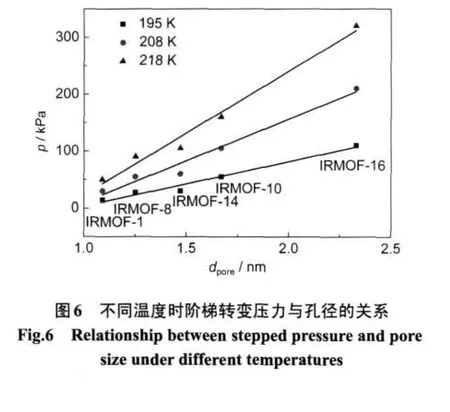
从图3可以看出,同一温度下,孔径越大,发生阶梯现象时的转变压力就越高,并且5种材料在195、208及218 K时均有明显的阶梯现象发生.为了更直观地阐释孔径及转变压力之间的关系,我们将几种材料在上述三个温度下的转变压力对孔径作图,结果如图6所示.从图6中可以看到,温度一定时,转变压力与孔径呈线性关系,且温度越高,转变压力增加的速度越快.这是因为阶梯现象的产生是由于二氧化碳分子之间的静电作用导致其迅速填满微孔所致,而填满大孔材料就需要更多的气体分子,故大孔材料在发生阶梯现象时转变压力相对较高.温度升高,材料对二氧化碳的吸附作用降低,只有在更高的压力下才能吸附足够多的分子,从而发生现阶梯现象.因此,温度越高,转变压力之间的差距越明显.
当孔径一定时,温度越低,越容易发生阶梯现象;而温度较高时,阶梯现象消失.通常情况下,低温有利于材料对气体分子的吸附,温度较高时,材料吸附的气体分子数相对较少,虽然压力有很大提高,但吸附分子数增加地很缓慢,故高温不利于阶梯现象的产生.
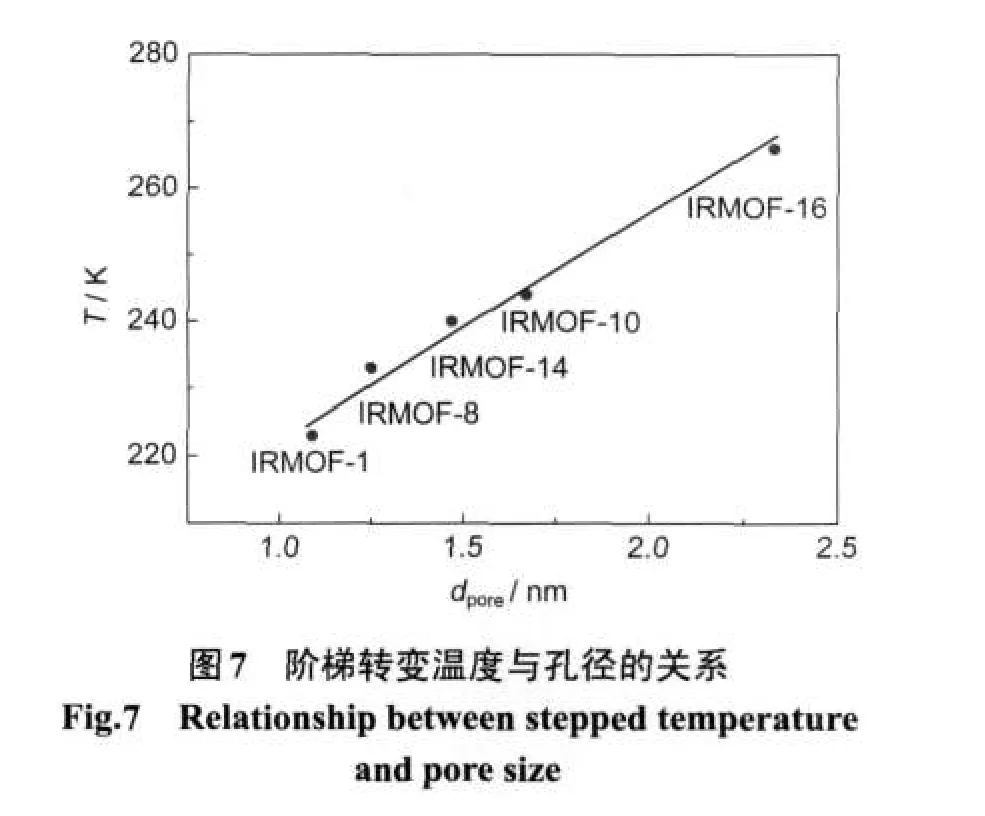
此外,孔径越大,发生阶梯现象的临界转变温度就越高,从图3中得出IRMOF-1,-8,-14,-10,-16分别在223,233,240,244,266 K之后不再有明显的阶梯现象发生,我们以发生阶梯现象时的临界转变温度对孔径作图,结果如图7所示.从图中可以得知,转变温度与孔径也呈直线关系.
以上结果表明,阶梯现象的发生与压力、温度、材料的孔径及二氧化碳分子间的静电力都有关系.发生阶梯现象后气体吸附量陡然增加,因此,可以利用此现象,在特定的温度及压力下大幅度提高MOFs对二氧化碳在混合气体中的分离选择性.
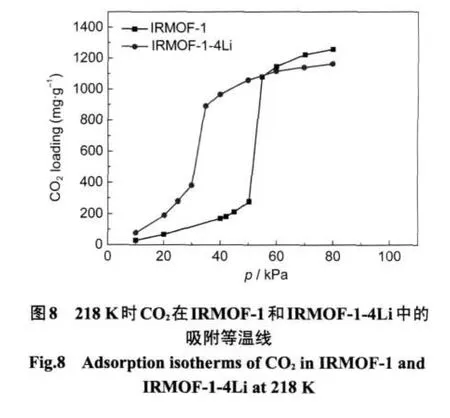
当二氧化碳的分离需要在低温下进行时,应考虑孔径小的IRMOFs.例如,在195 K、50 kPa时,IRMOF-1,-8,-14中均已发生阶梯现象,此时二氧化碳的分离选择性可能显著提高,而IRMOF-10,-16却未出现阶梯现象.当二氧化碳的分离需要在较高温度(如常温)下进行时,应考虑大孔的材料,因为小孔材料在较高温度下不能发生阶梯现象.但另一方面,此时所需要的转变压力就会很高(如图3(e)所示,IRMOF-16在266 K时的转变压力为1600 kPa),因此,可以考虑对材料进行适当的改性,引入特定的官能团,在同等条件下提高二氧化碳的吸附量,增加二氧化碳分子之间的静电作用,从而降低阶梯现象的转变压力,有利于实际操作.如用掺杂金属锂的方法对IRMOFs进行改性,可能会强化材料对二氧化碳的吸附,26进而降低发生阶梯现象的转变压力.图8中给出的是CO2在IRMOF-1和掺杂金属锂的IRMOF-126(IRMOF-1-4Li,结构同参考文献26中的chem-4Li)中的吸附等温线,很明显发生阶梯现象的压力从50 kPa降低到30 kPa左右.利用此方法可以进一步提高材料对二氧化碳在如CO2/CH4、CO2/N2等混合体系中的分离选择性.这将是我们下一步工作的重点.
4 结论
用GCMC模拟方法研究了二氧化碳在5种IRMOFs中吸附的阶梯现象.研究结果表明,在低温条件下,具有较大孔径的IRMOFs容易发生阶梯现象,并且发生阶梯现象时的转变压力及能够发生阶梯现象的转变温度都与孔径呈线性关系.此外,模拟结果还进一步验证了二氧化碳分子之间的静电作用是阶梯现象出现的重要原因.这些结果为新材料的设计提供了理论依据,可以根据实际应用条件选择适当孔径的MOFs,并利用阶梯现象提高二氧化碳的分离选择性.如通过掺杂金属锂或在有机配体上引入特定的官能团等方法,对具有较大孔径的IRMOFs进行改性,可以使IRMOFs能够在较适宜的温度、压力下发生阶梯现象,进而设计出具有较好的二氧化碳吸附分离性能的新型MOFs.
Supporting Information: available free of charge via the internet at http://www.whxb.pku.edu.cn
(1) Kuang,S.L.Modern Chemical Industry 2008,28,3.[邝生鲁.现代化工,2008,28,3.]
(2) Zukal,A.;Dominguez,I.;Mayerová,J.;Čejka,J.Langmuir 2009,25,10314.
(3)Xu,X.L.;Zhao,X.X.;Sun,L.B.;Liu,X.Q.J.Nat.Gas Chem.2008,17,391.
(4) Kim,B.J.;Cho,K.S.;Park,S.J.J.Colloid Interface Sci 2010,342,575.
(5)Yaghi,O.M.;O′Keeffe,M.;Ockwig,N.W.;Chae,H.K.;Eddaoudi,M.;Kim,J.Nature 2003,423,705.
(6) Dunbar,K.R.;Heintz,R.A.P.Inorg.Chem.1997,45,283.
(7) Gramaccioli,C.M.Acta Crystallogr.1966,21,600.
(8)Okada,K.;Kay,M.I.;Cromer,D.T.;Almodovar,I.J.Chem.Phys.1966,44,1648.
(9) Férey,G.Chem.Soc.Rev.2008,37,191.
(10) Farha,O.K.;Hupp,J.T.Acc.Chem.Res.2010,43,1166.
(11)Li,J.R.;Timmons,D.J.;Zhou,H.C.J.Am.Chem.Soc.2009,131,6368.
(12)Yu,Q.;Zeng,Y.F.;Zhao,J.P.;Yang,Q.;Bu,X.H.Cryst.Growth Des.2010,10,1878.
(13)Liu,Y.L.;Kravtsov,V.C.;Eddaoudi,M.Angew.Chem.2008,120,8574.
(14)Walton,K.S.;Millward,A.R.;Dubbeldam,D.;Frost,H.;Low,J.J.;Yaghi,O.M.;Sunrr,R.Q.J.Am.Chem.Soc.2008,130,406.
(15)Yang,Q.Y.;Liu,D.H.;Zhong,C.L.J.Chem.Ind.Eng.(China)2009,60,805.[阳庆元,刘大欢,仲崇立,化工学报,2009,60,805.]
(16)Yang,Q.Y.;Zhong,C.L.;Chen,J.F.J.Phys.Chem.C 2008,112,1562.
(17)Accelrys,Inc.Materials Studio,3.0 V;Accelrys,Inc.:San Diego,CA2003.
(18) Potoff,J.J.;Siepmann,J.I.AIChE J.2001,47,1676.
(19)Yang,Q.Y.;Zhong,C.L.Langmuir 2009,25,2302.
(20)Mayo,S.L.;Olafson,B.D.;Goddard,W.A.,III.J.Phys.Chem.1990,94,8897.
(21)Yang,Q.Y.;Zhong,C.L.J.Phys.Chem.B 2005,109,11862.
(22)Yang,Q.Y.;Zhong,C.L.J.Phys.Chem.B 2006,110,655.
(23) Liu,D.H.;Zheng,C.C.;Yang,Q.Y.;Zhong,C.L.J.Phys.Chem.C 2009,113,5004.
(24)Yang,Q.Y.;Zhong,C.L.ChemPhysChem 2006,7,1417.
(25) Li,J.R.;Kuppler,R.J.;Zhou,H.C.Chem.Soc.Rev.2009,38,1477.
(26)Xu,Q.;Liu,D.H.;Yang,Q.Y.;Zhong,C.L.;Mi,J.G.J.Mater.Chem.2010,20,706.
Stepped Behavior of Carbon Dioxide Adsorption in Metal-Organic Frameworks
AN Xiao-Hui LIU Da-Huan*ZHONG Chong-Li
(Laboratory of Computational Chemistry,School of Chemical Engineering,Beijing University of Chemical Technology,Beijing 100029,P.R.China)
O641;O647
Received:September 15,2010;Revised:November 22,2010;Published on Web:February 15,2011.
∗Corresponding author.Email:liudh@mail.buct.edu.cn;Tel:+86-10-64431705.
The project was supported by the National Outstanding Young Scientists Foundation of China(20725622)and National Natural Science Foundation of China(20876006,20821004,20906002).
国家杰出青年科学基金(20725622)和国家自然科学基金(20876006,20821004,20906002)资助项目

