非共价修饰碳纳米管/二氧化钛复合材料的合成及性能
王环颖 李文军 常志东 郭会超
(北京科技大学化学与生物工程学院化学系,北京 100083)
非共价修饰碳纳米管/二氧化钛复合材料的合成及性能
王环颖 李文军*常志东 郭会超
(北京科技大学化学与生物工程学院化学系,北京 100083)
采用溶胶-凝胶法在聚乙烯吡咯烷酮(PVP)非共价修饰的碳纳米管表面均匀沉积二氧化钛粒子制得纳米复合材料。用TEM、XRD、FTIR、N2吸脱附等对复合材料进行了表征。结果表明:纳米二氧化钛纳米粒子均匀沉积在被修饰碳纳米管表面,且二氧化钛为纯锐钛矿晶体结构,没有金红石和板钛矿相。非共价修饰碳纳米管/二氧化钛复合材料具有良好的介孔结构,其孔径分布主要集中在6~10 nm,且比表面积与纯的二氧化钛相比明显增大,在紫外光照射下降解亚甲基蓝,相比纯的二氧化钛和碳纳米管/二氧化钛,具有较高的催化活性。
非共价修饰;碳纳米管;二氧化钛;聚乙烯吡咯烷酮
纳米复合材料是一种新型的复合结构,它不仅仅具有纳米粒子各自的特性,而且能够产生新的性能。与块体材料相比,纳米复合材料有它们独特的光、电、磁和催化等方面的性能[1-2]。碳纳米管(CNTs)是纳米材料研究的重点,由于它特殊的比表面积和空隙结构,表面的键态和电子态与颗粒内部不同,表面原子配位不全导致表面的活性位置增加,使碳纳米管有独特的电学、热学和力学性能,且拥有纳米级管腔结构、较高的比表面积和表面活性[3]。以碳纳米管作为TiO2的载体具有提高反应速率、降低反应温度、选择优良的反应路径等作用[4-5]。
近年来,以碳纳米管为载体制备的纳米复合材料因在电子、化工、环境等方面广泛应用而受到关注[6-7]。碳纳米管/二氧化钛(CNTs/TiO2)纳米复合材料能够显示明显的协同效应[8-9]。人们已将CNTs/TiO2复合材料应用于染料敏化太阳能电池[10]以及各种传感器[11]、有机污染物分解[12-13]等,由于TiO2团聚颗粒大量吸附在碳纳米管的内外壁上,而碳纳米管的导电结构又抑制了催化产生的电子-空穴对的复合,因此提高了TiO2催化活性。另外,碳纳米管具有较高的比表面积,不同层次的孔径结构,其内孔和外壁均可用来吸附溶液中的氧和有机物,提供了一个可以增强有机物催化降解效率的新途径。
由于碳纳米管的疏水性和长/径比大引起的缠绕和高比面积引起的高表面能,通常制备CNTs/TiO2复合材料有明显的异质性。二氧化钛纳米粒子没有均匀覆盖碳纳米管表面,相反二氧化钛纳米粒子聚合在一起形成团聚,并且这些粒子群只是附在碳纳米管上的部分表面[14-16]。这样的碳纳米管/二氧化钛涂层结构存在很多缺陷:(1)二氧化钛纳米粒子聚集在一起可能会改变他们的量子属性。(2)大部分这种团聚的二氧化钛米粒子没有真正的与碳纳米管发生耦合反应,这种复合材料的性质只是二氧化钛粒子和碳纳米管的简单复合。通过对碳纳米管非共价修饰可以更好解决这个问题[17-18]。
本工作采用溶胶-凝胶法制备二氧化钛纳米粒子均匀负载在PVP修饰碳纳米表面的纳米复合材料。非共价修饰碳纳米管与二氧化钛质量分数分别为5%,10%,20%。以透射电子显微镜、X射线衍射仪,UV-Vis漫反射光谱等技术,对复合材料进行结构表征,利用其对碱性染料亚甲基蓝的降解,评价复合材料的催化活性,并探讨了复合材料的复合机理。
1 实验部分
1.1 实验原料
钛酸四丁酯(C16H36O4Ti,A.R.);异丙醇((CH3)2CHOH,A.R.);硝酸(HNO3,A.R.);亚甲基蓝(C16H18CIN3S·3H2O,A.R.); 二 茂 铁((C5H5)2Fe,A.R.); 二 甲 苯(C8H10,A.R.);聚乙烯吡咯烷酮k30(PVP),均为北京化工厂提供。
1.2 实验过程
1.2.1 碳纳米管制备
制备:化学气相沉积法,以二甲苯为碳源,二茂铁作为催化剂,将二茂铁溶解在二甲苯中,超声振荡10 min形成均匀的红褐色透明溶液。石英片放入石英管中恒温区。升温过程通入N2(200 mL·min-1)作为保护气。达到设定温度800℃后,通过医用注射器把前驱液滴入石英管入口处,保持前驱液的下滴速度为 10 drop·min-1左右。同时开通 H2(400 mL·min-1)作为还原性气体,调大 N2流量(1000 mL·min-1),带动前驱液均匀流向石英管中部位置。反应40 min后,停止前驱液的供给,关闭H2,在N2的保护下降至室温。
1.2.2 非共价修饰碳纳米管(ncCNTs)
取1.0 g碳纳米管粗品于三颈圆底烧瓶中,加入100 mL浓硝酸,于120℃回流1 h,冷却、过滤、用5%NaOH溶液洗涤,再用二次蒸馏水反复洗涤碳纳米管直至洗液pH值为7.0,洗净的碳纳米管在80℃干燥8 h,备用。这种方法不仅起到了纯化的作用,还会对碳纳米管的末端及侧壁进行功能化。将一定量纯化后的碳纳米管与12 mg·L-1PVP溶液混合,利用超声分散过夜,采用0.2 μm多孔过滤膜过滤,用乙醇溶液多次清洗后干燥。
1.2.3 非共价修饰碳纳米管/二氧化钛(ncCNTs/TiO2)复合材料制备
经非共价修饰的碳纳米管在10%异丙醇水溶液中超声分散15 min,滴入浓硝酸溶液调节pH=2,作为溶液(a),取一定量的钛酸四丁酯(非共价修饰后碳纳米管与二氧化钛的质量百分数分别为5%、10%、20%)溶于纯的异丙醇溶液中搅拌60 min作为溶液(b)。在室温下将溶液(a)慢慢滴入溶液(b)中强烈搅拌1后完成水解反应。过滤并用乙醇和水洗涤3次,100℃烘干1.5 h,样品在500℃烧结30 min。 样品分别标记为CT5,CT10,CT20,对应的是表面修饰后碳纳米管与二氧化钛的质量百分数分别为5%、10%、20%。
1.3 样品表征
用日本电子公司JEM1011型透射电子显微镜(TEM))观察样品的微观形貌(10 kV加速电压);粉体的物相结构采用日本岛津公司D/MAX-RB型全自动X射线粉末衍射仪(XRD)鉴定,采用铜靶Cu Kα(λ=0.154 18 nm)靶电压 40 kV,靶电流 40 mA,石墨单色器滤波,闪烁计数器记录X-射线强度,扫描范围 2θ=10°~100°;用北京谱析通用 TU-1901 型紫外-可见漫反射光谱分光光度计(UV-Vis)测量样品的光吸收性,波长扫描范围300~700 nm,狭缝宽度1 nm;复合材料比表面积和孔容通过液氮温度下N2吸附法测定,用Buider SSA-4200孔径及比表面积分析仪(北京彼奥德电子技术有限公司);傅里叶变换红外光谱(FTIR)测定用Nexus670红外光谱仪(美国Nicolet公司)采用KBr压片法。
1.4 催化降解实验
亚甲基蓝是常见的碱性染料,系典型污染物代表。光催化实验在不锈钢容器中进行,以亚甲基蓝水溶液(浓度为50 mg·L-1)为测试溶液,24 W的紫外灯(照射波长λ=287 nm)为光源,用循环水冷却体系,以保持系统的恒定温度。将100.0 mg材料样品放入200 mL的亚甲基蓝水溶液中,避光条件下超声波振荡10 min,液面与紫外灯距离10 cm,每隔30 min取样1次,离心分离,取上部清液,用UV-Vis分光光度计检测亚甲基蓝的吸光度(检测波长610 nm)。根据光照前后溶液吸光度的变化,计算亚甲基蓝的降解率,并以此评价复合材料的光催化活性,计算公式为:

其中,C为亚甲基蓝降解率,C0为光照前亚甲基蓝溶液的浓度,Ct为光照时间t时亚甲基蓝溶液的浓度。
2 结果与讨论
2.1 非共价修饰碳纳米管/二氧化钛(ncCNTs/TiO2)复合材料表征
2.1.1 ncCNTs/TiO2复合材料透射电镜图
图(a~c)是CNTs/TiO2复合材料TEM图。图像揭示了碳纳米管表面有二氧化钛涂层的复合微观结构。确认了二氧化钛和碳纳米管之间的接触。二氧化钛纳米粒子团聚成群,随机聚集在碳纳米管局部,甚至部分碳纳米管表面没有负载。二氧化钛纳米粒子的聚集说明碳纳米管是起到生长和沉淀中心的作用。
图(d~h)是ncCNTs/TiO2复合材料的TEM图像。我们可以观察到二氧化钛和碳纳米管之间的紧密接触。碳纳米管经修饰后呈单根分散,二氧化钛粒子均匀分散负载在经PVP非共价修饰碳纳米管表面,呈球形、粒径均匀、直径约10 nm。图(d~f)所示是非共价修饰的碳纳米管与二氧化钛的质量百分数为20%,图(g~h)所示是非共价修饰的碳纳米管与二氧化钛的质量百分数为5%。随着二氧化钛溶胶浓度的增加,在碳纳米管表面沉积的纳米粒子也随之增加。图(h)所示几乎所有的碳纳米管的表面都被二氧化钛粒子包覆,均匀负载在PVP修饰的碳纳米管表面。从图(f)电子衍射图上可以清晰地看到衍射斑和衍射环, 计算出的晶面间距如下:0.352(101),0.237(004),0.187(200)nm。从计算的晶面间距可以推测显示样品高温烧结已具有锐钛矿型晶体结构。
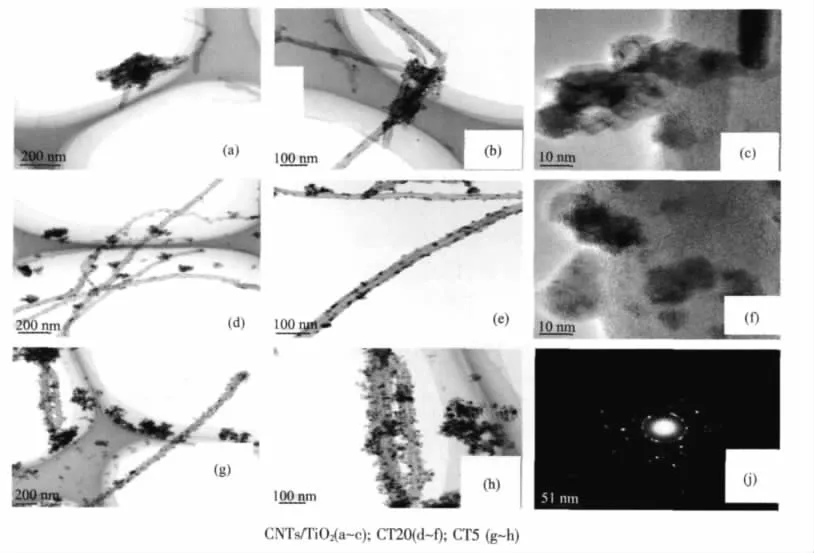
图1 CNTs/TiO2和ncCNTs/TiO2复合材材料透射电镜图Fig.1 TEM images of CNTs/TiO2and ncCNTs/TiO2composites
2.1.2 ncCNTs/TiO2复合材料的 XRD 图
X射线衍射考察了修饰后碳纳米管因含量不同对样品结晶化的影响。各种复合催化剂经煅烧,从图2可知样品CT5,CT10,CT20皆形成二氧化钛纯锐钛矿晶体,没有金红石和板钛矿相结构。在复合材料的光谱范围内没有非共价碳纳米管的特征峰,这可能是因为非共价修饰碳纳米管(002)和TiO2锐钛矿相(001)主峰位置接近,二者之间的质量百分数有比较大差异有关。观察所有复合材料可知,CT20质量分数为20%样品,当非共价修饰碳纳米管在复合材料中比例增大时,出现峰宽化现象,这意味着在二氧化钛和非共价碳纳米管之间应该有紧密的界面结构,可能形成异质结。异质结结构出现会提高电子迁移率,避免氧化钛电子-空穴复合,提高催化活性。结合复合材料的样品CT5,CT20的TEM图,表明二氧化钛连续沉积在PVP修饰的碳纳米管表面。

图2 TiO2,ncCNTs,ncCNTs/TiO2复合材料XRD图Fig.2 XRD patterns of TiO2,ncCNTs and ncCNTs/TiO2composites
2.1.3 ncCNTs/TiO2复合材料 N2吸附-脱附曲线
图3a,3b给出了各样品的N2吸附-脱附等温曲线。从图中可以看出样品均是典型的LangmuirⅣ型吸附-脱附等温线和滞后环,这是典型的介孔材料的特征吸附类型。二氧化钛和非共价修饰碳纳米管之间根据滞后环的位置形状,仍然可以清楚看到区别。非共价碳纳米管的H1循环是毛细管凝结,通常存在相对较高的孔径和均匀的简单孔隙网络。相反二氧化钛H3的循环是普遍存在于颗粒松散组合孔。图3(b)在ncCNTs/TiO2复合材料有H1和H3重叠。这种等温线可以说明有大腔的物质存在(非共价碳纳米管)。说明在管之间形成了均匀的没有填充的孔。这又意味着,管状结构与二氧化钛涂层之间表面接枝,这与透射电子显微镜图像一致。
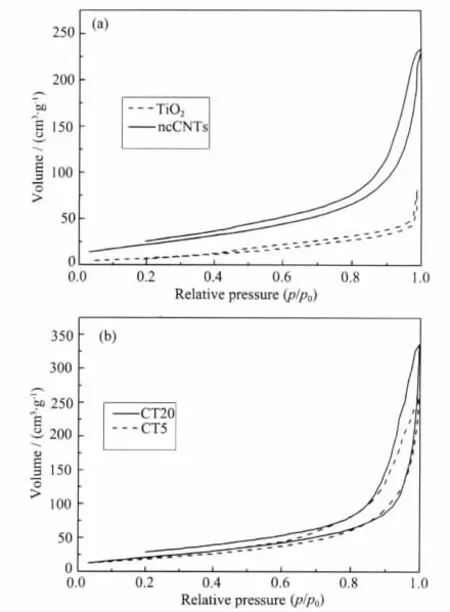
图3 TiO2,ncCNTs,ncCNTs/TiO2复合材料的 N2吸附-脱附曲线Fig.3 N2adsorption-desorption isotherms of TiO2,ncCNTs,ncCNTs/TiO2composites
ncCNTs/TiO2复合材料的孔径分布由表1可知,样品CT5,CT10,CT20的孔径分布较窄,分布主要集中在6~8 nm左右,说明其具有规整的一维孔道结构。随着非共价碳纳米管在复合材料中含量增加,表面积和孔数量逐渐增加。非共价修饰碳纳米管有大的比表面积160 m2·g-1,其孔径分布较广,它的存在导致了复合材料表面积增加。相较于PVP修饰碳纳米管,复合材料显示孔隙率明显减少,孔隙率下降可以归因于两个方面:(一)二氧化钛纳米粒子在PVP修饰碳纳米管内发生堵塞;(二)二氧化钛的比例增加,从而减少了PVP修饰碳纳米管可用为N2的吸附的表面积和孔隙度。
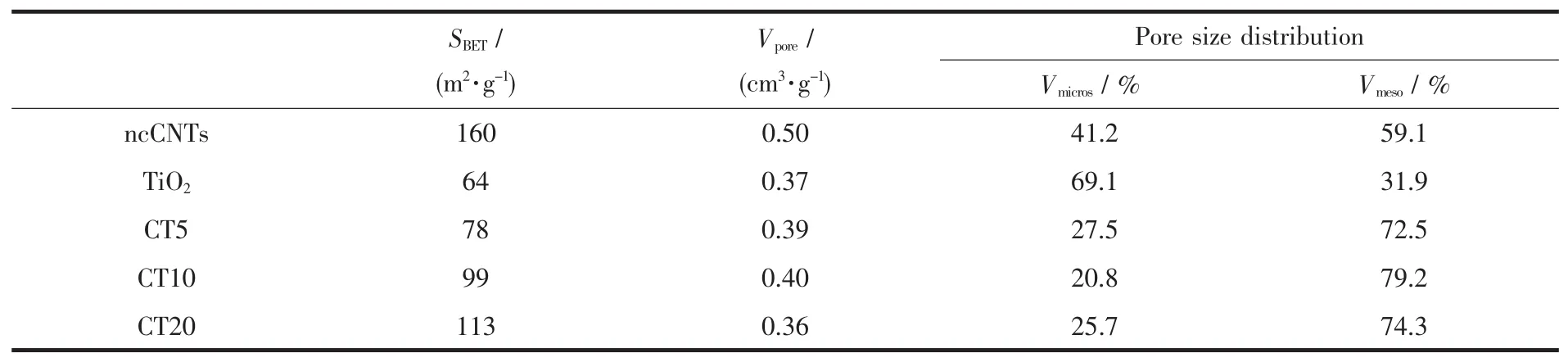
表1 ncCNTs,TiO2及ncCNTs/TiO2复合材料的表面性质Table 1 Surface properties of ncCNTs,TiO2and ncCNTs/TiO2
2.1.4 ncCNTs/TiO2复合材料紫外-可见漫反射吸收光谱图
图4为ncCNTs/TiO2复合材料的紫外-可见吸收光谱图样品的紫外-可见吸收光谱图。可见,样品在400 nm以下均有连续宽化的吸收带,其中在330 nm附近的吸收峰为六配位的锐钛矿相TiO2的特征峰。纯的二氧化钛的吸收范围在400 nm以内,而复合材料的吸收光谱范围进入可见光部分,CT10的红移现象非常明显。这主要是因为碳纳米管具有半导体性质,碳纳米管可以转移吸收光致电子,注入二氧化钛粒子的导带。ncCNTs/TiO2纳米复合材料费米能级的明显降低,可以更有利于吸收长波光,提高催化活性[19]。ncCNTs/TiO2质量比高20%时,可见光拓展范围反而降低,主要是因为时碳纳米管含量过高时也会降低复合材料对光的吸收。

图4 TiO2,ncCNTs/TiO2复合材料的UV-Vis吸收光谱Fig4 UV-Vis absorption spectrum of TiO2,ncCNTs/TiO2
2.2 非共价修饰碳纳米管/二氧化钛(ncCNTs/TiO2)复合材料的光催化活性
ncCNTs/TiO2复合材料催化活性高于未非共价修饰CNTs/TiO2的复合材料。CNTs/TiO2复合材料,二氧化钛粒子随机聚集在碳纳米管表面,二氧化钛不足以覆盖碳纳米管,光子通过裸露的碳纳米管吸收和散射,降低催化效率。非共价修饰ncCNTs/TiO2复合材料的催化活性,可大幅度提高10%~38%,主要因为(一)PVP修饰碳纳米管表面二氧化钛粒子均匀分布。碳纳米管的表面裸露的减少,避免光子因碳纳米管的吸收和散射造成的损失。非共价修饰碳纳米管和二氧化钛的紧密接触意味着二者在界面之间存在更强的相互作用,并可能形成了异质结,提高电子的迁移率,减少电子-空穴对复合,提高催化活性;(二)考虑到碳纳米管半导体性质,碳纳米管可以转移吸收光致电子,注入二氧化钛粒子的导带。ncCNTs/TiO2纳米复合材料费米能级的明显降低,可以更有利于吸收长波光,提高催化活性[20]。随着二氧化钛比例提高,非共价修饰ncCNTs/TiO2催化活性提高,但碳纳米管与二氧化钛质量比低于5%时催化活性降低。 主要由于非共价修饰碳纳米管含量在复合材料中降低时,复合材料比表面积减小。ncCNTs/TiO2降解亚甲基蓝最佳质量比是 5~20。ncCNTs/TiO2质量比高于20时,催化活性反而很低,主要是因为二氧化钛质量分数的减小,同时碳纳米管含量过高时也会降低复合催化剂对光的吸收。
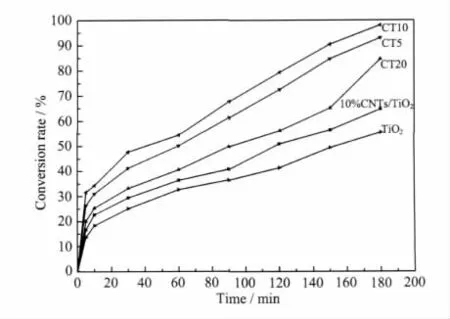
图5 不同复合材料对亚甲基蓝的光催化降解曲线Fig.5 Degradation curves of methylene blue for composite photocatalysts
2.3 非共价修饰碳纳米管/二氧化钛(ncCNTs/TiO2)复合材料的复合机理
图6a非共价修饰前后CNTs的傅里叶变换红外谱图。可以看出改性前的CNTs没有明显的振动吸收峰,经PVP非共价修饰的CNTs(ncCNTs)出现明显的PVP振动峰。2931 cm-1是亚甲基的对称伸缩振动吸收峰。1709 cm-1是吡咯烷酮环上的羰基伸缩振动吸收峰,1457 cm-1是亚甲基剪式弯曲振动吸收峰。1248 cm-1是C-N伸缩振动吸收峰。因此PVP被成功引进CNTs表面。对比纯的PVP的红外吸收谱图发现,非共价修饰碳纳米管有些峰位发生了位移1671 cm-1(C=O)发生了红移至1709,1280 cm-1(C-N)发生了蓝移至1248 cm-1。表明由于CNTs离域大π键存在,影响聚乙烯吡咯烷酮电子发生转移。这也进一步证实CNTs与PVP之间发生了相互作用。PVP是两亲性聚合物具有特殊的结构,既有亲水基团,而又具有亲油基团,因此其能溶于水和许多有机溶剂中,利用两亲聚合物修饰CNTs,其良好的溶解性能会明显改善CNTs在水、有机溶剂和聚合物中的分散性能[19]。PVP枝接到CNTs表面的基团可以改善CNTs的分散性和亲水性。

图6 (a)PVP,CNTs,ncCNTs及(b)PVP,PVP-TiO2,ncCNTs/TiO2红外谱图Fig.6 FTIR of(a)PVP,CNTs,ncCNTs and(b)PVP,PVP-TiO2,ncCNTs/TiO2
图6b谱图中1 286 cm左右处均有一明显的吸收峰,这是PVP中C-N的特征吸收峰,说明Ti02-PVP和ncCNTS/TiO2纳米复合材料中C-N键与PVP中C-N没有明显不同。在纯的PVP谱图中1671 cm-1是羰基的伸缩振动峰,在PVP-TiO2红外谱图中该峰移至1 637 cm-1说明在PVP的羰基与TiO2间通过Ti-O键有缔合作用见图7。此外PVP与其他金属离子间的相互作用也有报[20-21]。同样在ncCNTs/TiO2谱图中可以看到羰基的伸缩振动峰由1671移至1 627 cm-1,说明ncCNTS/TiO2同样存在PVP与TiO2缔和作用,如图8所示。Ti02-PVP和ncCNTS/TiO2纳米复合材料红外谱图中均在400~600 cm-1处有一强宽吸收带,这是由[TiO6]八面配位体振动产生的,是Ti02的特征振动峰。

图7 PVP与TiO2间的价键作用示意图Fig.7 Schematics of the coordination mode between PVP and TiO2

图8 ncCNTs/TiO2复合材料制备示意图Fig.8 Schematics for synthesis of ncCNTs/TiO2composite
PVP在制备ncCNTs/TiO2复合材料的过程中主要有两大作用:一是通过与碳纳米管的非共价的交联作用在水中分散并且增溶多壁碳纳米管,二是PVP为两亲聚合物,具有特殊结构。它的侧链是亲水性的,能较稳定地吸附二氧化钛纳米颗粒。分子主链是憎水性的,可以提高氧化钛颗粒间排斥力的ζ电位,还可以形成空间位阻效应,由于空间位阻效应会减少不同分子间反应基团的相互接触机会,使钛酸四丁酯水解反应速率降低[22],控制了二氧化钛粒子的颗粒形成及分散性,促使二氧化钛均匀沉积在碳纳米管表面。复合机理示意图见图8。碳纳米管的表面功能团是有利改善碳纳米管和二氧化钛之间的界面结合。因此,碳纳米管的表面状态是有利于纳米二氧化钛颗粒的可控沉积关键。
3 结 论
通过将PVP成功引入碳纳米管表面,PVP起到桥接作用,二氧化钛粒子均匀沉积在碳纳米管表面,制备碳纳米管/半导体涂层复合材料。未修饰碳纳米管,二氧化钛粒子是随机聚集在其表面局部,甚至部分碳纳米管表面没有负载。PVP修饰的碳纳米管表面二氧化钛粒子均匀分布,碳纳米管的表面裸露减少,避免光子因碳纳米管的吸收和散射造成的损失。非共价修饰碳纳米管和二氧化钛的紧密接触意味着二者在界面之间存在更强的相互作用,并可能形成了异质结,提高电子的迁移率,减少电子-空穴对复合。
[1]SHEN Lai-Fa(申来法),ZHANG Xiao-Gang(张校刚),YUAN Chang-Zhou(原长洲),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2009,25(9):1214-1219
[2]WU Xiao-Li(吴小莉),YUE Tao(岳涛),LU Rong-Rong(陆 荣 荣 ),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2005,10(10):1505-1508
[3]LIU Ji-Ping(刘 吉 平 ),SUN Hong-Qiang(孙 洪 强).Carbon Nano-material(碳 纳 米 材 料).Beijing:Science Press,2004:10
[4]Luo Y,Liu J,Xia X,et al.Mater.Lett.,2007,61:2467-2472
[5]Coleman J N,Curran S,Dalton A B,et al.Phys.Rev.B,1998,58(12):7492-7495
[6]PENG Feng(彭峰),JIANG Jing-Wen(姜靖雯),WANG Hong-Juan(王红娟),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2004,20(2):231~235
[7]Luo Y,Liu J,Xia X,et al.Mater.Lett.,2007,61:2467-2472
[8]An G M,Ma W H,Sun Z Y,et al.Carbon,2007(45):1795-1801
[9]Huang H,Zhang W K,Gan X P,et al.Mater.Lett.,2007(61):296-299
[10]Ueda T K,Takahashi F,Mitsugi T.Diamond&Related Materials,2009,18:493-496
[11]Jitianu A,Cacciaguerra T,Benoit R,et al.Carbon,2004,42:1147-1151
[12]Yen C Y,Lin Y F,Hung C H,et al.Nanotechnology,2008,19:045604-045611
[13]Wang W,Serp P,Kalck P,et al.Mater.Res.Bull.,2008,43:958-967
[14]Sun J,Gao L,Iwasa M.Chem.Comm.,2004,7:832-833
[15]Jitianu A,Cacciaguerra T,Berger M H,et al.J.Non-Cryst Solids,2004,345-346:596-600
[16]Wang S,Ji L J,Wu B,et al.Appl.Surf.Sci.,2008,255:3263-3266
[17]Gao B,Peng C,George Z,et al.Appl.Catal.B:Environ.,2008,85:17-23
[18]O′Connell M J,Boul P,Ericson L M,et al.Chem.Phys.Lett.,2001,342:265-271
[19]Wang W D,Serp P,Kalck P,et al.J.Mol.Catal.A:Chem.,2005,235:194-199
[20]Vladimir V,Didenko,Valerie C,et al.Nano Lett.,2005,1(5):81563-81567
[21]Du D B,Song H W,Olusegun J.Mate.Sci.Eng.C,2007,27:414-420
[22]HUMei-Long(扈玫珑),BEIChen-Guang(白晨光),XU Sheng-Ming(徐 盛 明),et al.Acta Phys.-Chim.Sin.(Wuli Huaxue Xuebao),2008,24(12):2287-2292
Synthesis and Properties of Non-covalently Modified Carbon Nanotubes/Titanium Dioxide Composites
WANG Huan-YingLI Wen-Jun*CHANG Zhi-Dong GUO Hui-Chao
(School of Chemistry and Biological Engineering,University of Science and Technology Beijing,Beijing 100083,China)
Carbon nanotubes/titanium dioxide(CNTs/TiO2)composite photocatalyst was prepared by a modified solgel method.The nanoscaled TiO2particles were uniformly deposited on the CNTs modified with poly(vinyl pyrrolidone)(PVP).The composites were characterized by HTEM,XRD,FTIR and low temperature N2adsorptiondesorption.The results show that the CNTs are covered with PVP in core-shell structure and the nanoscaled TiO2particles are uniformly deposited on the surface of CNTs.The diameter of pores mainly ranges from 6~10 nm,and the surface area increases obviously.The results of photodegradation of methylene blue (MB)show that the photocatalytic activities of non-covalently modified CNTs/TiO2composites are improved.
non-covalently modification;CNTs;TiO2;poly(vinyl pyrrolidone)
O613.71;O614.41+1;TB333
:A
:1001-4861(2011)02-0269-07
2010-08-24。收修改稿日期:2010-09-28。
国家自然科学基金(No.20876157);国家重大基础研究发展规划973计划(No.2007CB714305)国家重点科技项目(No.2008ZX7207-0035)资助。
*通讯联系人。 E-mail:wjli@sas.ustb.edu.cn,wanghy127@yahoo.com.cn

