环境激素双酚A与蛋白质相互作用的电化学研究
王 辰,付艳丽,王 振,高云涛
(云南民族大学化学与生物技术学院民族药资源化学国家民委-教育部重点实验室,云南昆明650031)
环境激素双酚A与蛋白质相互作用的电化学研究
王 辰,付艳丽,王 振,高云涛
(云南民族大学化学与生物技术学院民族药资源化学国家民委-教育部重点实验室,云南昆明650031)
采用电化学法研究环境激素双酚A与牛血清蛋白的相互作用.实验表明牛血清蛋白存在使双酚A的氧化峰峰电流减小.双酚A在加入牛血清蛋白后参与反应的质子数和电子数都为2.牛血清蛋白与双酚A的结合数m=2,结合常数β=5.81×1010.由此推测双酚A进入牛血清蛋白的疏水空腔内,使游离双酚A浓度变小.
双酚A;牛血清蛋白;循环伏安法;相互作用
双酚A(BPA)是应用广泛的有机化工原料[1],其化学结构式如图1.具有较强的类雌激素的作用,干扰人类和动物的正常内分泌功能[2-3].近年来的研究表明,双酚A能改变遗传信息的某些基因,导致细胞的畸变,产生肿瘤[4],具有致癌、致畸、致突变的毒性[4].蛋白质是药物发挥药效的重要载体和靶分子,探讨BPA与蛋白质的相互作用对于在分子水平了解BPA的作用机制具有重要意义[5].本文利用多壁碳纳米管(MWNT)[6-7]修饰玻碳电极(MWNT/GCE)研究了BPA与牛血清蛋白相互的作用,对二者之间的作用机理进行研究,为深入了解BPA类环境激素的生物毒性提供进一步的实验依据.
1 实验部分
1.1 仪器与试剂
MEC-12B型多功能电化学分析系统(江苏江分电分析仪器有限公司).三电极系统:工作电极为修饰玻碳电极,参比电极为饱和甘汞电极(SCE),对电极为铂电极,超声波清洗器AS3120A.
双酚A(BPA,国药集团上海化学试剂有限公司)溶于乙醇配成2.0×10-3mol/L储备液;多壁碳纳米管(厦门大学提供);牛血清蛋白(BSA,北京元亨圣马生物技术研究所),用2次重蒸水配成1.0×10-4mol/L储备液,4℃冰箱保存;KH2PO4-Na2HPO4缓冲溶液.所用试剂均为分析纯,实验用水为2次重蒸水.
1.2 实验方法
1.2.1 MWNT/GCE的制备
将MWNT在浓HCl中超声72 h进行纯化,纯化后的MWNT加浓HNO3在140℃下回流8 h,用2次重蒸水洗至中性,在100℃烘干,研成粉末,经浓HNO3回流处理后的MWNT,在打开其端口的同时,引入羧基和羟基等官能团.
称取功能化的MWNT粉未10.0 mg,超声分散于10 mL 2次重蒸水中,形成黑色悬浊液备用.玻碳电极先用0.05 μm Al2O3抛光粉抛光成镜面,然后分别在无水乙醇和2次重蒸水中超声清洗5 min.用微量进样器取4 μL悬浊液滴加在玻碳电极表面,红外灯下烘干,即得MWNT/GCE.
1.2.2 循环伏安法(CV)分析
取一定量的BPA至10 mL比色管,加入KH2PO4-Na2HPO4缓冲溶液,稀释至刻度后,转移至电解池中.采用三电极体系,在0.2~0.8 V电位范围内,以0.10~0.40 V/s的扫描速度进行循环伏安扫描,记录伏安曲线.
2 结果与讨论
2.1 电极的选择
用玻碳电极和多壁碳纳米管电极分别进行循环伏安扫描,以0.15 V/s的扫速速度在0.2~0.8 V范围内循环伏安扫描发现:BPA在玻碳电极上无氧化还原峰信号;在多壁碳纳米管电极上有一灵敏的氧化峰.因此,采用多壁碳纳米管电极作为工作电极.
2.2 支持电解质的选择
分别在HAc-NaAc,B-R,KH2PO4-Na2HPO4缓冲体系中进行测试,均会出现相应的氧化还原峰,但峰电位、峰形、峰电流大小不同.结果表明BPA在KH2PO4-Na2HPO4缓冲体系中峰形好,灵敏度高,实验选用KH2PO4-Na2HPO4缓冲溶液为测定支持电解质.
2.3 缓冲溶液酸度的影响
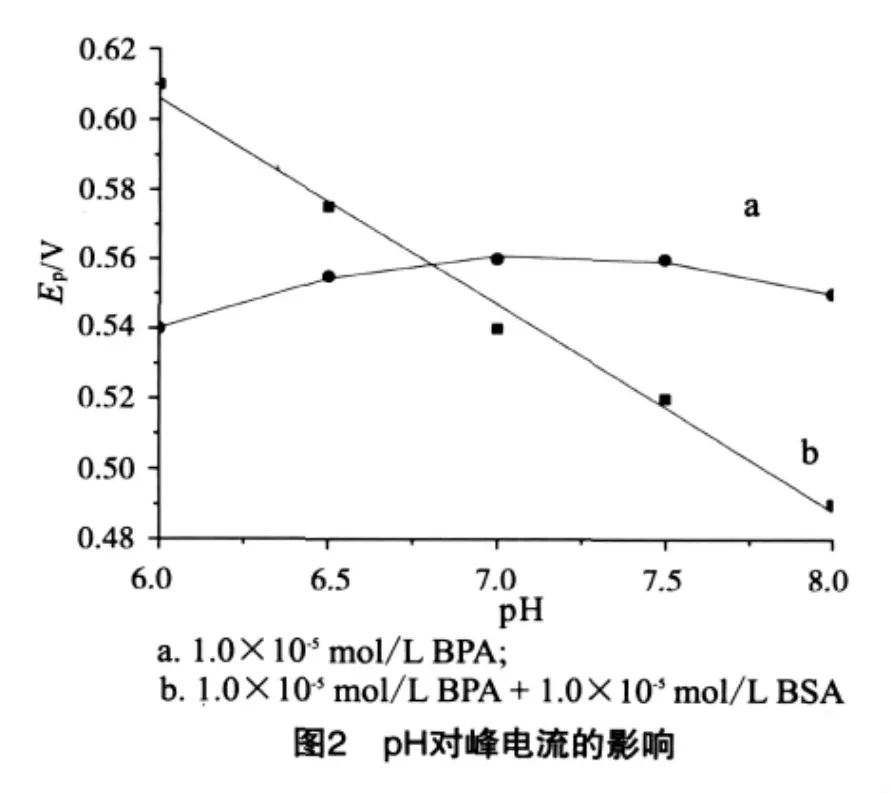
在KH2PO4-Na2HPO4缓冲溶液(pH 6.0~8.0),BPA+BSA体系在不同pH条件下,峰电位不变,而峰电流却有不同程度的降低.电位Ep与pH的关系结果见图2,线性回归方程 Ep(V)=0.96-0.059 pH,r=0.995 6 .
2.4 反应时间对峰电流的影响
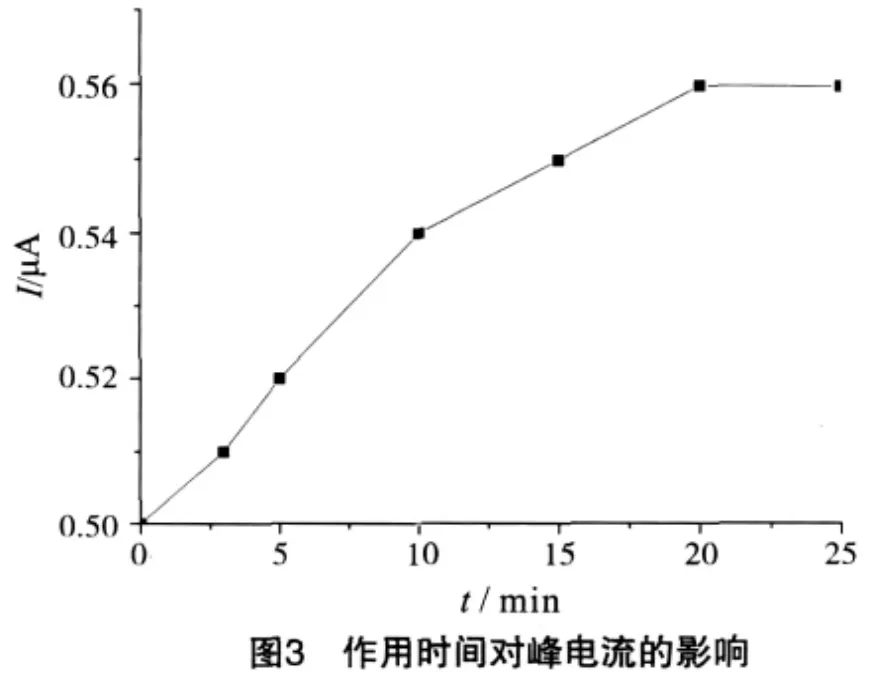
BPA与牛血清蛋白相互作用,随着二者反应时间的增加,峰电流有一定的增加(见图3).当相互作用20 min后,峰电流基本稳定.因此,选择BPA与牛血清蛋白相互作用时间20 min.
网络空间主权理念下,网络恐怖主义这一非传统领域的安全威胁构成对本国主权的侵犯,对国家安全产生严重影响,才能迫使国家积极主动对外寻求合作防范网络恐怖主义的袭击。同时各国在行使网络空间主权时应秉承互相尊重的理念,防止借网络反恐之名干涉别国内政。明确网络空间主权,也使得各国打击网络恐怖主义有了明确的分工,有助于建立和平安全有序的网络格局。我国政府对网络主权非常重视,在《国家安全法》和《网络安全法》中均确立了“网络空间主权”的概念,表达了我国捍卫网络空间主权、积极开展国际合作的态度和立场。
2.5 扫描速度的影响
2.5.1 扫速对峰电位的影响
对1.0×10-5mol/L BPA和1×10-5mol/L BSA同时存在的溶液进行测定,观察扫速对峰电位的影响.结果表明,当扫速在0.10~0.40 V/s范围内变化时,峰电位均随扫速的增加而增加,且峰电位Ep与扫速的自然对数值lnv之间存在着良好的线性关系,线性方程Ep=0.462+0.0196 lnv,r=0.995 2.
2.5.2 扫速对峰电流的影响
对1.5×10-5mol/L BPA和1×10-5mol/L BSA同时存在的溶液进行测定,考察扫速对二者作用完全峰电流的影响.结果表明,当扫速在0.10~0.40 V/s范围内变化时,峰电流均随扫速的增加而增加,与扫速的平方根成线性,线性方程为Ip=0.074 3+0.088 9 v1/2,r=0.991 6.说明此条件下电极反应过程主要受扩散控制[7].
对于只有1.5×10-5mol/L BPA的体系,当扫速v在0.05~0.40 V/s之间,无论是峰电位Ep还是峰电流Ip都是与扫速的一次方成正比,氧化峰电流与扫速的关系式为Ip=23.27v+0.926,r=0.991,说明此时BPA在电极表面上的电极反应过程受吸附控制[7].
2.6 静止时间的影响
对1.0×10-5mol/L BPA和1×10-5mol/L BSA同时存在的溶液进行测定,静止时间基本对电流没有影响,本实验的静止时间选择10 s.
2.7 双酚A与BSA相互作用的电化学行为
图4中的曲线为BPA与BSA在MWNT/GCE的循环伏安谱(CV).由图4可知,BPA在0.10 mol/L,pH=7.0的KH2PO4-Na2HPO4缓冲液中,有一个氧化峰,其电化学行为具有典型的不可逆特征,氧化峰电位(Ep)为0.56 V,随着1×10-5mol/L BSA加入,峰电位基本不变,峰电流减小.

2.8 反应的电子数与质子数求算
参照文献[8]可知不可逆波峰电位方程式为:

式中α为转移系数,D为扩散系数,KS为电极反应速率常数,F为法拉第常数,n为电子转移数.

又根据扫速与峰电位的关系

由式(2)、(3)可以得到:

根据不可逆吸附体系峰电流Ip与吸附电量Q关系式:

可测得电极反应的电子数n,式中Q=nFAΓ,为循环伏安单一过程的峰面积(以电量计),F为法拉第常量,A为电极面积,Γ为吸附量,R为摩尔气体常量,T为热力学温度.由上可知,不必知道电极吸附量及电极面积的绝对值,只要测得某扫描速度下CV图上的面积Q即可求得n.
以不同浓度BPA测得的Ip、Q,由式(5)计算得:n=2,即在电极反应中有2个电子参与反应.又由(4)式得αn值为0.655,所以α =0.328.
又根据Nernst方程:

由上面n=2,计算得出转移的质子数m=2.03≈2,即参与反应的质子数为2.
2.9 BPA与BSA结合常数β和结合数m
对于BPA-BSA的复合物,可根据文献[9]算出两者之间的结合比和结合常数,假定BPA与BSA只形成一种简单的复合物BSA-mBPA,则结合反应如下:

式中β为结合常数.
氧化峰电流Ip与BPA浓度及ΔIp与BPA浓度的关系见图5.图中曲线a为没有加入BSA时BPA的氧化峰电流Ip随BPA浓度变化的关系曲线,曲线b为加入1.0×10-5mol/L BSA反应后,Ip随双酚A浓度变化的关系曲线,曲线c为曲线a和曲线b的氧化峰电流差值ΔIp(=Ip,a- Ip,b) 随 BPA 浓度变化的关系曲线.
经推导可得下式:

式中,ΔIp,max为加入BSA前后氧化峰电流差值的最大值.

[1]STAPLES A C,DORN B P,KKECKA M G,et al.A review of the environmental fate,effects,and exposures of bisphenol A[J].Chemosphere,1998,36(10):2 149 -2 173.
[2]KASHIWADA S,ISHIKAWA H,MIYAMOTO N,et al.Fish test for endocrine - disruption and estimation of water quality of Japanese rivers[J].Water Research,2002,36(8):2 161 -2 166.
[3]KIM K B,SEO K W,KIM Y J,et al.Estrogenic effects of phenolic compounds on glucose-6 -phosphate dehydrogenase in MCF-7 cells and uterine glutathione peroxidase in rats[J].Chemosphere,2003,50(9):1 167 -1 173.
[4]WANG P H.Environmental hormones and their harmful effects[J].North Environment,2005,30(2):33 -36.
[5]熊何键,马英,汪琳,等.紫外辐射诱导牡蛎细胞DNA损伤的单细胞凝胶电泳检测[J].云南民族大学学报:自然科学版,2010,19(6):400 -404.
[6]SUN Y Y,WU K B,HU S S.Voltammetric behaviors of diethylstilbestrol and its determination at multi- wall carbon nanotubes modified glassy carbon electrode[J].Acta Pharm Sinica,2003,38(5):364 -366.
[7]DONG S J,CHE G L,XIE Y W.Chemically Modified Electrodes[M].Beijing:Science Press,2003:54.
[8]BARD A J,FAULKNER L R.Electrochemistry methods:fundamentals and applications[M].NewYork:John Wiley&Sons,1980:222.
[9]LABIRON E.General expression of the linear potential sweep voltammogram in the case of diffusionlesselectrochemical systems[J].Journal of Electroanalyticak Chemistry,1979,101(1):19 -28.
(责任编辑王 琳)
Electrochemical Studies of the Interaction between Environmental Hormone Bisphenol A and Protein
WANG Chen,FU Yan-li,WANG Zhen,GAO Yun-tao
(Key Laboratory of Ethnic Medicine Resource Chemistry,State Ethnic Affairs Commission& Ministry of Education,School of Chemistry and Biotechnology,Yunnan University of Nationalities,Kunming 650031,China)
The interaction between environmental hormone bisphenol A and bovine serum albumins was investigated by the means of electrochemical method.The results indicated that the oxidation peak currents of bisphenol A decreased when bovine serum albumins was added.Both proton and electron of electrochemical oxidation of bisphenol A at the electrode were 2.The combining ratio of bisphenol A to bovine serum albumins was 2∶1,with the combining constants of 5.81 ×1010.The proposed interactions is that BPA enters the hydrophobic water cavity of bovine serum albumins,causing the decrease of the dissociative concentration.
bisphenol A;bovine serum albumins;cyclic voltammetry;interaction
O 657.13
A
1672-8513(2011)02-0092-04
10.3969/j.issn.1672 -8513.2011.02.004
2010-12-02.
云南省社会发展科技计划项目(2007B148M);民族药资源化学国家民委-教育部重点实验室开放基金(MJY090101).
王辰(1982-),女,硕士研究生.主要研究方向:分析化学.
高云涛(1962-),男,教授.主要研究方向:电分析化学.

