辅酶催化安息香缩合反应的实验探讨
李中华 白亦穷
(华中师范大学化学学院 湖北武汉430079)
芳香醛在乙醇-水溶液中发生双分子缩合,生成1,2-二苯基羟乙酮即安息香(benzoin)的反应称为安息香缩合反应。安息香缩合在化学工业和药物合成等方面有广泛的应用[1],如抗癫痫药物二苯基乙内酰脲以及二苯基乙二酮、二苯基乙二酮肟、乙酸安息香等制备都用到此反应。我院开设的中级有机化学实验,以苯甲醛为原料,经安息香缩合、氧化和重排多步反应制备二苯羟乙酸,其中安息香缩合是关键步骤。以前使用剧毒的氰化物为催化剂极为不便[2],近年改用辅酶(维生素B1)作催化剂[3-4],价廉易得,操作安全,效果良好,但实验中产率较低或有时得不到产品,影响后续实验的进行。我们经过多次试验探讨,在实验中采用四丁基溴化铵作为相转移催化剂,通过控制反应体系的pH和反应温度,安息香产率在70%以上,实验成功率亦大大提高。安息香缩合反应式为:

1 试剂与仪器
苯甲醛(CP)、维生素B1(CP)、四丁基溴化铵(AR)和NaOH(AR)均为国药集团化学试剂有限公司产品;95%乙醇(AR),天津市东丽天大化学试剂厂;XT4A型显微熔点测定仪,上海荆和分析仪器有限公司,温度未校正。
2 实验步骤
在100mL圆底烧瓶中加入1.7g(5mmol)维生素B1、0.2g四丁基溴化铵和4mL水,溶解后加入15mL 95%乙醇。将烧瓶置于冰水浴中冷却,同时取3mL 10% NaOH溶液于一试管中,也置于冰浴冷却,在冰浴中将NaOH液在5min内边摇动边逐滴加入反应烧瓶,然后加入10.6g(100mmol)新蒸苯甲醛,装上回流冷疑管于70~80℃水浴上加热90min,保持反应液pH=8~9,反应液呈橘黄色,经冷却后析出白色晶体,抽滤,用2×25mL冷水洗涤,干燥得产品7.6g(72%),熔点:132~134℃,用95%乙醇重结晶得白色针状结晶,熔点:134~136℃。
3 结果讨论
(1) 安息香缩合原指以氰化钠(钾)为催化剂的碳负离子对羰基的亲核加成反应,其反应机理见图1。
我们知道酶可以使有些反应更加巧妙、更加有效并且在更温和的条件下进行。维生素B1是一种辅酶,又称硫胺素或噻胺(thiamine),它常作为生物化学反应的催化剂,在生命过程中起重要作用,主要对α-酮酸脱羧和形成偶姻(α-羟基酮)等3种酶促反应发挥辅酶的作用。其结构见图2。
辅酶分子中噻唑环C2上的质子由于受氮和硫原子影响,具有酸性,在碱的作用下容易脱除质子,产生的碳负离子与芳醛的羰基加成,最终形成苯偶姻产物,反应机理见图3。

图1 氰离子催化安息香缩合反应机理

图2 辅酶的结构式
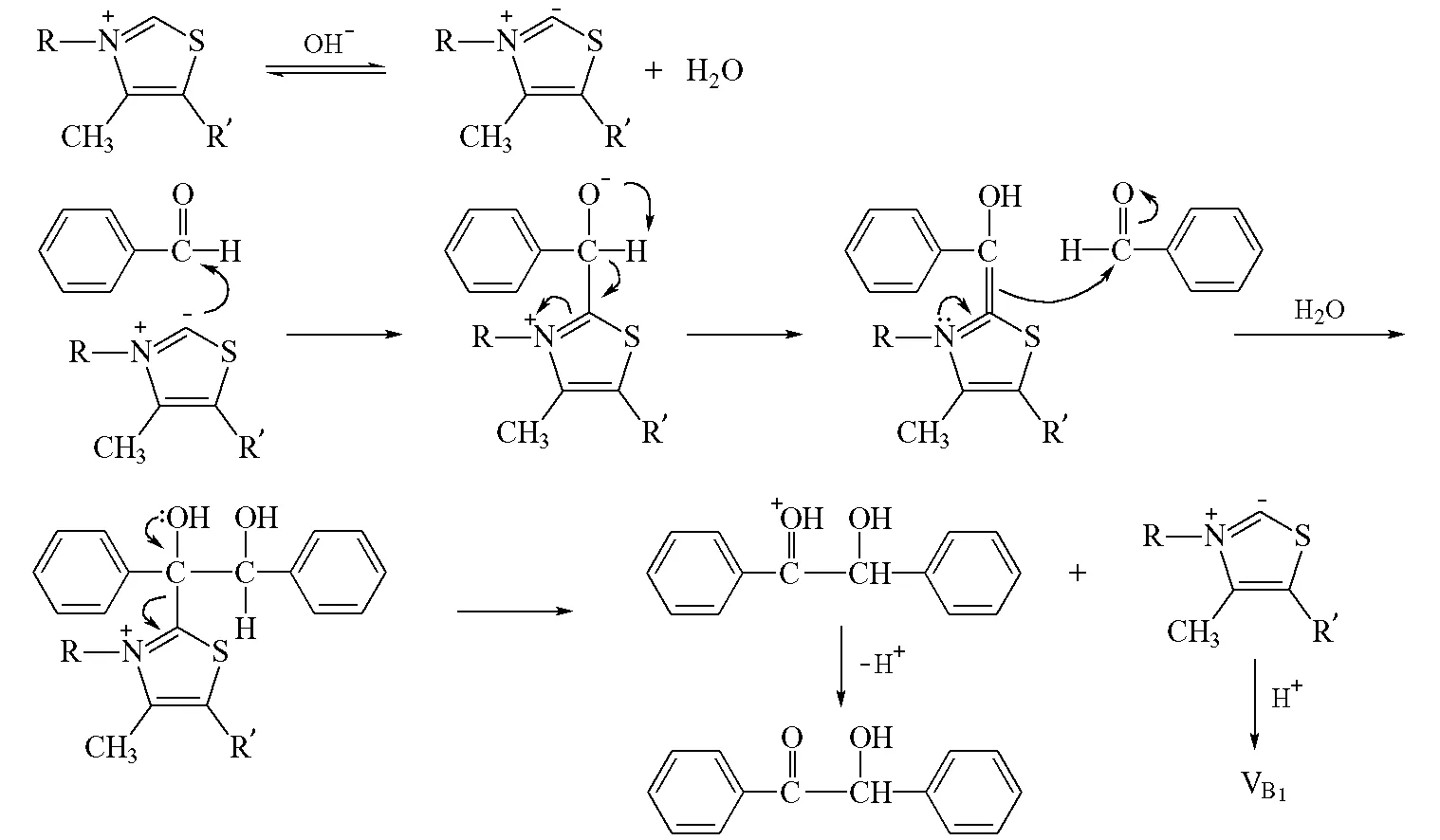
图3 辅酶催化安息香缩合反应机理
(2) 辅酶催化安息香缩合反应对pH的要求很高,否则产率较低甚至难得到产品。该反应在碱性条件下进行,pH在8~9为宜。由于维生素B1通常为盐酸盐,如果pH较低,不能形成碳负离子,则无法进行反应。随着反应进行,会导致pH发生变化,所以反应进行一段时间后应检查和调节pH,若pH过低需要适当补加碱液,但如果pH过高(大于10),维生素B1中噻唑环容易被破坏,或发生苯甲醛歧化等副反应,将难得到所需产品。
相转移催化剂通常可以大大加快油水两相反应的速度。本实验在水相产生的碳负离子容易水解,难以起到催化作用,加入相转移催化剂可将碳负离子从水相迅速转移至有机相苯甲醛中,避免与水的作用,从而促进缩合反应进行。安息香缩合是一个经典的有机化学反应,我们在苯甲醛、维生素B1和NaOH用量不变,反应温度为70~80℃条件下,考察了相转移催化剂对反应的影响(表1)。结果表明,四丁基溴化铵用量对反应产率有很大影响,不用时反应产率比较低,加入少量则反应速度和产率均有显著提高,其用量为0.2g时反应效果比较好。

表1 四丁基溴化铵(TBAB)对反应产率的影响
反应温度对实验也有影响,但没有pH的影响明显。实验中采取分段升温法有利于提高反应效率。首先将维生素B1和NaOH溶液在冰浴中冷却,加入苯甲醛之后,反应初期控制温度70~75℃,约1h后再提高至80℃反应30min。
(3) 产品为白色针状晶体,经测定其熔点为134~136℃,与文献值[5]吻合。实验中有时可能会出现白色油状物,即尚未结晶的安息香产品,放置一段时间后可形成结晶;若pH低于8,加入少量碱有利于晶体析出。
4 结论
在辅酶催化安息香缩合反应中,四丁基溴化铵作为相转移催化剂,可以有效地提高反应速度和产率。实验表明,当苯甲醛和维生素B1用量为100mmol和5mmol时,四丁基溴化铵用量为0.2g,控制反应体系的pH为8~9,反应温度70~80℃,安息香产率可达70%以上。
[1] 王汝龙,原正平.药物.第4版.北京:化学工业出版社,2005
[2] Walter I,Buck J.OrganicReaction,1948,4:269
[3] 张功成,沈永雯,李小龙.大学化学,2001,16(3):49
[4] 张国升,程俊,孙玉亮,等.安徽中医学院学报,2003,22(6):46
[5] 曾昭琼.有机化学实验.第3版.北京:高等教育出版社,1999

