HPLC法同时快速测定万古霉素和去甲万古霉素的血药浓度
崔艳丽,武 峰(1.北京市石景山医院药剂科,北京 100043;.首都医科大学附属北京同仁医院临床药理基地,北京 100730)
万古霉素、去甲万古霉素同属三环糖肽类抗生素,对革兰阳性细菌有强大的抗菌作用,尤其对目前临床较为棘手的严重耐药金黄色葡萄球菌和表皮葡萄球菌感染有较好疗效,且不易产生细菌耐药性,因而深受临床重视。由于万古霉素和去甲万古霉素具有耳、肾毒性,临床应用时常需进行血药浓度监测(TDM),特别是对于老年患者和肾功能不全者,需通过TDM来及时调整给药方案,以避免耳、肾功能损害。万古霉素、去甲万古霉素的血药浓度测定方法,已报道的有微生物法、荧光偏振免疫法和高效液相色谱法(HPLC)等。本研究拟通过建立适宜的HPLC-UV法,同时快速测定血清中万古霉素和去甲万古霉素浓度,以用于临床TDM及药代动力学研究。
1 材料与方法
1.1 药品与试剂
万古霉素对照品,含量:100%;去甲万古霉素对照品,含量:83.4%,均购自中国药品生物制品检定所。乙腈为色谱纯,其余试剂均为分析纯。
1.2 仪器
Hp1100型高效液相色谱仪,含 G1311A型四元泵、G1313A型自动进样器、G1314A型紫外检测器、Agilent色谱工作站,Agilent公司。
1.3 标准曲线制备
精密称取去甲万古霉素及万古霉素对照品,去离子水充分溶解得标准溶液,其中去甲万古霉素/万古霉素的浓度为400/460 μg·mL-1。取不同量的标准溶液,分别以空白人血清稀释至浓度为 80.7/92.0、40.4/46.0、20.2/23.0、8.1/9.2、4.0/4.6、2.0/2.3、0.8/0.9 μg·mL-1(去甲万古霉素/万古霉素)的血清标本。同时稀释得低、中、高3种浓度的质控血清标本,使其浓度分别为 57.7/65.7、14.1/16.1、3.0/3.5 μg·mL-1。
1.4 色谱条件
流动相:50 mM KH2PO4缓冲液∶乙腈 =90∶10(pH=2.5);色谱柱:Phenomenex C18柱(150 ×4.6 mm,5 μm);流速:1.0 mL·min-1;检测波长:236 nm;柱温:25 ℃。
1.5 样本处理方法
取待测样本 200 μL,加入 6% 高氯酸 180 μL,漩涡混合2 min,13 000 转/分离心 10 min;取上清液 300 μL,加入1.5 mm NaOH溶液 40 μL,漩涡混合 1 min,取上清液 20 μL 进样测定。
2 结果
2.1 专属性考察
在本实验条件下,万古霉素和去甲万古霉素分离度良好,无血清内源性杂质干扰。去甲万古霉素的保留时间约为6 min;万古霉素的保留时间约为8 min,血清色谱图见图1。
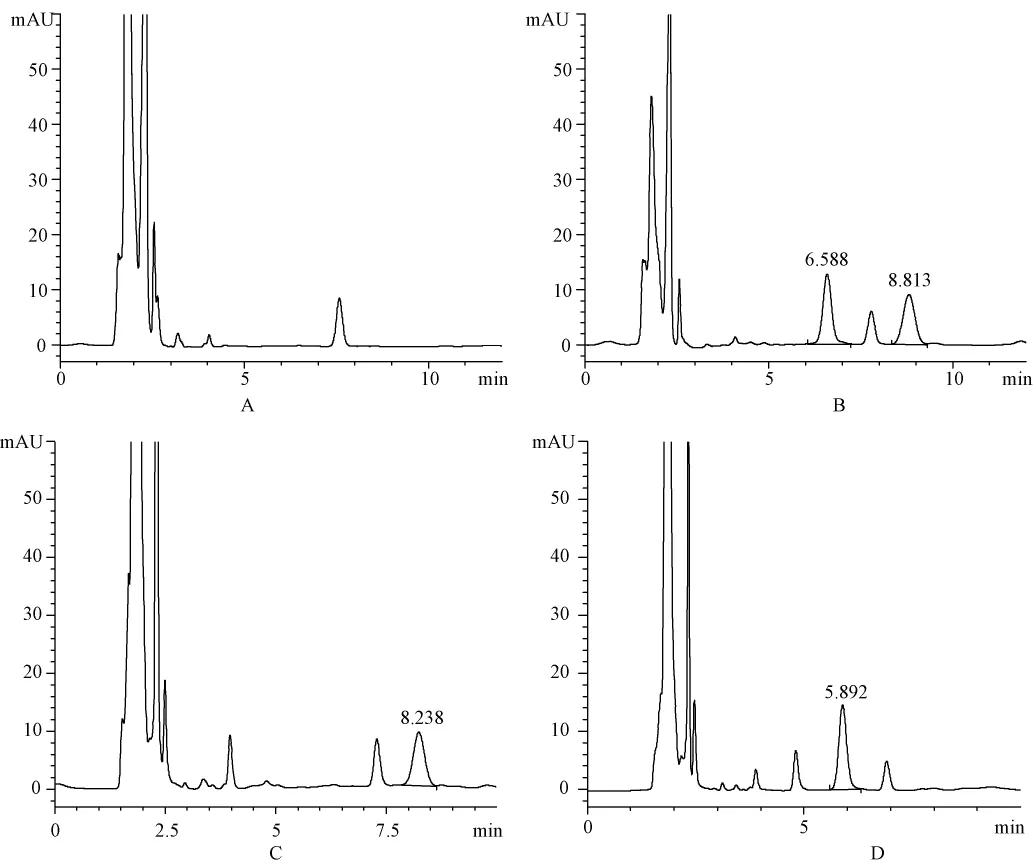
图1 万古霉素和去甲万古霉素的血清色谱图Fig 1 HPLC Chromatograms of serum vancomycin and norvancomycin
2.2 标准曲线
测定标准曲线样本,以去甲万古霉素/万古霉素的峰面积为纵坐标,样本浓度为横坐标进行线形回归。结果显示:去甲万古霉素在0.8 ~80 μg·mL-1,万古霉素 0.9 ~92 μg·mL-1的浓度范围内,呈良好的线性。去甲万古霉素的线性方程为:Y=10.678X-0.615,r=0.999 98;万古霉素的线性方程为:Y=8.597X+5.585,r=0.999 94。根据标准曲线,本实验的定量下限为去甲万古霉素 0.8 μg·mL-1,万古霉素0.9 μg·mL-1。
2.3 准确度与精密度
分别测定低、中、高3种浓度的血清质控标本各5组,计算准确度和日内精密度(RSD);连续测定5日,计算日间精密度。结果显示,本方法测定血清去甲万古霉素/万古霉素的准确度分别为97.79% ~104.82%及96.49% ~110.75%;日内、日间精密度均<8%,见表1。
2.4 稳定性实验
取低、中、高3种浓度的血清质控标本各3组,处理后将上清液在室温分别放置4、24、48 h后重复测定,计算变异系数(CV%);将配制好的血清质控标本置于-40℃冰箱分装保存,每隔1周重复测定1次,其中低、中、高浓度各测定3组,计算CV%。结果显示,去甲万古霉素和万古霉素的血清标本在上述情况下稳定性良好,测定值CV%均<10%,见表2。

表1 血清去甲万古霉素/万古霉素的准确度及精密度(n=5)Tab 1 Degree of accuracy and precision of vancomycin and norvancomycin in serum(n=5)
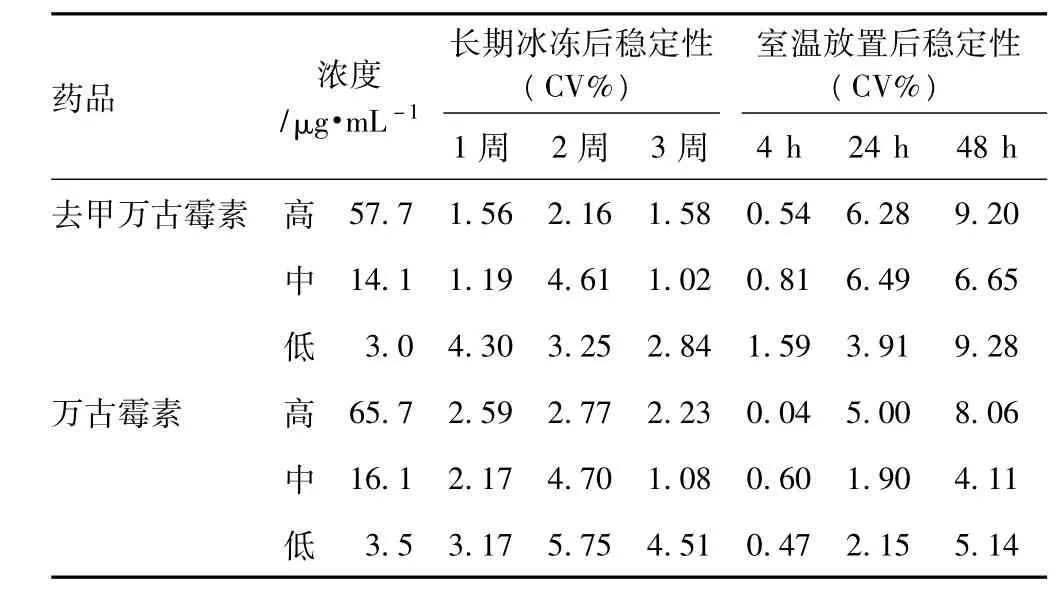
表2 血清去甲万古霉素/万古霉素的稳定性Tab 2 Stability of vancomycin and norvancomycin in serum
3 讨论
目前临床上主要应用荧光偏振免疫法(FPIA)测定血清万古霉素的药物浓度。尽管FPIA法具有操作简便,精密度高等诸多优点,但有国外文献认为[1,2],与 HPLC法相比,FPIA法所测万古霉素浓度值容易偏高,其原因可能是由于万古霉素的降解产物(CDP-1)与万古霉素发生交叉反应。在慢性肾功能不全的患者,由于万古霉素排泄显著延长,体内CDP-1产生增多,FPIA所测浓度值偏高更易发生。日本学者Tanaka等的研究表明,在血透患者中,测定值偏高的情况更为明显[1]。此外,FPIA标准血样的稳定性也可能影响测定结果,Morishige等人[2]曾对FPIA标准血样稳定性进行研究,结果显示,在4℃和25℃贮存30 d后,万古霉素含量分别下降20%和60%。因此,有必要建立快速、准确的HPLC法,以应用于万古霉素以及去甲万古霉素的临床TDM以及药代动力学研究。
有关万古霉素和去甲万古霉素测定的HPLC方法,国内外文献中多采用反向色谱法和离子对色谱法[3-6]。由于离子对色谱法存在平衡时间长,不易洗脱等缺点,故本研究采取了的反向色谱法。在流动相的组成上,本实验进行了适当改进,采用乙腈为有机相,调节其与水相的比例为10∶90,并将pH值调至2.5,使万古霉素和去甲万古霉素与血清杂质分离完全,且峰形良好,保留时间合理,提高了检测效率。在检测波长的选择上,本文对比了280 nm(《中华人民共和国药典》中规定的检测波长)和文献中多采用的236 nm,发现两药在236 nm的吸收度均较280 nm处更为理想。
有关血样处理方法,国内文献中曾使用乙腈:异丙醇沉淀血样后,再用氯仿或二氯甲烷萃取上清液的方法进行血样提取,但提取方法较为繁琐[3]。也有学者采用10%硫酸锌溶液[4]和10%三氯乙酸溶液[5]直接沉淀血清蛋白的方法,但前者沉淀蛋白不完全,后者则内源性干扰较多以致无法完全色谱分离。本实验采用6%高氯酸作为沉淀剂直接沉淀蛋白,蛋白沉淀完全,操作简单,且消耗血量极少(200 μL)。但由于高氯酸的强酸性可造成药物在上清液的稳定性减低,故本文采用NaOH调节上清液的pH值。
有文献报道,去甲万古霉素在血清中容易降解,稳定性较差[7]。本研究对不同浓度的血清质控样本进行了稳定性实验,结果表明,血清样本处理后上清液在室温放置48 h,以及血清标本-40℃保存3周,去甲万古霉素和万古霉素的稳定性均符合要求。
综上所述,本实验建立HPLC法同时测定去甲万古霉素和万古霉素的血药浓度,方法快速简捷、灵敏度高,经考察准确度和精密度良好,可满足临床开展TDM和进行人体药代动力学研究的需要。
[1]Tanaka M,Orii T,Gomi T,et al.Clinical estimation of vancomycin measurement method on hemodialysis patient[J].Yakugaku Zasshi,2002,122(4):269.
[2]Morishige H,Shuto H,Ieiri I,et al.Instability of standard calibrators may be involved in overestimating vancomycin concentrations determined by fluorescence polarization immunoassay[J].Ther Drug Monit,1996,18(1):80.
[3]丰嘉驹,顾嘉钦.高效液相色谱法测定去甲万古霉素血药浓度[J].中国医院药学杂志,2000,20(8):458.
[4]张 虹,方 昱,李 英,等.反相高效液相色谱法测定临床联合用药时血浆中万古霉素浓度[J].药物分析杂志,2008,28(4):591.
[5]祝永明,涂厉标,王 真.互为内标法测定去甲万古霉素与万古霉素的血药浓度[J].中国医院药学杂志,2005,25(12):1126.
[6]Saito M,Santa T,Tsunoda M,et al.An automated analyzer for vancomycin in plasma samples by column-switching high-performance liquid chromatography with UV detection[J].Biomed Chromatogr,2004,18(9):735.
[7]裔照国,岳 峰,季宏建,等.HPLC法测定人血清中去甲万古霉素浓度及临床应用[J].药学与临床研究,2009,17(6):522.

