钕-邻苯二胺配合物的合成、表征及性能研究
苏进雄,何福兰,祁晓婷,王 娟
(湖北大学化学化工学院,湖北 武汉 430062)
稀土元素具有独特的物理化学性质[1],与有机配体形成的配合物在发光材料、结构探针、生物活性研究、生物传感器及其它稀土材料(如稀土超磁致伸缩材料、巨磁阻材料、磁致冷材料、光致冷材料、磁光存储材料等[2~5])等领域引起人们的广泛关注。
钕是一种轻稀土元素,粉红且带有紫色光泽,Nd3+在含有共轭体系的有机配体体系中发射较强的荧光。作者在此采用水热法合成了钕-邻苯二胺配合物,通过元素分析、红外光谱、紫外光谱、荧光光谱对其结构进行表征,并对其电化学性质进行了研究。
1 实验
1.1 试剂和仪器
Nd(NO3)3·6H2O,AR,天津市光复精细化工研究所;邻苯二胺(≥98.5%),上海五联化工厂。试剂使用前未处理。
Vario EL型元素分析仪,德国Elementar公司;170SXFT-IR型红外光谱仪(KBr压片),美国Nicolet公司;UV-240型光谱仪,Shimadzu;RF-540型荧光分光光度计,日本岛津公司。
1.2 配合物的合成
将0.2185 g(0.5 mmol)Nd(NO3)3·6H2O溶解于蒸馏水中,向其中加入0.1638 g(1.5 mmol)邻苯二胺,搅拌至完全溶解。将混合物转移至聚四氟乙烯内衬的不锈钢反应釜中(规格为25 mL,填充度为80%),90℃反应3 d,得褐色针状晶体,即钕-邻苯二胺配合物。
2 结果与讨论
2.1 配合物的元素分析
配合物的元素分析实测值(理论值,%):C 53.66(52.93),H 5.54(5.43),N 20.54(20.60)。可确定配合物的组成为NdC30N10H37,分子式为:Nd(C6N2H7)3·(C6N2H8)2。空间结构式为:

2.2 配体及配合物的红外光谱分析
分别取少量配体邻苯二胺及钕-邻苯二胺配合物,加KBr研匀,采用KBr压片法测定红外光谱,结果如图1所示。
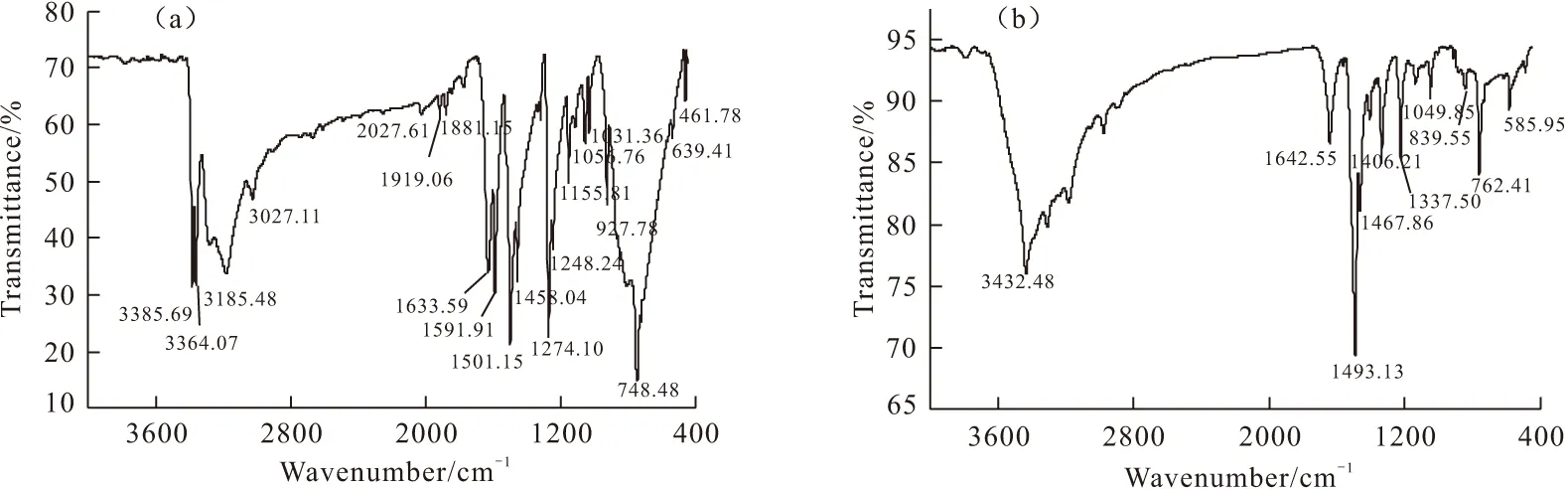
图1 配体(a)与配合物(b)的红外光谱图
由图1可以看出,与配体的红外光谱相比,配合物的红外光谱的某些特征吸收峰发生了明显位移,强度也有较大变化。配体邻苯二胺属于一级胺,它的红外光谱(图1a)在3300~3500 cm-1处出现了两组吸收峰,峰值分别为3385.69 cm-1和3364.07 cm-1,属于N-H的伸缩振动,和文献中一级胺在3300~3500 cm-1范围内只有两个吸收峰相吻合。而配合物的红外光谱(图1b)中,在3300~3500 cm-1范围内只出现一个吸收峰,峰值为3432.48 cm-1,归属于N-H的伸缩振动,和文献中二级胺在3300~3500 cm-1范围内只有一个吸收峰相吻合[6]。由此可以说明,配体邻苯二胺与Nd3+发生了配位。此外,配体在650~900 cm-1范围内的N-H面外摇摆振动特征吸收峰748.48 cm-1在配合物中发生了明显的蓝移(+14 cm-1);配体在1800~2100 cm-1范围内的吸收峰在配合物中都消失了,说明配体上的N原子与Nd3+配位后N-C及N-H的振动吸收峰的强度都有一定程度的减弱[7,8]。由此进一步说明配体邻苯二胺与Nd3+发生了配位。
2.3 配合物的紫外光谱分析(图2)

图2 配合物的紫外光谱
由图2可以看出,配合物在259 nm和419 nm处出现了两个吸收峰。其中,259 nm处的吸收峰是由配合物中配体的π→π*跃迁引起的,419 nm处的吸收峰对应Nd3+的4I9/2→4G5/2跃迁,表现为Nd3+的f→f超灵敏跃迁吸收[9,10]。
2.4 配合物的荧光光谱分析
以RF-540型荧光分光光度计的氙灯作为激发光源,在室温下对配合物进行荧光测试,结果如图3所示。

图3 配合物的荧光光谱(激发波长352 nm)
由图3可以看出,配合物水溶液在激发波长为352 nm时的荧光发射光谱的特征带为360~600 nm。其中,520~580 nm内有一强峰,峰值为543.7 nm;430~480 nm内有一弱峰。这表明配合物在室温下具有荧光性能。根据文献报道,Nd3+的两个最特征的跃迁为4I9/2→2P1/2和4I9/2→4G5/2、2G7/2[11];另外,由于高灵敏度的4I9/2→4G5/2、2G7/2跃迁显示在所有f→f跃迁中,因此可判定在520~580 nm范围内的强吸收峰归属于4I9 /2→4G5 /2、2G7/ 2跃迁,另一个弱峰归属于4I9/2→2P1/2跃迁。
2.5 配合物的电化学性质
采用三电极系统:工作电极为铂电极,参比电极为饱和甘汞电极,辅助电极为铂电极;在-0.4~0.4 V(vs.SCE)的电势范围内,以HCl水溶液(pH≈4)为支持电解质,对配合物进行电化学性质的研究,其循环伏安图见图4。

图4 配合物水溶液的循环伏安图(扫描速率为500 mV·s-1)
由图4可以看出,配合物的循环伏安曲线出现了明显的氧化还原峰,峰电位及其电位差分别为Epa=-0.216 V、Epc=-0.148 V、ΔEp=-68 mV;对应的半峰电位为-0.187 V。对于可逆过程,有|Ep-Ep/2|=56.5/n,根据这个公式计算出反应的电子转移数n=2。因此可推测反应过程如下:
Nd3+-2e-=Nd5+
3 结论
以邻苯二胺为配体,合成了一种新型的钕配合物Nd(C6N2H7)3·(C6N2H8)2。通过元素分析、红外光谱、紫外光谱和荧光光谱对其结构进行了表征。荧光光谱分析表明,配合物在室温下具有荧光性能。在HCl水溶液中,配合物在-0.4~0.4 V(vs.SCE)电势范围内具有明显的电化学活性。
[1] 熊家齐.关于稀土产业的某些思考[J].稀土,2002,23(1):72-78.
[2] 蒋建生,杜红林,张文勇.电负性、原子赝势半径与稀土永磁材料[J].中国稀土学报,2003,21(3):287-290.
[3] 刘行仁,王晓君,何大伟.加入WTO 后我国稀土发光材料面临的机遇和挑战[J].中国稀土学报,2002,20(6):491-494.
[4] 郑群,陈云贵,王金国,等.退火处理对快淬贮氢合金显微组织及电化学性能的影响[J].中国稀土学报,2003,21(4):417-420.
[5] Fu Xixian,Yang Qiuhua,Wang Junzhen.Photocatalytic degradation of water-soluble does by CaClO3[J].Journal of Rare Earths,2003,21(4):424-429.
[6] 董庆年.红外光谱法化学[M].北京:化学工业出版社,1979:194-196.
[7] 周红波,陈友存.两种过渡金属配合物的合成和光谱表征[J].安庆师范学院学报(自然科学版),2007,13(4):42-44.
[8] 中本一雄,著,黄德和,汪任庆,译.无机和配位化合物的红外和拉曼光谱(第四版)[M].北京: 化学工业出版社,1991:253-260.
[9] 常建华,董绮功.波谱原理及解析[M].北京: 科学出版社,2001:29-36.
[10] 邓芹英,刘岚,邓惠敏.波谱分析教程(第二版)[M].北京:科学出版社,2007:19-23.
[11] Mondry Anna,Starynowicz Przemyslaw.Optical spectroscopy of neodymium(Ⅲ) complexes with diethylenetriaminepentaacetic acid in solution and in [C(NH2)3]2[Nd(dtpa)(H2O)]·7H2O single crystal[J].Polyhedron,2000,19(7):771-777.

