三乙烯四胺、三聚氰胺对Au催化NaBH4直接氧化的改善
余丹梅,张代雄,李小艳,申 燕
(重庆大学化学化工学院,重庆 400044)
直接硼氢化钠燃料电池(DBFC)以硼氢化钠(NaBH4)为负极燃料,具有燃料效率高、产物无污染及运输方便等优点。理论上,当DBFC工作时,1 mol NaBH4可提供8 mol电子,但在实际放电过程中,BH4-的水解和BH4-的不完全氧化[1],导致NaBH4在阳极催化剂上释放的电子数(n)很难达到8,使法拉第效率降低,因此BH4-氧化的反应式一般可写为:
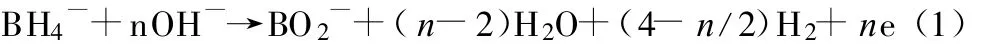
BH4-氧化反应的电子转移数反映了NaBH4直接氧化的性能,并与阳极催化剂有关,其中,金(Au)作催化剂时 n值较高[2]。用Au作DBFC阳极催化剂研究的热点是纳米Au催化剂的制备,但面临着工艺复杂、成本高昂等问题[3]。电解液添加剂可改善DBFC阳极催化剂的性能[4],但目前的研究仅限于改善铂(Pt)对NaBH4直接氧化催化性能,本文作者尚未见到改善Au对NaBH4直接氧化催化性能的报道。
添加剂对NaBH4在电极表面直接氧化的促进作用与添加剂的基团有关[4],而氨基被认为是一种能够促进NaBH4直接氧化的基团。本文作者就添加剂三乙烯四胺和三聚氰胺对Au催化下NaBH4直接氧化的影响进行了研究。
1 实验
1.1 电极的活化处理和电解液的配制
将金电极(美国产,Φ=1 mm)用碳化硅干湿两用金相砂纸(P2000#)打磨后,在丙醇(重庆产,AR)、乙醇(重庆产,AR)和蒸馏水中依次超声清洗,以除去表面的杂质;然后置于0.5 mol/L H2SO4(重庆产,AR)中,以0.01 V/s的速度在-1.5~1.5 V循环扫描1次,进行预处理,将电极活化。
将3 mol/L NaOH(重庆产,AR)+0.1 mol/L NaBH4(天津产,AR)溶液混合作为电解液,并分别向其中加入三乙烯四胺(重庆产,AR)、三聚氰胺(重庆产,CP)。三乙烯四胺的浓度分别为 80μ mol/L、160 μ mol/L 和 240μ mol/L;三聚氰胺的浓度分别为 0.8 μ mol/L、1.6 μ mol/L 和 2.4 μ mol/L。
1.2 电化学性能测试
以金电极为工作电极,Hg/HgO电极为参比电极,石墨棒(Φ=10 mm)为辅助电极组成三电极体系,在CHI660B电化学工作站(美国产)上进行循环伏安、交流阻抗测试。循环伏安法的扫描范围为-1.0~0.8 V,扫描速度为0.05 V/s;交流阻抗测试的频率为105~10-2Hz,交流振幅为0.005 V。
2 结果与讨论
2.1 三乙烯四胺的影响
2.1.1 循环伏安曲线
NaBH4在含三乙烯四胺电解液中的循环伏安曲线见图1。
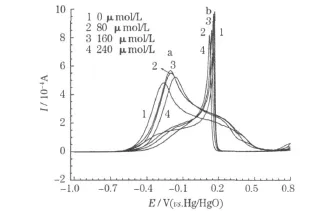
图1 NaBH4在含三乙烯四胺电解液中的循环伏安曲线Fig.1 CV curves of NaBH4in electrolytes containing triethylene tetramine
从图1可知,无论有无添加剂,BH4-在金电极上的氧化峰a都出现在-0.25 V左右。没有添加剂时,大量的BH4-吸附在金电极表面,导致BH4-的数量比催化点多[5],吸附在Au上的BH4-的4个H原子中,只有较少的能接触到催化点而发生反应,其他的H原子只能在水溶液中发生水解反应,因此BH4-的电子转移数较少,峰电流较小。随着浓度的增加,氧化峰a的电流先增大、后减小,表明添加适量的三乙烯四胺能使BH4-有更多的H原子与催化点接触、发生反应,电子转移数增加,促进NaBH4在金电极表面的氧化。若浓度过大,添加剂会阻碍BH4-在金电极上的氧化。实验证明:三乙烯四胺的最佳浓度为160 μ mol/L。在回扫时,吸附在电极表面未来得及离开的BH4-可继续发生氧化反应,因此在0.2 V附近出现氧化峰b,意味着BH4-在阴极上也能氧化,导致燃料利用效率降低。添加三乙烯四胺后,氧化峰b的电流下降,并随着浓度的增加而降低,说明添加剂能抑制BH4-在阴极上的氧化,有利于提高燃料利用率。
三乙烯四胺对NaBH4在金电极上氧化的促进作用,可能与其结构有关:三乙烯四胺分子中有4个N原子,N的原子序数是7[6],电子排布式为1s22s22p3,每个N原子都有一对孤电子对,能与Au形成配位键,容易吸附到金电极表面,从而减少BH4-在电极上的吸附量,使每个BH4-有更多的H原子可接触到催化点而发生氧化,提高了电子转移数,促进了 BH4-在金电极表面直接的氧化,因此,氧化峰a的电流增加;随着浓度的提高,过多的三乙烯四胺吸附在金电极表面,挤占了催化点,使BH4-在电极上的吸附量减少,抑制了电极反应,导致峰电流降低。三乙烯四胺的吸附导致BH4-在电极表面的吸附量减少,因此回扫时氧化峰b的电流降低,抑制了BH4-在阴极上的氧化,提高了燃料利用率。
2.1.2 交流阻抗谱
NaBH4在含三乙烯四胺电解液中的交流阻抗谱见图2,图中半圆弧的直径反映了电化学反应阻抗的大小,可近似看作电极反应电荷传递电阻,阻抗越小,反应产生的法拉第阻抗越小,越有利于电极反应的进行[7]。
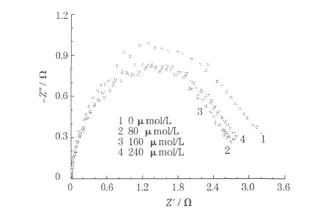
图2 NaBH4在含三乙烯四胺电解液中的交流阻抗谱Fig.2 AC impedance plots of NaBH4in electrolytes containing triethylene tetramine
从图2可知,交流阻抗与循环伏安实验的结果一致。电解液中添加三乙烯四胺后,电化学阻抗先减小,后增大。三乙烯四胺浓度为160μ mol/L时,电化学阻抗最小,表明此时氧化反应最容易发生,Au对NaBH4氧化的催化作用最强。
2.2 三聚氰胺的影响
2.2.1 循环伏安曲线
NaBH4在含三聚氰胺电解液中的循环伏安曲线见图3。
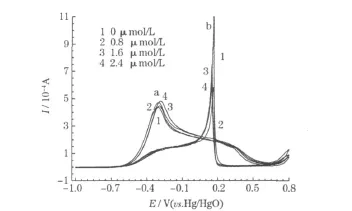
图3 NaBH4在含三聚氰胺电解液中的循环伏安曲线Fig.3 CV curves of NaBH4in electrolytes containing melamine
从图3可知,随着三聚氰胺浓度的增加,氧化峰a的电流先增大,后减小,表明添加适量的三聚氰胺能使BH4-上更多的H原子与催化点接触、发生反应,电子转移数增加,促进NaBH4在金电极表面的氧化。实验证明:三聚氰胺的最佳浓度为1.6 μ mol/L。氧化峰b的电流随着三聚氰胺浓度的增加而减小,说明三聚氰胺的加入,抑制了BH4-在阴极上氧化,减少了燃料的损耗。
2.2.2 交流阻抗谱
NaBH4在含三聚氰胺电解液中的交流阻抗谱见图4。
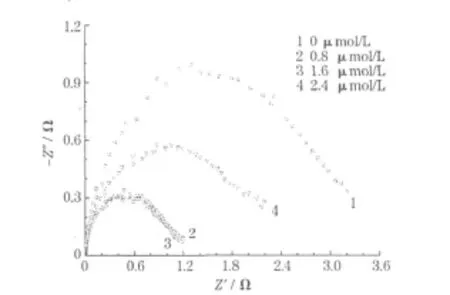
图4 NaBH4在含三聚氰胺电解液中的交流阻抗谱Fig.4 AC impedance plots of NaBH4in electrolytes containing melamine
从图4可知,随着三聚氰胺浓度的增加,电化学阻抗先减小,后增大,当三聚氰胺浓度为 1.6 μ mol/L时,电化学阻抗最小,表明此时氧化反应最容易发生,Au对NaBH4氧化的催化作用最强。这与循环伏安研究的结论一致。当三聚氰胺浓度超过1.6 μ mol/L时,阻抗弧增大,说明羟基上的 O原子吸附在金电极表面挤占的催化点增多,使反应性能下降。
与三乙烯四胺相比,三聚氰胺对NaBH4在金电极上的直接氧化的促进作用稍弱,原因是三聚氰胺遇到强碱溶液会发生水解反应[8],胺基逐步被羟基取代,最后生成三聚氰酸。
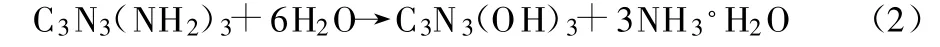
三聚氰酸有3个羟基和3个具有孤电子对的N原子,羟基中的O原子的原子序数为8[6],电子排布式为1s22s22p4,每个O原子含有两对孤电子对,因此与Au形成配位键的能力远远强于N原子,使三聚氰酸更容易紧密吸附在金电极表面。O原子的紧密吸附会挤占金电极表面的催化点,部分抵消N原子的吸附对BH4-在金电极表面氧化的促进作用,使添加三聚氰胺后BH4-上能够接触到催化点发生反应的H原子个数比添加三乙烯四胺时的少,电子转移数也相对较少。另外,三聚氰酸中的O原子能够挤占较多的催化点,使得三聚氰胺的最佳浓度(1.6 μ mol/L)低于三乙烯四胺的最佳浓度(160 μ mol/L)。回扫时,氧化峰 b的峰电流下降更多,更好地抑制了BH4-的阴极氧化,提高了燃料的利用率。
3 结论
在碱性溶液中,添加适量的三乙烯四胺和三聚氰胺可减少金电极表面上BH4-的数量,使每个BH4-有更多的H原子能够接触到催化点、发生反应,从而改善Au对NaBH4直接氧化的催化作用。水解产生的羟基紧密吸附在电极表面而导致电极表面催化点减少,因此三聚氰胺的添加效果弱于三乙烯四胺。研究结果表明:三乙烯四胺和三聚氰胺的最佳浓度分别为 160μ mol/L、1.6 μ mol/L 。
相对于复杂的纳米Au催化剂的制备,添加剂改善Au对NaBH4直接氧化催化性能的方法简便易行、成本低廉。添加剂的种类与基团、分子结构等的关系,需要深入研究。
[1]Wee J H.A comparison of sodium borohydride as a fuel for proton exchange membrane fuel cells and for direct borohydride fuel cells[J].J Power Sources,2006,155(2):329-339.
[2]Chatenet M,Micoud F,Roche I.Kinetics of sodium borohydride direct oxidation and oxygen reduction in sodium hydroxide electrolyte(Ⅰ).BH4-electro-oxidation on Au and Ag catalysts[J].Electrochim Acta,2006,51(25):5 459-5 467.
[3]PEI Fu(裴斧),WANG Xian-you(王先友),HE Pei-ying(何培瑛),et al.催化剂载体对硼氢化钠在纳米金电极上电氧化行为的影响[J].Acta Chimica Sinica(化学学报),2010,68(2):136-142.
[4]LEI Shu(雷淑).添加剂对硼氢化钠直接氧化的影响[D].Chongqing(重庆):Chongqing University(重庆大学),2009.
[5]WANG Gui-ling(王贵领),LAN Jian(兰剑),CAO Dian-xue(曹殿学),et al.直接NaBH4/H2O2燃料电池的研究进展[J].Journal of Chemical Industry and Engineering(化工学报),2008,59(4):806-813.
[6]CAO Xi-zhang(曹锡章),SONG Tian-you(宋天佑),WANG Xing-qiao(王杏乔).无机化学[M].Beijing(北京):Higher Education Press(高等教育出版社),1994.470-513.
[7]Patnaik R S M,Ganesh S,Ashok G.Heat management in aluminium/air batteries:sources of heat[J].J Power Sources,1994,50(3):331-342.
[8]LI Feng-ge(李锋格),YAO Wei-qin(姚伟琴),SU Min(苏敏),et al.气相色谱-质谱法快速测定牛奶中的三聚氰胺和三聚氰酸[J].Chinese Journal of Chromatography(色谱),2009,27(2):232-236.

