湖北民族地区IgA肾病71例临床分析
石 磊
湖北民族学院附属民大医院肾病内科(湖北恩施 445000)
IgA肾病(immuno globulin A nephropathy,IgAN)是最常见的原发性肾病,在不同地区和种族之间存在着明显的差异,我国IgA肾病约占原发性肾小球疾病的30%~40%,该病以IgA或弥漫沉积于肾小球系膜区及(或)毛细血管袢为免疫病理学特征,起病多隐匿,轻重不一,临床表现和组织形态学改变多样化,预后相差悬殊,约1/3的患者会进展到慢性肾衰竭[1]。IgAN发病机制目前尚不完全清楚,多认为与感染、免疫反应、炎症介质和遗传有关[2],笔者收集了71例 IgAN患者临床与病理资料,分析其特点和相关性,供临床诊治参考。
1 资料和方法
1.1 病例选择 收集湖北民族学院附属医院2007年1月~2010年3月经肾活检确诊的IgA肾病患者71例,均符合WHO1995年修订的肾活检病理诊断标准指导意见,排除心、脑、肝及糖尿病等疾病和系统性红斑狼疮、过敏性紫癜、慢性肝脏疾病、强直性脊柱炎、肿瘤等继发性IgA肾病。男28例,女33例,男∶女 =1∶1.18;年龄12~69岁,平均(37.2±8.3)岁,其中30~39岁年龄段37例,占52.11%。直接诱因为:上呼吸道感染28例(39.44%)、劳累15 例(21.13%)、急性胃肠炎 7 例(9.86%)、其它21例(29.58%)。71例IgAN患者均有蛋白尿,24h蛋白定量平均(3.8±2.7)g;血压平均 (142.7±28.5)/(93.8±22.6)mmHg,45 例(63.38%)合并有高血压。
1.2 检测项目和方法
1.2.1 常规检测 使用全自动尿液分析仪(H-800Unine Aha-lyzer)检测尿常规,以 Rxl max HM定量生化分析仪测定1、24 h尿蛋白、以LX-20型生化分析仪测定血清肌酐、血脂和肝功能。
1.2.2 肾组织标本活检 在超声引导下采用活检自动穿刺针(16~18F)一次性快速穿刺,取肾脏活组织2~3块,在光镜下行HE、PAS、Masson和PASM检查,免疫荧光检查 IgA、IgG、IgM、补体 C3、C4、Clq和Fib,观察肾小球系膜细胞、系膜基质的增生程度及电子致密物的沉积部位、程度和分布特点。
1.3 统计学处理 采用SPSS15软件,数据以均数±标准差(±s)表示,计量资料比较用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 分类标准 (1)临床表现分为5型,即单纯血尿型、单纯蛋白尿型(<3.5 g/24 h)、血尿+蛋白尿型(>200 mg/24 h)、肾病综合征型、肾衰竭型。(2)病理分型根据Lee氏分级分为5级。Ⅰ级:肾小球轻度系膜增生,小管-间质无明显病变;Ⅱ级:肾小球局灶节段增生和硬化(<50%);Ⅲ级:弥漫系膜增生伴小新月体形成;Ⅳ级:重度弥漫系膜增生和硬化(部分或全部)伴新月体(45%)小管萎缩,间质浸润,偶见间质泡沫细胞;Ⅴ级:病变性质类似Ⅳ级,但更严重,新月体(>45%)[3]。
2.2 诊断结果 71例IgA肾病患者中,系膜增生性肾炎43例(60.56%)、局灶性节段性肾小球硬化22 例(30.07%)、增生硬化性肾炎2 例(2.82%);膜增生性肾小球肾炎、毛细血管内增生性肾炎、良性肾小动脉硬化和肾小球轻微病变各1例(1.97%)。见表1。
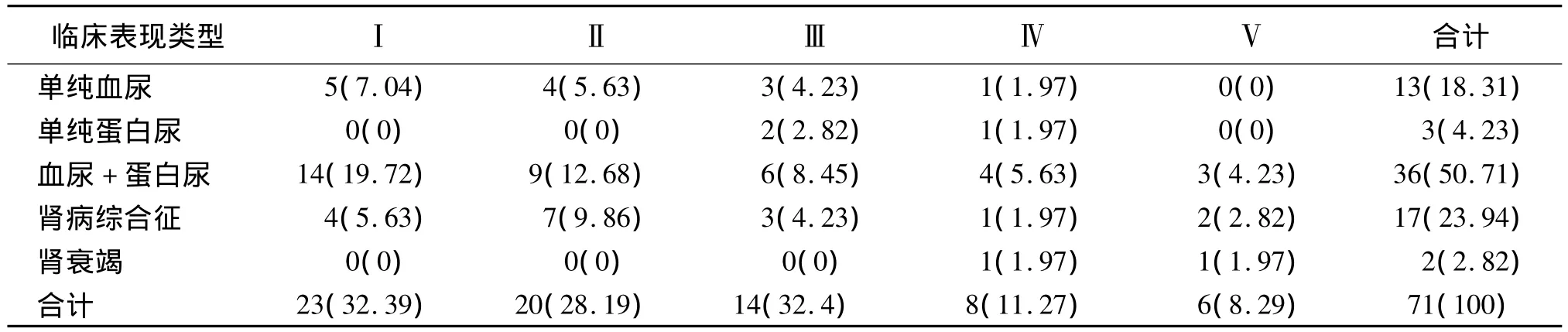
表1 71例IgA肾病临床表现与病理分级统计(n,%)
2.3 免疫荧光强度及分型 71例IgA肾病患者中,荧光强度 1+30例 (42.25%)、2+20例(28.19%)、3+17 例(23.94%)、4+4 例(5.63%);以单纯IgA沉积为主占23.94%(17/71),依次为合并 IgM 沉积 19.72%(14/71)、合并 IgG沉积11.27%(8/71)、合并 IgG+IgM 沉积4.23%(3/71),另伴C3沉积14例(19.72%)、伴 C4沉积 4例(5.63%)、伴 Fib5 例(7.04%)。
3 讨论
文献[4]报道,IgA肾病多见于男性,可以发生于任何年龄,以儿童和青年人最为常见,而本观察中,女性略多于男性,30~39岁的中年人占一半以上,这可能与湖北民族地区生活习俗和条件有关,如中年女性吸烟者多,且普遍劳动强度大、饮食生活规律性差等。在诱发病因方面上呼吸道感染、劳累和急性胃肠炎就占了70.43%,也证明改变不良生活习惯、加强保健是预防IgA肾病的重要措施之一,对危险人群尤其要注意控制上呼吸道感染。
IgA肾病临床表现并不典型,本观察中,大部分病人没有明显的临床症状,小部分是在体检中发现可能有肾病综合征、慢性肾炎、急性肾炎等而入院进一步确诊的,其中,血尿+蛋白尿高达50.71%,对无症状而出现血尿和蛋白尿患者宜尽早行肾活检术。IgA肾病的病理类型包括了几乎所有原发性肾小球疾病的病理类型,本组中Ⅰ、Ⅱ级病变占60.58%,病理改变以系膜增生性肾小球肾炎和局灶增生硬化性肾小球肾炎为主,占我院同期收治原发性肾小球肾炎的38.5%,在各种肾小球疾病中位居第一。说明IgA肾病各种临床表现之间存在一定的相关性,临床诊断中不能从临床表现上去主观判断,要进行必要的肾脏穿刺活组织病理检查,最好在超声引导下进行,以更好地指导临床诊断和治疗。IgA肾病的免疫复合物沉积多为IgA或IgA为主的免疫球蛋白在系膜区弥漫沉积,本研究中,IgA荧光强度以1+和2+分别占了42.25%和28.19%,荧光强度是否反映病情的严重程度,还需要进一步观察与探讨。71例IgA肾病患者中,单纯IgA沉积和IgM较多,AGM型比较少见,本组中仅占4.23%,本组中有23例伴补体沉积,这提示补体可能经各种途径参与了部分IgA肾病的发生与发展。
需要指出的是,IgA肾病易被临床误诊,IgA肾病的病理和临床表现之间缺乏带规律性的对应关系,仅依据血液中的免疫学检查结果容易导致误诊,本院同期诊断时曾有266例与IgA肾病相似病理,最后经活检确诊为IgA肾病的仅此71例,因此,我们认为,对临床疑诊IgA肾病应尽量接受肾活检。
目前大多数研究[5]认为IgA肾病并非一良性病变,预后也不一致,IgA肾病的治疗和预后与肾小球硬化和肾小管间质病变的严重程度相关,原则上,病理类型等级越高,其预后越差。有报道[6]称,临床实践中,仅有30%左右的IgA肾病患者可完全缓解,30%左右的IgA肾病患者仍存在不同程度的肾功能下降。30%~40%的患者在确诊后5~25年内可发展至终末期肾衰竭(ESRF)。因此,确诊后一定要早治疗,如肾功能进展的速度超过9 ml/min/yr,血肌酐(Scr)超过3 mg/d时,如不加干预,肾功能就会进入不可逆阶段。肾小球硬化、间质纤维化、活动或慢性化的血管炎损伤指标(如新月体形成、节段性毛细血管袢坏死、球囊粘连以及节段性硬化)都属危险因子。高血压患者易患IgA肾病,本组中就有高达63.38%的患者合并有高血压病,而合并有高血压的IgA肾病患者又容易进展到慢性病变,因此,积极有效地控制高血压,有助于延缓疾病进展。蛋白尿持续存在或蛋白尿程度不断加重是进行性肾损害的重要因素之一,应对不同程度的蛋白尿进行积极干预。
[1]陈玮玲,林华鹏,刘华锋.粤西地区IgA肾病临床与病理特点[J].南方医科大学学报,2010,30(5):1150-1151.
[2]耿兴花,陈志,王飞宇,等.85例IgA肾病病理与临床分析[J].中国实验诊断学,2010,14(5):729-731.
[3]阿达莱提,苏建华,汪忠诚.雷公藤多甙片治疗18例原发性IgA肾病综合症的临床随机对照观察[J].当代医学,2008,14(6):16-17.
[4]魏敏,赵晓山,孙晓敏,等.表现为孤立性血尿的IgA肾病36例临床分析[J].热带医学杂志,2009,9(10):37-38.
[5]欧继红,万青松,谢红萍.不同程度蛋白尿的IgA肾病的临床与病理分析[J].医学临床研究,2009,26(1):126-127.
[6]李栋,林珊,郑振峰,等.局灶增生硬化型IgA肾病的肾血管病变及其临床意义[J].天津医科大学学报,2008,14(1):110-111.

