HPLC同时测定喘舒片中5种蒽醌类成分的含量
王瑞芬, 郭海丽
(1.濮阳市食品药品检验所,河南濮阳 457000;2.河南华峰制药有限公司,河南濮阳 457000)
1 仪器与试药
1.1 仪器 Waters高效液相色谱仪:515型高压泵;2487紫外检测器;N2000工作站。Precisa 92SM-202A电子分析天平,感量0.01 mg(普利赛因国际贸易(上海)有限公司),KQ 2200超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药 芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚对照品,批号分别为:110795-200806、0757-200206、 110756-200110、 110796-200513、110758-200509,均购自中国药品生物制品检定所;喘舒片批号为:20091202,20091203,20091204 河南华峰制药有限公司;甲醇为进口色谱纯(美国);水为重蒸水;其它试剂均为分析纯。
2 试验方法与结果
2.1 色谱条件 色谱柱:Lanbo® Kromasil C18柱(250 mm ×4.6 mm,5 μm);流动相:甲醇-0.3% 磷酸(80:20);检测波长:254 nm;流速:1.0 mL/min;柱温:30℃;进样量:20 μL;理论塔板数按芦荟大黄素峰计均不低于7 000;分离度大于1.5。按以上色谱条件得到对照品溶液、供试品溶液、阴性对照溶液色谱图,见图1。
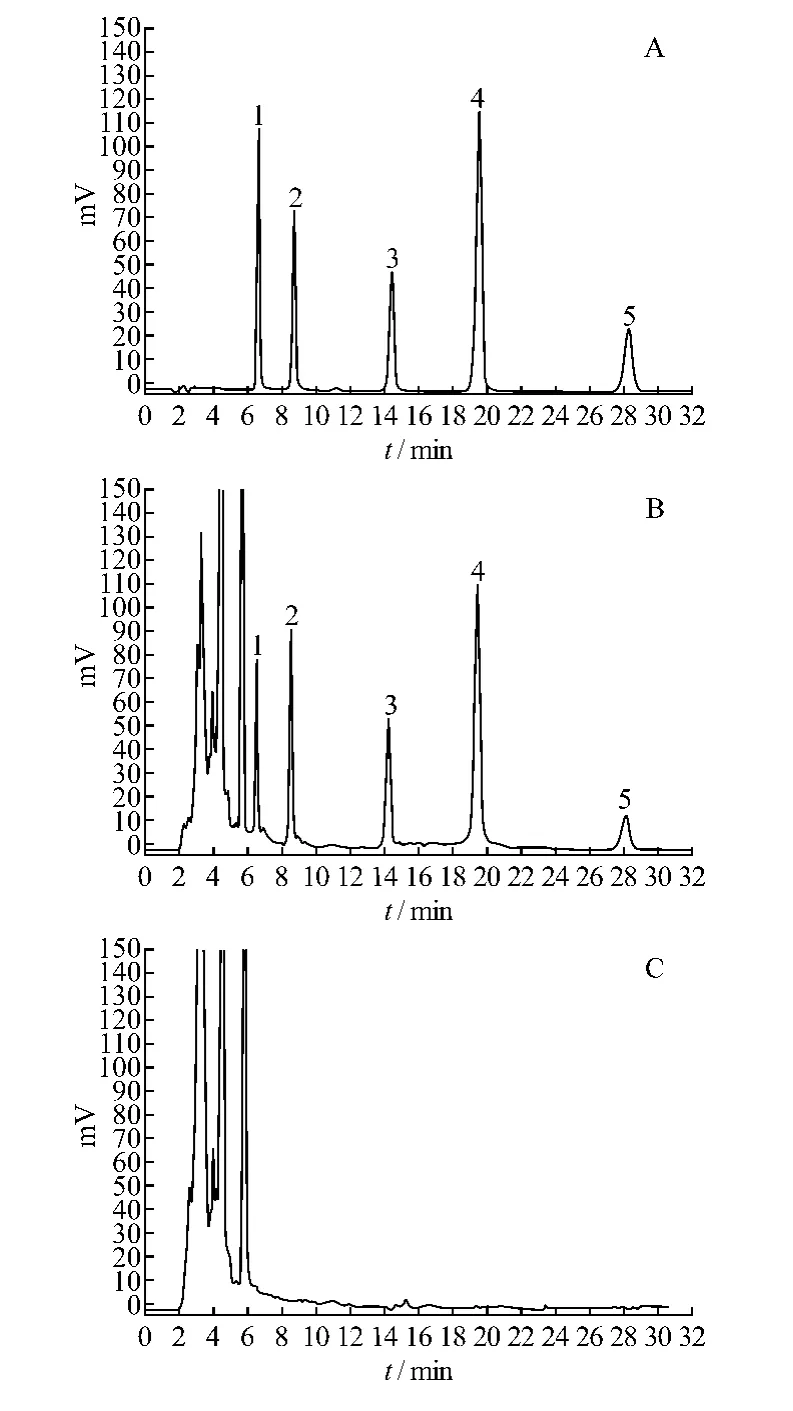
图1 喘舒片HPLC色谱图
2.2 对照品溶液与供试品溶液的制备
对照品溶液的制备:分别精密称取芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚对照品适量,置50 mL量瓶中,加甲醇制成含芦荟大黄素46.8 μg/mL、大黄酸 49.0 μg/mL、大黄素 53.0 μg/mL、大黄酚116 μg/mL、大黄素甲醚73.8 μg/mL 的混合对照品溶液,备用。
供试品溶液的制备:取供试品20片,除去包衣,精密称定,研细,取约3 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,密塞,称定重量,超声处理30 min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液10 mL,置烧瓶中,蒸干,残渣加水10 mL、盐酸2 mL和三氯甲烷20 mL,加热回流1 h,立即冷却,分取三氯甲烷层,水层再用三氯甲烷振摇提取3次,每次10 mL,合并三氯甲烷液,蒸干,残渣加甲醇溶解,转移至10 mL量瓶中,并稀释至刻度,摇匀,滤过,取续滤液,即得。
测定法:分别精密吸取对照品和供试品溶液各20 μL,注入液相色谱仪,测定,即得。
2.3 线性关系考察 分别精密吸取对照品混合液1、2、3、4、5 mL 置 10 mL 量瓶中,加甲醇稀释至刻度,摇匀,精密吸取各浓度对照品混合液20 μL,注入液相色谱仪,按上述色谱条件测定峰面积,以进样量为横坐标(X)、峰面积为纵坐标(Y),进行线性回归,得回归方程。

实验结果表明:芦荟大黄素在进样量0.093 6 μg~0.468 μg、大黄酸在进样量 0.098 μg ~ 0.49 μg、大黄素在进样量0.106 μg ~0.53 μg、大黄酚在进样量0.232 μg ~1.16 μg、大黄素甲醚在进样量0.147 6 μg~0.738 μg范围内与峰面积呈良好线性关系。
2.4 阴性对照试验 准确称取按处方比例除去大黄粉的其它药材适量,依照喘舒片的制备工艺和供试品溶液的制备方法制得缺大黄粉的空白对照溶液,作为阴性对照液。按上述色谱条件测定,供试品色谱中5种待测成分色谱峰保留时间与相应对照品峰的保留时间一致,阴性对照色谱图上在此保留时间无干扰。见图1。
2.5 精密度试验 精密吸取供试品溶液20 μL(批号为:20091204),按上述色谱条件,平行进样5次,根据峰面积,测得芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚的 RSD分别为0.63%、0.62%、1.02%、0.82% 、1.14% 。
2.6 稳定性试验 精密吸取同一供试品溶液,分别于0、2、4、6、8、10、12 h 进样 20 μL,测定峰面积,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰面积RSD分别为 0.96%、1.04%、1.12%、1.06%、0.92%。结果表明供试品溶液在12 h内稳定。
2.7 重复性试验 取同一批次样品5份,按供试品溶液制备方法制得供试品溶液,进样20 μL,分析测定,芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚峰面积的RSD分别为1.04%、1.34%、1.09%、1.32%、1.15%,表明重复性良好。
2.8 加样回收率试验 精密称取已知含量的同一批号样品(批号:20091204)约2.0 g,精确加入一定量对照品,按供试品制备项下方法操作,测定含量,计算回收率,结果见表1~5。
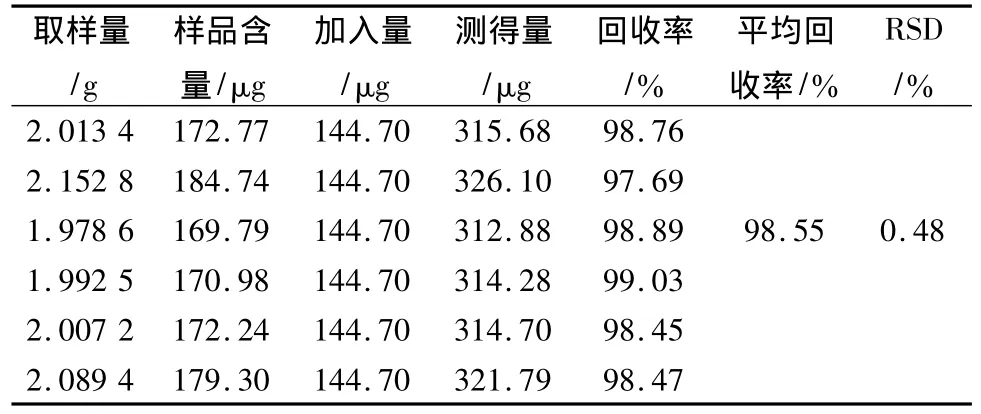
表1 芦荟大黄素加样回收率实验结果

表2 大黄酸加样回收率实验结果
2.9 样品含量测定 取样品3批,按供试品制备项下方法制得供试品溶液,分别精密吸取供试品溶液各20 μL,注入液相色谱仪,记录色谱图,分别代入回归方程,计算样品中各组分含量,结果见表6。
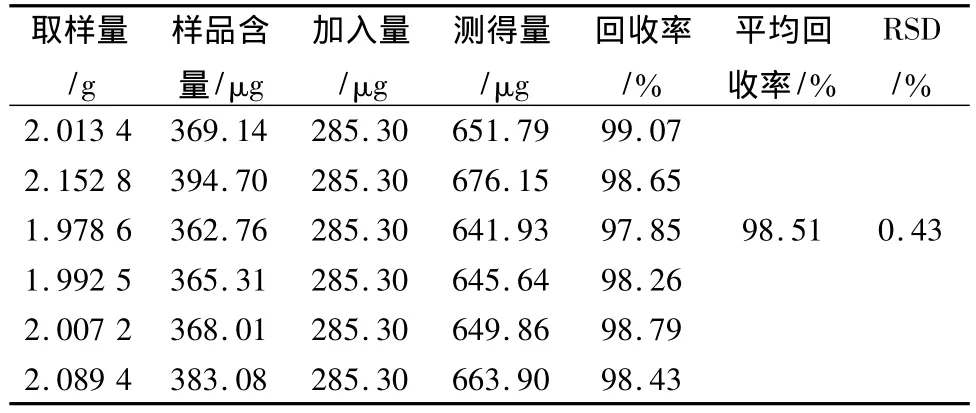
表3 大黄素加样回收率实验结果

表4 大黄酚加样回收率实验结果

表5 大黄素甲醚加样回收率实验结果
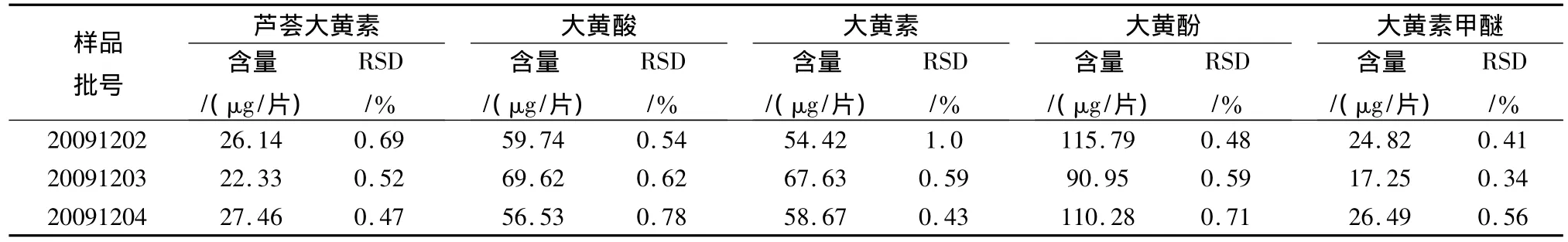
表6 5种蒽醌类成分含量测定结果(n=3)
3 讨论
本实验参考文献报道的蒽醌类成分含量测定方法,经大量试验最终确定流动相为甲醇-0.3%磷酸(85:15)[9-10],样品中5种待测成分分离良好。
在试验过程中,对样品的前处理,曾先后采用超声处理15 min、30 min、45 min 与加热回流 30 min、1 h、2 h两种方法,实验结果表明超声处理30 min,样品中各待测成分已基本溶出。回流提取1 h和超声提取30 min均可达满意结果,考虑到超声提取操作简便,时间易于控制等优点,最终选定该方法为宜。
[1]王 猛,孙忠亲,宫瑞萍.HPLC测定喘舒片中盐酸克仑特罗含量[J]. 中成药,2003,25(4):85-86.
[2]王家和,郭桂秋,李俊田,等.PHLC法测定喘舒片中黄芩苷的含量[J]. 中国药业,2003,12(1):43-44.
[3]潘成学,姬生国,申小静.高效液相色谱法测定喘舒片中黄芩苷的含量[J].河南中医学院学报,2005,20(3):34-35.
[4]岳淑梅,冯玲玲,齐潇潇,等.肝宁颗粒中大黄所含5中蒽醌苷元的 HPLC 测定[J].中成药,2008,30(8):1155-1158.
[5]汪 霞.反相HPLC法测定黄连上清片中大黄酸、大黄素、大黄酚的含量[J]. 药物分析杂志,2008,28(8):1310-1312.
[6]徐韧柳,刘会英.RP-HPLC测定珍黄散中大黄素和大黄酚的含量[J]. 中成药,2004,26(2):108-110.
[7]张 丹,蒋心惠.反相高效液相色谱法测定大黄药材中游离及结合型蒽醌类衍生物的含量[J].分析化学,2003,31(4):459-462.
[8]张 村,李 丽,肖永庆,等.HPLC法同时测定大黄不同来源药材中2个蒽醌苷类成分的含量[J].药物分析杂志,2010,30(1):53-55.
[9]马志刚,曹秋娥,丁中涛,等.反相高效液相色谱测定大黄及其制剂中蒽醌类成分[J].云南大学学报:自然科学版,2006,28(S1):255-258.
[10]王燕萍,武新安.HPLC测定烧烫伤凝胶中蒽醌类成分的含量[J].中成药,2006,28(8):1120-1122.

