肿瘤细胞增殖特异性分子影像探针3'-脱氧-3'-[18F]氟胸苷的自动化生产
王明伟 章英剑 张勇平
(复旦大学附属肿瘤医院核医学科 复旦大学上海医学院肿瘤学系 上海 200032)
3'-脱氧-3'-[18F]氟胸苷(18F-FLT)是胸苷激酶-1(TK-1)的底物,参与DNA合成,是一种特异性细胞增殖显像探针[1,2]。放射性核素标记胸苷用于检测细胞增殖早已成为生命科学领域内重要的研究手段,用于体外细胞实验的3H标记胸苷已近半个世纪,短半衰期核素11C(t1/2=20.4 min)标记胸苷用于荷瘤鼠PET显像实验则始于1978年Crawford等的研究[3]。1991年后,较长半衰期的理想核素18F(t1/2=109.6 min)标记胸苷类似物18F-FLT[4]、1-(2'-脱氧-2'-[18F ]氟-b-D-阿拉伯呋喃糖基)-5-甲基尿嘧啶(18F-FMAU)[5]和 2'-脱氧-2'-[18F]氟胸苷(18F-FT)[6],相继用于细胞增殖显像或基因显像,三者化学结构式见图1。目前,临床上18F-FLT PET/CT显像已广泛用于包括脑瘤和肺癌等的研究[2,7]。因此,有必要建立18F-FLT自动化生产方法以满足临床需要。

图1 胸苷及其18F标记类似物Fig.1 Thymidine and its 18F-labeled analogues.
18F-FLT自动化生产主要取决于放射化学合成和自动化合成模块。从1991年Wilson等[4]开始,根据标记前体化合物的结构类型,18F-FLT放化合成的第一步反应即亲核[18F]氟化标记可分为两大类:3-N-和5'-O-受保护的胸苷衍生物(I)为前体[8–10]和2,3'-脱水胸苷衍生物(II)为前体[11,12](图2)。其中(I)较好,优化放化产率的研究表明,其最佳结构为R1=Ns,R2= DMTr,R3=BOC[9,10],对应的化合物为3-N-t-叔丁氧羰基-5'-O-二甲氧基三苯基-3'-O-对硝基苯磺酰基-胸苷(BDNT)。目前,BDNT作为标记前体是18F-FLT自动化合成的首选,其放化产率可为20%–40%(因合成模块而异)[13–17]。然而,由于合成模块自身的局限性,现有18F-FLT自动化合成法存在反应条件不易控制、无连续多次合成的能力等缺点。
基于PET分子影像探针药物自动化合成法[18–20],本文以BDNT为标记前体,采用“一锅-两步”法,用升级改进的Explora GN模块和半制备HPLC分离纯化系统,完成亲核放射[18F]氟化反应、水解反应、分离纯化与质量控制,发展了18F-FLT的快速、稳定和高产率的自动化生产,实现18F-FLT的常规化生产。

图2 18F-FLT的两类前体化合物Fig.2 Two types of precursors of 18F-FLT.
1 实验材料和仪器
1.1 试剂与材料
前体3-N-t-叔丁氧羰基-5'-O-二甲氧基三苯基-3'-O-对硝基苯磺酰基-胸苷(BDNT)、参考品3'-脱氧-3'-[19F]氟胸苷(FLT),德国ABX公司产品;K222(Kryptofix 222)、无水乙腈和无水碳酸钾,美国Sigma- Aldrich公司产品;HPLC/光谱纯乙腈,美国TEDIA公司产品;富[18O]氧水,以色列Rotem公司产品。药用乙醇,南京化学试剂有限公司产品。醋酸钠、浓盐酸、甲醇和二氯甲烷等均为国产分析纯或光谱纯,购自国药集团上海化学试剂公司。所有化学药品均未进一步纯化,直接使用。
Sep-Pak Plus QMA和中性 Al2O3柱,美国Waters公司产品;GF254薄层层析硅胶板(2.5 cm×10.0 cm,玻璃基片),山东烟台汇友硅胶开发有限公司产品;MillexÒ-GS 0.22 mm 微孔过滤器,Milipore公司产品。
1.2 仪器
医用回旋加速器(Eclipse ST,40 mA×11 MeV)、18F正电子药物合成模块(Explora GN, 配有可编写合成控制软件)和半制备型高效液相色谱仪(HPLC,Explora LC, 配有紫外和放射性检测器),德国Siemens公司产品;ODS-BP C18半制备柱 (10 μm, 10×250 mm),中国大连依利特分析仪器公司产品;分析型 HPLC(1200系列),配有四元梯度泵、可变波长检测器、流式g放射性检测器(Gabi Star,德国 Raytest 公司)、Zorbax 300SB-C18 分析柱(4.6×250 mm, 5 mm)、真空脱气机和 ChemStation 色谱控制和分析软件,美国Agilent公司产品;放射性薄层色谱扫描仪(miniGita Star),配有BGO-V探头、miniGita仪器控制软件和GINA- Star TLC色谱分析软件,德国 Raytest 公司产品;超纯水制备系统(Synergy®UV),美国Milipore公司产品;放射性活度计(CRC®-15PET),美国Capintec公司产品。
2 实验内容
2.1 18F-FLT的放射化学合成路线
本文取BDNT为标记前体[9,13]和“一锅-两步”法,图3为18F-FLT的合成路线,包括前体BDNT的亲核放射[18F]氟化反应、水解反应、中和与分离纯化。具体过程如下:首先,干燥活化的18F离子与前体BDNT在无水乙腈中120oC加热氟化反应5 min,产生标记中间体 3-N-t-叔丁氧羰基-5'-O-二甲氧基三苯基-2'-脱氧-3'-[18F]氟胸苷(18F-BDFT);再加入盐酸溶液,110°C加热水解反应5 min;最后,加入醋酸钠溶液中和,经过 HPLC分离纯化即获得18F-FLT注射液。
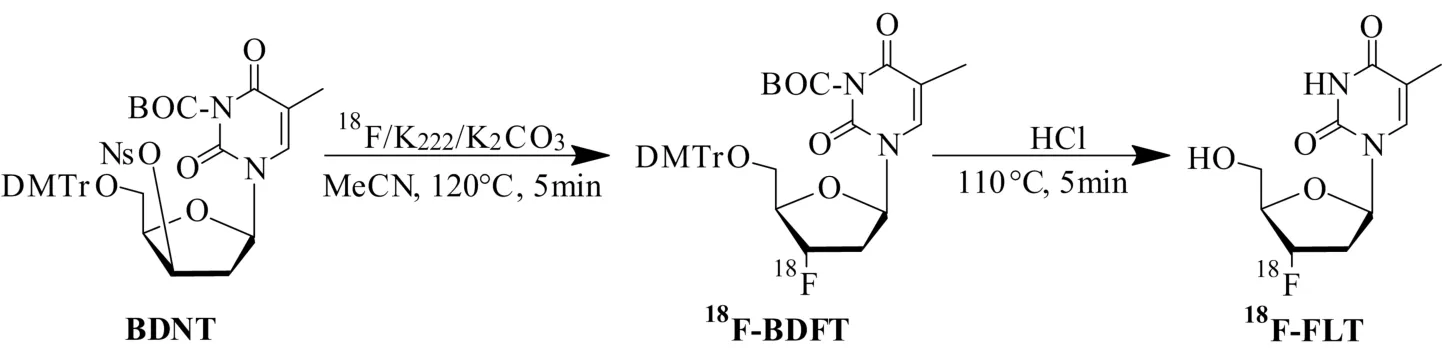
图3 18F-FLT的放射化学合成Fig.3 Radiochemical synthesis of 18F-FLT.
2.2 自动化合成模块
合成模块是经过升级改进即配有Explora LC分离系统的 Explora GN模块,其详细结构参见文献[21]。其中,Explora GN是多功能18F标记PET显像探针药物的自动化合成模块,具有连续多次合成的特点。Explora LC是集成化半制备HPLC分离系统,适合安装于屏蔽热室内,而且自身配有紫外和放射性检测器,方便用于放射性药物的分离纯化。
2.3 18F-FLT的自动化合成
运行合成模块的自动化清洗程序,进行模块准备工作。将各种反应试剂、试剂瓶和预处理后的QMA柱和Al2O3柱等放置于对应位置,正确连接,并进行压力和真空测试。准备就绪,关闭热室,运行预先编写的18F-FLT自动化合成程序,控制合成模块执行所有自动化合成步骤。
18F-FLT的自动化合成过程如下:质子轰击后,用N2压力使含有18F离子的富[18O]氧水通过QMA柱,18F离子被吸附而留在柱上,富[18O]氧水被收集到回收瓶中;定量转移1.2 mL K222/K2CO3的乙腈-水溶液(K222: 15.0 mg/mL, K2CO3: 2.75 mg/mL, 乙腈:水=39:1 (V/V)),淋洗QMA柱,18F离子的洗脱液收集在反应瓶中;100ºC加热,通气鼓泡,蒸发吹干,除去溶剂;再加入1.5 mL无水乙腈,110ºC加热,通气鼓泡,蒸发吹干,完全除去水分;转移前体BDNT(30.0 mg)的无水乙腈溶液(1.0 mL)到反应瓶内,120ºC加热回流5.0 min,进行放射氟化反应。反应液被冷却后,转移 2.0 mL HCl溶液(1.0 mol/L)到反应瓶中,110ºC加热回流5.0 min,完成水解反应。冷却反应液后,加入3.5 mL NaOAc溶液(1.0 mol/L)进行中和。将18F-FLT反应混合物溶液过 Al2O3柱和微孔过滤器(0.45 mm, 水相),收集在HPLC进样器内,体积约5.0 mL。
2.4 18F-FLT的分离纯化
启动HPLC进样器,将其中18F-FLT粗产品溶液注射到5.0 mL进样环内。运行Explora LC程序,开始18F-FLT的分离纯化,其条件是:流动相为药用乙醇:水=10:90 (V/V),流速为3.0 mL/min,分离柱为半制备反相ODS-BP C18柱。18F-FLT的保留时间为20.0 min,收集时间在19.5–21.5 min。所得组份峰溶液经过0.22 μm无菌过滤器,收集在产品瓶,即获得无色、透明的18F-FLT注射液。
2.5 18F-FLT的质量控制
开展如下实验,评价18F-FLT溶液的质量控制指标。分析型 HPLC和放射性薄层扫描色谱(radio-TLC)用于测定18F-FLT的放射化学纯度和化学纯度。HPLC流动相是乙腈:水=10:90(V/V),流速为1.0 mL/min,分析柱为Zorbax 300SB-C18柱,采取260 nm UV和放射性检测器。radio-TLC的展开剂是三氯甲烷:甲醇=4:/1(V/V),薄层板为GF254硅胶板。用HPLC测定18F-FLT的比活度,检测其3个半衰期内的放射化学纯度,检验其稳定性。目测其外观颜色和澄清度,用精密pH试纸测pH值,TLC层析和碘蒸汽显色法检测K222。参考2005年版国家药典进行异常毒性实验、细菌内毒素实验、无菌实验等。
3 结果与讨论
本文以BDNT为标记前体,基于“一锅-两步”法,利用经过升级改进即配有HPLC分离系统的Explora GN模块,发展了18F-FLT的自动化生产方法,其主要参数与实验结果见于表1。该方法合成18F-FLT的总时间小于65 min,放射化学产率为15%–25%(未衰减校正,n>20),放射化学纯度大于99%,满足了18F-FLT的常规临床肿瘤PET/CT显像诊断的需求。
18F-FLT自动化合成的首要条件是其成功的放射化学合成路线。目前,成功用于18F-FLT合成的标记前体化合物主要分为(I)和(II)两大类(图2),其选择决定了18F-FLT的放化合成路线和产率高低。化合物(II)为标记前体时,通常反应条件较为苛刻(DMSO为溶剂、加热温度高达160ºC),18F-FLT的放化产率<10%[11,12],故很少被自动化合成法采用[22]。大量研究表明,化合物(I)、特别是BDNT(结构式中R1=Ns, R2=DMTr, R3= BOC)是18F-FLT理想的标记前体,成为发展18F-FLT自动化合成法的首选,其反应条件温和(乙腈为溶剂、温度通常为110–130ºC),放化产率高(20%–40%)[8–10,13–17]。进一步优化BDNT为前体的实验发现,BDNT用量和碱K2CO3用量是影响18F-FLT放化产率的主要因素[10,23]。Suehiro等[23]报道,BDNT与K2CO3摩尔比大于1.5,18F-FLT的产率趋于饱和而稳定。我们的前期实验发现,K2CO3用量不变,BDNT为10–15 mg时,18F-FLT的产率低且不稳定;而为30 mg时,产率高并且稳定。因此,本文中BDNT和K2CO3的用量分别为30 mg和3.3 mg,其摩尔比为1.5,18F-FLT的放化产率为15%–25%(未衰减校正),以(4.44–5.55)×1010Bq的18F离子开始,其典型产量为(0.74–1.11)×1010Bq18F-FLT。
18F-FLT的自动化合成还依赖于合适的放射性药物化学合成模块。到目前为止,以BDNT为起始反应物,已有多种商品化模块被用于18F-FLT自动化合成,它们的主要参数和结果见表1。然而,Oh等[13]使用的TracerLab Mx模块无冷却功能,[18F]氟化反应需先高温-后低温的两阶段加热,并于结束后先将反应液转移到相邻的注射器内以降低压力,使其步骤多并导致放射性残留损失。其它模块的主要局限性是不能连续多次合成,一次试剂准备,只能进行单次合成[14–16]。本文采取的Explora GN模块具备快速加热升温和冷却、及多次定量转移、添加试剂的能力,具有多次合成18F-FLT的优势。另外,分离纯化功能是自动化合成模块的重要组成部分。根据所用模块的特点,不同作者使用了HPLC[13,14]或固相萃取(SPE)分离纯化18F-FLT[15,16]。Bourgeois等[24]认为,HPLC分离纯化18F-FLT最为可靠,各项指标均严格符合临床用放射性药物的质量标准。我们的实验表明,18F-FLT合成过程中产生大量化学杂质,进行HPLC时须仔细检验流动相,以免杂质混入产品18F-FLT溶液(图4)。例如,流动相为乙醇:水=20:80(V/V)时,保留时间为9.5 min,产品18F-FLT的放射性峰与杂质的紫外峰紧密相连(图4a);流动相为10/90(V/V)时,保留时间延长为20.0 min,则产品峰与相邻杂质峰完全分开(图4b),充分保证了18F-FLT的化学纯度。
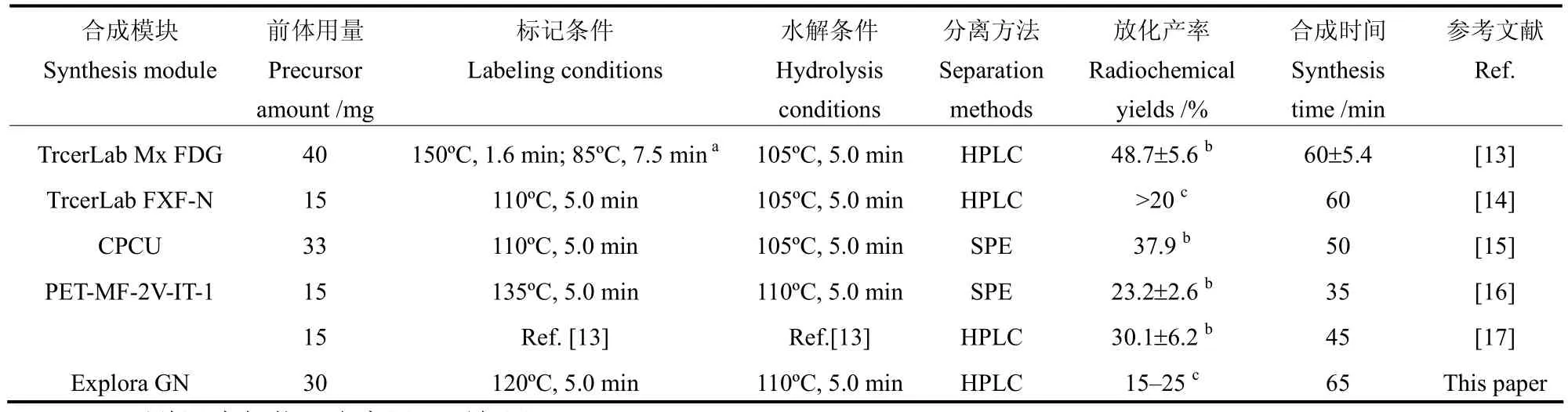
表1 18F-FLT各种自动化合成的主要参数与结果 (BDNT为前体)Table 1 Major parameters and results of various automated syntheses of 18F-FLT (BDNT as precursor)
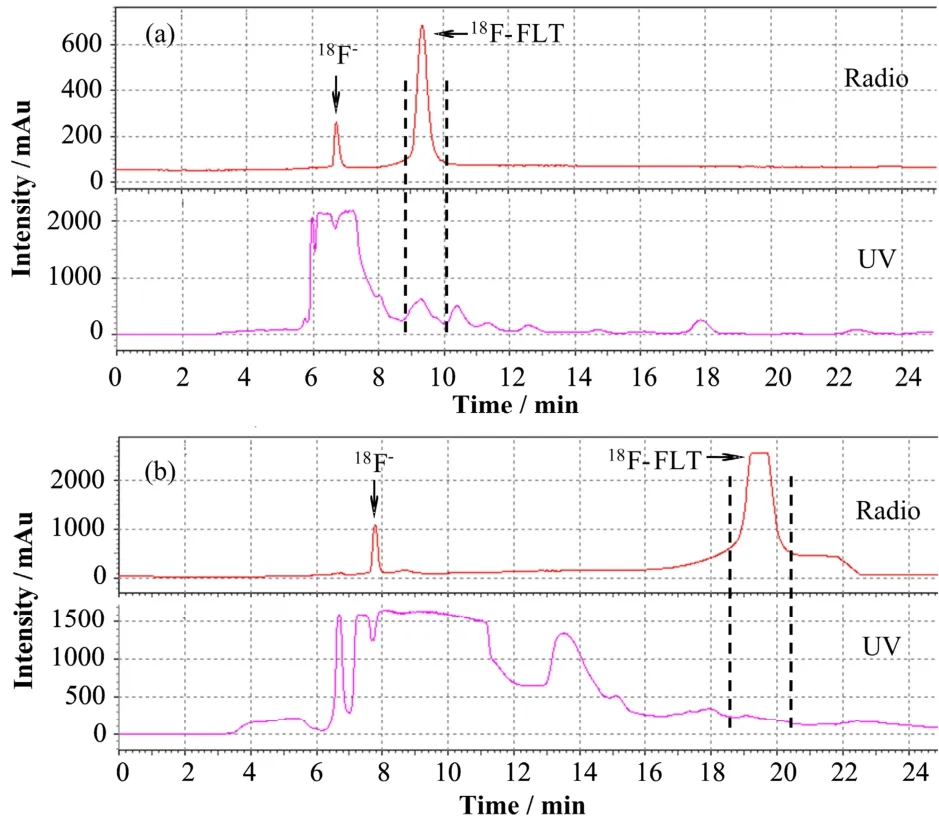
图4 18F-FLT分离的半制备HPLC谱图。流动相乙醇:水的体积比为20:80 (a) 和 10:90 (b)Fig.4 Semipreparative HPLC of 18F-FLT separation.EtOH/H2O in 20/80 (a) and 10/90 (b) as mobile phase.
18F-FLT注射液的各项质量控制指标均符合临床放射性药物的质控要求,具体实验结果如下。HPLC和radio-TLC的结果显示,18F-FLT的放射化学纯度大于99%,对应的保留时间和比移植分别为6.2 min(图5a)和0.58(图5c),前者与参考标准品FLT的保留时间一致(图5d)。HPLC的UV色谱进一步表明其化学纯度高(图5b),除了容积峰以外,没有其它化学杂质存在。18F-FLT注射液外观呈无色透明,pH 值为 7.0,比活度为(2.32±0.27)×1014Bq/mmol,放射性浓度大于 1.11×109Bq/mL。经过HPLC检验,18F-FLT注射液的稳定性良好,3个半衰期之内放射化学纯度没有明显变化。细菌内毒素实验和无菌实验结果均为阴性,异常毒性实验结果正常,所有实验动物均无异常行为表现。
4 结论
利用升级改进的Explora GN模块和半制备HPLC,采取基于标记前体BDNT的“一锅-两步”法的放射化学合成路线,我们发展了18F-FLT的自动化生产方法。18F-FLT的总合成时间小于65 min,放射化学产率为15%–25%(未衰减校正,n>20),放射化学纯度大于99%,并具有很高的化学纯度和比活度。该方法实现了18F-FLT快速、稳定和高产率的自动化生产,又具有连续多次合成的能力,将会大大方便18F-FLT临床应用、特别有利于其多中心临床研究的大量药物配送。
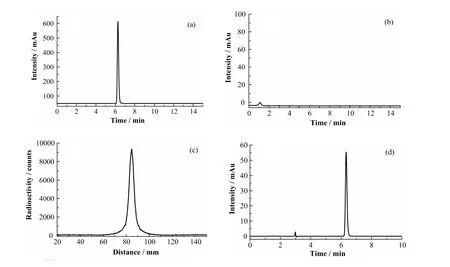
图5 18F-FLT注射液的分析型HPLC (放射性信号(a)和紫外信号(b))和radio-TLC ((c), 展开距离为50–110 mm) 图谱和标准品FLT的HPLC图谱(d)Fig.5 Analytical HPLC spectrums of the 18F-FLT radioactive trace (a) and UV trace (b), the radio-TLC (c) with 50–110 mm as developing distance, and HPLC spectrum of standard FLT(d).
1 Vallabhajosula S.18F-Labeled positron emission tomographic radiopharmaceuticals in oncology: an overview of radiochemistry and mechanisms of tumor localization [J].Semin Nucl Med, 2007, 37(6):400–419
2 Salskov A, Tammisetti V S, Grierson J, et al.FLT:measuring tumor cell proliferation in vivo with PET and 3¢-Deoxy-3¢-[18F]fluorothymidine [J].Semin Nucl Med,2007, 37(6):429–439
3 Crawford E J, Christman D, Atkins H, et al.Scintigraphy with positron-emitting compounds—I.carbon-11 labeled thymidine and thymidylate [J].Int J Nucl Med Biol, 1978,5(2-3):61–69
4 Wilson I K, Chatterjee S, Wolf W.Synthesis of 3′-fluoro-3′-deoxythymidine and studies of its18F-radiolabeling, as a tracer for the noninvasive monitoring of the biodistribution of drugs against AIDS[J].J Fluorine Chem, 1991, 55(3): 283–289
5 Alauddin M M, Shahinian A, Park R, et al.Synthesis and evaluation of 2'-deoxy-2'-18F-fluoro-5-fluoro-1-beta-D-arabinofuranosyluracil as a potential PET imaging agent for suicide gene expression [J].J Nucl Med, 2004,45(12):2063–2069
6 Sun W, Wilson J, Kumar P.Radiosynthesis of 2’-deoxy-2’-[18F]fluorothymidine ([18F]FT), a putative PET agent for imaging HSV-TK expression [J].Curr Radiopharm,2009, 2(1), 75–82
7 Been L B, Suurmeijer A J H, Cobben D C P, et al.[18F]FLT-PET in oncology: current status and opportunities [J].Eur J Nucl Med Mol Imaging, 2004,31(12): 1659–1672
8 Grierson J R, Shields A F.Radiosynthesis of 3'-deoxy-3'-[18F]fluorothymidine: [18F]FLT for imaging of cellular proliferation in vivo [J].Nucl Med Biol, 2000, 27(2):143–156
9 Martin S J, Eisenbarth J A, Wagner-Utermanna U, et al.A new precursor for the radiosynthesis of [18F]FLT [J].Nucl Med Biol, 2002, 29(2): 263–273
10 Yun M, Oh S J, Ha H-J, et al.High radiochemical yield synthesis of 3′-deoxy-3′-[18F]fluorothymidine using (5′-O-dimethoxytrityl-2′-deoxy-3′-O-nosyl-β-D-threo pentofuranosyl)thymine and its 3-N-BOC-protected analogue as a labeling precursor [J].Nucl Med Biol, 2003, 30(2):151–157
11 Machulla H J, Blocher A, Kuntzsch M, et al.Simplified labeling approach for synthesizing 3´-deoxy-3´-[18F]fluorothymidine ([18F]FLT) [J].J Radioanal Nucl Chem, 2000, 243(3): 843–846
12 Blocher A, Kuntzsch M, Wei R, et al.Synthesis and labeling of 5'-O-(4,4'-dimethoxytrityl)-2,3'-anhydrothymidine for [18F]FLT preparation [J].J Radioanal Nucl Chem, 2002, 251(1): 55–58
13 Oh S J, Mosdzianowski C, Chi D Y, et al.Fully automated synthesis system of 3′-deoxy-3′-[18F]fluorothymidine [J].Nucl Med Biol, 2004, 31(6): 803–809
14 唐刚华, 唐小兰, 王明芳, 等.一锅法自动化合成 3′-脱氧-3′-18F-氟代胸苷和 O-(2-18F-氟代乙基)-L-酪氨酸[J].核技术, 2009, 32(2): 154–160 TANG Ganghua, TANG Xiaolan, WANG Mingfang, et al.Automated synthesis of 3′-deoxy-3′-[18F]fluorothymidine and O-(2-18F-fluoroethyl-L-tyrosine as tumor imaging agents [J].Nucl Tech, 2009, 32(2): 154–160
15 Tand G, Tang X, Wen F, et al.A facile and rapid automated synthesis of 3′-deoxy-3′-[18F]fluorothymidine[J].Appl Radiat Isot, 2010, 68(9): 1734–1739
16 Teng B, Wang S, Fu Z, et al.Semiautomatic synthesis of 3′-deoxy-3′-[18F]fluorothymidine using three precursors[J].Appl Radiat Isot, 2006, 64(2): 187–193
17 张锦明, 张晓军, 李云钢, 等.双管 18F多功能合成模块的研究[J].中华核医学杂志, 2010, 30(6):410–413 ZHANG Jinming, ZHANG Xiaojun, LI Yungang, et al.Research on multifunctional18F synthesis module with two vessels [J].Chin J Nucl Med, 2010, 30(6):410–413
18 王明伟, 章英剑, 张勇平, 等.基于Explora FDG4模块的18F-FMISO的自动化合成[J].核技术, 2008, 31(6):460–464 WANG Mingwei, ZHANG Yingjian, ZHANG Yongping,et al.Automated synthesis of18F-FMISO using Explora FDG4 module [J].Nucl Tech, 2008, 31(6):460–464
19 王明伟, 章英剑, 张勇平, 等.肿瘤分子显像剂18F-氟乙基胆碱的自动化合成[J].核技术, 2008, 31(11):859–863 WANG Mingwei, ZHANG Yingjian, ZHANG Yongping,et al.Automatic synthesis of18F-FeCH as molecular imaging agent for tumor diagnosis [J].Nucl Tech, 2008,31(11): 859–863
20 王明伟, 章英剑, 张勇平, 等.乳腺癌雌激素受体分子影像探针 16a-[18F]氟-17b-雌二醇的自动化合成[J].核技术, 2009, 32(11): 839–844 WANG Mingwei, ZHANG Yingjian, ZHANG Yongping,et al.Automated synthesis of 16a-[18F]fluoro-17b-estrogen as estrogent receptor imaging probe of breast cancer [J].Nucl Tech, 2009, 32(11): 839–844
21 张勇平, 章英剑, 王明伟, 等.基于 Explora GN/LC双模块的 16a-[18F]氟-17b-雌二醇全自动化合成[J].中华核医学杂志, 2011, 31(3):196–200 ZHANG Yongping, ZHANG Yingjian, WANG Mingwei,et al.Fully automated synthesis of 16a-[18F]fluoro-17b-estradial using Explora GN/LC dual module [J].Chin J Nucl Med, 2011, 31(3):196–200
22 Nandy S K, Rajan M G R.Fully automated and simplified radiosynthesis of [18F]-3′-deoxy-3′-fluorothymidine using anhydro precursor and single neutral alumina column purification [J].J Radioanal Nucl Chem, 2010, 283(3):741–748
23 Suehiro M, Vallabhajosula S, Goldsmith S S, et al.Investigation of the role of the base in the synthesis of[18F]FLT [J].Appl Radiat Isot, 2007, 65(12): 1350–1358
24 Bourgeois M, Mougin-Degraef M, Leost F, et al.Purification of [18F]-fluoro-l-thymidine ([18F]-FLT) for positron emission tomography imaging [J].J Pharm Biomed Anal, 2007,45(1): 154–157

