功能性消化不良患者胃排空与症状的相关性及影响因素分析
李妮矫,姚树坤,张艳丽,符 思,王 微
1.北京中医药大学,北京 100029;2.卫生部中日友好医院消化内科;3.卫生部中日友好医院中医消化科
功能性消化不良(functional dyspepsia,FD)是指存在一种或者多种起源于胃十二指肠区域的以上腹痛、上腹饱胀感、上腹烧灼感、早饱、恶心为主要症状,并且缺乏能够解释这些症状的任何器质性或代谢性疾病。23%~59%的 FD患者存在胃排空延缓[1,2],但多数研究没有找到胃排空延缓与消化不良症状之间的确切联系。本研究的目的在于了解胃排空异常与消化不良症状的相关性,分析影响功能性消化不良患者胃排空的因素。
1 对象与方法
1.1 研究对象 2009年7月~2010年7月就诊于中日友好医院,按照罗马Ⅲ诊断标准确诊为 FD的患者32例,男 15例,女17例;平均年龄(41.00+13.54)岁;平均体质量指数(BMI)(20.35+3.33)kg/m2。
1.2 仪器 γ照相机(Mellennium Hawkeye,GE, USA),140千电子伏能峰,50%窗宽,1.5倍放大倍数,低能通用型准直器。
1.3 标准试餐成分及制备 参考国际推荐的标准固体低脂试餐,其成分包括 65 g油煎鸡蛋、95 g非油炸方便面,植物油10 g,用500 m L沸水冲泡。标准试餐的营养成分构成为:碳水化合物42%、蛋白质 10%、脂肪8%,总热量为500 Kcal。油煎鸡蛋的制备过程:将新鲜生鸡蛋1只(60 g)去壳放入一次性纸杯中,向鸡蛋黄中注入标记有99mTc-DTPA的2 mCi,静置约2min后将生鸡蛋充分搅匀,放入不粘锅用 5 g花生油煎熟成饼状,并切成约 2 cm大小,放入泡好的方便面中。
1.4 方法 受试者在10 min内摄入标准试餐,进食完后立即仰卧于检查床上,使用 γ照相机采集第一帧图像(前后位图像),之后每15m in采集1帧,共9帧(2 h)。观察指标:半排空时间(T1/2)、1 h残留率(Retention%1 h)、2 h残留率(Retention%2 h),诊断标准参考美国胃肠动力学会、神经胃肠学会及核医学联合推荐的标准。分别量化记录餐后上腹饱胀、上腹痛、上腹烧灼感、早饱、嗳气、恶心、呕吐 7组症状得到相应的症状指数,测量胃排空检查完毕时静息状态的坐位心率两次,取平均值。
1.5 统计学方法 采用Pearson相关及Spearman秩相关检验胃排空指标与各因素的相关性,非条件 Logistic回归分析各因素对胃排空指标的影响。根据心率的中位数将其转化为二分类变量进行非条件Logistic回归分析统计,P<0.05为差异有统计学意义。
2 结果
2.1 总体情况 32例患者中,8例(25%)T1/2延迟, 24例T1/2正常,7例(21.88%)Retention%2 h增加, Retention%1 h均在正常范围内。
2.2 胃排空指标与消化不良症状之间的关系 Retention%2 h升高组较Retention%2 h正常组恶心指数升高(P=0.003)。Retention%2 h与恶心(r=0.527, P=0.002)呈正相关。恶心(OR=2.267,P=0.119)是Retention%2 h增加的独立因素。
2.3 胃排空指标与心率之间的关系 T1/2延长组较T1/2正常组心率快(P=0.022,见图1);Retention%2 h升高组较Retention%2 h正常组心率快(P=0.031,见图2);心率与T1/2(r=0.423,P=0.016)、Retention%2 h(r=0.448,P=0.01)均呈正相关,心率>70 bpm是T1/2延长(OR=8.180,P=0.072)、Retention%2 h(OR =12.378,P=0.042)增加的独立因素。
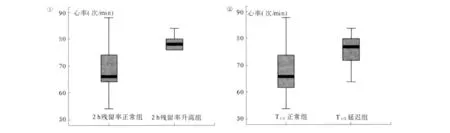
图 1 2h残留率正常组与异常组静息心率的差异;图 2 半排空时间正常组与异常组静息心率的差异Fig 1 Difference of heart rate between normal Retention%2 h and rised Retention%2 h groups;Fig 2 Difference of heart rate between norma l T 1/2 and p ro longed T1/2 groups
3 讨论
胃排空是指胃内容物通过幽门进入到十二指肠的动力过程。在除外消化道机械性梗阻存在的情况下,胃半排空时间、2 h残留率或 4 h残留率超过正常范围被定义胃胃排空延迟,或胃轻瘫。Tack等[3]的研究发现胃排空延缓与早饱、恶心、呕吐、上腹饱胀症状相关,他在另一项研究[4]中发现与胃排空延迟相关的消化不良症状常常联合成组出现,这些成组出现的组合是: a.恶心、呕吐、早饱及体质量减轻;b.餐后饱胀及胃胀气。本研究发现恶心与胃排空指标呈正相关,恶心是胃排空延缓的独立影响因素,FD病人出现恶心提示胃排空延缓,症状在一定程度上反映了 FD的病理生理学机制,与既往的研究相符。
在动物模型和临床研究中发现,迷走神经损伤会导致胃排空障碍及严重胃潴留[5]。糖尿病患者常存在胃排空障碍[2,6,7],尤其是病程较长者,约 50%病程超过 3年的糖尿病患者存在胃排空延缓[8-10],其中出现自主神经病变症状是这些糖尿病患者出现胃排空延缓的独立预测因素[11-14],研究已经发现 FD患者存在自主神经功能的异常[15],FD病人存在迷走神经张力的降低,交感神经张力增高[16]。Hauskne等[17]发现FD患者迷走神经张力较健康人低,应激时健康组出现反射性胃窦运动降低,而FD患者缺乏这种正常反应。
本研究发现T1/2、Retention%2 h与胃排空检查当时的静息心率呈正相关,而且较高的心率是胃排空延缓的一个独立影响因素。正常机体为适应不同生理需要,自主神经处于动态平衡的调节状态—迷走/交感平衡状态。睡眠、卧位及安静时迷走神经水平高,迷走/交感张力比升高,觉醒、直立位、应激时迷走神经张力下降,迷走/交感张力比降低。迷走/交感升高时,迷走神经张力增高,心率较低,胃肠运动兴奋,消化腺体分泌旺盛;而当交感神经张力升高或迷走神经功能受损时,迷走/交感降低,心率上升、消化腺体分泌减少,胃肠运动减慢。本研究发现 FD患者心率与T1/2、Retention%2 h呈正相关,且心率升高是胃排空延缓的一个独立影响因素,较高心率代表着较高交感张力,这一结果提示胃排空延缓的FD患者较胃排空正常的患者迷走/交感比值下降,存在交感神经张力升高或迷走神经功能受损。因此,存在胃容受性功能受损或胃排空功能受损的 FD患者有着共同的病理生理基础,均存在自主神经功能障碍。对FD患者进行自主神经功能的检测,可全面了解患者的胃肠功能状态,对个体化治疗有较大的指导意义。
[1]Mimidis K,Tack J.Pathogenesis of dyspepsia[J].Dig Dis,2008, 26(3):194-202.
[2]Talley NJ,Verlinden M,Jones M.Can symptoms discrim inateamong those with delayed or normal gastric emptying indysmotility-like dyspepsia[J]?Am JGastroenterol,2001,96(5):1422-1428.
[3]Tack J,Bisschops R,Sarnelli G.Pathophysiology and treatment of functional dyspepsia[J].Gastroenterology,2004,127(4): 1239-1255.
[4]Fischler B,Tack J,De GuchtV,et al.Heterogeneity of symptom pattern,psychosocial factors,and pathophysiological mechanisms in severe functionaldyspepsia[J].Gastroenterology,2003,124(4):903-910.
[5]Wang Y,Kondo T,Suzukamo Y,et al.Vagal nerve regulation isessential for the increase in gastricmotility in response tom ild exercise[J]. Tohoku JExp Med,2010,222(2):155-163.
[6]Rabine JC,Barnett JL.Managementof the patientwith gastroparesis[J]. JClin Gastroenterol,2001,32(1):8-11.
[7]Jones KL,Russo A,Stevens JE,et al.Predictors of delayed gastric emptying in diabetes[J].DiabetesCare,2001,24(7):1264-1269.
[8]HorowitzM,Harding PE,Maddox A,et al.Gastric and oesophageal emptying in insulin dependent diabetesmellitus[J].J Gastroenterol Hepatol,1986,1(2):97-113.
[9]Keshavarzian A,Iber FL,Vaeth J.Gastric emptying in patients with insulin-requiring diabetesmellitus[J].Am JGastroenterol,1987,82 (1):29-35.
[10]Lartigue S,Bizais Y,Bruley S,etal.Inter-and intrasubjectvariability ofsolid and liquid gastricemptying parameters-a scintigraphic study in healthy subjectsand diabetic patients[J].Dig Dis Sci,1994,39 (1):109-115.
[11]Feldmann M,Schiller LR.Disorders of gastrointestinal motility associated with diabetesmellitus[J].Ann Intern Med,1983,98(3): 378-384.
[12]Barnett JL,Owyang C.Serum glucose concentration as amodulator of interdigestive gastric motility[J].Gastroenterology,1988,94(3): 739-744.
[13]Fraser R,Horowitz M,Dent J.Hyperglycaemiastimulates pyloricmotility in normal subjects[J].Gut,1991,32(2):475-478.
[14]Jones KL,Russo A,Stevens JE,et al.Predictors of delayed gastric emptying in diabetes[J].Diabetes Care,2001,24(7): 1264-1269.
[15]Zhou CY,Hu FP,HeWQ.Autonomic function test in patients with functional dyspepsia[J].Clinical Focus,2000,3(5):412.
周成元,胡飞鹏,贺卫权.功能性消化不良患者植物神经功能状态的检测[J].临床荟萃,2000,3(5):412.
[16]Hveem K.Effect ofmental stress and cisapride on autonom ic nerve functions in functional dyspepsia[J].Scand JGastroenterol,1998, 33(2):123-127.
[17]Hauskne T.Low vagual tone and antral dysmortility in patients with functional dyspepsia[J].Psychosom Med,1993,55(1):12.

