盐酸倍他司汀含量测定的不确定度分析
杨迎东 张慧文
盐酸倍他司汀含量测定的不确定度分析
杨迎东 张慧文
目的 通过分析盐酸倍他司汀含量测定的不确定度,使盐酸倍他司汀含量测定方法受控。方法 通过建立数学模型,分析出影响盐酸倍他司汀含量测定的不确定度的因素,并评估各个分量的不确定度,计算合成的不确定度,最终获得测定结果的扩展不确定度和置信水平,记录相关数据,进行统计学分析。结果 氢氧化钠滴定液浓度的不确定度为±0.000083mol/L,按均匀分布换算成标准偏差为 0.000083√3 =0.000048mol/L;供试品称样量W盐酸倍他司汀的不确定度±0052mg,重复性不确定度为±0.07mg,两项合成的不确定度为:UC[W盐酸倍他司汀]=[(0.052)2+(0.07)2]1/2=0.088mg;滴定液消耗的体积的不确定度为±0.001ml,按均匀分布换算成标准偏差为0.001√3=0.00058ml;水分的不确定度为±0.00001,UC[G]=0.0000√3 =0.0000058,G对盐酸倍他司汀含量的不确定度影响最大,其次为C(NaOH)和W盐酸倍他司汀,对比V对盐酸倍他司汀含量的不确定度的影响差异显著(P<0.05),具有统计学意义。结论 建立不确定度评估方法对于评估使用电位滴定法测定盐酸倍他司汀含量的不确定度有重要的意义。
盐酸倍他司汀;含量测定;不确定度;数学模型
盐酸倍他司汀(BETAHISTINE HYDROCHLORIDE),属于血管扩张药,主要用于治疗内耳眩晕症(梅尼埃综合征)、脑供血不足引起的眩晕、头晕、呕吐或耳鸣等。为了使测量数据的表达、处理及质量评定等方面更科学、准确,并根据中国实验室国家认可委员会对认可实验室在测量不确定度方面的要求,应用电位滴定法对盐酸倍他司汀含量的不确定度进行测量与评估,通过建立数学模型,分析出影响盐酸倍他司汀含量测定的不确定度的因素,并评估各个分量的不确定度[1],为检验报告提高科学依据,最终获得测定结果的扩展不确定度和置信水平,从而提高检测结果表达的准确性及客观性。本文通过通过分析盐酸倍他司汀含量测定的不确定度,使盐酸倍他司汀含量测定方法受控。总结如下。
1 资料与方法
1.1 一般资料 选用盐酸倍他司汀为N-甲基-2-吡啶乙胺酸盐。按干燥品计算,含C8H12N2·2HCl不得少于98.0%,乙醇为分析纯及由河北省药品检验所标定0.1002mol/L的0.1mol/L氢氧化钠滴定液,分别使用由瑞士Mettler toledo公司生产DL50型自动电位滴定仪、AE240型电子天平及V30型卡尔费休水分测定仪,通过建立数学模型,分析出影响盐酸倍他司汀含量测定的不确定度的因素,并评估各个分量的不确定度,计算合成的不确定度,最终获得测定结果的扩展不确定度和置信水平,记录相关数据,进行统计学分析。
1.2 方法
1.2.1 测定法 精密称取0.1g盐酸倍他司汀,加入乙醇50ml,使之溶解,按照电位滴定法(《中国药典》2005版附录ⅦA),使用0.1002mol/L氢氧化钠滴定液滴定至第2个突跃点,并用空白试验对滴定结果校正,每1毫升0.1mol/L氢氧化钠滴定液相当于10.46mg的C8H12N2·2HCl[2]。
1.2.2 数学建模 盐酸倍他司汀含量计算公式为:盐酸倍他司汀含量(%)=U[盐酸倍他司汀含量(%)]/盐酸倍他司汀含量(%)=[V(氢氧化钠)×C(氢氧化钠)×T(D)]×100%/W盐酸倍他司汀×0.1×(1-G)。注:W盐酸倍他司汀为盐酸倍他司汀的试品称样量,C(氢氧化钠)为氢氧化钠滴定液浓度,V(氢氧化钠)为滴定液消耗的体积[3]。
1.2.3 识别分析各量值的不确定度 (1)滴定液消耗的体积的不确定度:①校准不确定度,自动电位滴定仪检定证书给出的测量体积的不确定度为0.001ml,滴定液的平均消耗体积为9.48ml;②温度,滴定时严格控制实验室温度,故温度对结果的影响可忽略不计;③仪器终点检测,该方法的终点检测采用自动电位滴定仪对结果进行终点判断,其计量证书中给出电位值扩展不确定度为U95=0.05%,由于电位突跃几十毫伏到几百毫伏,仪器校准的不确定度对终点检测的影响非常小,可忽略不计。(2)氢氧化钠滴定液浓度的不确定度;(3)供试品称样量W盐酸倍他司汀的不确定度;(4)水分的不确定度。以上量值均按均匀分布换算成标准偏差,套入数学模型计算出U[盐酸倍他司汀含量(%)],从而算出相对扩展不确定度[4]。
1.3 统计学方法 本组数据采用SPSS13.0统计学软件进行处理,计量单位采用±s表示,组间比较采用均数t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 盐酸倍他司汀含量的不确定度的有关量值计算
氢氧化钠滴定液浓度的不确定度为±0.000083mol/L,按均匀分布换算成标准偏差为0.000083√3=0.000048mol/L;供试品称样量W盐酸倍他司汀的不确定度±0052mg,重复性不确定度为±0.07mg,两项合成的不确定度为:UC[W盐酸倍他司汀]= [(0.052)2+(0.07)2]1/2=0.088mg,平均称样量为100.2mg;滴定液消耗的体积的不确定度为±0.001ml,按均匀分布换算成标准偏差为0.001√3=0.00058ml;水分的不确定度为±0.00001,UC[G]= 0.0000√3=0.0000058。G对盐酸倍他司汀含量的不确定度影响最大,其次为C(NaOH)和W盐酸倍他司汀,对比V对盐酸倍他司汀含量的不确定度的影响差异显著(P<0.05),具有统计学意义。见表1。
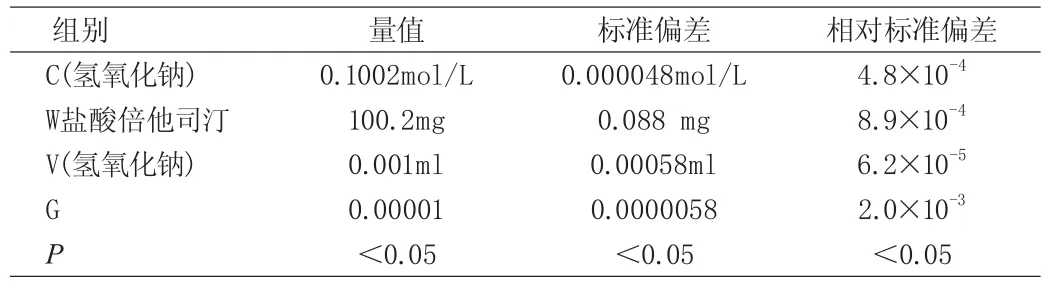
表1 盐酸倍他司汀含量的不确定度的有关量值
由表1可计算:盐酸倍他司汀含量(%)=(9.48×0.1002×10.46)/ [100.2×0.1×(1-0.1)%]×100%=99.26%;U[盐酸倍他司汀含量(%)]/盐酸倍他司汀含量(%)=[(4.8×10-4)2+(8.9×10-4)2+(6.2×10-5)2+(2.0×10-3)2]1/2=2.3×10-2;U[盐酸倍他司汀含量(%)]= 2.3×10-2×99.26%=0.23%。
2.2 扩展不确定度计算
取置信概率为95%,由分布确定包含因子k=2,相对扩展不确定度=相对合成标准不确定度×包含因子=2×0.23%=0.46%;盐酸倍他司汀含量(%)测量结果=99.3%±0.5%,k=2。
3 讨论
电位滴定法是在滴定过程中通过测量电位变化以确定滴定终点的方法,和直接电位法相比,电位滴定法不需要准确的测量电极电位值,因此,温度、液体接界电位的影响并不重要,其准确度优于直接电位法,普通滴定法是依靠指示剂颜色变化来指示滴定终点,如果待测溶液有颜色或浑浊时,终点的指示就比较困难,或者根本找不到合适的指示剂。电位滴定法是靠电极电位的突跃来指示滴定终点。在滴定到达终点前后,滴液中的待测离子浓度往往连续变化n个数量级,引起电位的突跃,被测成分的含量仍然通过消耗滴定剂的量来计算。电位滴定法具有操作简便、设备简单、人为误差小及精确度高等优点,使用电位滴定法测定盐酸倍他司汀的含量,可提升结果的准确性及客观性[5]。本文的测定过程中由电子天平、自动电位滴定仪、滴定液、水分仪及重复性测定引入的不确定度进行评估,为了减少工作量,在实际应用的过程中,可事先估算出各分量所占的比例,并去掉一些比例较小的分量,将重点转移为对不确定度贡献较大的分量的评定上,如文中在盐酸倍他司汀含量测定的不确定度的有关分量中贡献最大是G,其次是C(NaOH)和W盐酸倍他司汀,V对不确定度的影响最小,表明在盐酸倍他司汀含量测定过程中,应严格控制水分的测定结果,可减小对含量测定结果的影响。
综上所述,建立不确定度评估方法对于评估使用电位滴定法测定盐酸倍他司汀含量的不确定度有重要的意义。
[1]国家药典委员会.中华人民共和国药典二部[M].北京:化学工业出版社,2005:162.
[2]中华人民共和国国家计量技术规范.测量不确定度评定与表示[S]. JJF:1059-1999.
[3]佘伟鸣.药品检验中测量不确定度的评定[J].中国新药杂志,2003,12(9):775.
[4]梁春慧,宋更申.盐酸倍他司汀含量测定的不确定度评估[J].制剂与技术,2010,17(26):121-122.
[5]魏昊编.化学分析中不确定度的评估指南[M].北京:中国计量出版社,2002:20-28.
10.3969/j.issn.1009-4393.2011.18.021
510800 广州市花都区新华社区卫生服务中心 (杨迎东) 广州市药品检验所 (张慧文)