人参消渴胶囊中人参皂苷Rg1和人参皂苷Re的含量测定
李 俨,李敬华
(1.吉林省吉林市食品药品检验所,吉林 吉林 132011; 2.北华大学附属医院,吉林 吉林 132011)
人参消渴胶囊中人参皂苷Rg1和人参皂苷Re的含量测定
李 俨1,李敬华2
(1.吉林省吉林市食品药品检验所,吉林 吉林 132011; 2.北华大学附属医院,吉林 吉林 132011)
目的建立人参消渴胶囊中人参皂苷Rg1、人参皂苷Re含量测定的高效液相色谱法。方法色谱柱为Hytersil BDS C18柱(250 mm×4.6 mm,5 μm),流动相为乙腈 -0.05%磷酸(20 ∶80),流速 0.9 mL/min,柱温 40 ℃,检测波长 203 nm,进样量 10 μL。结果人参皂苷 Rg1、人参皂苷 Re的进样量线性范围分别为 0.25 ~ 2.75 μg 和 0.50 ~5.51 μg,平均回收率分别为 96.75% 和 98.66%,RSD分别为 2.1%和 1.4% 。结论建立的方法准确、简便、快速,可用于该产品的质量控制。
人参消渴胶囊;高效液相色谱法;人参
人参消渴胶囊(原名降糖胶囊)由人参、人参茎叶皂苷等加工提取制成,具有清热生津、滋阴润燥之功,用于消渴症,症见多饮、多尿、多食、消瘦、体倦无力及全身综合征[1]。人参、人参茎叶总皂苷为细贵药,人参皂苷Rg1和人参皂苷Re为其主要成分。笔者采用高效液相色谱(HPLC)法对制剂中的Rg1和人参皂苷Re进行了含量测定,作为其内在质量控制的方法,现报道如下。
1 仪器与试药
2010C型高效液相色谱仪(日本岛津);Class-VP数据处理机(日本岛津);UV-2401型紫外-可见分光光度计(日本岛津);Mettler AE24型电子天平(瑞士)。人参皂苷 Rg1对照品(批号为110703-200322,供含量测定用)、人参皂苷 Re对照品(批号为754-200115,供含量测定用)均由中国药品生物制品检定所提供;人参消渴胶囊(通化鸿淘茂药业有限公司,批号为060101,060102,060103,060104,060105;通化林海药业有限公司,批号为20060104);甲醇为色谱纯。
2 方法与结果
2.1 色谱条件与系统适用性试验[2]
色谱柱:Hytersil BDS C18柱(250 mm ×4.6 mm,5 μm);柱温:40 ℃;流动相:乙腈 -0.05% 磷酸(20 ∶80);流速:0.9 mL/min;检测波长:203 nm;进样量:10 μL。在此条件下,理论板数按人参皂苷Re峰计算为11 647,人参皂苷Rg1和人参皂苷Re的分离度为1.8,色谱图见图1。

图1 高效液相色谱图
2.2 溶液制备
精密称取人参皂苷Rg1、人参皂苷Re对照品适量,加甲醇制成每1 mL含人参皂苷Rg10.25 mg、人参皂苷Re0.5 mg的混合溶液,作为对照品溶液。取本品装量差异项下的内容物,研细,取1 g,精密称定,置索氏提取器中,加三氯甲烷,加热回流1 h,弃去三氯甲烷液,药渣挥去三氯甲烷,加甲醇50 mL,连同滤纸筒移入具塞锥形瓶中,加热回流3 h;过滤,提取液挥干,加水20 mL使溶解,加石油醚(30~60℃)提取2次,每次10 mL,弃去醚液,水液通过D101型大孔吸附树脂柱(内径1.5 cm,长15 cm),以水80 mL洗脱,弃去水液,再用20%乙醇80 mL洗脱,弃去20%乙醇洗脱液,继续用80%乙醇100 mL洗脱,收集洗脱液90 mL,蒸干;残渣加甲醇溶解并定量转移至10 mL容量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液,即得供试品溶液。取不含人参及人参茎叶皂苷的处方,按制备工艺方法制成阴性对照品,取1 g,按供试品溶液的制备方法制成阴性对照品溶液。
2.3 方法学考察
干扰试验:吸取2.2项下阴性对照品溶液10 μL,注入色谱仪,依法测定。结果阴性对照品溶液色谱图在人参皂苷Rg1和人参皂苷Re相应的保留时间附近无干扰峰,表明方法可行。
线性关系考察:分别精密吸取人参皂苷Rg1和人参皂苷Re对照品混合溶液 1,3,5,7,9,11 μL,注入高效液相色谱仪中,以进样量(μg)为横坐标、峰面积积分值为纵坐标绘制标准曲线,人参皂苷Rg1和人参皂苷Re回归方程分别为Y=4697.3905+348734.6285X(r=0.999 9)和Y=19 583.785 58+325 320.703 6X(r=0.999 9),进样量线性范围分别为 0.25 ~2.75 μg和 0.50 ~5.51 μg。
稳定性试验:精密吸取同一供试品溶液(避光保存),每隔一定时间进样1次,依法测定。结果人参皂苷Rg1和人参皂苷Re峰面积的RSD分别为0.3%和1.2%,表明供试品溶液在避光条件下10 h内基本稳定。
精密度试验:取同一对照品溶液,进样6次,依法测定。结果人参皂苷Rg1和人参皂苷Re峰面积的RSD分别为2.7%和1.9%(n=6),表明仪器精密度良好。
重现性试验:取同一批样品,依法独立测定6次。结果含量人参皂苷Rg1和人参皂苷Re含量的RSD分别为2.6%和1.5%(n=6),表明方法重现性良好。
加样回收试验:称取样品 0.250 0,0.500 0,0.625 0 g,分别精密加入对照品的混合溶液(精密称取人参皂苷Rg116 mg和人参皂苷Re11.2 mg,分别置200 mL量瓶中,加甲醇至刻度,精密量取上述溶液各 1 mL,置 200 mL 量瓶中,加甲醇至刻度)1.0,2.0,2.5 mL,按供试品溶液制备方法制备待测溶液并依法测定含量,计算回收率。结果见表1。

表1 加样回收试验结果(n=3)
2.4 样品含量测定
药材含量测定:取人参和人参茎叶皂苷(通化鸿淘茂药业有限公司)各1批,按2005年版《中国药典(一部)》人参项下方法测定,结果人参药材中人参皂苷Rg1和人参皂苷Re的总含量为0.9%,符合总含量不得少于0.30%的规定;按《化学药品地升国标(第七册)》方法测定了人参茎叶皂苷中人参皂苷Rg1、人参皂苷 Re的总含量为54.10%,符合总含量不得少于30.0%的规定。结果见表2。
样品含量测定及含量限度:依法测定6批样品,结果见表3。可见,6批样品的人参皂苷Rg1、人参皂苷Re的平均总量为3.13 mg/粒。考虑到按处方投料的理论值(人参皂苷总量为1.96 mg/粒)、原料本身含量的变化及生产中的波动,暂订每粒样品含人参皂苷Rg1、人参皂苷Re的总量不得少于1.5 mg/粒。
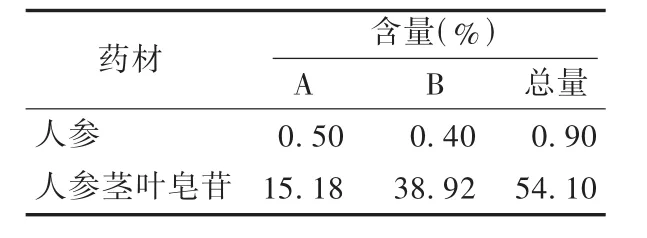
表2 药材含量测定结果

表3 样品含量测定结果(mg/粒)
3 讨论
取对照品溶液,在190~400 nm波长范围内进行紫外光谱扫描,结果在203 nm波长处有最大吸收,因此以203 nm为检测波长。参照2005年版《中国药典(一部)》人参叶含量测定项下方法,以乙腈-0.05%磷酸(20∶80)为流动相;供试品提取溶剂为三氯甲烷、甲醇,以索氏加热回流提取。
根据试验结果,两公司提供的样品在拟订的色谱条件下(流动相比例有所改变),被测的两组分分离效果不好,因此样品生产工艺等条件有必要统一。
[1]中华人民共和国卫生部药典委员会.中华人民共和国药典(一部)[M].北京:人民卫生出版社,1977:9.
[2]国家药典委员会.中华人民共和国药典(一部)[M].北京:化学工业出版社,2005:7.
R284.1;R286.0
A
1006-4931(2011)02-0042-02
2009-12-02;
2010-06-02)

