纳米HgS/聚苯乙烯复合材料的制备及其光学性质研究
秦德志,张丽,杨维春,张秋霞,贺国旭
(平顶山学院 化学化工学院,河南 平顶山 467000)
硫属半导体材料因其特殊的光学、光化学、电学和非线性光学性质已逐渐引起人们的重视[1-4].其中HgS是一种直接带隙宽禁带Ⅱ-Ⅵ族半导体材料,在光热、光电转换器件以及红外图像传感方面有广泛的应用[5],但是目前对材料的发光强度和发光峰位还不能实现有效的控制.纳米化的HgS半导体材料存在显著的尺寸效应、量子效应和表面效应,而且可以通过控制合成粒径的大小来得到一些特殊的光学性质,极大的扩展了材料的应用范围.
半导体纳米材料的制备方法有很多种,包括气相沉积法、高温固相烧结法、凝胶-溶胶法、水热合成法和电沉积液相合成等等[6-9].液相法以操作方便,所得的产品易控制等优点引起人们的关注.Holger等采用胶体合成的方法制备了CdS/HgS/CdS量子点量子阱以及CdS/HgS/CdS/HgS/CdS量子阱[10].Lv等采用简单的液相合成方法在联氨溶液中制备了HgS空心纳米球[11].Ding等在多羟基化合物溶液中合成了PbS和HgS纳米晶[12].本文采用液相化学共沉淀的方法,以醋酸汞和硫代乙酰胺(TAA)为原料在聚苯乙烯溶液中制得分散均匀的纳米硫化汞与PS的复合材料,通过粉末X线衍射、红外光谱、紫外可见和荧光光谱等表征手段对产物的结构和光学性能进行了研究和探讨.
1实验部分
1.1试剂及原料醋酸汞、硫代乙酰胺(TAA)、苯乙烯(st)、四氢呋喃(THF)、偶氮二乙丁腈(AIBN)、氯仿均为国产分析纯试剂,实验用水为自制去离子水.
1.2样品制备将25 mL苯乙烯、150 mL四氢呋喃(THF)和一定物质的量的醋酸汞加入到500 mL的三颈烧瓶中,常温在高纯氮气保护条件下磁力搅拌30 min,然后缓慢升温至60 ℃.再加入一定量的引发剂偶氮二乙丁腈(AIBN),恒温搅拌反应8 h.冷却至室温后,用无水乙醇洗涤数次,再向烧瓶中加入30 mL的氯仿并搅拌15 min.在15 min内将溶于水的硫代乙酰胺(TAA)溶液缓慢加入到上述溶液中,并使TAA与Hg2+的化学计量比保持在1.5∶1.反应24 h后,将得到的产物反复醇洗,与70 ℃真空干燥36 h后,即得到了纳米HgS/PS微粒.按照反应流程制备HgS质量含量(按醋酸汞投料含量计算wt%)分别为2%、4%、6%、8%、10%的样品.
1.3样品表征用D8-Advance型X射线衍射仪对样品进行物相与结构分析;用JEM-2010型透射电子显微镜(JEOL,Japan)对产物形貌进行分析;傅里叶红外光谱(FT-IR)用KBr压片,采用Bio-Rad FTS-40红外光谱仪;紫外光谱在Perkin-Elmer Lambda 20型紫外可见分光光度计上测定;采用Shimadzu RF-540 PC型荧光分光光度计测定样品的荧光光谱.
2 结果与讨论
图1为HgS质量分数为6%的样品的粉末X射线衍射图,谱图中并无杂峰出现,产物为立方晶系闪锌矿型的HgS,晶格常数a=0.581 6 nm,与JC-PDS卡(NO.6-0261)相一致.根据Debye-Scherrer公式:L=Kλ/βcosθ,其中,L为晶粒尺寸,K为Sherrer 常数,β为衍射峰的物理宽化值,θ为衍射角,可以估算出其粒径约为4.8 nm.
图2给出了HgS质量分数为6%的样品的电子能谱图(EDS).根据图谱分析,样品中原子序数大于8的元素有Hg、S和Si,Si为在研钵中研磨样品时带入,Hg和S的化学计量比为1∶1.137.这可能是因为反应中的汞硫比为1∶1.5,纳米晶生成后吸附了少量的S导致化学计量比发生了变化.
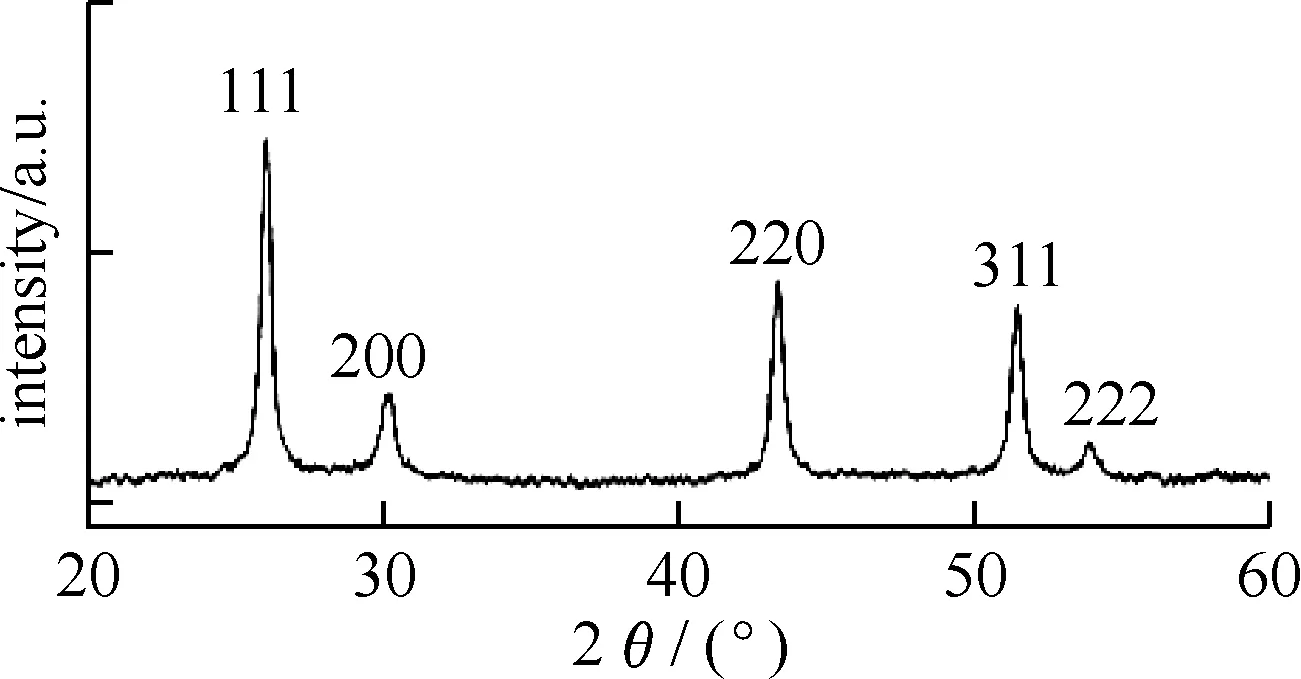
图1 HgS纳米晶的X射线衍射图(XRD)

图2 样品的电子能谱图(EDS)
图3A、B分别示出了HgS质量分数分别为为6%和2%样品的透射电子显微镜(TEM)图片.从电镜照片可知6%的HgS样品中纳米晶的粒径在8~12 nm左右,这说明微粒是由更小的初级的HgS晶粒(~4.8 nm)组成.根据能谱分析得出纳米晶吸附了一定的S,我们推测其中的原因可能为纳米晶之间和表面修饰的有机物质通过氢键作用力聚集在一起.图4为不同含量HgS样品中纳米晶的平均粒径分布图.根据纳米晶的一般生长规律,当基质浓度增大时,纳米颗粒的直径减小.由图4的粒径分布可知,HgS含量为6%时粒径最小,可以推测当颗粒直径进一步减小时,纳米晶由于表面积增大导致表面能迅速升高,颗粒愈发不稳定更容易团聚使纳米晶变大.这一点从图3A中也可以观察出来,较小的纳米晶直径在4~5 nm之间,但平均粒径在15 nm左右.另外,从TEM图片还可以发现HgS纳米晶的生长具有一定的取向生长习性,说明在纳米晶的生长过程中聚苯乙烯基质会抑制某些晶面的生长,并阻碍晶粒间的聚集.图3B中在纳米晶的周围发现了一些短棒的物质(如箭头所示),这可能是由聚苯乙烯的空间位阻效应造成的,HgS纳米晶的生长和形成机理还有待于进一步的深入研究.
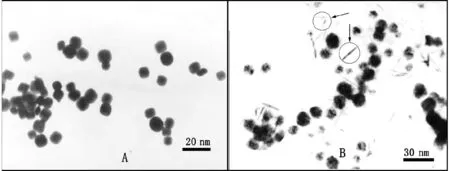
图3 样品的透射电镜图片HgS质量分数(A:6%, B: 2%)

图4 纳米晶平均粒径随HgS含量的变化
图5为样品的红外光谱图,从图中可以看到在3 070~2 840 cm-1,1 600~1 350 cm-1和700 cm-1处有吸收峰,峰位置分别对应了芳香环的骨架振动和芳环上氢原子的伸缩振动,以及CH的弯曲振动.从这些特征吸收峰的出现可以证明样品中存在聚苯乙烯,在纳米晶的形成过程中起到了重要的作用.

图5 HgS/聚苯乙烯复合纳米材料的红外光谱图

图6 不同HgS含量样品的紫外可见光谱图

图7 不同HgS含量样品的荧光发射光谱
图6为不同含量HgS样品在室温下的紫外可见吸收光谱.从图中可见,由于纳米粒子粒径有一定的分布导致峰形较宽,最大吸收峰位置大约在342 nm左右,并且随着HgS含量的升高吸收强度逐渐增大,说明吸收主要为硫化汞纳米晶的吸收.对于半导体纳米材料来说,与体相同种材料相比吸收光谱往往会出现明显的蓝移,粒子尺寸越小蓝移越明显.对于半导体材料可以通过下面公式来计算其能带带隙(band gap).这里a为吸收系数,Eg为带宽,
a(v)=A(hv/2-Eg)m/2.
对于直接转换m=1,(aEphot)2对Ephot作图,外延图形至a=0即可得到能带带隙.通过计算得到HgS质量分数为2%、6%、10%的样品的能带带隙分别为2.65、2.73、2.67 ev,相对于体相材料(Eg=2.0 ev)有明显的蓝移.这主要是由纳米晶的量子尺寸效应所造成的,使纳米材料具备了与常规体相材料所不同的光学性质.
图7为HgS质量分数分别为2%、6%和10%的样品的荧光发射光谱,发光峰的位置没有明显的变化,大致在380 nm,但发光强度有所区别.其中HgS含量6%的样品发射峰强而宽,而2%和10%含量的样品发光峰相对来说窄而弱.从不同样品的粒径分布可以解释这个现象,硫化物半导体发光一般都源于硫空位引起的缺陷发射峰[13].当纳米晶颗粒相对较小时,表面缺陷较多,在能隙中形成缺陷能级,通过表面缺陷态间接复合发光.而大的颗粒由于晶粒表面较完好,故对光生载流子的缺陷俘获能力弱,表面发光也较弱.这也是由纳米材料的表面效应所导致,是常规体相粗晶所不具备的性质.
3 结论
以聚苯乙烯为基质,采用醋酸汞和硫代乙酰胺(TAA)为原料合成了纳米HgS/PS复合材料.合成的复合材料中HgS纳米晶为立方闪锌矿构型,粒径小于15 nm并且表现出一定的取向生长性.紫外可见吸收光谱表明产物吸收峰的位置相对与体相材料有明显的蓝移,主要是量子限域效应所造成.荧光光谱显示由于复合材料中HgS纳米晶的表面效应荧光发射峰的强度随着产物粒径的变化而改变,表现出良好的发光性能.
致谢:感谢河南大学特种功能材料教育部重点实验室在分析测试方面给予的帮助.
参考文献:
[1] Qin D,Ma X, Yang L, et al.Biomimetic synthesis of HgS nanoparticles in the bovine serum albumin solution[J].J Nanopart Res,2008,10:559-566.
[2] Xia Y,Yang P, Sun Y, et al.One-dimensional nanostuctures:synthesis, characterization, and applications[J].Adv Mater,2003,15:353-398.
[3] Monroy E,Omnes F, Calle F, et al.Wide-band gap semiconductor ultraviolet photodetectors[J].Semicond Sci Technol,2003,18:33-51.
[4] Penn S,He L, Michael J, et al.Nanoparticles for bioanalysis[J].Current Opinion in Chemical Biology,2003,7(5):609-615.
[5] 黄波.固体材料及其应用[M].广州:华南理工大学出版社,1994.
[6] 李雪梅,杨延钊,孙思修,等.溶剂热合成法制备(Zn,Hg)S微晶和薄膜[J].无机化学学报,2002,18(9):961-964.
[7] 舒磊,俞书宏,钱逸泰.半导体硫化物纳米微粒的制备[J].无机化学学报,1999,15(1):1-7.
[8] Zhu J,Aruna S, Koltypin Y, et al.A novel method for the preparation of lead selenide:pulse sonoelectrochemical synthesis of lead selenide nanoparticles[J].Chem Mater,2000,12:143-147.
[9] 丁轶,刘仁茂,张祖德,等.氧化物直接转化法制备汞的硫属化合物纳米材料[J].高等学校化学学报,2000,21(3):344-346.
[10] Holger B,Dirk D,Colm M,et al.Photoemission study of onion like quantum dot quantum well and double quantum well nanocrystals of CdS and HgS[J].J Phys Chem,2003,107:7486-7491.
[11] Lv J,Feng Y,Zhang S,et al.Simple solution approach to hollow nanospheres of cubic HgS[J].Materials letters,2005,59:3109-3111.
[12] Ding T,Zhang J,Long S,et al.Synthesis of HgS and PbS nanocrystals in a polyol solvent by microwave heating[J].Microelectronic Engineering,2003,66:46-52.
[13] Chestnoy N,Harris T, Hull R, et al.Luminescence and photophysics of cadmium sulfide semiconductor clusters:the nature of the emitting electronic state [J].J Phys Chem,1986,90:3393-3399.

