NH+4对甲酸在炭载Pd催化剂上氧化性能的影响
李焕芝 唐亚文 陆天虹
(南京师范大学化学与材料科学学院,南京 210097)
NH+4对甲酸在炭载Pd催化剂上氧化性能的影响
李焕芝 唐亚文 陆天虹*
(南京师范大学化学与材料科学学院,南京 210097)
为了解HClO4、NH4ClO4和NaClO4电解液对炭载Pd(Pd/C)催化剂电极对甲酸氧化的电催化性能的影响,在用X射线衍射(XRD)谱、能量色散谱(EDS)和透射电子显微镜(TEM)对Pd/C催化剂进行表征的基础上,采用电化学方法测量了Pd/C催化剂在不同电解液中对甲酸氧化的电催化性能.发现在不同电解液中,Pd/C催化剂对甲酸氧化的电催化活性和稳定性按NH4ClO4>NaClO4>HClO4的次序降低.由于甲酸的存在,不同电解液的pH相差较小,因此,电解液的pH影响较小,而阳离子的影响较大.在NaClO4电解液中的性能优于在HClO4电解液中的性能是pH的影响.在NH4ClO4电解液中的性能优于在NaClO4电解液中是由于NH4+能降低CO在Pd/C催化剂电极上的吸附强度和吸附量,这一发现对提高直接甲酸燃料电池(DFAFC)的性能很有意义.
甲酸;电解液;钯;直接甲酸燃料电池
近年来,人们越来越认识到,与直接甲醇燃料电池(DMFC)相比,直接甲酸燃料电池(DFAFC)有很多优点而越来越受到人们的关注[1-8].如甲酸无毒,不易燃,存储和运输安全方便;甲酸电化学氧化的性能要比甲醇好很多;由于质子交换膜中的磺酸基团与甲酸阴离子间有排斥作用,因此,甲酸对Nafion膜的渗透率要比甲醇小很多.一般报道,甲酸氧化可通过两种途径进行,在Pd催化剂上主要通过希望的直接途径进行,所以,Pd催化剂对甲酸氧化的电催化活性很好.但Pd催化剂有一个很大的问题就是对甲酸的氧化电催化稳定性不好,因此,近年来在提高Pd催化剂的电催化稳定性方面做了很多的工作,主要研究Pd催化剂稳定性不好的原因及解决办法.一般认为,虽然甲酸在Pd催化剂上的氧化主要是通过直接途径进行,但还是有一部分是通过CO途经进行的.因此,许多研究是通过制备Pd基复合催化剂,如 PdAu[911]、PdCo[1213]、Pd-Ir[14]、PdPb[15]、PdSb[16]、PdFe[17]、PdP[1819]、PdB[20]和Pd-杂多酸[2122]等来降低CO在Pd上的吸附强度或吸附量来提高Pd催化剂的电催化活性和稳定性.
最近有一些关于电解液对Pd催化剂电催化性能影响的报道,如Masel研究组[23]最近的研究表明,当电解液的pH增加时,CO在Pd上的吸附强度会随溶液pH值增加而减弱,因此,Pd催化剂对甲酸氧化的电催化稳定性随溶液pH值增加而改进.魏子栋研究组[24]的研究表明,由于Pd在酸性溶液中慢慢溶解,所以用(NH4)2SO4代替H2SO4作电解质.目前一般使用H2SO4和HClO4作电解质,Hoshi等[25]指出,考虑到SO42-会吸附到Pd上产生一些不良影响,因此,电解质最好使用HClO4而不用H2SO4.鉴于上述情况,本文系统比较了Pd/C催化剂在HClO4、NH4ClO4和NaClO4三种电解质溶液中对甲酸氧化的电催化性能,以得到DFAFC中最好的电解质溶液.
1 实验部分
1.1 试剂和仪器
Vulcan XC-72活性炭为美国Cabot公司产品,质量分数(w)为5%的Nafion溶液为美国Aldrich化学公司产品,其余试剂均为分析纯级,所有溶液均用三次蒸馏水配制.
电化学测试用CHI600B电化学分析仪(美国CHI仪器公司)和常规的三电极体系的电化学池进行.用Vantage IV型X射线能谱仪(美国热电公司)进行X射线能量色散(EDS)谱测量.X射线衍射(XRD)谱测量用D/max-r C型转靶X射线衍射仪(日本理学公司)进行,靶压200 kV,靶流100 mA,Cu Kα射线源为光源,波长为0.15406 nm.透射电子显微镜(TEM)照片用100 kV分析型JEM-1011透射电子显微镜(日本电子公司)拍摄.
1.2 Pd/C催化剂和工作电极的制备
Pd/C催化剂用普通液相还原法制备.将60 mg Vulcan XC-72活性炭和3.13 mL 0.04504 mol·L-1PdCl2水溶液混合,超声30 min后,继续搅拌4 h.用Na2CO3调节溶液pH值至8-9后,缓慢滴加10 mL 1.0 g·L-1的NaBH4溶液,超声和搅拌1 h后,过滤、洗涤至无Cl-,60℃真空干燥12 h后,即得含20%(w) Pd的Pd/C催化剂.
将玻碳电极依次用5#金相砂纸、0.3和0.05 μm的Al2O3粉磨至镜面,洗涤、干燥后,将8 mg催化剂与4 mL乙醇配制成2 g·L-1悬浮液,超声分散30 min.移取8.9 μL悬浮液至直径为4 mm的玻碳电极表面,50℃干燥后,移取3.0 μL 5%(w)Nafion溶液于催化剂表面,干燥后得工作电极.电极上Pd/C催化剂载量为28 μg·cm-2.
1.3 电化学测试
进行电化学测量时,对电极为Pt片,参比电极为饱和甘汞电极(SCE),文中所述的电位均相对于SCE,Pd/C催化剂电极为工作电极,三种电解液中的电解质浓度及甲酸浓度均为0.50 mol·L-1.在电化学测试前,溶液通高纯N210 min以除去溶解的氧,测量时在溶液上方通N2保护.在进行循环伏安测量时,电位扫描速率为50 mV·s-1.在测量吸附CO电化学氧化性能时,先将Pd/C催化剂电极电位固定在0 V,然后向溶液通CO 20 min,再改通高纯N230 min,以除去溶解在溶液中的CO.电位扫描速率为10 mV·s-1.实验都在(30±2)℃下进行.
2 结果与讨论
2.1 Pd/C催化剂组成和结构分析
图1是Pd/C催化剂的EDS谱.由图可见,在EDS谱中有两个谱峰,Pd峰和C峰,计算表明,在Pd/C催化剂中Pd的质量分数为18.25%(w),与理论值接近,表明在制备催化剂时,PdCl2基本上全部还原为Pd.
图2为Pd/C催化剂的XRD谱.由图可见,在2θ=24.7°处对应的是XC-72活性炭中的碳(002)晶面的衍射峰,其他四个衍射峰的2θ值分别为39.9°, 44.6°,67.7°和81.1°,它们分别相应于具有面心立方结构的 Pd晶体的 Pd(111)、Pd(200)、Pd(220)和Pd(311)的晶面衍射峰,表明在Pd/C催化剂中的Pd粒子具有面心立方晶体结构.按照Antolini的方法[26],计算得到的Pd/C催化剂中Pd粒子的相对结晶度为1.37.利用Scherrer公式[26],计算出Pd/C催化剂中Pd粒子的平均粒径为3.57 nm.
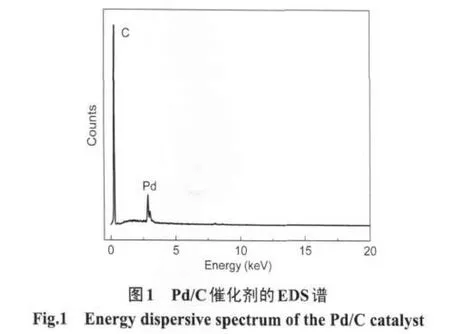
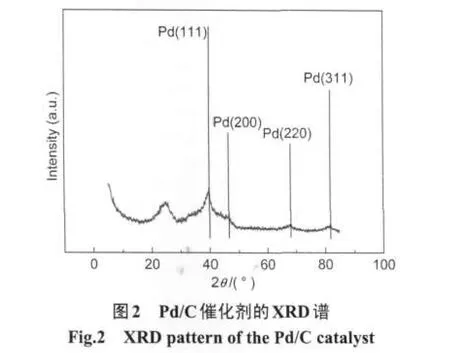
图3为Pd/C催化剂的TEM照片.由图统计出Pd/C催化剂中Pd粒子的平均粒径为4.8 nm,与XRD实验结果基本一致.
2.2 Pd/C催化剂对甲酸氧化的电催化性能测量
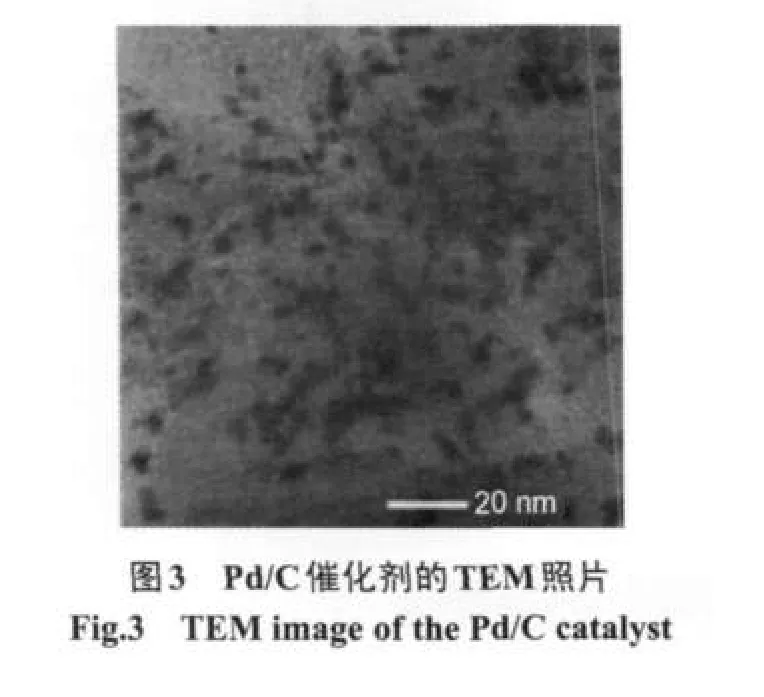
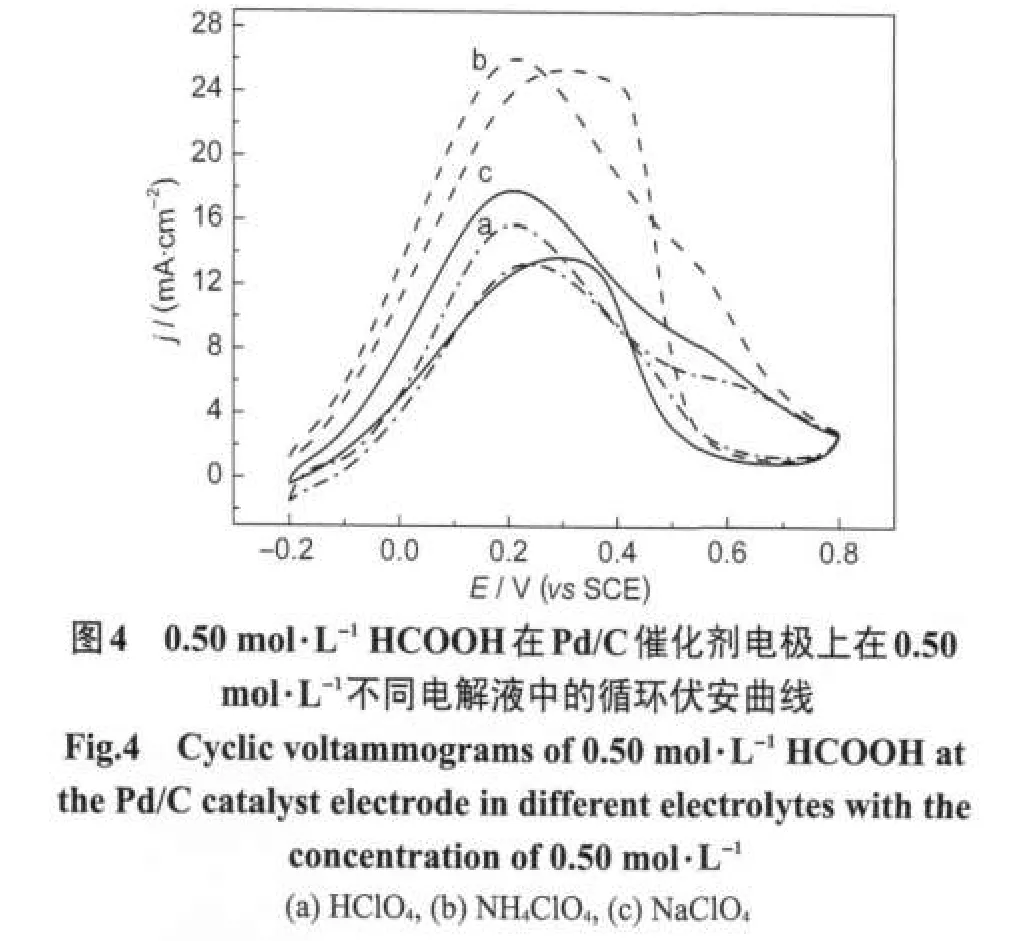
图4为甲酸分别在HClO4、NH4ClO4和NaClO4电解液中,在Pd/C催化剂电极上的循环伏安曲线.由图可见,甲酸在不同电解液中的氧化峰峰电位基本相同,在0.21 V左右,但峰电流密度不同,在HClO4、NH4ClO4和NaClO4电解液中的峰电流密度分别为15.7、26.1和17.8 mA·cm-2,表明在NH4ClO4电解液中,Pd/C催化剂对甲酸氧化的电催化活性最好,这表明NH4+可能起特殊的作用.
图5为甲酸分别在不同电解液中的Pd/C催化剂电极上,在0.20 V时的计时电流曲线.由图可知,在6000 s时,甲酸在HClO4、NH4ClO4和NaClO4电解液中,在Pd/C催化剂电极上氧化电流密度分别为0.61、3.23和2.09 mA·cm-2,表明Pd/C催化剂在NH4ClO4溶液中对甲酸氧化的电催化稳定性最好,而在HClO4电解液中的电催化稳定性最差.

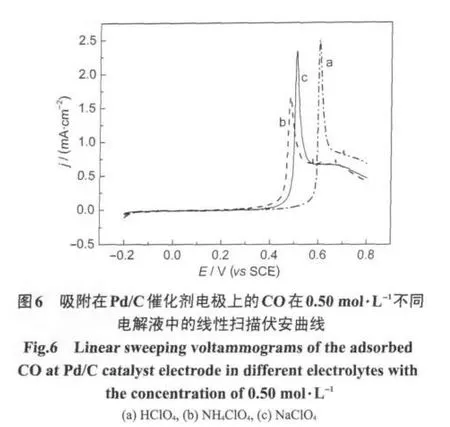
图4和图5的结果表明,在不同电解液中,Pd/C催化剂对甲酸氧化的电催化活性和稳定性按NH4ClO4>NaClO4>HClO4的次序降低.虽然文献报道[23]电解液的pH值对催化剂的电催化性能影响很大,但是由于电解液中有大量甲酸存在,所以不同电解液的pH值相差不大,测量表明,在含甲酸的NH4ClO4、NaClO4和HClO4电解液的pH值分别为1.72、1.79和0.57,因此,在NaClO4电解液中性能比在HClO4电解液中好主要是电解液的pH在起作用.
图6为吸附在Pd/C催化剂电极上的CO的线性扫描伏安曲线.由图可见,CO在HClO4、NH4ClO4和NaClO4电解液中,在Pd/C催化剂电极上的氧化峰峰电位分别为0.60、0.48和0.51 V,表明CO在HClO4电解液中在Pd/C催化剂上的吸附强度最大,而在NH4ClO4电解液中的吸附强度最小.氧化峰峰电流密度按HClO4、NaClO4和NH4ClO4次序减小,表明CO在HClO4电解液中在Pd/C催化剂上的吸附量最大,而在NH4ClO4电解液中的吸附量最小.这结果说明NH4+能降低CO在Pd/C催化剂上的吸附强度和吸附量.由于甲酸氧化时有一定的能使Pd催化剂中毒的中间产物CO,因此,NH4+能降低CO在Pd/C催化剂上的吸附强度和吸附量,表明在NH4ClO4电解液中,催化剂不易中毒,而使Pd/C催化剂对甲酸氧化的电催化活性和稳定性都得到提高.
3 结论
Pd/C催化剂电极分别在HClO4、NH4ClO4和NaClO4电解液中对甲酸氧化的电催化活性和稳定性的比较表明,不同电解液中,Pd/C催化剂电极对甲酸氧化的电催化性能以下列的次序下降:NH4ClO4> NaClO4>HClO4.首先,含甲酸的电解液pH值对Pd/C催化剂电极对甲酸氧化的电催化性能有一定的影响,酸性电解液不利于甲酸在Pd/C催化剂上的氧化.其次,在NH4ClO4电解液中,Pd/C催化剂对甲酸氧化的电催化性能好的主要原因是由于NH4+能降低CO在Pd/C催化剂上的吸附强度和吸附量.因此,在DFAFC中,应使用NH4ClO4电解液.
1 Rhee,Y.;Ha,S.;Masel,R.I.J.Power Sources,2003,117:35
2 Lu,T.H.;Tang,Y.W.;Zhang,L.L.;Gao,Y.Batt.Ind.,2007,12:412 [陆天虹,唐亚文,张玲玲,高 颖.电池工业,2007,12:412]
3 Ha,S.;Larsen,R.;Masel,R.I.;Waszczuk,P.;Wieckowski,A.; Barnard,T.J.Power Sources,2002,111:83
4 Li,X.G.;Hsing,I.M.Electrochim.Acta,2006,51:3477
5 Yu,X.W.;Pickup,P.G.J.Power Sources,2009,187:493
6 Wang,X.;Hu,J.M.;Hsing,I.M.J.Electroanal.Chem.,2004,562:73
7 Ha,S.;Larsen,R.;Masel,R.I.J.Power Sources,2005,144:28
8 Ha,S.;Larsen,R.;Zhu,Y.Fuel Cells,2004,4:337
9 Wang,X.;Tang,Y.W.;Lu,T.H.Electrochemistry,2008,14:6 [王 新,唐亚文,陆天虹.电化学,2008,14:6]
10 Jiang,J.H.;Kucernak,A.Electrochim.Acta,2009,54:4545
11 Chen,C.H.;Liou,W.J.;Lin,H.M.;Wu,S.H.;Mikolajczuk,A.; Stobinski,L.;Borodzinski,A.;Kedzierzawski,P.;Kurzydlowski,K. Phys.Status Solid A,2010,207:1160
12 Wang,X.M.;Xia,Y.Y.Electrochem.Commun.,2008,10:1644
13 Matolınova,I.;Fabk,S.;Masek,K.Vacuum,2003,71:41
14 Wang,X.;Tang,Y.W.;Gao,Y.;Lu,T.H.J.Power Sources,2008, 175:784
15 Yu,X.W.;Pickup,P.G.J.Power Sources,2009,192:279
16 Yu,X.W.;Pickup,P.G.Electrochem.Commun.,2010,12:800
17 Cao,S.;Wang,Y.E.;Lu,T.H.;Tang,Y.W.Chin.J.Appl.Chem., 2009,26:613 [曹 爽,王彦恩,陆天虹,唐亚文.应用化学,2009, 26:613]
18 Zhang,L.L.;Tang,Y.W.;Bao,J.C.;Lu,T.H.;Li,C.J.Power Sources,2006,162:177
19 Yang,G.X.;Chen,Y.;Zhou,Y.M.;Tang,Y.W.;Lu,T.H. Electrochem.Commun.,2010,12:492
20 Wang,J.Y.;Kang,Y.Y.;Yang,H.;Cai,W.B.J.Phys.Chem.C,2009, 113:8366
21 Yang,G.X.;Deng,L.J.;Tang,Y.W.;Lu,T.H.Chem.J.Chin.Univ., 2009,30:1173 [杨改秀,邓玲娟,唐亚文,陆天虹.高等学校化学学报,2009,30:1173]
22 Yang,G.X.;Chen,T.T.;Tang,Y.W.;Lu,T.H.Acta Phys.-Chim.Sin., 2009,25:2450 [杨改秀,陈婷婷,唐亚文,陆天虹.物理化学学报, 2009,25:2450]
23 Haan,J.L.;Masel,R.I.Electrochim.Acta,2009,54:4073
24 Liao,C.;Wei,Z.D.;Chen,S.G.;Li,L.;Ji,M.B.;Tan,Y.;Liao,M.J. J.Phys.Chem.C,2009,113:5705
25 Hoshi,N.;Kuroda,M.;Ogawa,T.;Koga,O.;Hori,Y.Langmuir,2004, 20:5066
26 Feliu,J.M.;Herrero,E.//Vielstich,W.;Gasteiger,H.A.;Lamm,A. Handbook of fuel cells.New York:Wiley,2003:679
Effect of NH4+on the Electrocatalytic Performance of Carbon Supported Pd Catalyst for Formic Acid Oxidation
LI Huan-Zhi TANG Ya-Wen LU Tian-Hong*
(College of Chemistry and Material Science,Nanjing Normal University,Nanjing 210097,P.R.China)
We investigated the effect of HClO4,NH4ClO4,and NaClO4electrolytes on the electrocatalytic performance of a Pd/C catalyst electrode for formic acid oxidation.The Pd/C catalyst was characterized by X-ray diffraction(XRD),energy dispersive spectroscopy(EDS),and transmission electron microscopy (TEM).The performance of the Pd/C catalyst electrode during formic acid oxidation in different electrolytes was measured using electrochemical methods.We found that the electrocatalytic activity and stability of the Pd/C catalyst electrode for formic acid oxidation decreased in the following order:NH4ClO4>NaClO4>HClO4.The difference in pH between the different electrolytes was small because of the presence of formic acid.Therefore,the electrolyte pH has a small effect and the cations have a large effect.The better performance of the NaClO4electrolyte compared to the HClO4electrolyte is due to a pH effect.The better performance of the NH4ClO4electrolyte compared to the NaClO4electrolyte is due to NH4+decreasing the adsorption strength and amount of CO on the Pd/C catalyst.This finding has large significance for the increase in the performance of the direct formic acid fuel cell(DFAFC).
Formic acid;Electrolyte;Palladium;Direct formic acid fuel cell
O643
Received:August 16,2010;Revised:October 10,2010;Published on Web:October 26,2010.
∗Corresponding author.Email:tianhonglu@263.net;Tel:+86-13809029980.
The project was supported by the National Natural Science Foundation of China(20873065,21073094).
国家自然科学基金(20873065,21073094)资助项目
ⒸEditorial office ofActa Physico⁃Chimica Sinica

