超声辐照降解MC-RR动力学的影响因素
欧桦瑟,高乃云,隋铭皓,黎雷,姚娟娟
(同济大学 污染控制与资源化研究重点试验室,上海,200092)
随着工业化和国民经济的发展,近年来水体富营养化问题日益严重,我国太湖和滇池常年有大量藻类滋生,由此产生的各类副产物特别是藻毒素对人类健康产生极大威胁,同时造成巨大的经济和社会损失,引起人们广泛的关注[1-4]。藻毒素中,微囊藻毒素(microcystins, MCs)等肝毒素最为常见。MCs是一类环状多肽类物质且具有很强的肝毒性[5-7]。经调查,黄浦江源水中总MC-LR(Microcystin-LR)质量浓度为100~250 ng/L,总MC-RR(Microcystin-RR)质量浓度为450~650 ng/L[8],且常规的混凝→沉淀→过滤→消毒等自来水处理工艺过程对其几乎没有去除效果[9],因此,研发新型高效去除微囊藻毒素的技术是亟待解决的问题。目前,针对MCs的去除研究方法主要包括化学氧化法、光催化氧化法、活性炭吸附法、声化学法以及生物氧化法,而超声辐照技术是近年来发展起来的一门新型技术[10-13],与其他方法相比具有操作和控制简单,便于自动化操作,处理过程不引入其他化学物质,反应条件温和以及无二次污染等优点[14-15]。本试验考察超声辐照去除水中 MC-RR的动力学过程并研究超声频率和pH等因素对去除反应的影响规律。
1 材料与方法
1.1 材料
1.1.1 试验设备
试验采用的超声装置购买于中国科学院上海声学研究所,型号为SF型。图1所示为超声反应器示意图。
1.1.2 MC-RR的提取
试验所用藻种取自太湖,在试验室培养。藻培养液通过离心处理后阴干,研磨成干藻粉备用。试验时将干藻粉溶于去离子水中,随后在-18 ℃的冰箱中冰冻12 h 后解冻,并重复3次使藻毒素释放彻底,之后经过离心处理提取上清液。最后,使上清液通过0.45 μm的混合纤维素酯微孔过滤膜并经过 SPE(Solid phase extraction)处理提取出其中的MC-RR,最终将得到的提纯液用于试验及HPLC(High performance liquid chromatography)分析。
1.1.3 其他试验试剂
微囊藻毒素标样 MC-RR(购自武汉水生生物研究所),HPLC级;双氧水采用体积分数为30%的过氧化氢分析纯;NaCl,Na2CO3,NaNO3以及 Na2SO4溶液由分析纯固体溶解配制而成;调节pH值,所用HCl和 NaOH溶液由分析纯浓盐酸和分析纯固体分别配制;试验用水均采用Milli-Q出水。
1.2 试验方法
采用超声辐照工艺去除MC-RR,分别进行不同超声频率、MC-RR初始浓度、超声功率、pH条件、声能密度以及投加4种阴离子的对照试验。
1.3 MC-RR分析方法
MC-RR浓度采用高效液相色谱仪(岛津LC-2010AHT)测定;采用岛津VP-ODS色谱柱(250 mm×4.6 mm);流动相为甲醇(Sigma-Aldrich, USA)和Milli-Q 出水(Millipore, Molsheim, France),预加φ(三氟乙酸)=0.05%,φ(甲醇)/φ(H2O)=60/40;分析时间为10 min,流动相流速为1 mL/min,柱温为40 ℃。
2 结果与分析
2.1 反应动力学
2.1.1 超声降解MC-RR机理
MC-RR基本分子结构为大环并间隔双键,具有较强的热稳定性,其化学结构在100 ℃加热保持不变;其分子结构中含有多个羧基、氨基、酰氨基等极性官能团,属于亲水性有机物,易溶于水、难挥发。分子结构图如图2所示。图中带苯环的长支链为ADDA基团,是重要的生物毒性基团。
超声降解水体中的有机污染物属于物理化学过程,超声辐照诱发水体产生空化泡并历经振动、生长、崩溃闭合的动力学过程[16];空化气泡溃灭的极短过程中,其内部及其周围极小空间范围内产生极端高温和高压。Mason等[17]的研究表明,空化泡内产生的最高温度Tmax和最大压力pmax可以采用式(1)~(2)进行推导:
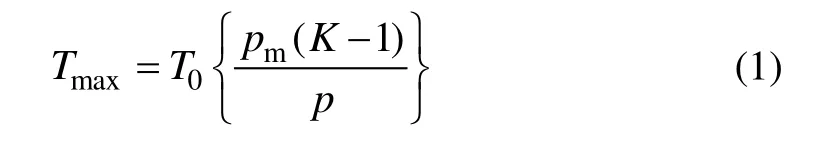
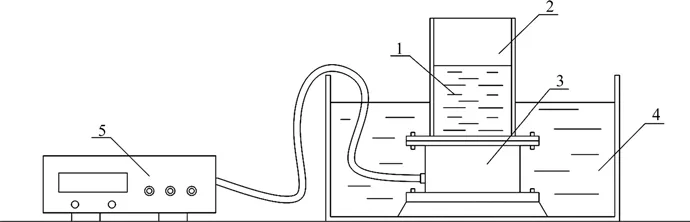
图1 超声反应器示意图Fig.1 Schematic diagram of ultrasonic reactor

式中:pm为空化泡崩溃时的内部压力;p为空化泡达到最大体积时的内部压力;K=Cp/Cv,Cp和Cv分别为空化泡空气的定压比热容和定容比热容。理论上,pmax可达50.662 5×106Pa,Tmax可达5.0×103K以上。在极端的温度和压力条件下能产生一系列复杂反应,如将空化泡内水蒸汽和水-气临界面的水分子分解,产生诸如·O,·OH,·H和H2O2等强氧化性物质。
超声降解 MC-RR包括羟基自由基反应、热解反应和临界面水解反应等,根据反应类型和位置不同可以将超声降解 MC-RR反应区域分为如下几部分,如图3所示。
(1)空化泡内部气态区域。MC-RR属于低挥发性物质,因此,不会出现在空化泡内部,该区域内环境变化剧烈,能够将水蒸汽和水-气临界面的水分子分解并产生·O,·OH,·H和H2O2等强氧化性物质。强氧化性物质主要产生于空化泡内部并由内向外扩散参与降解反应。
(2)水-气临界面区域。在水-气临界面内可能发生的反应有羟基自由基氧化和水解/热解反应。MC-RR存在于该区域的部分主要为憎水基团ADDA,带有亲水基团的环状结构则分布于溶液中,因此,主要为ADDA在该区域反应。当ADDA处于该区域时,其长链上的C=C双键会受到羟基自由基等强氧化剂的进攻而受到破坏生成中间产物并最后矿化,Maria等[5]的研究证实了该反应,并指出可能的中间产物为带苯环基团C9H10O,如图4所示。ADDA是MCs毒性活性基团之一[18],故该区域反应能有效去除水中 MCs的毒性。
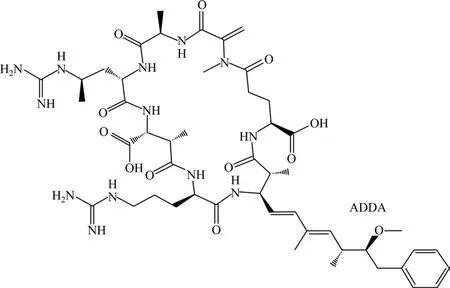
图2 MC-RR分子结构图Fig.2 Structure of MC-RR

图3 MC-RR分布示意图Fig.3 Proposed location of MC-RR during cavitation

图4 中间产物C9H10O的结构Fig.4 Structure of intermediate product C9H10O
此外,水解/热解等反应对MC-RR也有破坏作用,除单独针对ADDA基团外,还有一定概率对MC-RR上较易受到攻击的部位产生破坏作用。Song等[19]的研究表明该区域内部羟基自由基氧化和水解/热解对MCs的降解分别占MCs总体降解的35%和26%。
(3)液态溶液区域。液态溶液区域的温度和压强基本与普通溶液的相同,该区域发生的反应主要为羟基自由基氧化反应。羟基自由基等氧化物主要攻击MC-RR上的ADDA基团及其环状结构上的C=C基团,破坏藻毒素的结构并生成多种中间产物。Song等[19]的研究表明该区域的反应占总反应的39%。该区域反应的详细机理还有待研究。
以上多种反应过程中氧化物均相对于 MC-RR过量,理论上分析降解反应符合准一级动力学规律。
2.1.2 不同初始质量浓度下反应动力学
反应动力学类型的确定对后续试验研究具有重要意义。试验配制藻毒素储备液,用HPLC测得MC-RR的初始质量浓度为500 μg/L,调节pH约为7.0,之后分别配制质量浓度为500,250和125 μg/L的反应溶液,各取30 mL放于反应容器中,调节超声频率为400 kHz、功率为100 W进行超声辐照,其降解效果如图5所示。可见:随着反应进行,MC-RR得到降解。
图5和表1显示初始质量浓度对MC-RR的降解影响甚小。当MC-RR初始质量浓度为125 μg/L时,降解速率常数k=0.122 min-1,而初始质量浓度为250 μg/L和 500 μg/L时,k分别为 0.117 min-1和 0.105 min-1,影响不明显;去除率的变化在 3%以内,可以认为 MC-RR初始质量浓度对反应基本没有影响,试验中出现的细微差别应为误差所致。
不同 MC-RR 质量浓度时,ln(ρt/ρ0)与反应时间t之间呈线性关系,如图 6所示。其决定系数R2≥0.990 8,可认为超声降解MC-RR的反应是准一级动力学反应,用以下公式来表达反应类型:
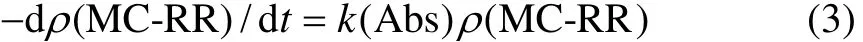

图5 MC-RR初始浓度对降解MC-RR的影响Fig.5 Effect of different initial concentrations on degradation of MC-RR
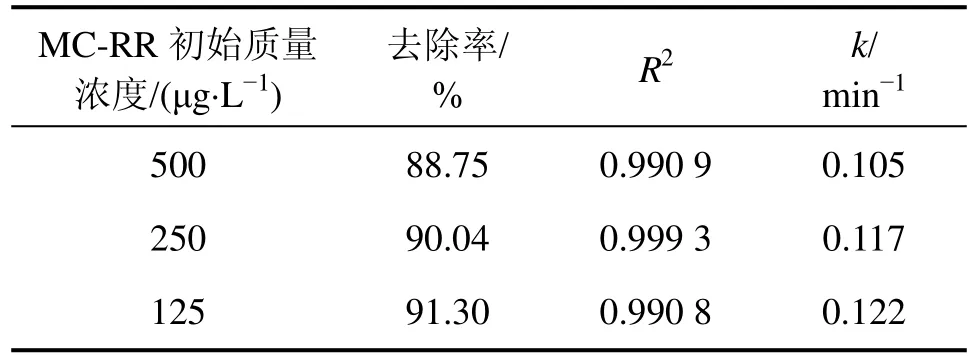
表1 不同初始浓度下MC-RR降解的准一级动力学模型数据Table 1 Degradation parameters of kinetics models (pseudo first order)under different initial concentrations of MC-RR
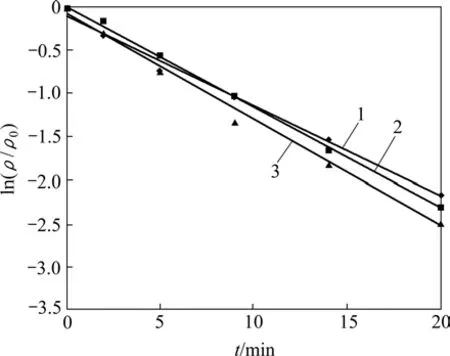
图6 MC-RR氧化反应的准一级动力学曲线Fig.6 Pseudo first-order kinetics plot of MC-RR oxidation reaction
式中:ρ( M C-RR)为MC-RR的浓度;k(Abs)为表观动力学反应常数;t为反应时间。该式是表观动力学降解速率方程,MC-RR浓度是反应速率限制因素,k(Abs)为(0.11±0.01)min-1。
2.2 超声频率的影响
MC-RR 溶液初始质量浓度约为 500 μg/L,pH=7.0,功率为100 W,选择频率为60,200,400和800 kHz的超声波对反应液进行辐照,反应时间为40 min,在0,5,10,20和40 min时取样进行检测,藻毒素浓度变化见图7,反应速率常数k,决定系数R2以及MC-RR半衰期如表2所示。由试验结果可知,各个频率的超声波对藻毒素 MC-RR均有降解,其中频率为400 kHz时的效果最好,40 min去除率接近100%;频率为800 kHz时次之,40 min去除率达到92.7%;而频率为60和200 kHz时,40 min去除率分别为40.4%和66.1%,可见:400 kHz是MC-RR的最佳降解频率,中频超声波对藻毒素的降解效果最好,低频和高频的超声效果均不理想。
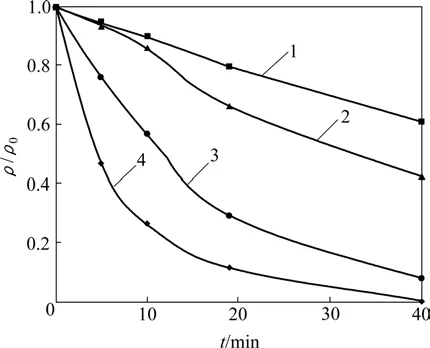
图7 不同频率超声降解MC-RR的影响Fig.7 Effect of different frequency on degradation of MC-RR by ultrasonic irradiation
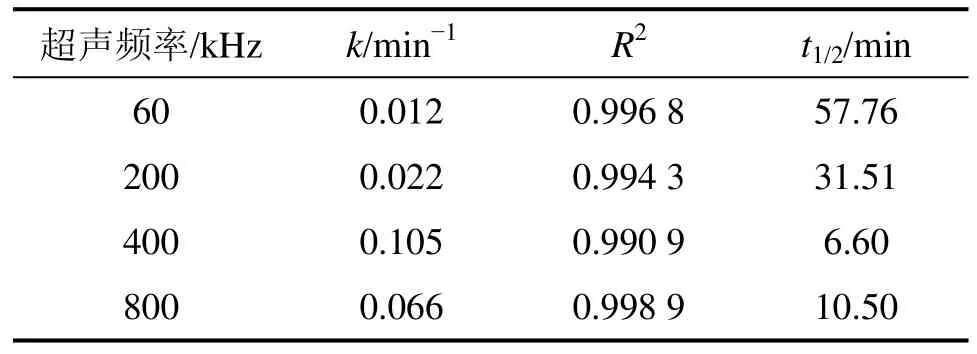
表2 不同频率超声降解MC-RR的准一级动力学模型的拟合参数Table 2 Fitting parameters of kinetics models (pseudo first-order)on degradation of MC-RR under different ultrasonic frequencies
不同频率作用下生成空化泡的数量、密度、空化泡溃灭时产生的温度、压力以及释放的自由基数量都不同,这些都影响降解效果。适当提高超声频率可提高降解效果,因为可产生更多空化泡/自由基和热解/水解反应;但当频率增大到一定极值之后反而不利于降解,随着频率不断增加,空化泡数量不再增加而趋于饱和状态,同时频率升高引起空化阈升高,使空化难以进行;空化泡存在周期缩短,溃灭强度也随之减弱,以上2种作用使空化发生概率和强度减小,降解速率降低,因此,超声波对于不同的化学物质存在不同的最佳降解频率。相关研究结果也证实了该结论,Song等[20]研究超声对二甲基异冰片(MIB)和二甲萘烷醇(GSM)的降解效果,结果表明:当频率为 640 kHz时,降解速度最快;张光明[21]采用超声处理水中的多氯联苯,其反应符合拟一级反应,最佳降解频率为358 kHz;Koda等[22]采用 20,40,45,96,130,200,400,500和1 200 kHz的超声辐照KI水溶液,发现碘的释放量最大频率为200 kHz。
值得注意的是:溶解气体也是影响因素之一。Inez等[11]在不同频率、不同溶解气体下研究超声的最优化工作条件,发现溶解气体类型和超声频率能影响反应效率,且溶有Kr气的溶液配合500 kHz的超声能得到最优工况。本试验得到的MC-RR最佳降解频率在400 kHz附近,实际最佳频率需采用连续变频超声发生装置可检测,限于试验条件本试验均采用400 kHz超声装置。
2.3 反应液pH值的影响
MC-RR反应液质量浓度为 500 μg/L,采用 400 kHz超声发生器,功率为100 W,反应时间为20 min,在0,3,8,14和20 min时取样进行检测,pH值从1.90调到12.21,在7个不同pH值条件下进行反应,并用反应速率常数k来表征反应速度。k随pH值变化见图 8;反应速率常数k、决定系数R2以及 MC-RR半衰期如表3所示。由图8可见:pH值在4~10时对反应影响甚小;当pH值大于10时,反应速率有一定下降;在pH值小于4的酸性条件下,反应速率明显提升,最快时(pH=1.9),k=0.400 min-1。
超声降解主要发生在空化泡气-液界面及其周围溶液中,离子/极性分子不易接近气-液界面且难以进入空化泡内,中性分子则较易接近空化泡并以更大比例分布于空化泡周围。研究表明:溶液酸碱性使有机污染物以中性分子的形态存在,并易于挥发进入气泡核内部,能有效促进降解反应[23]。而MC-RR在低pH值条件下可能以中性分子存在,其环状结构上单独存在可电离的 2个羧基,等电点分别是 2.09和 2.19。Maagd等[24]采用辛醇/水互溶体系研究MCs的亲疏水性,发现MCs在两相中的溶解平衡随pH值的变化而变化,且pH值在2.09~2.19时MCs以近似中性分子存在,较易从水相进入辛醇相中,同理,可推断 pH值为2.09~2.19时,MC-RR较易接近空化泡进而加速其降解,故较低 pH值有利于降解。国内外相关研究也证实了该理论,Maria等[5]研究不同条件下 TiO2光催化法对 MCs的降解效果,结果表明在酸性溶液(pH=3.0)中反应速率比中性溶液(pH=6.82)提升了 6倍;而陈伟等[25]采用超声波降解氯苯,发现pH值对氯苯降解的影响甚小,其原因是氯苯不随 pH值改变形态,从反面证实了 pH值对反应的影响。值得注意的是:酸碱性还影响到超声反应时溶液中 H2O2与OH·等强氧化物质的最大产率。因此,其影响是多因素综合作用的结果,详细机理还需进一步深入研究。本试验结果表明,最佳pH值小于2。

图8 pH值对超声降解MC-RR的影响Fig.8 Effect of different pH values on degradation of MC-RR by ultrasonic irradiation
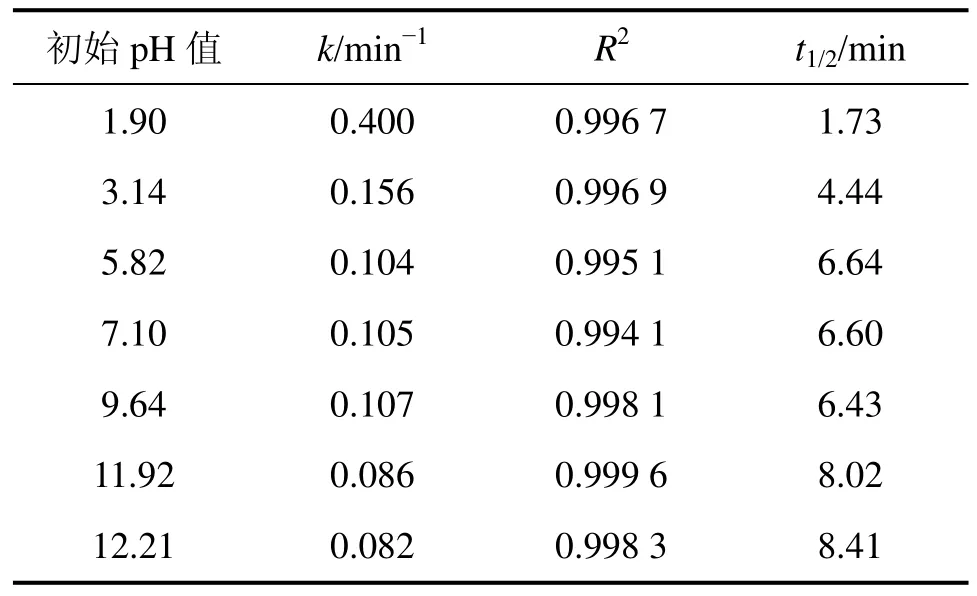
表3 不同pH值条件下超声降解MC-RR的准一级动力学模型数据Table 3 Degradation parameters of kinetics models (pseudo first order)under different pH values
随着反应进行,溶液pH值发生变化,测得5个初始pH值条件下变化情况如图9所示。可见:pH值均随着反应进行而下降,但在不同初始 pH值下变化幅度不同。反应过程中可能发生以下反应:

以上反应表明:空气中CO2溶解到水中不断消耗OH-,且超声波对水中有机物的矿化降解最终也产生CO2,理论上pH值应不断下降。实际反应过程符合理论分析。图9表明:当初始pH值较高或较低时,pH值随反应变化不明显,此时溶液中OH-或H+相对于溶解的 CO2充分过量,起到一定的缓冲作用;pH值为5~10时则无上述作用,当pH值为9.64时,经过20 min反应后pH值下降到6.80左右。pH值的变化影响超声降解MC-RR速率,但pH值变化较大的区间内MC-RR结构和分布变化较小,因此,对降解效果影响不明显。

图9 超声系统中不同初始pH值下溶液pH值随时间的变化Fig.9 Change of pH in solution with time in ultrasonic system under different initial pH
2.4 阴离子的影响
由图10可见:在相同反应条件下,阴离子的加入不利于MC-RR降解,加入后降解速率均有所下降;对反应影响较大,加入后降解速率仅为原来的68.37%;而影响较小。试验结果表明对反应存在部分抑制作用,证实了·OH是超声降解藻毒素的有效物质,但还存在其他降解作用如热解/水解,这与Song等[19]的研究结果相符。张光明等[26]在中性条件(pH=7.2)下采用不同频率的超声降解二氯联苯,并往反应溶液中加入碳酸盐,发现358 kHz时的超声降解效果比加入前降低了77%。郭照冰等[27]研究了加入不同阴离子对超声降解2, 4-二硝基酚的影响,结果显示 CO32-能使去除率降低约 60%。除阴离子外,对于其他·OH清除剂也可得到相似结论。岑科达等[28]采用甲醇和碘酸钾抑制·OH,通过紫外分光光度检测显示,在甲基橙的超声降解过程中·OH是主要有效成分。本试验中,4种离子对MC-RR降解的影响由大至小为:
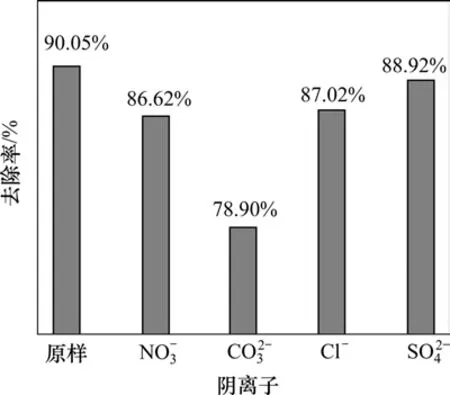
图10 不同阴离子条件下超声辐照对MC-RR的去除率Fig.10 Removal efficiency of MC-RR under different anions of ultrasonic irradiation

表4 加入不同阴离子条件下MC-RR降解的准一级动力学模型数据Table 4 Degradation parameters of kinetics models (pseudo first order)under different anions
2.5 声能密度的影响
声能密度指单位体积物质受到的超声波能量,在本反应中指单位体积溶液受到的超声辐照能量,单位为 W/mL。国内对有关超声降解有机物过程中声能密度的研究甚少。声能密度作为超声反应的1个基本参数,需要对其影响进行定量分析。本试验 MC-RR反应液质量浓度为500 μg/L,超声频率为400 kHz,功率为100 W,pH值为7.0,反应时间为20 min,采用不同的声能密度即1.67,3.33和6.67 W/ mL,在0,3,8,14和20 min时取样进行检测,藻毒素浓度变化见图11,反应速率常数k、决定系数R2以及MC-RR半衰期如表5所示。
由图 11可见:反应速率随着声能密度增大而加快,去除效果改善。声能密度越大,表明单位体积溶液受到超声辐照功率越大,且能产生更多的·OH和H2O2促进MC-RR的降解。国内外相关研究表明声能密度是超声反应中的影响因素之一。在超声降解机理分析方面,尹周澜等[29]采用茜素紫光度法检测超声辐照水体系产生的·OH浓度变化,在频率为20 kHz,声能密度约为12 W/mL时,·OH的产量基本达到饱和,且超声波作用产生的·OH与作用时间呈良好的线性关系。Gonze等[30]对不同结构的反应容器进行研究,所涉及的声能密度为0.1~10.0 W/mL,发现相同结构条件下声能密度是超声反应的主要影响因素。在降解试验研究方面,宁平等[31]采用超声降解焦化废水中的CODCr,发现声能密度对降解效果影响显著;Rong等[32]采用溶液循环反应器结合超声辐照降解氯苯,结果表明:随着声能密度增加降解速率升高。可见:降解速率受声能密度影响并与其成正比。本试验结果也证实了该理论。
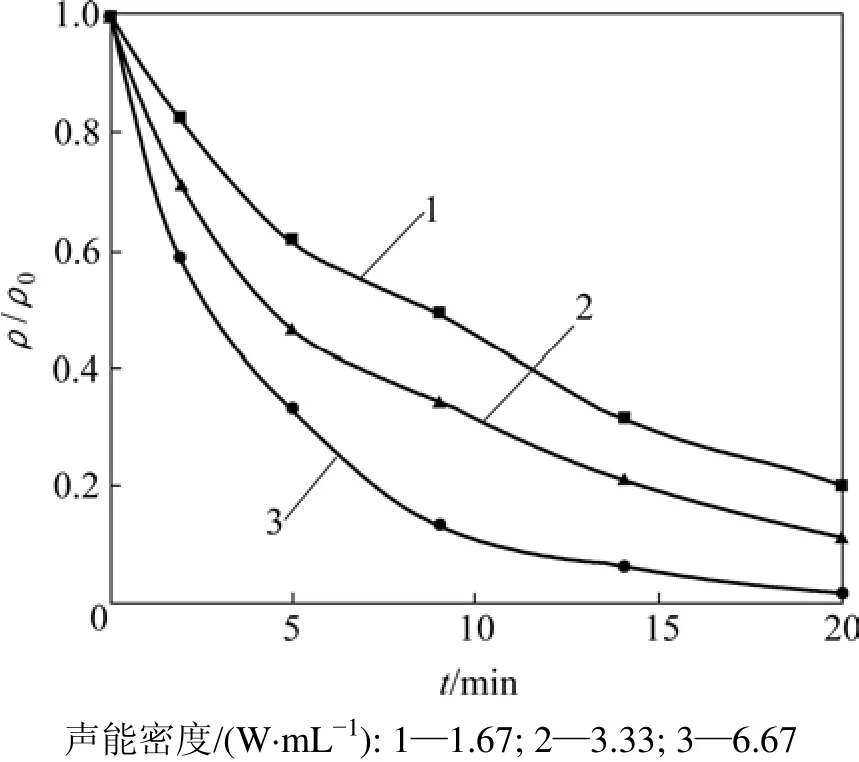
图11 不同声能密度对超声降解MC-RR的影响Fig.11 Effect of different sound-energy densities on degradation of MC-RR by ultrasonic irradiation
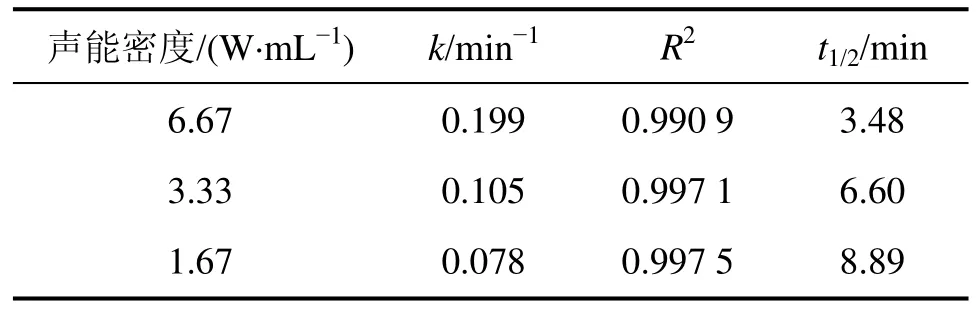
表5 不同声能密度下MC-RR降解的准一级动力学模型数据Table 5 Degradation parameters of kinetics models (pseudo first order)under different sound-energy densities of ultrasonic irradiation
3 结论
(1)超声辐照技术能有效降解MC-RR,降解反应符合准一级动力学模型。
(2)超声降解MC-RR受超声频率、初始pH值、声能密度以及影响较大。超声频率能改变水中空化泡分布和特性,中频超声降解效果最佳;溶液酸碱性对反应有明显影响,在酸性条件下,MC-RR化学结构和分布发生变化,反应速率提高;能有效清除·OH并阻碍MC-RR的降解,对降解速率影响不明显,反应速率常数由大至小顺序为:降解速率随声能密度的增加而提高,而初始浓度对反应速率无影响。
[1] 王波, 张光明, 马伯志, 等. 微囊藻毒素在超声场中的降解研究[J]. 环境科学, 2005, 26(6): 101-104.WANG Bo, ZHANG Guang-ming, MA Bo-zhi, et al. Study of sonochemical degradation of microcystins[J]. Environmental Science, 2005, 26(6): 101-104.
[2] Qiao R P, Li N, Qi X H, et al. Degradation of microcystin-RR by UV radiation in the presence of hydrogen peroxide[J]. Toxicon,2005, 45(6): 745-752.
[3] Rodriguez E, Onstad G D, Kull T P J, et al. Oxidative elimination of cyanotoxins: Comparison of ozone, chlorine,chlorine dioxide and permanganate[J]. Water Research, 2007,41(15): 3381-3393.
[4] Smg L R, Chen W, Peng L, et al. Distribution and bioaccumulation of microcystins in water columns: A systematic investigation into the environmental fate and the risks associated with microcystins in Meiliang Bay, Lake Taihu[J]. Water Research, 2007, 41(13): 2853-2864.
[5] Antonion M G, Shoemaker J A, de La Cruz A A, et al.LC/MS/MS structure elucidation of reaction intermediates formed during the TiO2photocatalysis of microcystin-LR[J].Toxicon, 2008, 51(6): 1103-1118.
[6] Hyenstrand P, Rohrlack T, Beattie K A, et al. Laboratory studies of dissolved radiolabelled microcystin-LR in lake water[J].Water Research, 2003, 37(14): 3299-3306.
[7] Rodriguez E M, Acero J L, Spoof L, et al. Oxidation of MC-LR and -RR with chlorine and potassium permanganate: Toxicity of the reaction products[J]. Water Research, 2008, 42(6/7):1744-1752.
[8] 刘成, 高乃云, 严敏, 等. 黄浦江源水中藻类和微囊藻毒素状况调查[J]. 中国给水排水, 2006, 22(15): 5-8.LIU Cheng, GAO Nai-yun, YAN Min, et al. Survey on algae and microcystin in source water of Huangpu River[J]. China Water &Wastewater, 2006, 22(15): 5-8.
[9] 左金龙, 崔福义, 徐勇鹏, 等. 饮用水源中藻毒素污染控制研究[J]. 水资源保护, 2005, 21(5): 1-5.ZUO Jin-long, CUI Fu-yi, XU Yong-peng, et al. Study on pollution control for cyanobacteria toxin in drinking water[J].Water Resources Protection, 2005, 21(5): 1-5.
[10] 陈伟, 梅滨, 范瑾初. 声化学研究的现状与发展[J]. 上海化工,1999, 24(3/4): 24-27.CHEN Wei, MEI Bin, FAN Jin-chu. The recent research and development of sonochemistry[J]. Shanghai Chemical Industry,1999, 24(3/4): 24-27.
[11] Hua I, Hoffmann M R. Optimization of ultrasonic irradiation as an advanced oxidation technology[J]. Environmental Science &Technology, 1997, 31(8): 2237-2243.
[12] 赵继华, 陈启元. 超声场对种分反应动力学过程的影响[J].中国有色金属学报, 2002, 12(4): 822-826.ZHAO Ji-hua, CHEN Qi-yuan. Effect of ultrasound on kinetics of aluminium trihydroxide precipitation Bayer process[J]. The Chinese Journal of Nonferrous Metals, 2002, 12(4): 822-826.
[13] Ding W C, Li D X, Zeng X L, et al. Enhancing excess sludge aerobic digestion with low intensity ultrasound[J]. Journal of Central South University of Technology, 2006, 13(4): 408-411.
[14] 吴纯德, 范瑾初. 超声空化降解水体中有机物的研究及发展[J]. 中国给水排水, 1997, 13(6): 28-30.WU Chun-de, FAN Jin-chu. Progress on research of ultrasonic technology for organic pollutant in water[J]. China Water &Wastewater, 1997, 13(6): 28-30.
[15] 唐玉霖, 高乃云, 庞维海. 超声波技术在饮用水中应用的研究进展[J]. 给水排水, 2007, 33(12): 113-118.TANG Yu-lin, GAO Nai-yun, PANG Wei-hai. Progress on research of ultrasonic technology for drinking water[J]. Water &Wastewater Engineering , 2007, 33(12): 113-118.
[16] 李占双, 闫冰, 李凯峰. 超声降解水体中有机污染物的研究现状[J]. 应用科技, 2003, 30(6): 45-47.LI Zhan-shuang, YAN Bing, LI Kai-feng. Study of organic pollutant in ultrasonic decomposed water[J]. Applied Science and Technology, 2003, 30(6): 45-47.
[17] Mason J, Lorimer P. Ultrasound: theory, applications and uses of ultrasound in chemistry[M]. Chichester: Ellis Horwood Ltd,1981: 252.
[18] Ressom R, Soong S, Fitzgerald J, et al. Health effects of toxic cyanobacteria (blue-green algae)[M]. Canberra: Australian Government Publishing Service, 1994: 180.
[19] Song W H, Teshiba T, Rein K, et al. Ultrasonically induced degradation and detoxification of microcystin-LR(cyanobacterial toxin)[J]. Environmental Science & Technology,2005, 39(16): 6300-6305.
[20] Song W H, O'Shea K E. Ultrasonically induced degradation of 2-methylisoborneol and geosmin[J]. Water Research, 2007,41(12): 2672-2678.
[21] 张光明. 超声波处理多氯联苯微污染技术研究[J]. 给水排水,2003, 29(13): 30-33.ZHANG Guang-ming. Ultrasonic abatement of aqueous trace lever pollutants: polychlorinated biphenyls[J]. Water &Wastewater Engineering, 2003, 29(13): 30-33.
[22] Koda S, Kimura T, Kondo T, et al . A standard method to calibrate sonochemical efficiency of an individual reaction system[J] . Ultrasonics Sonochemistry, 2003, 10(3): 149-156.
[23] 马军, 赵雷. 超声波降解水中有机物的影响因素[J]. 黑龙江大学自然科学学报, 2005, 22(2): 142-153.MA Jun, ZHAO Lei. Influencing factors on ultrasonic degradation of organic compound in water[J]. Journal of Natural Science of Heilongjiang University, 2005, 22(2): 142-153.
[24] De Maagd P G J, Hendriks A J, Seinen W, et al. pH-Dependent hydrophobicity of the cyanobacteria toxin microcystin-LR[J].Water Research, 1999, 33(3): 677-680.
[25] 陈伟, 陈玲, 范瑾初, 等. 超声辐照降解水中氯苯的研究[J].给水排水, 2001, 27(12): 34-37.CHEN Wei, CHEN Ling, FAN Jin-chu, et al. Study on degradation of chlorobenzene in aqueous solution by ultrasonic irradiation[J]. Water & Wastewater Engineering, 2001, 27(12):34-37.
[26] 张光明, 周吉全, 张锡辉, 等. 超声波处理难降解有机物影响参数研究[J]. 环境污染治理技术与设备, 2005, 6(5): 42-45.ZHANG Guang-ming, ZHOU Ji-quan, ZHANG Xi-hui, et al.Study of sonication parameters for refractory organic chemicals[J]. Techniques and Equipment for Environmental Pollution Control, 2005, 6(5): 42-45.
[27] 郭照冰, 郑正, 费正皓, 等. 水中2, 4-二硝基酚超声降解的研究[J]. 环境化学, 2008, 27(2): 186-189.GUO Zhao-bing, ZHENG Zheng, FEI Zheng-hao, et al. Study on degradation of 2, 4-Dinitrophenol by ultrasonic-wave[J].Environmental Chemical, 2008, 27(2): 186-189.
[28] 岑科达, 殷福才, 程建萍. 超声降解水溶性偶氮染料甲基橙的实验研究[J]. 合肥工业大学学报, 2007, 30(1): 77-81.CEN Ke-da, YIN Fu-cai, CHENG Jian-ping. Experimental study on sonochemical degradation of methyl orange in aqueous solution[J]. Journal of Hefei University of Technology: Natural Science, 2007, 30(1): 77-81.
[29] 尹周澜, 张牧群, 刘吉波, 等. 茜素紫光度法检测超声波辐照水体系产生的羟自由基[J]. 中南大学学报: 自然科学版, 2004,35(5): 793-796.YIN Zhou-lan, ZHANG Mu-qun, LIU Ji-bo, et al. Assay of hydroxy producted from ultrasonic using alizarin violet spectphotometry[J]. Journal of Central South University: Science and Technology, 2004, 35(5): 793-796.
[30] Gonze E, Gonthier Y, Boldo P, et al. Study on pentachlorophenol oxidation under different geometric parameters of high-frequency sonoreactors[J]. Canadian Journal of Chemical Engineering, 1997, 75(1): 245-255.
[31] 宁平, 徐金球, 黄东宾, 等. 超声辐照-活性污泥联合处理焦化废水[J]. 环境科学, 2003, 24(3): 65-69.NING Ping, XU Jin-qiu, HUANG Dong-bin, et al. Treatment of carbonization effluent by the ultrasonic radiation and activated sludge process[J]. Environmental Science, 2003, 24(3): 65-69.
[32] Rong L, Koda S, Nomura H. Study on degradation rate constant of chlorobenzene in aqueous solution using a recycle ultrasonic reactor[J]. Journal of Chemical Engineering of Japan, 2001,34(8): 1040-1044.

