应用实时三平面应变率成像评价心房纤颤患者左心房功能
吕启凤,王志斌,聂 晶,李 艳,付秀秀
(青岛大学医学院附属医院心脏超声科,山东 青岛 266003)
心房纤颤(AF)患者左心房功能的变化对预后有重要的影响。AF患者的储备功能和管道功能明显受损,持续性AF和发作时的阵发性AF患者的助力泵功能消失[1-2]。实时三平面应变率成像能够在同一心动周期、同一时相、同步显示三个运动切面,可以直接反映局部心肌功能,不受邻近节段心肌运动及心脏整体运动的影响,较以往的单平面应变率成像更具有优势[3]。本研究旨在应用实时三平面应变率成像技术检测AF患者左心房局部心肌功能,并进一步探讨其临床价值。
1 资料与方法
1.1 研究对象
选取2008年12月~2009年3月我院门诊和住院的AF患者82例作为AF组,男45例,女37例,年龄 35~79 岁,平均(58±12)岁。 其中阵发性 AF(持续时间<7d)患者35例,持续性AF(持续时间≥7d)患者47例。病例入选标准:①心电图表现符合AF的心电图诊断标准;②无其他心律失常或心脏传导异常;③无轻度以上二尖瓣和/或主动脉瓣反流;④超声图像质量理想;⑤入选患者均停用除颤药物至少2周以上。选取年龄、性别和AF组相匹配的健康志愿者33例为正常对照组,男19例,女14例,年龄38~78 岁,平均(52±12)岁。
1.2 仪器与方法
GE Vivid 7 Dimension彩色多普勒超声诊断仪,配有超宽频电子相控阵探头和实时三维心脏探头,探头频率范围1.5~4.3MHz,并同步记录心电图。
受检者左侧卧位,平稳呼吸。首先应用二维超声心动图在胸骨旁左心室长轴切面测量室间隔舒张末厚度、左心室后壁舒张末厚度、左心室舒张末内径、左心房内径和左心房短轴缩短率。以Teichholtz公式计算左心室射血分数。然后,应用脉冲多普勒在心尖四腔心切面记录舒张期二尖瓣口血流,测量舒张早期与心房收缩期峰值流速的比值以及舒张早期减速时间,再于左心房底部右上肺静脉入口处记录肺静脉血流频谱,测量右上肺静脉血流频谱S峰、D峰、A谷的峰值流速。之后,实时三维心脏超声探头于心尖部记录心尖四腔心图像,启动实时三平面成像技术,同时获得心尖四腔、心尖两腔和心尖长轴切面,进行应变率分析。取应变长度为12cm,取样容积为4mm×2mm,将取样容积分别置于左心房侧壁、房间隔、前壁、下壁和后壁中间段心内膜下心肌组织内,获取应变率曲线,测量上述5个心房壁的收缩期、舒张早期和心房收缩期峰值应变率,其平均值为收缩期、舒张早期和心房收缩期左心房心肌平均峰值应变率(MSR)。
在研究过程中,超声图像资料均在受检者呼气末屏气状态下采集并储存,然后进行联机分析,每个指标至少测量3个连续心动周期,取平均值。
1.3 统计学分析
应用SPSS 13.0统计学软件,计量资料以x±s表示,组间变量比较采用单因素方差分析和S-N-K检验。P<0.05为差异有统计学意义。
2 结果
对33例健康志愿者、35例阵发性AF患者、47例持续性AF患者进行分析,以排除年龄和性别对测值的影响。对照组、阵发性AF和持续性AF各组间的性别构成、年龄差异无统计学意义(P>0.05)。与年龄匹配的对照组相比,收缩期左心房心肌平均峰值应变率(MSRs)和舒张早期左心房心肌平均峰值应变率(MSRe)在阵发性 AF 组偏低(P<0.05,0.01),并且在持续性AF组显著偏低 (P<0.01),MSRs和MSRe在持续性和阵发性AF组之间有明显差异 (P<0.01),MSRs和MSRe在对照组、阵发性AF组和持续性AF组中逐渐减小。年龄匹配的阵发性AF组和对照组之间的心房收缩期左心房心肌平均峰值应变率(MSRa)没有显著的差异(P>0.05),见表1。 对照组左心房各壁心肌平均峰值应变率的测量结果见表2。

表1 3组患者一般临床资料、常规超声心动图和应变率成像参数的比较
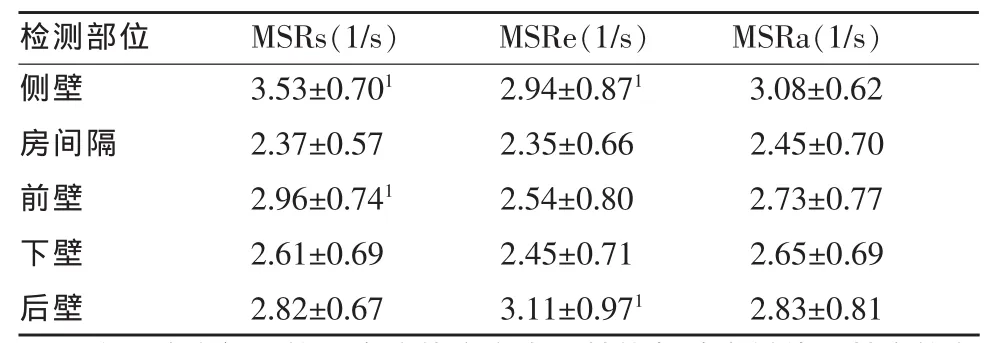
表2 对照组左心房各壁心肌平均峰值应变率的测量结果
3 讨论
实时三平面成像技术是以一个二维标准切面为基准切面,在此基准切面的基础上,以空间60°角的切割关系,获取与此基准切面互成60°角和120°角的两个切面,因此该技术可在同一心动周期、同一时相、同步显示三个运动切面。因此,此项新技术只需在一个标准成像方位上扫取图像,即可同时获取3个运动切面,不仅节省了扫查时间,而且可以对同一心动周期、同一时相的左心房各个心肌节段进行同步分析,因此可以避免不同心动周期和时相的变异对左心房各壁定量分析的影响,使得各壁心肌运动更具可比性[3]。应变率成像技术作为一种无创的新的成像技术,能够直接反映局部心肌功能,且不受周围心肌节段和心脏整体运动的影响,与以往的技术相比能更直观准确的反映心肌的运动,可以对心脏的局部心肌功能作出更好的评价[4-5]。
左心房在心动周期的不同时相主要表现为具有储备功能、管道功能、助力泵功能等3种主要功能[5]。这3种功能在应变曲线上分别表现为:①储备功能,是左心室收缩期左心房壁的被动拉伸运动产生的,反映心房舒张期的充盈,可用收缩期峰值应变率来评价;②管道功能,在心室舒张早期血液从肺静脉经过左心房流入左心室,左心房类似一个通道,在应变曲线上可用舒张早期峰值应变率来评价;③助力泵功能,是左心室舒张晚期左心房壁的缩短运动,反映左心房壁的主动收缩能力,在应变曲线上可用心房收缩期峰值应变率来评价[2]。
研究结果表明MSRs在持续性AF组有明显的下降,MSRs是反映收缩期应变率的参数的正性运动,即左室收缩期左房壁的被动牵张,故该结果说明持续性AF患者的左心房壁的被动伸拉运动明显下降,舒张期的心房充盈明显受损。MSRe在持续性AF组也有明显的下降,说明AF患者左心房作为一个左心室的通道功能也明显受损。对照组和阵发性AF组均无左房扩大和肥厚,MSRa在对照组和阵发性AF组中没有发现明显的差别,该结果说明阵发性AF患者的左心房主动收缩能力与对照组相比没有明显的损害,说明持续时间较短的AF患者的心房收缩功能损害不明显,以往研究也证实了这点[6]。房间隔的MSR比其他各壁有减低的趋势,可能与左心房不同部位的心肌分布有关。本研究结果也表明了与以往的常规左心房的研究方法相比,实时三平面应变率成像技术能更准确的表示出对照组和持续性AF组、阵发性AF组的不同时期心肌的运动差异,能更加敏感的反映AF患者的左心房功能的变化。
超声心动图测量的AF患者的左心房较健康志愿者增大,反映出心房内压力较健康志愿者升高,这是因为AF时由于左心房丧失主动收缩功能,使心功能降低甚至恶化,加重心功能不全患者的负担,左心房由于进一步排空功能的丧失及心室收缩早期的主动舒张能力的显著降低,心房内压力升高。压力的升高对心肌功能的影响有待进一步研究。然而由于心房内压力升高,肺静脉血向左心房内回流减少,舒张早期房室间压差降低,左心室充盈的动力减少,左心房血液不能有效排空而容易淤积形成心房附壁血栓,血栓脱落可致体循环栓塞[2]。应变率成像技术可以直接反映心肌的运动,它不受心脏旋转及邻近室壁牵拉的影响,因此在评价心房肌局部功能方面具有明显优势,并且有很好的敏感性,故该技术可以作为研究左心房功能的新手段,并且可以对AF的并发症(如血栓栓塞)的预防起到相应的提示作用。
本研究在技术上仍有不足之处。实时三平面应变率成像技术对图像的质量有较高的要求,由于左心房形态不规则,仍难以全面评价左心房的功能。实时三平面成像技术是以一个二维标准切面为基准切面,在此基准切面的基础上,以空间60°角的切割关系,获取与此基准切面互成60°角和120°角的两个切面,后两个切面的定位是以第一个基准切面的定位为基础的,在心房变形严重的患者中切面显示尤其欠佳。如何更好的获得满意的图像质量和显示所有标准切面,可以做进一步的研究和改进。
综上所述,AF患者的储备功能和通道功能明显受损。实时三平面应变率成像技术能够应用于评价AF引起的左心房功能受损,并具有重要的临床意义。

[1]Schneider C,Malisius R,Krause K,et al.Strain rate imaging for functional quantification of the left atrium:atrial deformation predicts the maintenance of sinus rhythm after catheter ablation of atrial fibrillation[J].Eur Heart J,2008,29:1397-1409.
[2]Inaba Y,Yuda S,Kobayashi N,et al.Strain rate imaging for noninvasive functional quantification of the left atrium comparative studies in controls and patients with atrial fibrillation[J].J Am Soc Echocardiogr,2005,18:729-736.
[3]张静,谢明星,王新房,等.实时三平面组织多普勒超声心动图评价心脏手术对左心室局部收缩功能的影响[J].中华超声影像学杂志,2005,14(12):892-895.
[4]Wang ZH,Tan HW,Zhong M,et al.Strain rate imaging for noninvasive functional quantification of the left atrium in hypertensive patients with paroxysmal atrial fibrillation[J].Circulation,2008,109:15-24.
[5]田新桥,钱蕴秋,李军,等.组织速度、应变率与应变成像诊断冠心病的临床对比研究[J]. 中国超声医学杂志,2007,23(3):194-196.
[6]Reant P,Lafitte S,Ja觙s P,et al.Reverse remodeling of the left cardiac chambers after catheter ablation after 1 year in a series of patients with isolated atrial fibrillation[J].Circulation,2005,112(19):2896-2903.

