As2O3对胃癌的黏附分子、VEGF、nm23表达的影响
于齐宏 杨幼林 蔡朋朋
胃癌是我国常见的消化系统恶性肿瘤,其发病率高,早期诊断率低,中晚期时常规放疗、化疗效果不理想,目前尚缺乏有效的治疗手段。因此,寻找新的治疗药物及治疗手段,抑制肿瘤的浸润、发展、转移,乃是当务之急。
近年的研究热点三氧化二砷抑制胃癌细胞生长、浸润和转移作用,已成功地在多种培养肿瘤细胞株的体外实验和动物实体肿瘤中得以验证,且对其抑制肿瘤细胞生长、浸润和转移分子生物学机制亦有一定程度的阐述。三氧化二砷目前应用于临床在初治、复发、耐药的急性早幼粒细胞白血病治疗上疗效显著,且不良反应较轻,是一种相对安全有效的新药物,这一点已获国际共识,但是,对胃癌的临床应用尚未见相关报道。
本实验通过对胃癌病人短时间、小剂量三氧化二砷的应用,观察用药前后CD44、E-CD、VEGF、nm23的变化,探讨三氧化二砷抑制胃癌生长、浸润和转移的机制,以期寻找治疗胃癌的新途径。
1 材料与方法
1.1 实验材料
1.1.1 实验标本
标本是在2007年9月至2007年11月间分别取自哈尔滨医科大学附属第一医院、解放军211医院、大庆油田总医院的病理科的存档蜡块,26块胃癌均为腺癌,术前接受三氧化二砷化疗,均未接受放疗。
1.1.2 实验试剂
①苏木素染液;②0.01mol/L PBS缓冲液;③兔抗人E-CD多克隆抗体IgG1浓缩液:购自博士德生物制剂有限公司;④鼠抗人VEGF单克隆抗体:购自北京中山生物制剂有限公司5、鼠抗人nm23单克隆抗体:购自北京中山生物制剂有限公;⑥鼠抗人CD44单克隆抗体:购自北京中山生物制剂有限公司;⑦山羊抗小鼠IgG抗体-HRP多聚体:购自北京中山生物制剂有限公司;⑧辣根过氧化物酶显色剂DAB:购自北京中山生物制剂有限公司;⑨三氧化二砷注射液。
1.1.3 仪器及设备
①酒精灯;②电热恒温干燥箱;③切片机;④高压锅;⑤光学显微镜;⑥天平;⑦胃镜。
1.2 实验方法
①在胃镜提取癌组织标本,并经病理证实。留取癌组织标本。②化疗:对该患者应用5%葡萄糖注射液500mL中加入As2O3注射液(浓度5mmol/10mL)2支,1次/d静脉滴注,共3d。③同一患者化疗后手术中:再取组织标本。④所有组织均经10%中性甲醛固定,石蜡包埋。以4μm厚度做连续片。分别作HE染色和免疫组织化学染色。⑤采用免疫组织化学二步法分别检测各组织中E-CD、VEGF、nm23、CD44的表达情况。免疫组织化学具体步骤如下:①将石蜡切片常规二甲苯脱蜡,梯度酒精水化;②3%过氧化氢-甲醇溶液孵育10min,阻断内源性过氧化物酶;③石蜡切片高压抗原修复法进行抗原修复;④滴加一抗(阴性对照以磷酸盐缓冲液PBS代替一抗,以已知阳性反应片作为阳性对照),37℃孵化12h;⑤PBS缓冲液冲洗,5min,3次;⑥滴加山羊抗小鼠IgG抗体-HRP多聚体(PV-6000),37℃孵化20min;⑦PBS缓冲液冲洗,5min,3次;⑧DAB显色;⑨蒸馏水冲洗3min,苏木素复染;⑩酒精脱水,二甲苯透明,封片。
1.3 实验指标检测
①E-CD:一抗为兔抗人多克隆抗体IgG1浓缩液,免疫组织化学结果以化学显微镜观察,阳性细胞为胞质着色棕黄色。②VEGF:一抗为鼠抗人单克隆抗体IgG1浓缩液,免疫组织化学结果以光学显微镜观察,阳性细胞为胞质着色棕黄色。③nm23:一抗为鼠抗人单克隆抗体IgG2a浓缩液,免疫组织化学结果以光学显微镜观察,阳性细胞为胞质着色棕黄色。④CD44:一抗为鼠抗人单克隆抗体IgG2a浓缩液,免疫组织化学结果以光学显微镜观察,阳性细胞为胞质着色棕黄色。
1.4 结果判定
E-CD、VEGF、nm23、CD44表达在癌细胞胞膜和细胞质,胞质有棕黄色颗粒沉着的为阳性细胞,观察5个具有代表性的高倍视野,计数阳性细胞数与总细胞数比值。
1.5 统计学处理
应用非参数检验中秩和检验,P<0.05差异显著性。
2 结 果
2.1 E-CD、VEGF、nm23、CD44在胃癌组织中的表达
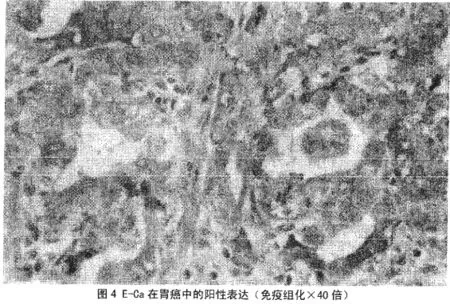
化疗前后E-CD在胃癌肿瘤组织中表达情况,见表1和图3、图4。

表1 化疗前后E-CD在胃癌肿瘤组织中表达情况(%)
E-CD在术前与术后胃癌肿瘤组织中表达的比较,采用非参数秩和检验,结果显示,P<0.05,有统计学意义。E-CD在术前癌组织与术后癌组织中的表达明显降低。
2.2 化疗前后CD44在胃癌肿瘤组织中表达情况,见表2和图1、图2。
表2结果显示,CD44术前癌组织与术后癌组织中表达的比较采用非常熟秩和检验,P<0.05,有统计学意义。CD44在术前癌组织与术后癌组织中的表达明显降低。

表2 化疗前后CD44在胃癌肿瘤组织中表达情况(%)
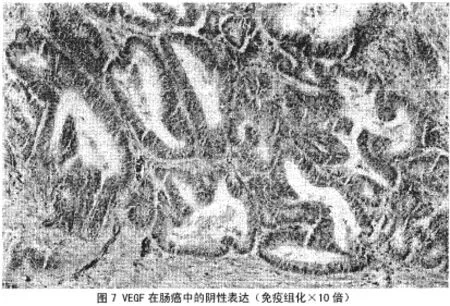
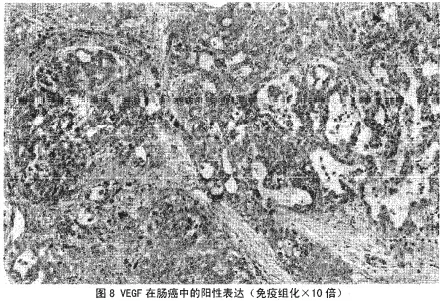
2.3 化疗前后VEGF在胃癌肿瘤组织中表达情况,见表3和图7、图8。
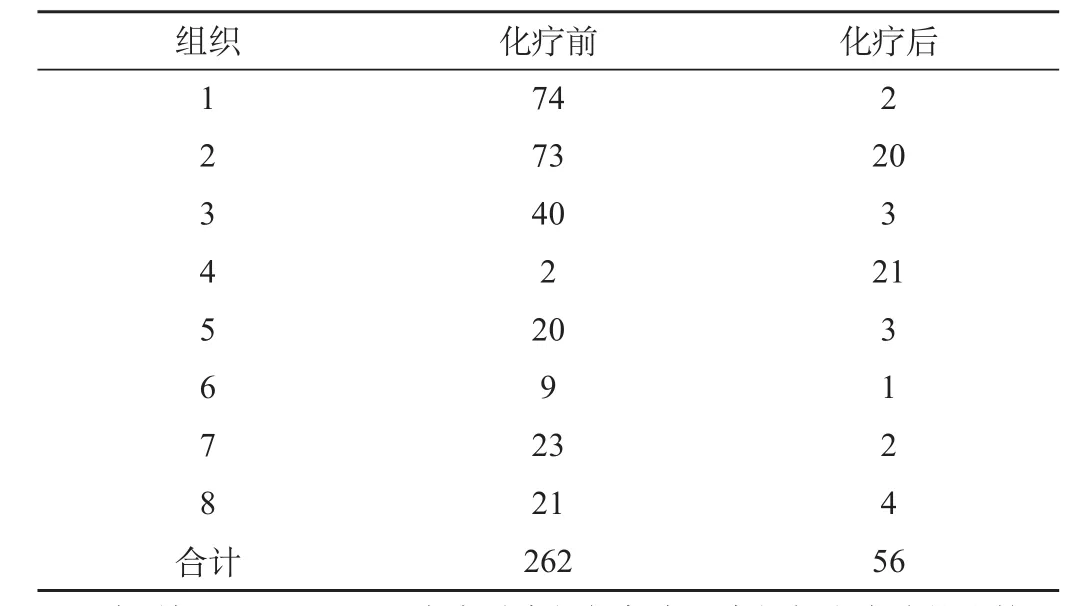
表3 化疗前后VEGF在胃癌肿瘤组织中表达情况(%)
表3结果显示,VEGF在术前癌组织与术后癌组织中表达的比较,采用非参数秩和检验,P<0.05,有统计学意义。VEGF在术前癌组织中与术后癌组织中的表达明显降低。
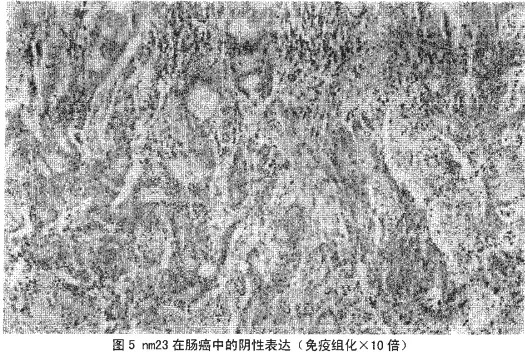
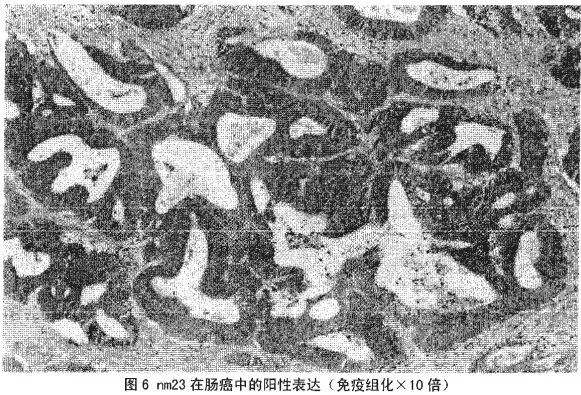
2.4 化疗前后nm23在胃癌肿瘤组织中表达情况,见表4和图5、图6。

表4 化疗前后nm23在胃癌肿瘤组织中表达情况(%)
表4结果显示,nm23在术前癌组织与术后癌组织中的比较采用非参数秩和检验,P<0.05,有统计学意义。nm23在术前癌组织与术后癌组织中的表达明显升高。
3 讨 论
胃癌是常见的恶性肿瘤,多数患者在诊断时已达中晚期,无法手术;而目前治疗中晚期胃癌,对于多数患者来说药物单一,且疗效较差。三氧化砷注射液是我国自行开发研制的抗癌新药,近年来在急性早幼粒细胞白血病的治疗中已取得明显突破,引起世人瞩目。目前已有一些三氧化二砷注射液治疗实体瘤的实验研究报道,但是有关临床研究较少,仅见原发性肝癌[1-3]、胆囊癌[4]、口腔鳞癌[5]和食管癌[6]等。
肿瘤细胞的侵袭与转移是十分复杂的生物学现象,是多因素、多
阶段的过程,与许多基因的异常表达有关。目前体外癌细胞培养和动物模型研究表明,E-CD、VEGF、CD44、nm23是这些调控因子中较为重要的,在癌的侵袭与转移中发挥着重要的作用。因此,促使CD44、E-CD、VEGF、nm23在癌组织中的正常表达有利于成为抑制肿瘤的转移的新途径。本实验中,主要对胃癌的患者短时间,小剂量的应用三氧化二砷化疗,研究三氧化二砷对肿瘤组织中E-CD、VEGF、CD44、nm23的作用,探讨三氧化二砷抗肿瘤侵袭和转移的作用。
3.1 三氧化二砷对肿瘤组织中E-CD、CD44的作用
E-CD、CD44同属于黏附分子,在肿瘤侵袭转移的各个环节中都涉及细胞黏附作用。肿瘤细胞从原发瘤体脱离,与瘤细胞间黏附力降低有关;肿瘤细胞在血管内形成同质或异质性瘤栓,亦是黏附作用的结果;在侵袭过程中肿瘤细胞和血管内皮及内皮下基底膜的黏附;以及肿瘤细胞穿出血管壁与宿主细胞的黏附等。这些黏附作用是位于细胞表面的细胞黏附分子介导的。
3.1.1 三氧化二砷对胃癌肿瘤组织中CD44的作用
CD44属于黏附分子家族透明质酸受体类,CD44的主要配体为透明质酸(HA),此外,层粘连蛋白、纤维链接蛋白的肝素结构域以及Ⅰ型和Ⅳ型胶原等也可作为其配体。大量研究表明,它的表达与多种肿瘤的浸润和转移有关。CD44分布十分广泛,除少量分布于增生分裂功能旺盛的正常组织(如造血组织)外,大量表达于癌前病变和恶性肿瘤。CD44高表达,促进癌的侵袭和转移。
本实验结果显示,术前癌细胞与术后癌细胞中CD44表达的比较采用非参数秩和检验,有明显统计学意义(P<0.05)。化疗前后CD44在胃癌肿瘤组织中表达显著降低,提示三氧化二砷对胃癌肿瘤组织中CD44有抑制作用。
3.1.2 三氧化二砷对胃癌肿瘤组织中E-CD的作用
E-CD是介导细胞与细胞间互相黏附的同质型钙依赖型跨膜蛋白。E-CD介导的细胞黏附系统失活减少细胞与细胞间黏附从而导致了细胞极性的丢失及组织结构的溶解、破坏。故而E-CD介导的细胞黏附系统在肿瘤的侵袭及转移中起着重要作用。国内为大量文献报道,E-CD的表达缺失与肿瘤的侵袭及转移相关。
本实验结果显示,化疗前后E-CD在胃癌肿瘤组织中表达降低。提示三氧化二砷对胃癌肿瘤组织中E-CD无作用。
目前有明显报道,三氧化二砷能降低细胞质内游离的钙离子,而E-CD为钙依赖型跨膜蛋白,三氧化二砷化疗后,E-CD无意义可能与三氧化二砷化疗时间不够,应用剂量小,未能引起肿瘤组织的去甲基化,及调节E-CD多肽酶的变化有关。另外,也可能与三氧化二砷代谢导致E-CD的分布异常有关,而出现了上述结果。三氧化二砷对胃癌肿瘤组织中E-CD的表达影响有待于进一步研究。
3.2 三氧化二砷对胃癌肿瘤组织中VEGF的作用
肿瘤新生血管的形成,不仅为肿瘤的增长提供营养和气体交换,而且也是肿瘤细胞浸润、转移的直接途径。肿瘤血管的起动是由肿瘤细胞分泌的促内皮细胞增殖和迁移的多种血管生长因子所诱发,诸如血管内皮生长因子通过内皮细胞上的特异性受体刺激血管内皮细胞增殖和毛细血管攀形成,并产生PAs和胶原酶。这不仅有利于血管生成,而且还促使癌细胞脱落进入血管或扩散至邻近纤维蛋白和结缔组织基质,为肿瘤浸润、转移创造条件。VEGF增加血管通透性导致血浆蛋白和纤维蛋白外渗至细胞外间隙,外渗的纤维蛋白与其他蛋白质如纤维连结蛋白等凝结成纤维凝胶,为成纤维细胞、内皮细胞和其他细胞移动、侵入提供暂时的基质成分,并最终将它转化为血管化的连接组织。
本实验结果显示,化疗前后VEGF在胃癌肿瘤组织中表达率分别为46.2%和3.8%。术前癌组织与术后癌组织中VEGF表达的比较采用Fisher确切概率法,组间差异有统计学意义(P<0.05)。化疗前后VEGF在胃癌肿瘤组织中表达率显著降低。提示三氧化二砷对胃癌肿瘤组织中有VEGF抑制作用。
考虑三氧化二砷对胃癌肿瘤组织中VEGF抑制作用可能是通过以下途径。国内外大量文献报道三氧化二砷诱导肿瘤细胞凋亡。三氧化二砷能够调节凋亡相关基因H-ras、K-ras、p53的表达。H-ras、K-ras、p53对VEGF有调控作用[7,8]。因此,H-ras、K-ras、p53表达上调抑制VEGF的表达。
3.3 三氧化二砷对胃癌肿瘤组织中nm23的作用
nm23是一个重要的肿瘤转移抑制基因,nm23定位于人17号染色体长臂远端,它可以抑制参与细胞转移连锁反应中蛋白质或直接作用于转移相关基因的RNA或DNA。nm23基因的低表达已经在多种高转移肿瘤中被证实。通过分析乳腺癌、卵巢癌、肝癌、恶性黑色素瘤等均发现[9-12],nm23基因缺乏及其产物低表达与疾病进展及高转移潜力呈正相关,且预后也差。
本实验结果显示,化疗前后VEGF在胃癌肿瘤组织中表达率分别为11.5%和61.5%。术前癌组织与术后癌组织中VEGF表达的比较采用Fisher确切概率法,组间差异有统计学意义(P<0.05)。化疗前后VEGF在胃癌肿瘤组织中表达率显著增高。提示三氧化二砷对胃癌肿瘤组织中有调节nm23作用。
三氧化二砷作为一种细胞毒药物,长期以来被认为能抑制细胞DNA的合成,干扰细胞代谢,致染色体畸变或损害细胞基因。三氧化二砷对癌细胞的效应是广泛的,可引起多种肿瘤细胞的多种基因的表达改变。本实验提示,三氧化二砷对胃癌肿瘤的表达均有影响,证实了其作用的广泛性。作为癌组织的调控因子,参与肿瘤的浸润与转移。三氧化二砷对它们表达的影响,从而抑制了肿瘤的浸润与转移,从一个新角度探讨三氧化二砷的抗肿瘤的作用。初步提示了三氧化二砷的抗肿瘤作用除了传统的抗凋亡,抑制肿瘤细胞增殖作用外,可能还与抑制肿瘤的浸润及转移有关。并为三氧化二砷抗肿瘤提供新的依据。
4 结 论
本实验中,主要对胃癌的患者短时间、小剂量的应用三氧化二砷化疗,研究三氧化二砷对胃癌肿瘤组织中E-CD、VEGF、CD44、nm23的作用,得出以下结论:①三氧化二砷对胃癌肿瘤组织中CD44表达有抑制作用。②三氧化二砷对胃癌肿瘤组织中E-CD的表达有抑制作用。③三氧化二砷对胃癌肿瘤组织中VEGF的表达有抑制作用。④三氧化二砷对胃癌肿瘤组织中nm23的表达增高。
三氧化二砷对胃癌肿瘤组织中VEGF、CD44抑制作用,nm23促进作用,推测出三氧化二砷抑制胃癌肿瘤组织的浸润及转移。
[1] 秦叔选,钱军,马军,等.三氧化二砷肿瘤原发性肝癌获缓解1例[J] .临床肿瘤学杂志,1999,4(2):51-52.
[2] 余萍,涨英潮,陈萍,等.三氧化二砷肿瘤原发性肝癌2例报告[J] .肿瘤防治杂志,2001,8(4):373-374.
[3] 朱安龙,刘连新,朴大勋,等.应用三氧化二砷连续区域化疗治疗肝癌[J] .中华肝胆外科杂志,2003,9(4):205-206.
[4] 秦叔连,钱军,何泽明,等.三氧化二砷注射液肿瘤晚期胆囊癌[J] .临床肿瘤杂志,2000,5(4):286-287.
[5] 竺涵光,王跃平,张志愿,等.三氧化二砷经导管动脉介入治疗口腔鳞癌:附3例报告[J] .口腔医学纵横,2000,16(1):35-37.
[6] 焦智民,王俊生,杜景富.亚砷酸注射液治疗复发转移的食道癌临床观察[J] .中国中西医结合杂志,2002,22(9):713-714.
[7] Larcher-F,Robles-AI,Duran-H,et al. Up-regulation of vascular endothelial growth factor vascular permeability factor in mouse skin carcinogenesis correlates with malignant progression state and activated H-ras expression levels[J] .Cancer Res,1996,56(23):5391-5396.
[8] 张延龄,抗血管生成疗法在治疗外科中的作用[J] .国外医学外科分册,1999,26(5):259.
[9] Florences VA,Amdal S,Myklebost O,et al. Levels of nm23 essenger-RNA in metastatic malignant melanogas: inversecorrelation to disease progression[J] .Cancer Res,1992,52(21):6088.
[10] Bevilacqua G,Sobel ME,Liotta LA,et al. Association of low nm23 RNA levels in human primary infiltrating ductal breast carcinomas with lymph node involvement and other histopathological in dicators of high metastatic potiential[J] .Cancer Res,1989,49(18):5189.
[11] Martinez JA,Prevot S,Nordlinger B,et al. Overexpression of nm23-HI and nm23-H2 genes in colorectal carcinomas and loss of nm23-HI expression in advenced tumor stages[J] .Gut,1995,37(5):721.
[12] Nakayama T,Ohtsarn A,Nakao K,et al. Expression in human hepatocellular carcinoma of nucleoside diphosphate kinase,a homologue of the nm23 gene product[J] .Clin EXP Metastasis,1993,11(2):1151.

