联吡啶钌体系电致化学发光测定盐酸苯海索的研究
盐酸苯海索(Benzhexol hydrochloride),又名安坦、盐酸三己芬迪,化学名α-环己基-α-苯基-1-哌啶丙醇盐酸盐。盐酸苯海索为中枢抗胆碱抗帕金森病药,能选择性阻断纹状体的胆碱能神经通路,而对外周作用较小,从而有利于恢复帕金森病患者脑内多巴胺和乙酰胆碱的平衡,改善患者的帕金森病症状[1]。
盐酸苯海索在甲醇、乙醇或三氯甲烷中溶解,在水中微溶。目前测定盐酸苯海索的方法有高效液相色谱法[2~4]、流动注射化学发光法[5]、毛细管电化学法[6]、LC-MS法[7,8]、气相色谱法[9]、原子吸收法等[10]。
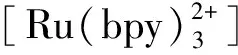
1 实验
1.1 试剂和仪器
1.00×10-4mol·L-1盐酸苯海索标准溶液:准确称取0.0034 g盐酸苯海索,定容于100 mL棕色容量瓶中,超声波除气后冷藏于冰箱中备用。
1.00×10-4mol·L-1联吡啶钌储备液:准确称取六水合三(2,2-联吡啶)氯化钌(Aldrich公司)0.0748 g 定容于100 mL棕色容量瓶中,超声波除气后放入冰箱中(4℃)冷藏。其它试剂为分析纯或化学纯,实验用水均为二次石英亚沸水。
MPI-E型电致化学发光分析系统,西安瑞迈电子科技有限公司;DL-60D型超声波清洗器,上海之信仪器有限公司。
1.2 方法
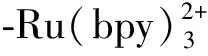

2 结果与讨论
2.1 电化学行为和电致化学发光行为的研究
2.1.1 盐酸苯海索的电化学行为
用循环伏安法考察了1.4×10-4mol·L-1的盐酸苯海索在pH值为8.0的磷酸盐缓冲溶液中的电化学行为,结果见图1。

图1 盐酸苯海索的循环伏安图
由图1可知,当电位从0.2 V扫向1.3 V时,未观察到盐酸苯海索在金电极上的电化学行为。
2.1.2 盐酸苯海索的电致化学发光行为(图2)
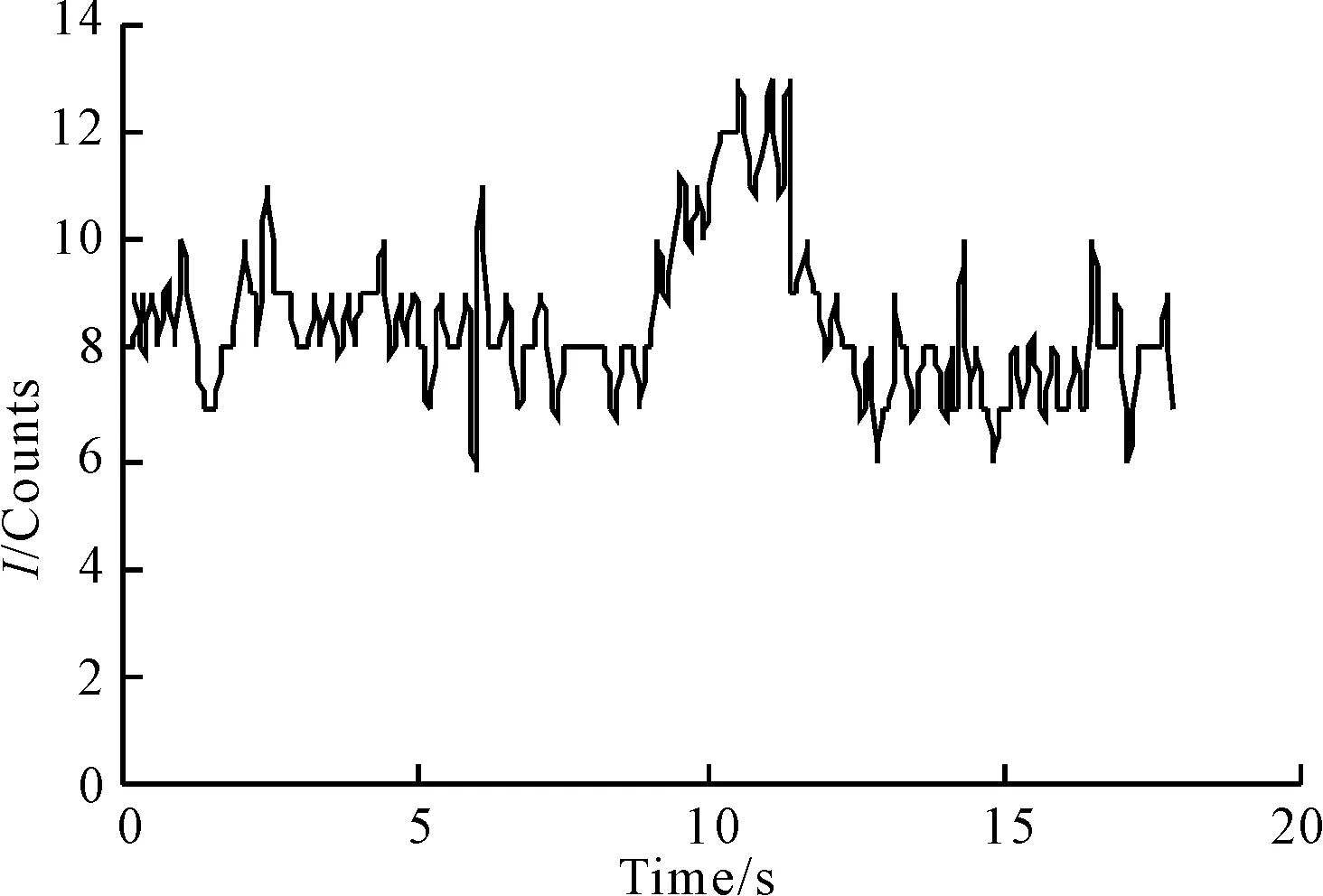
图2 盐酸苯海索的电致化学发光图
由图2可知,没有观察到盐酸苯海索的电致化学发光现象。
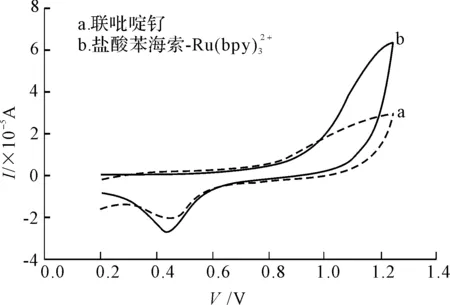
图3 联吡啶钌和盐酸苯海索体系的循环伏安图
由图3可知,联吡啶钌在0.44 V左右出现一个氧化峰(曲线a),当有盐酸苯海索存在时(曲线b),原有的阳极电流升高,阴极电流下降,但氧化峰电位仍在0.44 V左右,这表明盐酸苯海索对联吡啶钌的氧化电流具有增敏作用[12]。
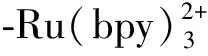
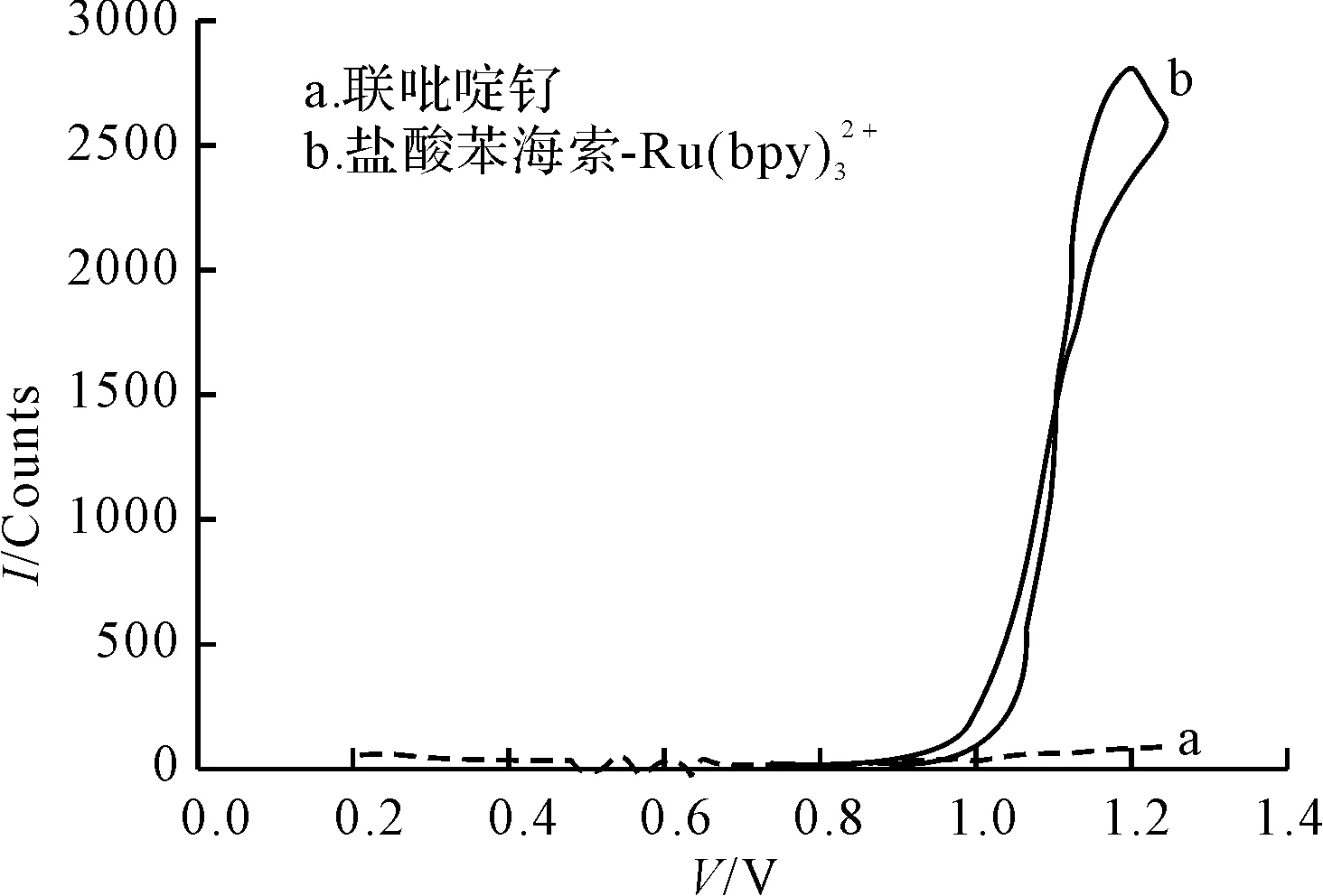
图4 联吡啶钌和盐酸苯海索体系的电致化学发光图
由图4可知,2个体系的ECL强度的增加始于1.0 V,且强度的最高值均位于1.2 V。在联吡啶钌体系中加入盐酸苯海索后,体系的ECL强度从83 Counts(曲线a)增加到2537 Counts(曲线b),可见在相同的条件下,盐酸苯海索对联吡啶钌的ECL具有显著增强作用。
2.2 电致化学发光行为研究参数的选择
2.2.1 MPI-E参数
2.2.1.1 光电倍增管高压
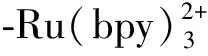
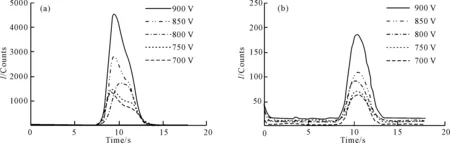
图5 盐酸苯海索体系(a)和联吡啶钌(b)的电致化学发光图
由图5可知,随着光电倍增管高压从700 V变化到900 V,ECL强度不断增加,且变化趋势增强,同时对应的空白值也增大,其趋势和ECL强度规律相一致。因此,在参考最佳信噪比条件下,选择光电倍增管高压为850 V。
2.2.1.2 扫描速率
考察了扫描速率为0.06 V·s-1、0.08 V·s-1、0.10 V·s-1及0.12 V·s-1时对盐酸苯海索ECL强度的影响。结果发现,随着扫描速率的加快,ECL强度逐渐增大;当扫描速率达到0.10 V·s-1时,ECL强度较好;继续加快扫描速率对ECL强度的影响不大。因此,选择扫描速率为0.10 V·s-1。
2.2.2 联吡啶钌浓度
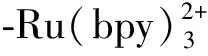
2.2.3 缓冲溶液及pH值
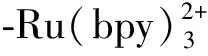

a.PBS Buffer solution b.Na2B4O7-H3BO3 Buffer solution
2.2.4 共存物质的影响

2.3 方法的评价
2.3.1 线性回归方程
在最佳条件下,通过电致化学发光工作站记录不同浓度盐酸苯海索标准溶液在金电极上的ECL强度响应曲线,结果见图7。
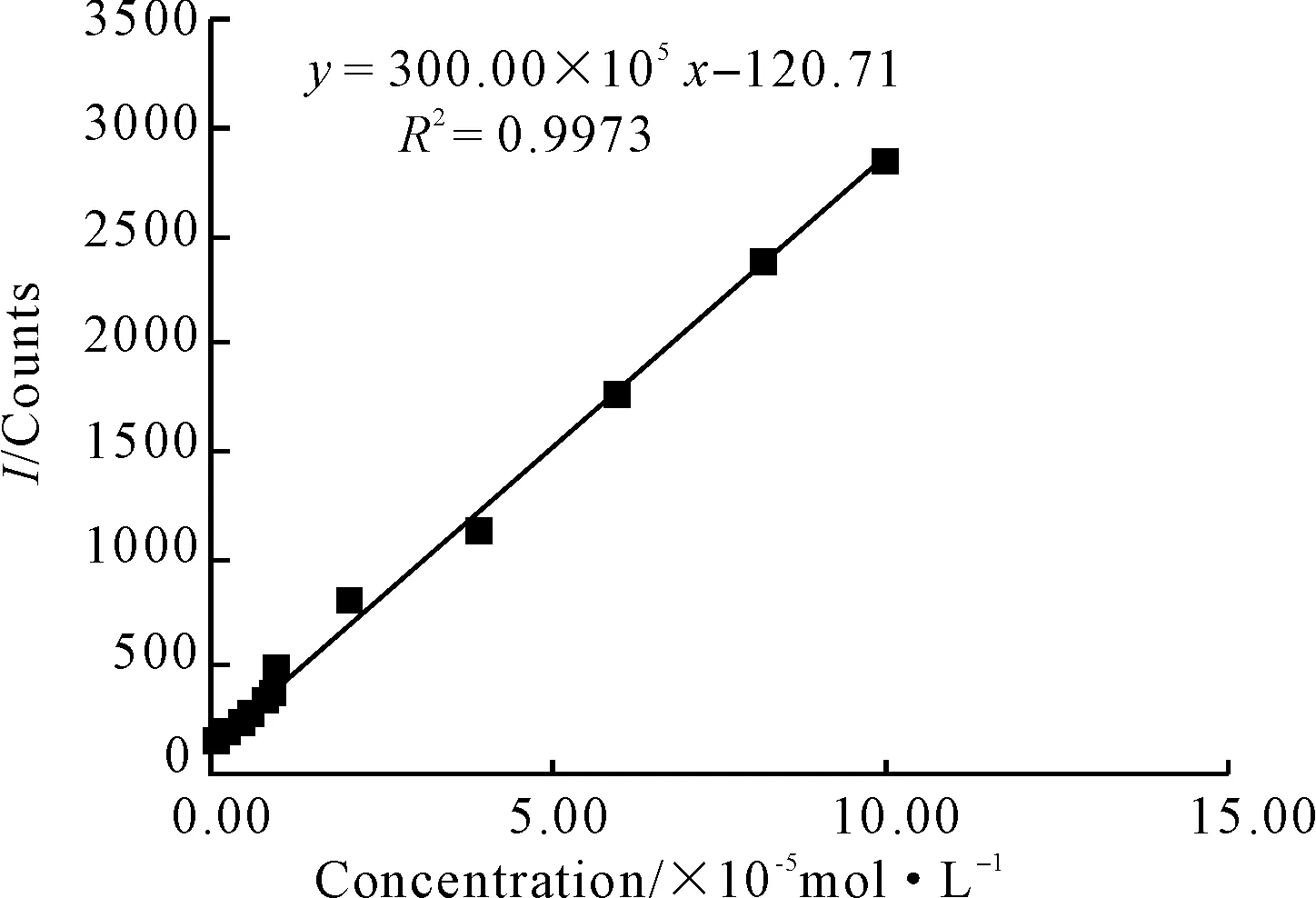
图7 盐酸苯海索体系的线性回归方程
由图7可知,盐酸苯海索浓度在2.00×10-7~1.00×10-4mol·L-1范围内与相对峰高呈良好线性关系,其线性回归方程为:I(Counts)=300.00×105c-120.71。方法检出限为1.00×10-8mol·L-1(s/n=3)。
在不同时段测定5.9184×10-5mol·L-1的盐酸苯海索片溶液4次,所测样品含量值的RSD为1.55%,表明方法具有较高的灵敏度。
2.3.2 回收率
对样品进行加标回收率实验,结果见表1。
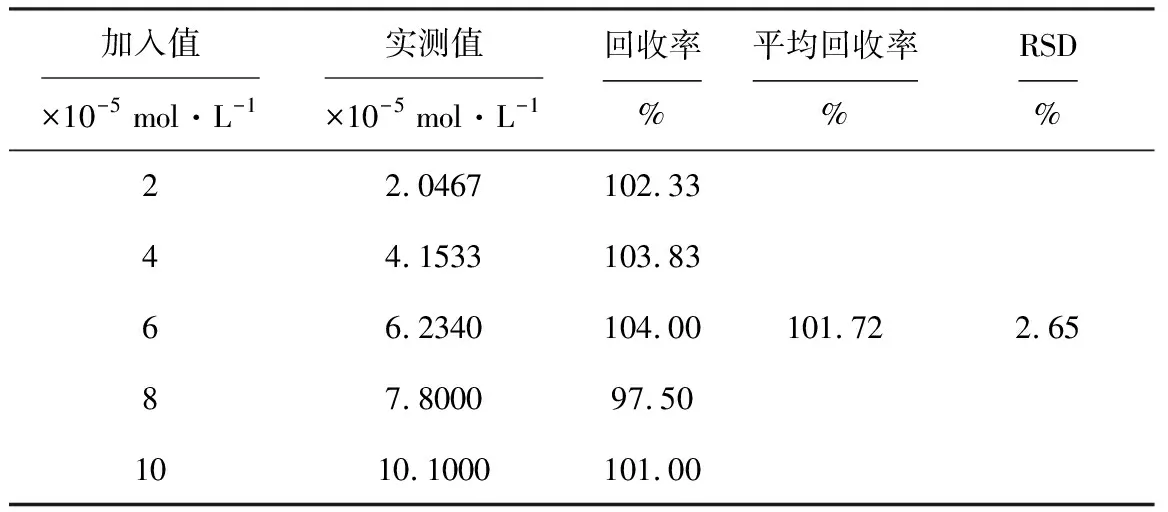
表1 盐酸苯海索片回收率测定
由表1可知,回收率在97.50%~104.00%,平均回收率为101.72%,RSD为2.65%,表明方法具有较好的重现性。
2.4 样品分析
取10片盐酸苯海索,准确称量,研碎,混合均匀后称取相当于1片盐酸苯海索含量的样品,超声溶解于一定量水中,过滤后定容于100 mL棕色容量瓶中,稀释后在最佳实验条件下进行测定,结果如表2所示。

表2 盐酸苯海索片含量的测定
由表2可知,该方法可有效用于分析、测定盐酸苯海索片。
3 结论
参考文献:
[1] 国家药典委员会.中华人民共和国药典[M].北京:化学工业出版社,2006:530.
[2] 王砚,赖可,黄园.RP-HPLC测定盐酸苯海索片中主药[J].华西药学杂志,2008,23(3):351-352.
[3] Ma C K,Mok C S,Hon P K.Determination of benzhexol hydrochloride and ethambutol hydrochloride in tablets by liquid chromatography[J].Anal Chim Acta,1995,314(1-2):77-85.
[4] Mahadik K R,Aggarwal H,Kaul N.Development and validation of HPLC method for simultaneous estimation of trihexylphenidyl hydrochloride and chlorpromazine hydrochloride from tablet dosage form[J].Indian Drugs,2002,39(8):441-445.
[5] 张泾凯,李建国,屠一锋.铈(Ⅳ)-亚硫酸盐体系流动注射化学发光法测定苯海索新方法研究[J].苏州大学学报(自然科学版),2009,25(3):68-71.
[6] Yan Jilin,Liu Jifeng,Cao Weidong,et al.Determination of benzhexol hydrochloride by capillary zoneelectrophoresis with an end-column electrochemiluminescence detection[J].Microchemical Journal,2004,76(1-2):11-16.
[7] 龚志成.人血浆中盐酸苯海索浓度的LC-MS法测定[J].中国医药工业杂志,2007,38(10):717-719.
[8] Cápka Vladimír,Xu Yan,Chen Yonghong.Stereoselective determination of trihexyphenidyl in humanserum by LC-ESI-MS[J].Journal of Pharmaceutical and Biomedical Analysis,1999,21(3):507-517.
[9] 杨昌金,杜兴.气相色谱法测定盐酸苯海索片的含量[J].中国医药工业杂志,1990,21(10):463-464.
[10] Liu Y M,Li G Z.Indirect determination of benzhexol in tablets by inductively coupled plasma atomic-emission spectroscopy[J].Chinese J Anal Chem,2001,29(1):66-69.
[11] 岳衢,毛建霏,徐泽民,等.电致化学发光分析法测定苯酚的研究[J].化学研究与应用,2008,20(5):660-662.
[12] 蓝苏梅,李利军,蔡卓,等.联吡啶钌体系电化学发光法测定克林霉素的研究[J].分析测试学报,2009,28(4):466-469.

