64层螺旋CT对冠状动脉支架术后再狭窄的评价
王耀彬 刘烨 韩向东 温友信 朱栓庄
冠状动脉支架置入术作为冠心病的主要治疗手段之一,在临床的应用越来越广泛,但其面临的主要问题是支架内再狭窄(In Stent Restenosis,ISR),诊断ISR的传统方法是冠状动脉造影,但高费用和有创性限制了该技术的广泛应用。近年来,随着多层螺旋CT的广泛应用,其在冠状动脉支架植入术后综合评价的价值已为大家接受,成为首选的检查手段[1]。笔者采用64层螺旋CT对32例冠状动脉支架置入术后的患者进行CT冠状动脉成像(Computed Tomographic Angiography,CTA)检查,并与其中23例冠状动脉造影(Conventional Coronary Angiograph,CCA)进行比较,评价64层螺旋CT诊断ISR的临床价值。
1 资料与方法
1.1 一般资料 收集2007年6月~2009年6月在我院行冠状动脉支架置入术后32例患者的冠状动脉CTA检查资料(置入支架54枚),其中23例(计39枚支架)在1~10d内行导管法冠状动脉造影。32例中男21例,女11例,年龄40~76岁,平均(56±10)岁。其中前降支29枚,第一对角支2枚,回旋支6枚,右冠状动脉17枚。放置4枚支架1例(前降支1枚、回旋支1枚、右冠状动脉2枚),3枚支架4例,2枚支架11例,1枚支架16例。支架置入术后时间为1~48个月,平均时间10个月。54枚支架均为金属支架,支架长度为18~33mm,直径为2.5~3.5mm。
1.2 检查方法
1.2.1 仪器设备 设备采用GE Ligh tSpeed64排容积CT。探测器覆盖宽度64mm×0.625mm,管电压120~140kV,管电流400~600m A,机架旋转速度0.35s/r,层厚0.625mm,螺距0.18~0.2。使用德国A lrich高压注射器,静脉注入非离子型对比剂造影剂碘普罗胺(370mg/m l),注射流速5.0m l/s,注射总量80m l和生理盐水50m l。32例患者在行冠状动脉CTA前均严格排除禁忌症,心率≥70次/m in者1h前含服倍他乐克25~50mg。扫描时平均心率为(62±5)次/m in。检查时患者仰卧于检查床,加心电监测,行回顾性心电门控图像重建,扫描时间为5~7s,扫描范围气管分叉下2cm至心脏膈面以下1cm。
1.2.2 MDCT冠脉图像重建 所有患者扫描结束后,首先常规重建R-R间期40%~80%(间隔10%)0.625mm的横断图像,选取最佳时相的横断位图像传至AW 4.3工作站重组三维冠状动脉图像,包括容积再现(VR)、最大密度投影(MIP)、曲面重组(CPR)及冠状动脉血管分析。
1.2.3 冠状动脉造影 设备采用GE公司的数字减影血管造影机(LCV+PLUS),造影剂使用碘普罗胺(370mg/m l)。本组23例共计39枚支架,其中18例常规经桡动脉穿刺插入5F多功能造影导管,剩余5例经股动脉穿刺插入6F多功能造影导管,分别进行选择性右冠状动脉(RCA)或左冠状动脉(LCA)造影,多轴位投照最佳体位的冠状动脉图像。应用DCR软件定量分析支架及邻近血管段。
1.2.4 MDCT图像评价方法 本组病例CTA以重建图像CPR为主,参考薄层(0.625mm)横断图像通过肉眼观察支架的形态、远侧的血管和支架内的密度,当支架发生变形、支架远侧的血管显示不佳或支架内出现充盈缺损时,均可提示ISR。以CCA(ISR≥50%)为金标准,参照评估64层螺旋CT在诊断支架再狭窄方面的可靠性,统计其敏感性、特异性、阳性预测值和阴性预测值。同时分析冠状动脉支架置入术后有无狭窄及狭窄分布部位情况。CTA诊断由2名有经验的放射科医生共同完成,CCA图像由2名资深心内科医生阅片,对置入支架直径≥3mm进行评估,以意见一致时为准。Kappa检验,比较两种方法诊断的各项准确性指标之间有无区别。
2 结果
所有患者64层螺旋CT检查冠状动脉均通过后处理并三维重建,54枚支架的CT重建图像中85.2%(46/54)能满足影像学评价,冠脉主干及重要分支均显影清晰。其余8枚支架不能满足影像学评价占14.8%(8/54),其中影响因素运动伪影2枚,邻近冠状动脉弥漫钙化4枚,心律失常2枚。CTA诊断12枚ISR,34枚无明确狭窄。
本组32例患者共计54枚支架,其中有23例患者计39枚支架与CCA有对照,其余9例计15枚支架不包括在CCA内不做分析,具体情况见表1。39枚支架中CCA检出ISR(≥50%)11枚(28.2%),无明确狭窄(包括ISR<50%)28枚(71.8%)。11枚支架ISR中,CTA仅3枚可以在支架内看到充盈缺损(如图1~3)。其余8枚未观察到支架内因内膜增殖而引起的充盈缺损,均属邻近支架两端血管5mm范围内管腔狭窄(边缘型再狭窄)。与CCA对照(如图4),CTA分别有8枚和24枚诊断相符,诊断ISR的敏感性、特异性、阳性预测值和阴性预测值分别为72.7%、85.7%、66.7%、88.9%。Kappa检验,一致性较好。
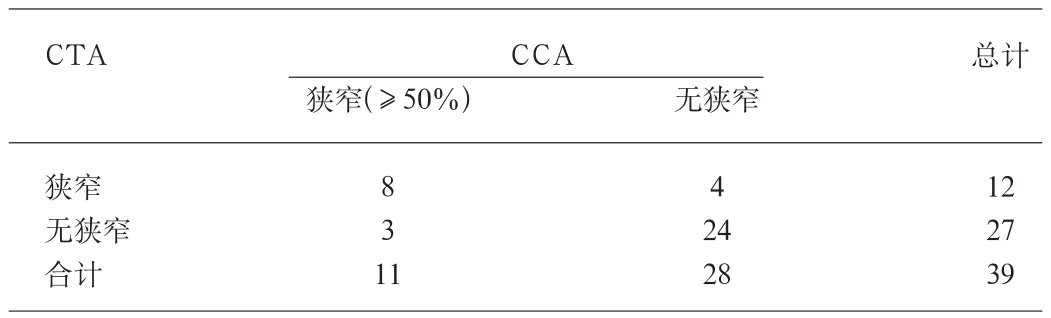
表1 39枚支架再狭窄的CTA与CCA分析对照

图1 图2 图3 图4
3 讨论
冠状动脉支架已被广泛应用于临床,治疗后复查准确性已是当前大家所关注的问题。在患者康复过程中,反复出现的心绞痛症状可以提示再狭窄的可能,但是准确评价再狭窄的“金标准”仍是冠状动脉造影。其他无创性技术目前主要包括磁共振血管造影和多层螺旋CT,而门控心肌显像评价支架再狭窄方法也有报道[2-4]。
3.1 CTA评价支架再狭窄定义 冠状动脉支架再狭窄包括支架内>50%的狭窄和支架边缘5mm范围内50%以上的管腔狭窄,后者也称为支架边缘型再狭窄。由于血管平滑肌细胞增生和血管重构等因素,置入的冠状动脉支架在1a内有近10%发生再狭窄[5-6],支架再狭窄由血管内膜纤维增生所致,一般不发生破裂或血栓形成而引发急性冠状动脉事件发生。支架再狭窄发生的高峰期在术后1~3个月。金属裸支架再狭窄的发生率较高,术后6个月平均再狭窄率是46%,而药物涂层支架术后6个月的平均再狭窄率仅为5.5%[7]。目前,CTA诊断ISR仍缺乏客观而统一的诊断标准,一般是通过肉眼观察:(1)支架的形态有无弯曲变形;(2)支架血管腔内有无充盈缺损;(3)支架两端5mm内血管有无再狭窄;(4)支架远侧血管充盈状况或造影剂的浓度。此外,对支架移位、断裂等异常CTA可以清楚显示。这些征象在CTA诊断中以曲面重组(CPR)图像结合对应血管横断位图像最为有意义,可以直接观察支架腔内长轴及短轴情况。
3.2 CTA的应用价值 64层螺旋CT的时间分辨率有了进一步提高(83~165ms),运动伪影明显减少,本组结果和相关报道显示[8],当心率低于65次/m in时,64层螺旋CT可获取高质量的冠状动脉图像。经过分析考虑CT判断支架置入后再狭窄主要根据支架变形、支架远端血管不显影和明显变细等几个方面,而当患者心率较快时,图像质量变差,则难以判断ISR存在。我科在冠脉CT图像后处理中,通过选择最佳重建期相对冠脉置入金属支架血管段采用骨算法可以提高密度分辨率,减少容积效应,使支架腔内及邻近血管段边缘清楚锐利,以此提升图像质量,对诊断ISR有一定的帮助。通过此法后处理,本组多层螺旋CT检出12枚支架ISR中有3枚可以在支架内看到充盈缺损被诊断为ISR(狭窄>50%),其中有8枚出现了支架边缘再狭窄,64层螺旋CT对支架边缘病变的诊断与冠状动脉造影结果几乎一致,表明对支架边缘型ISR显示了较好的准确性。另1枚诊断为ISR发生在右冠状动脉中段支架,分析原因考虑局部高密度钙化影与高密度支架影混合在一起干扰所致。Gaspar等[9]运用40层螺旋CT,主要通过肉眼观察支架内对比剂充盈缺损的程度来诊断ISR,以CCA(>60%)为标准,其诊断ISR的敏感性和特异性分别达到了88.9%和80.6%,笔者通过肉眼观察诊断ISR的敏感性为72.7%,而特异性较高85.7%。与本研究结果略有偏差,考虑其研究可能与病例来源、支架材料及重建方法有关。在欧洲心脏病学术会议上报道了日本Ehara等的研究,研究人员在观察了430处支架内病变后总结认为,多排螺旋CT造影能够精确测定支架内狭窄的程度;同时,支架内狭窄多发生在右冠状动脉,且多见于多枚支架或弯曲的病变处。上述试验与本研究结果相近,证实多层螺旋CT在冠状动脉支架置入后血管再狭窄诊断中具备非常重要的应用价值。
3.3 CTA判断支架再狭窄的限度 目前,阻碍64层螺旋CT准确诊断ISR的主要原因仍然是金属伪影。Maintz等[10]研究也显示支架材料是影响观察支架内结构的最重要因素,在比较了68种不同材料的支架之后,M aintz发现金属伪影小的合金支架十分有助于显示支架腔内的结构和密度变化。合金支架一方面会减轻血管内膜的增生,另一方面由于合金材料具有较高的硬度,在制造支架时,可减小支架金属丝的厚度,从而降低支架的金属伪影。目前临床广泛使用的冠状动脉支架,无论是裸支架还是药物支架,绝大多数为不锈钢材料,即使是合金支架也会或多或少地存在一些金属伪影。因此,要真正提高CT诊断ISR的准确性,必须采用特殊的图像处理技术减低或过滤掉支架的金属伪影。另外,当支架处冠状动脉管壁存在明显钙化时,高密度的钙化影与高密度的支架伪影混合在一起,也影响对支架再狭窄做出准确评价。荷兰鹿特丹大学医院Fey ter教授在2008年欧洲心脏病会议上同时强调,CT诊断冠状动脉病变的偏差除受到上述血管钙化干扰等因素外,也与放射技师影像学重建技术相关,影像学重建的精确性直接影响到CT结果的判定。
总之,目前64层螺旋CT冠状动脉成像技术诊断ISR(不包括边缘型ISR)尚有一定的限度,但对冠状动脉支架置入术后患者进行随访,评价冠状动脉支架腔内情况,对排除ISR仍然有一定的临床参考价值。
[1]Schuijf J D,Bax J J,Salm L P,et al.Noninvasive coronary imaging and assessment of left ventricular function using 16- slice computed tomography[J].Am J Cardiol,2005,95(5):571-574.
[2]Maintz D,Botnar RM,Fischbach R,et a1.Coronary magnetic resonance angiography for assessment of the stent lumen:a phantom study[J].J Cardiovasc Magn Reson,2002,4(3):359-367.
[3]冯建林,李殿富,程旭,等.99Tcm-MIBI门控心肌显像评价冠状动脉支架术后再狭窄的价值[J].中华核医学杂志,2006,26(6):363-365.
[4]Gjlard M,Cornily JC,Rioufol G,et a1.Noninvasive assessment of 1eft main coronary stent patency with 16一slice computed tomography[J].Am J Cardiol,2005,95(1):110-112.
[5]Mehran R,Dan gas G,Abizaid AS,et a1.Angiographic patterns of in—stent restenosis:classification an d implications for long—terra outcom[J]e.Circulation,1999,100:1872-1878.
[6]沈雳,葛均波.药物洗脱支架的应用现状和展望[J].中国组织工程研究与临床康复,2007,11(51):l0404-10408.
[7]Mahnken AH,Buecker A.Wildberger JE,et a1.Coronary artery stents in muhislice computed tomography:in vitro artifact evaluation[J].Invest Radiol,2004,39:27-33.
[8]Leschka S,Alkadhi H,Plass A,et a1.Accuracy of MSCT coronary angiography witlI 64 -slice technology:first experience[J].Eur Heart J,2005,26:1482-1487.
[9]Gaspar T,Halon DA,Lewis BS,et a1.Diagnosis of coronary in stent restenosis witlI muhidetector row spiral computed tomography.J Am Coil Cardiol,2005,46:1573-1579.
[10]Maintz D,Grude M,Fallenberg EM,et a1.Assessment of coronary arteria1 stents by multislice-CT angiography.Acta Radiol,2003,44(6):597-603.