两种含双键铱配合物的合成及其磷光性质
安保礼, 宋 健, 戴樊增, 张燕龄, 任媛媛
(1.上海大学理学院,上海 200444;2.上海大学新型显示技术及应用集成教育部重点实验室,上海 200072)
自从 Forrest等[1-2]发现重金属配合物能够作为高效的电致发光磷光材料以来,新型的电致磷光材料的研究和开发引起了人们的极大兴趣.重金属配合物分子如锇、铱、铂的有机配合物,能够产生强烈的自旋-轨道偶合,使原来禁阻的三重态跃迁解禁,可突破OLED最高内量子产率为 25%的上限,进而实现强的磷光发射,大大提高器件的电致发光效率[3-4].金属 Ir3+与有机配体形成的配合物由于具有更高的电致发光效率和在室温下具有很强的磷光而成为研究热点[4].从结构上划分,铱配合物可分为中性配合物和阳离子型配合物两种类型;按照辅助配体结构的不同,中性小分子铱配合物又可分为 Ir(C∧N)3结构和 (C∧N)2Ir (LX)结构[5].通过修饰 C∧N配体结构,(C∧N)2Ir(LX)结构配合物的发射波长在可见光波段内实现可调[6].近年来,人们通过设计合成适当的C∧N配体,得到从蓝色、绿色直到红色的铱金属配合物发光体,在提高器件性能 (包括外量子产率、发光亮度、器件寿命等)和简化器件制备等方面取得了一定的进展[7].获得电致磷光最常见的方法是将小分子重金属配合物掺杂到小分子或高分子主体材料中,利用主体与客体之间的能量转移原理实现.但是,采取掺杂的方式,存在晶化现象,易出现相分离,从而会导致器件寿命的下降[8].与磷光客体 /聚合物主体的掺杂体系相比,合成键合型的高分子磷光材料,可以实现分子内和分子间的能量转移,并有效抑制三线态激子的自猝灭,提高材料的稳定性[9].在合成键合型高分子磷光材料时,常用的合成方法是先把含有双键的小分子配体键合在高分子链上,再将其与重金属配合物中间体反应.I.Takeshi等[10]先把不同的小分子有机单体聚合成高分子配体(LX),再将其与 2-苯基吡啶为C∧N配体的铱配合物中间体反应,合成一系列的铱配合物高分子磷光材料.研究发现该磷光材料既有传输电子的能力,又有传输空穴的能力,当铯作为电子注入层时,用该聚合物制作的器件外量子产率为11.8%,发光效率为 38.6 lm/W.P.T.Furuta等[11]合成了集电子传输单体、空穴传输单体和发光铂配合物单体于一身的磷光材料,他们先合成电子传输单体、空穴传输单体和β-二酮单体,再聚合得到三聚体配体,然后与以2,4-二氟苯基吡啶(dfppy)为C∧N配体的铂中间体反应合成 Pt(Ⅱ)磷光材料的聚合物.通过改变各个单体之间的比例,实现了白光发射,驱动电压为8.0 V.合成键合型磷光材料的另一种方法是先合成配合物的磷光单体,之后将其聚合在聚合物主体材料的分子链上,利用这种方法可以更好地控制聚合物中重金属配合物单体的比例[12].
本研究设计、合成了 1,3-二苯基-2-烯丙基-1,3-丙二酮 (ADP)和 6-对乙烯基苯基-2,4-己二酮(VPHD)两种带有双键的β-二酮有机配体.以 2-苯基吡啶(ppy)为主配体,β-二酮为辅助配体分别合成了 Ir(ppy)2(ADP)和 Ir(ppy)2(VPHD)配合物单体,并考察了配合物的紫外吸收光谱和光致发光光谱性能.
1 试验部分
1.1 试剂和仪器
试剂:IrCl3·2H2O(上海久岳化工有限公司), 2-苯基吡啶(Alfa Aesar),二苯甲酰甲烷 (DBM,蚌埠市佳先化工),4-乙烯基卞基氯 (Alfa Aesar),其他均为分析纯化学试剂.
仪器:红外光谱仪 (AVATRA 370型,美国Thermo Nicolet公司),紫外可见分光光度计 (UV-2501PC型,日本岛津),核磁共振波谱仪 (Bruker, AV500 MHz),荧光光谱仪 (RF-5301PC型,日本岛津),数字熔点仪 (WRS-1B,上海精密科学仪器有限公司).
1.2 β-二酮配体的合成
1.2.1 1,3-二苯基-2-烯丙基-1,3-丙二酮 (ADP)的合成
参照文献[13]方法合成,产率 70%.

1H-NMR(CDCl3):7.953(4 H,d,3J=8.50 Hz),7.576(2 H,t,t,3J=7.40 Hz,4J=1.40 Hz), 7.456(4 H,t,3J=7.10 Hz),5.883(1 H,m), 5.302(1 H,t,3J=13.50 Hz),5.083(2 H,m,3J=17.02 Hz),2.881(2 H,t,3J=13.46 Hz).
1.2.2 6-对乙烯基苯基-2,4-己二酮(VPHD)的合成参照文献[14]方法合成.
1H-NMR(CDCl3,500 MHz)/δ:15.45(1 H, d),7.33(2 H,d,3J=8.0 Hz),7.14(2 H,d,3J= 8.0 Hz),6.68(1 H,d,3J=7.5 Hz),5.70(1 H, d,3J=15.5 Hz),5.46(1 H,s),5.20(1 H,d,3J= 11.0 Hz),2.91(2 H,t,3J=7.5 Hz),2.58(2 H, t),2.03(3 H,s).
1.3 铱配合物的合成
1.3.1 Ir(ppy)2(ADP)的合成
称取 0.489 g(3 mmol)2-苯基吡啶 (ppy)于50 mL反应瓶中,加入 20 mL 2-乙氧基乙醇,N2保护下搅拌,加入 0.494 g(1.5 mmol)水合三氯化铱(IrCl3·2H2O)和 6 mL去离子水,回流 24 h,冷却至室温,过滤,沉淀用无水乙醇洗涤,真空干燥得到[Ir(ppy)2Cl]2,产率 70%.
称取 0.36 g(0.34 mmol)[Ir(ppy)2Cl]2于50 mL反应瓶中,加入 20 mL N,N-二甲基甲酰胺(DMF),搅拌,N2保护下加入 0.36 g无水碳酸钠, 0.26 g(0.98 mmol)ADP,控温 80℃反应 12 h,反应混合液冷却至室温,加到冰水中产生沉淀,过滤,分别用去离子水、无水乙醇、无水乙醚洗涤,真空干燥得橙色粉末,产率 78%.
1H-NMR(CDCl3,500 MHz)/δ:8.77(2 H,d,3J=5.5 Hz),7.87(2 H,d,3J=8.5 Hz),7.75 (2 H,t,3J=7.0 Hz),7.54(2 H,d,3J=7.5 Hz), 7.16(10 H,m),6.77(4 H,t,3J=7.0 Hz),6.75 (1 H,t,3J=7.0 Hz),6.67(2 H,t,3J=7.0 Hz), 6.30(2 H,d,3J=7.5 Hz),5.37(1 H,m),4.40 (2 H,q),2.90(2 H,d,3J=1.5 Hz).
1.3.2 Ir(ppy)2(VPHD)的合成
合成方法与 Ir(ppy)2(ADP)的合成方法相似,产率为 76%,核磁谱图及归属如图 1所示.

图1 Ir(ppy)2(VPHD)的 NM R图及归属Fig.1 NM R spectrum of Ir(ppy)2(VPHD)complex
1H-NMR(CDCl3,500 MHz)/δ:8.47(1 H,d,3J=5.5 Hz),8.21(1 H,d,3J=5.5 Hz),7.83 (2 H,t,3J=8.5 Hz),7.72(2 H,m),7.55(2 H,t,3J=8.5 Hz),7.18(2 H,d,3J=8.0 Hz),7.11 (1 H,t,3J=6.0 Hz),6.97(1 H,t,3J=6.0 Hz), 6.90(2 H,d,3J=8.0 Hz),6.78(4 H,m),6.73 (1 H,m),6.28(2 H,m),5.68(1 H,d,3J=13.0 Hz),5.19(1 H,d,3J=13.0 Hz),5.18(1 H,s), 2.60(2 H,t,3J=7.5 Hz),2.36(2 H,m),1.75 (3 H,s).
1.3.3 Ir(ppy)2(acac)的合成
参照文献[4]方法合成,产率为 80%.
1H-NMR(CDCl3500 MHz,)/δ:8.47(2 H,d,3J=5.8 Hz),7.80(2 H,d,3J=8.0 Hz),7.68 (2 H,t,3J=7.4 Hz),7.50(2 H,d,3J=8.0 Hz),7.09(2 H,t,3J=7.4 Hz),6.76(2 H,t,3J =7.4 Hz),6.64(2 H,t,3J=5.8 Hz),6.22(2 H,d,3J=7.4 Hz),5.17(1 H,s),1.74(6 H, s).
1.4 光谱测定
紫外和荧光光谱均在室温下测定,荧光光谱测定的入射和出射狭缝宽度均为 5 nm,高灵敏度.
2 结果与讨论
2.1 紫外-可见吸收光谱
3种铱配合物的紫外光谱均由 4个吸收峰组成,如图 2所示.前 2个吸收峰为配体的自旋允许的单线态π→π*跃迁,460 nm处吸收峰为 ppy配体的三线态π→π*跃迁.根据此类配合物的性质以及Hay有关理论的计算结果可知,409和 492 nm处吸收峰分别对应于配合物单线态和三线态的从金属到配体的电荷跃迁 (1MLCT和3MLCT)[3-4].3MLCT的摩尔吸光系数比1MLCT的摩尔吸光系数小一些,但由于重金属铱配合物产生强烈的自旋-轨道耦合,使原来禁阻的3MLCT解禁,3MLCT的摩尔吸光系数还是比较大的.

图2 铱配合物在乙酸乙酯溶液中的电子吸收光谱Fig.2 UV absorption spectra for the complexes in ethyl acetate solutions
2.2 配合物的荧光光谱
Ir(ppy)2(acac)配合物和 Ir(ppy)2(VPHD)配合物在乙酸乙酯溶液中的最大激发波长和最大发射波长不随浓度的变化而发生改变.Ir(ppy)2(VPHD)和 Ir(ppy)2(acac)配合物的磷光光谱相似,最大发射波长为 520 nm,有强的绿色磷光,如图 3所示. VPHD取代 acac,保持了相应磷光材料的磷光性能,并且 VPHD中含有可以聚合的双键基团,因此, Ir(ppy)2(VPHD)可以作为良好的绿色磷光单体用于制备键合型铱有机配合物的聚合物磷光材料.

图3 配合物在乙酸乙酯溶液中的激发和发射光谱Fig.3 Excitation and em ission spectra for ethyl acetate solutions
与之前合成的 Eu3+-ADP配合物在室温条件下强的激基缔合物激发吸收光谱的情况类似,在Ir(ppy)2(ADP)配合物的磷光光谱中观察到较强的激基缔合物激发吸收和激基缔合物发射光谱,如图4所示.激基缔合物激发吸收和发射有两个主要特征:一是随着测试浓度的增加,最大激发波长和发射波长向长波长方向明显移动;二是样品的激发吸收强度和磷光发射强度随着测试浓度的变化而变化.激基缔合物吸收产生的一个重要因素是在邻近分子间存在π键的相互重叠作用[13,15].在配合物分子Ir(ppy)2(ADP)中,ADP,ppy配体中邻近的苯环、吡啶环间存在分子间的π键的相互重叠作用,随着浓度的增加,Ir(ppy)2(ADP)配合物单体会转化成二聚体、三聚体或多聚体,共轭程度增大,最大激发波长和最大发射波长都发生红移.
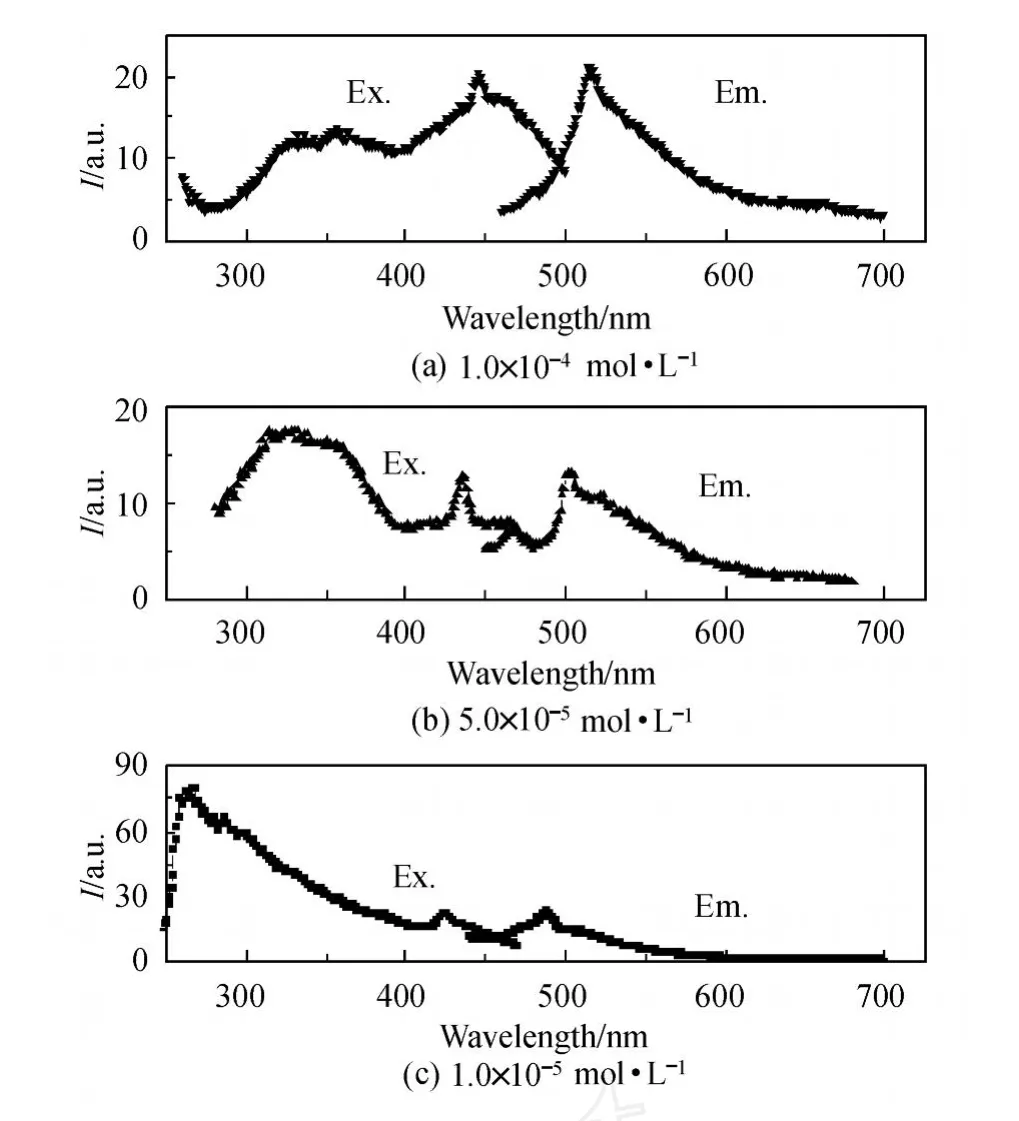
图4 Ir(ppy)2(ADP)在乙酸乙酯溶液中的激发和发射光谱Fig.4 Excitation and em ission spectra for Ir(ppy)2(ADP) ethyl acetate solutions
Ir(ppy)2(ADP)的磷光光谱与 Ir(ppy)2(acac)以及 Ir(ppy)2(VPHD)配合物的磷光光谱相比,最大发射波长发生蓝移.这是由于 Ir(ppy)2(acac)和Ir(ppy)2(VPHD)配合物最大发射波长处的发射来自于3MLCT能级发射[4],而 Ir(ppy)2(ADP)配合物的磷光光谱最大发射波长来自于激基缔合物激发态能级,激基缔合物激发态能级高于3MLCT能级,所以 Ir(ppy)2(ADP)的磷光发射波长向短波长方向移动.
配合物的量子产率可由下式计算[13]:

式中,qx和 qs为样品和标准物质的量子产率,Ax和As分别为样品和标准物质的吸光度,Δ Φx和Δ Φs分别为样品和标准物质的发射峰面的积分值.以Ir(ppy)2(acac)配合物为标准物质[4],可以测得Ir(ppy)2(ADP)和 Ir(ppy)2(VPHD)的量子产率分别为1.1%和 36.0%.
Ir(ppy)2(ADP)的磷光强度与 Ir(ppy)2(acac)以及 Ir(ppy)2(VPHD)配合物的磷光强度相比明显变弱,与文献[4]的研究结果一致.这是由于ADP的能级比(C∧N)2Ir分子的三线态能级低,从而导致部分能量传递到ADP的三线态能级,使配合物的磷光发光效率下降[3-4].
3 结束语
本研究用VPHD取代 acac合成了带有活性聚合基团双键的 Ir(ppy)2(VPHD)配合物,其磷光发光性能与 Ir(ppy)2(acac)的磷光性能相同.它们的激发光谱、发射光谱和发光效率基本相同,因此, Ir(ppy)2(VPHD)可以作为良好的绿色磷光单体用于制备含有铱有机配合物的聚合物磷光材料.用ADP取代 acac合成的带有活性聚合基团双键的Ir(ppy)2(ADP)配合物,其磷光发光效率明显下降,但ADP的加入使相应 Ir3+配合物的发射光谱明显向短波长方向移动,且其发射光谱随着浓度的不同而发生了明显的改变,这为合成新的 Ir3+配合物磷光材料提供了参考依据.
[1] BALDOM A,O’BR IEND F,YOUY,et al.Highly efficient phosphorescent emission from organic electroluminescent devices[J].Nature,1998,395:151-154.
[2] BALDOM A,THOMPSONM E,FORRESTS R.Highly efficient fluorescentorganic light-emitting devices using a phosphorescent sensitizer[J].Nature,2000,403:750-753.
[3] LAMANSKYS,DJAROV ICHP,MURPHYD,et al. Synthesis and characterization of phosphorescent cyclometalated iridium complexes[J]. Inorg Chem, 2001,40:1704-1707.
[4] LAMANSKYS,DJAROV ICHP,MURPHYD,et al. Highly phosphorescent bis-cyclometalated iridium complexes:synthesis, photophysicalcharacterization, and use in organic light emitting diodes[J].J Am Chem Soc,2001,123:4304-4312.
[5] 王小亮,孙岳明,蒋伟,等.有机小分子电致磷光材料研究进展[J].材料导报,2007,21:26-33.
[6] LU J P,L IU Q D,D ING J F, etal. New triscyclometalated iridium complexes for applications inphosphorescent light-emitting diodes[J]. Synthetic Metals,2008,158:95-103.
[7] XUM L,ZHOUR,WANGG Y,et al.Synthesis and characterization of phosphorescentiridium complexes containing trifluoromethyl-substituted phenyl pyridine based ligands[J]. Inorganica Ch imica Acta,2008, 361:2407-2412.
[8] ADACHIC,BALDOM A,THOMPSONM E,et al. Nearly 100% internal phosphorescence efficiency in an organic light-emitting device[J].App1 Phys,2001, 90:5048-5051.
[9] CHEUX,L IAOJ L,L IANGY,et al.High-eficiency red light emission from polyfluorenes grafted with cyclometalated iridium complexes and charge transport moiety[J].J Am Chem Soc,2003,125:636-637.
[10] SUZUKIM,TOKITOS,SATOF,et al.Highly efficient polymer light-emitting devices using ambipolar phosphorescent polymers[J].Appl Phys Lett,2005, 86:103507-103509.
[11] FURUTAP T,DENGL,GARONS,et al.Platinumfunctionalized random copolymers for use in solutionprocessible,efficient,near-white organic light-emitting diodes[J].J Am Chem Soc,2004,126:15388-15389.
[12] LAND,FURUTAP T,GARONS,et al.Living radical polymerization of bipolar transport materials for highly efficient light emitting diodes[J].Chem Mater,2006, 18:386-395.
[13] ANB L,ZHANGN,CHEAHK W,et al.High yield luminescence of a novel europium complex by excimer excitation and f-f absorption of Eu3+[J]. Journal of Alloys and Compounds,2008,458:457-461.
[14] THOMASM H,SANDRA B,CHARLESR H. Condensations of carbonyl compounds at theγ-position of β-ketoaldehydes bymeans of potassium amide or sodium hydride[J].J Am Chem Soc,1965:3186-3191.
[15] ANB L,HUAC W,MAH L,et al.High-yield luminescence of a novel homonuclear europium complex by exc imerexcitation absorption [J]. Journal of Luminescence,2007,127:297-301.
- 上海大学学报(自然科学版)的其它文章
- 非饱和土粘弹性地基一维固结特性分析

