警惕抗癫痫药可能存在的自杀风险
国家食品药品监督管理局
背景
2008年1月31日,美国食品药品监督管理局(FDA)向医务人员发布有关抗癫痫药的安全性信息,警示服用抗癫痫药患者可能存在自杀观念或自杀行为(包括自杀企图和自杀死亡)的风险。
FDA分析了11种抗癫痫药的安慰剂对照临床研究数据,数据显示服用这些药物的患者,自杀观念和自杀行为的风险约为服用安慰剂患者的2倍。鉴于此,FDA将与制药企业共同协作在抗癫痫药产品说明书上补充相关信息。
相关抗癫痫药品种情况
FDA分析的11种抗癫痫药物包括:卡马西平、非尔氨酯、加巴喷丁、拉莫三嗪、左乙拉西坦、奥卡西平、普瑞巴林、噻加宾、托吡酯、丙戊酸盐、唑尼沙胺。其中7个品种在我国有批准文号,包括卡马西平、加巴喷丁、拉莫三嗪、左乙拉西坦、奥卡西平、托吡酯、丙戊酸盐。普瑞巴林尚未在我国上市,但已获准进行临床研究。
抗癫痫药与自杀观念或自杀行为风险
2005年3月,美国FDA对几种抗癫痫药进行初步分析后发现,该类药物可能增加自杀观念及自杀行为的风险,因此要求抗癫痫药的制药企业提供相关信息,以便审核这些药物与自杀事件的相关性。
FDA分析了11种药物的199个安慰剂对照临床试验数据。研究的疾病包括癫痫、部分精神障碍以及其他疾病(包括偏头痛和神经性疼痛)。数据分析涉及药物治疗组27863例患者,安慰剂组16029例患者,纳入分析的患者均在5岁以上。分析结果显示:药物治疗组有4例患者自杀,安慰剂组无患者自杀;药物治疗组有0.43%的患者产生过自杀观念或行为,安慰剂组为0.22%。
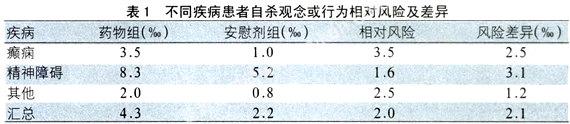
研究结果还显示(详见表1),在不同疾病研究对象中,癫痫患者出现自杀观念或行为的相对风险高于其他疾病;患者在开始服药的第1周就观察到自杀观念及自杀行为的风险增高,并至少持续到24周;不同药物和不同人群的研究结果大体一致,且各年龄组间差异无显著性。
国内抗癫痫药关于自杀观念或行为的不良反应情况
检索国家药品不良反应监测中心病例报告数据库,截至2008年6月10日,未检索到关于卡马西平、加巴喷丁、拉莫三嗪、左乙拉西坦、托吡酯、丙戊酸盐引起自杀观念及自杀行为的病例报告。检索到奥卡西平引起自杀观念病例报告1例。
以焦虑、激动、敌意、躁狂等(美国FDA信息中列为可能是自杀行为的前兆)为关键词检索国家药品不良反应监测中心病例报告数据库,检索到拉莫三嗪相关病例1例,不良反应为“焦虑”;托吡酯相关病例6例,不良反应名称分别为“烦躁、易怒、情绪激动”、“精神恍惚”、“精神异常”、“激动”、“抑郁”和“精神分裂样反应”;卡马西平相关病例5例,不良反应名称分别为“焦虑”(2例)、“精神分裂样反应”、“精神不集中”、“抑郁”:丙戊酸盐相关病例4例,不良反应名称分别为“躁狂”(3例)和“精神异常”。
建议
鉴于国外研究显示服用抗癫痫药患者可能存在自杀观念或自杀行为的风险,并且此类药物多由患者在家中自服或由看护者监督服用,建议医生处方抗癫痫药时,告知患者、患者家属及看护者关于抗癫痫药可能增加自杀观念或行为的风险:对于目前正在服用抗癫痫药的患者,在没有咨询医生之前,不要擅自停药或改变治疗方案;如发现患者出现焦虑、激动、敌意、躁狂、抑郁或抑郁加重等精神症状,或有伤害自己、远离家人和朋友等想法或行为时,患者家属及看护者应及时告知医生。

