屋尘螨集群免疫治疗过敏性鼻炎和哮喘的疗效和安全性:一项多中心前瞻性单臂干预研究


【摘要】 目的 探讨屋尘螨注射制剂4周集群免疫治疗尘螨过敏患者的疗效和安全性。方法 于2022年8月至2024年5月从北京协和医院等多中心招募屋尘螨过敏的过敏性鼻炎伴或不伴哮喘的患者80例,进行屋尘螨4周剂量递增方案皮下集群免疫治疗,在第0、1、6、12月统计患者的症状和药物、生活质量、哮喘控制测试结果以及局部和全身不良反应。结果 不同时间点集群免疫治疗的每日症状总评分(P < 0.001)、日均鼻部评分(P < 0.001)、日均眼部评分(P = 0.009)、症状和药物总评分(P = 0.003)差异均具有统计学意义,活动鼻结膜炎生活质量问卷(RQLQ)(P < 0.001)、睡眠RQLQ(P = 0.002)、非眼鼻症状RQLQ(P = 0.032)、实际问题RQLQ(P < 0.001)、鼻部症状RQLQ(P < 0.001)、情感RQLQ(P = 0.011)、总RQLQ(P < 0.001)以及儿童哮喘控制测试评分(P < 0.001)的差异亦有统计学意义,且时间越长,评分越低。剂量递增期间,共22例(27.5%)患者出现局部不良反应,5例(6.3%)患者出现了全身不良反应,35剂次(3.6%)出现不良反应,包括27剂次(2.8%)的局部不良反应和8剂次(0.8%)的全身不良反应。结论 屋尘螨4周集群免疫治疗对尘螨过敏的患者有显著的疗效。
【关键词】 屋尘螨;集群免疫;过敏性鼻炎;哮喘;疗效;安全性
Efficacy and safety of house dust mite cluster immunotherapy in the treatment of allergic rhinitis and asthma: a multicenter prospective single-arm interventional study
SHANG Tengze1*, LI Lisha1*, WANG Qing1, DENG Baiyu2, ZHANG Xiaoli3, HUANG Yan3 , JIN Xiuhong4 ,
MENG Wenxia5 , YAO Hui2, GUAN Kai1
(1.Department of Allergy, Peking Union Medical College Hospital, Chinese Academy of Medical Sciences, Peking Union Medical College, Beijing 100730, China;2. Department of Pediatrics, Beijing Yide Hospital, Beijing 100097, China;3. Department of Respiratory Allergy, Beijing Jingdu Children’ s Hospital, Beijing102208, China; 4. Department of Respiratory Medicine, Zhengzhou Children’ s Hospital, Zhengzhou 4511613, China; 5. Department of Allergy, the First Hospital of Hebei Medical University, Shijiazhuang 050031, China)
Co-first authors: SHANG Tengze, LI Lisha
Corresponding authors: HUANG Yan, E-mail: 13304280868@163.com; JIN Xiuhong, E-mail: doctorjin939@126.com; MENG Wenxia, E-mail: guomin645@126.com; YAO Hui, E-mail: yh_jinan@163.com; GUAN Kai, E-mail: dr_guankai@126.com
【Abstract】 Objective To investigate the efficacy and safety of 4-week cluster immunotherapy with house dust mite extracts in patients allergic to house dust mites. Methods From August 2022 to May 2024, 80 patients with house dust mite-induced allergic rhinitis, complicated with or without asthma, were recruited from multiple centers (including Peking Union Medical College, et al) to undergo 4-week dose-escalation subcutaneous cluster immunotherapy with house dust mites. Patient symptoms, medication use, quality of life, asthma control test (ACT) results, as well as local and systemic adverse reactions were recorded at 0, 1, 6, and 12 months, respectively. Results Significant differences were observed in the daily total symptom scores (P < 0.001), daily nasal scores (P < 0.001), daily ocular scores (P = 0.009), and total symptom and medication scores (P = 0.003) across different time points during cluster immunotherapy, respectively. Significant differences were also found in the activity RQLQ (P < 0.001), sleep RQLQ (P = 0.002), non-eye/nose symptom RQLQ (P = 0.032), practical problems RQLQ (P < 0.001), nasal symptom RQLQ (P < 0.001), emotional RQLQ (P = 0.011), total RQLQ (P < 0.001), and children’s ACT scores (P <
0.001), respectively. The longer the time, the lower the score. During the dose-escalation period, 22 patients (27.5%) experienced local adverse reactions, and 5 patients (6.3%) experienced systemic adverse reactions. A total of 35 (3.6%) injections resulted in adverse reactions, including 27 (2.8%) injections with local reactions and 8 (0.8%) injections with systemic reactions. Conclusion Four-week cluster immunotherapy with house dust mites shows significant efficacy in patients allergic to house dust mites.
【Key words】 House dust mite; Cluster immunotherapy; Allergic rhinitis; Asthma; Efficacy; Safety
过敏性疾病已经成为全球第六大慢性疾病,在过去的30年,过敏性疾病的发病率急剧上升,并且这个趋势还在加速[1]。根据世界变态反应组织(World Allergy Organization,WAO)的《变态反应白皮书》(2020版)估计,到2050年,全球过敏性疾病患病人数将达到40亿。2005 年到 2011年,我国过敏性鼻炎患病率从11.1%上升到17.6%[2]。支气管哮喘(哮喘)发病率也显著提升[3]。屋尘螨是过敏性鼻炎和哮喘患者的主要变应原之一,由于屋尘螨广泛分布,尤其是在室内,导致患者难以单纯通过隔离变应原的方法来缓解症状,需要通过抗组胺药,白三烯受体拮抗剂,鼻喷糖皮质激素等对症药物治疗,或应用变应原免疫治疗(allergen immunotherapy,AIT)。对症药物虽能减轻症状,但停药后易复发,且有不良反应的风险,部分重症患者用药后仍然控制不佳。
AIT是把变应原从少量到大量逐步导入人体,让患者对变应原产生耐受的针对病因的疗法,是目前唯一能阻止过敏性疾病进展的方法[4]。我国目前临床中最常用的AIT是皮下注射免疫治疗(subcutaneous immunotherapy,SCIT)。SCIT可分为2个阶段,变应原注射剂量逐步增加的剂量递增期,以及达到最大剂量以后保持该剂量规律注射的维持治疗期。传统SCIT方案的剂量递增期每次递增的剂量幅度较小,对应的递增步骤较多,需要花费4~6个月的时间才能达到最大维持治疗剂量。患者在此期间需要频繁就诊接受注射,治疗的积极性和依从性都会受到影响。集群免疫治疗是一种改良SCIT方案,精简了剂量递增期的注射步骤,患者每周来院1次,每次注射2~3针,3~6周后即可达到维持剂量。集群方案不仅能降低医疗的直接成本(交通、医药费用)和间接成本(花费时间),还能更早产生疗效[5],有助于提高患者的依从性。既往对多种变应原集群免疫治疗的研究结果显示,集群免疫治疗的长期疗效不低于传统的SCIT[6-8],同时不良反应发生率也相似[5, 9-13]。虽然国内已经有针对尘螨过敏原的集群免疫治疗的临床试验报道,但缺乏多中心前瞻性研究,而且使用的多是6周剂量递增方案,因此北京协和医院联合多家单位开展4周剂量递增集群方案多中心前瞻性单臂干预研究,探究屋尘螨集群免疫治疗对过敏性鼻炎和哮喘的疗效和安全性,现将目前结果报告如下。
1 对象与方法
1.1 研究对象
本研究是一个多中心前瞻性单臂干预研究,受试者来源于北京协和医院、北京京都儿童医院、河北医科大学第一医院、河南省儿童医院、北京怡德医院2022年8月至2024年5月临床确诊为尘螨过敏的患者。使用G*Power 3.1.9.7估算样本量,设定统计功效为0.95,显著性水平为0.05,选择重复测量方差分析,预期效应量大小为 0.25,重复测量之间的相关性估计为 0.3,得出需要总样本量为60例,考虑15%的失访率,研究共计纳入了80例患者。部分患者未完成全周期随访,后续将继续完成随访得到完整结果。
纳入标准:①年龄≥5岁;②具有典型的过敏性鼻炎和哮喘症状,哮喘诊断包括典型症状或症状不典型但伴以下试验至少一项为阳性:支气管舒张试验阳性,支气管激发试验阳性,呼气峰流速值变异率≥20%,病程≥2年;③屋尘螨皮内试验结果≥++(即皮试风团最长直径≥10 mm),且屋尘螨血清sIgE水平≥2级(Uni-CAP变应原sIgE检测系统);④肺功能:第1秒用力呼气容积(forced expiratory volume in 1 second,FEV1)≥80%预计值,一秒率(forced expiratory volume in 1 second to forced expiratory vital capacity,FEV1/FVC)≥70%;⑤除尘螨外的其他吸入变应原sIgE结果及皮试阴性。
排除标准:①伴有未控制的哮喘或重度哮喘以及不能逆转的呼吸道阻塞性疾病(如肺气肿);②妊娠或哺乳期的女性患者;③患有严重的心血管疾病,急慢性感染疾病,自身免疫性或免疫缺陷疾病,恶性肿瘤等疾病等患者;④正在使用β受体阻滞剂;⑤有严重的精神障碍。
本研究已获得中国医学科学院北京协和医院伦理委员会的批准(批件号:JS-2771)并在分中心备案,所有受试者均签署知情同意书。
1.2 干预方案
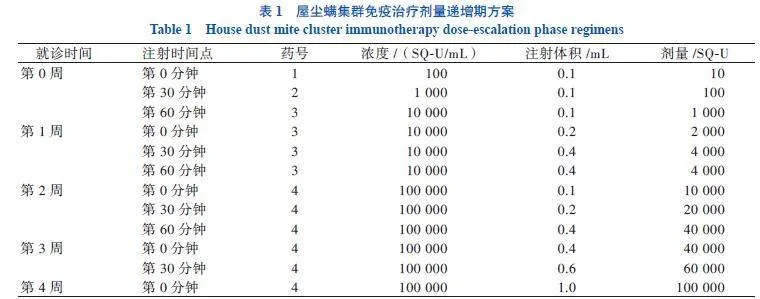
对纳入的研究对象进行“安脱达”屋尘螨注射制剂(ALK Abello,丹麦)集群免疫治疗。疗程分为2个阶段:剂量递增期和剂量维持期。剂量递增期间,每周就诊1次,注射2~3剂次,持续4周。在剂量维持期间,开始治疗的第6周注射1次,然后第10周注射1次,第16周注射1次,之后每间隔6周注射1次。具体剂量递增方案见表1。
1.3 评价指标
在开始前(第0个月)、1个月、6个月、12个月4个时间点统计患者的症状和药物综合评分、哮喘药物评分、哮喘控制测试评分、生活质量、局部和全身不良反应。
1.3.1 疗效评价
症状和药物综合评分(combined symptom and medication score,CSMS)[14]:CSMS是每日药物总评分(daily medication score,dMS)和每日症状总评分(daily symptom score,dSS)之和。dMS为以下评分之和:口服/局部使用抗组胺药,每天计1分;鼻用激素,每天计2分;口服糖皮质激素,每天计3分。dSS包含4个鼻部症状(鼻痒、喷嚏、流涕、鼻塞)和2个眼部症状(眼痒、流泪),均为0~3分,得分越高症状越重,所有症状评分的平均值即为dSS。
哮喘药物评分:根据Dahl等[15]的方法构建患者哮喘药物评分:收集患者用药情况,吸入短效β2-受体激动剂 (short-acting beta 2-agonists,SABA),如沙丁胺醇每100 μg为1分,每天最高为8分;吸入性糖皮质激素(inhaled corticosteroids,ICS):氟替卡松每125 μg为1分,布地奈德每200 μg为1分,每天最高为8分;口服糖皮质激素换算为等效泼尼松,每5 mg为1.6分,每天最高16分。
哮喘控制测试(asthma control test,ACT):评估和监测哮喘控制水平的有效方式,问卷调查评估近4周的临床症状,分为儿童[16]和成人[17]2个版本,儿童内容为7项,每项0~4分,前4项内容由患儿自己作答,后3项内容主要由家长代为完成;成人内容为5项,每项0~5分。分数越低,哮喘控制越差。
生活质量:采用变应性鼻结膜炎生活质量问卷(Rhinoconjunctivitis Quality of Life Questionnaire,RQLQ)[18],包括7个方面:活动、睡眠、情感、非眼鼻症状、实际问题、鼻部症状、眼部症状,共28个项目,每个项目评价为0~6分,得分越高,生活质量受影响越大,最终RQLQ得到的平均分用于评估患者的生活质量。
1.3.2 安全性评价
局部不良反应:根据欧洲变态反应与临床免疫学会指南,局部不良反应主要包括注射部位风团、硬结,本研究将直径5 mm作为局部反应的下限值。
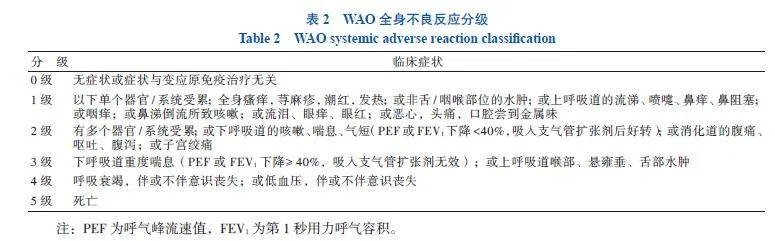
全身不良反应参考WAO对皮下注射变应原全身过敏反应的严重度分级[19],见表2。
1.4 统计学方法
定量资料如果符合正态分布则用表示,若不符合正态分布则采用M(P25,P75)表示,定性资料采用n(%)描述。本研究是重复测量数据,由于存在数据的缺失,采用广义估计方程(generalized estimating equation,GEE)评估集群免疫治疗的疗效。所有分析采用SPSS 27.0,以双侧P < 0.05为差异有统计学意义。
2 结 果
2.1 入组患者一般情况
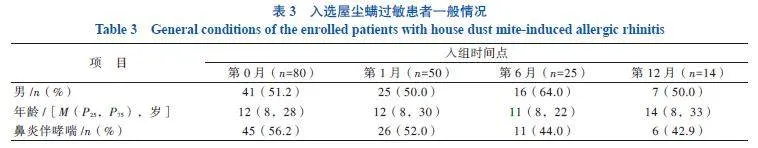
本研究共纳入80例患者,由于入组时间不同,部分患者未达到12个月的治疗时间。患者的基本信息见表3。
2.2 症状和药物综合评分结果
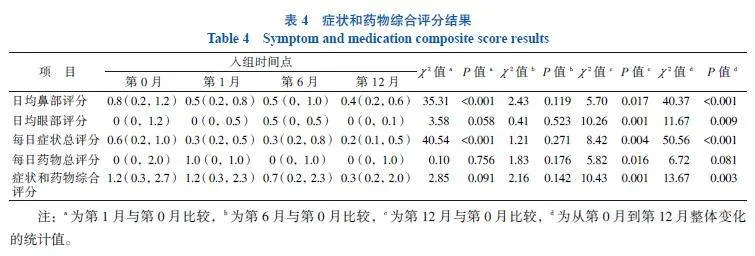
GEE的结果显示,不同时间点的日均鼻部评分(P < 0.001)、日均眼部评分(P = 0.009)、每日症状总评分(P < 0.001)、症状和药物综合评分(P = 0.003)差异均具有统计学意义,治疗时间越长,评分越低。虽然每日药物总评分(P = 0.081)在不同时间点的差异无统计学意义,但第12月和第0月的差异有统计学意义(P = 0.016)。具体来看,以第0月为基准,第1月时日均鼻部评分、每日症状总评分出现了下降,P均< 0.001;第12月时的所有评分都出现了明显的下降。见表4。
2.3 哮喘药物评分和控制测试问卷结果
对伴有咳喘的患者统计其哮喘药物评分,经过广义估计方程计算,结果显示,整体上哮喘药物评分的差异有统计学意义(P = 0.031),治疗时间越长,评分越低。但是,和第0月相比,第1月(P =0.090)、第6月(P = 0.684)、第12月(P = 0.794)的差异均无统计学意义。见表5。
因为儿童和成人的ACT问卷不同,所以将患者分为儿童和成人2组分析进行GEE分析。结果显示,成人不同时间点的ACT评分差异无统计学意义(P = 0.593),以第0月为参照,其他时间点也没有显示出差异性;儿童不同时间点的ACT评分差异有统计学意义(P < 0.001),以第0月为参照,第6月(P = 0.020)、第12月差异均有统计学意义(P < 0.001)。见表5。
2.4 变应性鼻结膜炎生活质量问卷结果
GEE的结果显示,不同时间点的活动RQLQ(P < 0.001)、睡眠RQLQ(P = 0.002)、非眼鼻症状RQLQ(P = 0.032)、实际问题RQLQ(P < 0.001)、鼻部症状RQLQ(P < 0.001)、情感RQLQ(P = 0.011)、总RQLQ(P < 0.001)的差异有统计学意义,治疗时间越长,评分越低。虽然眼部症状
RQLQ在不同时间点的差异无统计学意义(P = 0.057),但第12月和第0月相比,差异有统计学意义(P = 0.046)。具体来看,以第0月为基准,第1月时除了非眼鼻症状RQLQ(P = 0.072)无明显下降外,其他生活质量评分均下降,差异具有统计学意义;第12月时所有的生活质量评分均下降,差异有统计学意义。见表6。
2.5 不良反应
剂量递增期间,80例患者中22例(27.5%)患者出现了局部不良反应,5例(6.3%)患者出现了全身不良反应。80例患者共注射了960剂次,其中35剂次(3.6%)出现不良反应,包括27剂次
(2.8%)的局部不良反应和8剂次(0.8%)的全身不良反应。局部速发超敏反应共计19剂次(2.0%),风团直径平均为10.4 mm,出现症状的时间平均为22 min,且89.5%的患者是在30 min内出现症状。局部迟发超敏反应共计8剂次(0.8%)。共计8剂次(0.8%)全身超敏反应,严重程度均为Ⅰ级,只累及呼吸系统,口服抗组胺药物后均好转。见表7。
3 讨 论
过敏性疾病的发病率逐年增高,对儿童的生长发育和成人的工作生活都造成了严重的影响。虽然规避过敏原能有效地控制过敏性疾病,但尘螨的广泛分布导致规避过敏原几乎不可能。药物对症治疗能控制症状,但在实际中,患者常难以坚持规律用药。AIT能根治疾病,逆转或减缓疾病的进程,可以作为治疗过敏性疾病的有效手段。
虽然既往有研究屋尘螨集群治疗的疗效和安全性,但它们在剂量递增期使用的是6周方案,本研究使用的是北京协和医院的4周方案,这也是国内第一个使用协和4周方案的多中心屋尘螨集群治疗对过敏性鼻炎和哮喘疗效和安全性的研究。经过12个月的治疗,从症状和药物相关评分、哮喘药物评分、生活质量评分的结果来看,患者症状明显改善,和开始时的评分差异具有统计学意义。ACT评分在儿童中显示出明显的疗效,成人中的疗效不显著,考虑到成人哮喘患者随访时间达到12个月仅有3例,尚不能说明成人哮喘患者症状无改善,还需要延长随访时间得到更确切的结论。剂量递增期间局部不良反应为2.8%,全身不良反应为0.8%。总之,本研究发现屋尘螨注射制剂集群脱敏对患者有明显的疗效和较好的安全性。
国外有研究探究过屋尘螨注射制剂集群对尘螨过敏的鼻炎或哮喘患者的疗效,在一项前瞻性双盲随机对照研究中,对尘螨过敏的鼻炎伴或不伴哮喘的患者进行常规和集群脱敏,治疗12个月后发现常规脱敏和集群脱敏的疗效无显著差异,集群免疫患者的药物症状评分下降43%,患者的主观症状改善提高了21%[5]。另一项关于尘螨集群免疫的研究显示,治疗12个月后症状药物综合评分下降了40%[20]。以上研究的结果和本研究的结果一致,均发现集群脱敏治疗对患者症状有明显的改善。
根据既往的研究,常规脱敏的局部不良反应发生率在0.8%~80%,全身不良反应发生率在0.025%~3.2%[21-22]。美国的一个多中心回顾性集群免疫治疗研究收集了441例患者,10.9%的患者出现了全身过敏反应[23]。欧洲一项纳入1 147例患者的多中心回顾性研究发现[24],尘螨和花粉的集群免疫治疗剂量递增期间,3.4%患者发生全身不良反应,0.6%的注射次数发生全身不良反应。其他的大多数研究都表明集群和常规免疫治疗的安全性无显著差异[25-26]。本研究剂量递增期的局部不良反应发生率为2.8%,全身不良反应为0.8%,不高于既往安托达免疫治疗的不良反应发生率[27-31],发生全身不良反应的2例患者均为Ⅰ级全身不良反应,表现为咳嗽、胸闷,吸入SABA后均缓解。在剂量维持期间,未发现全身过敏性反应。
总之,和既往的研究相比,本研究的安全性良好,证实了屋尘螨注射制剂集群脱敏有明显的疗效和可靠的安全性,为临床工作提供了重要的参考。本研究通过多中心的数据证实了屋尘螨集群免疫治疗在中国人的有效性和安全性。当然,研究也存在一些不足,首先,本研究是单臂研究,没设置常规治疗组对比;其次,由于患者入组时间不同,部分患者尚未治疗满12个月,还须进一步随访收集数据;然后,欧洲变态反应和临床免疫年会建议脱敏治疗需要3~5年[32],本研究最长治疗时间只有1年,还需要更长的随访时间来进一步观察疗效和安全性。
参 考 文 献
[1] ANDERSSON E, LÖFVENDAHL S, OLOFSSON S, et al. Disease burden and unmet need for acute allergic reactions: a patient perspective[J]. 2024, 17(4): 100896. DOI: 10.1016/j.waojou.2024.100896.
[2] WANG X D, ZHENG M, LOU H F, et al. An increased prevalence of self-reported allergic rhinitis in major Chinese cities from 2005 to 2011[J]. Allergy, 2016, 71(8): 1170-1180. DOI: 10.1111/all.12874.
[3] LIN J, WANG W, CHEN P, et al. Prevalence and risk factors of asthma in mainland China: the CARE study[J]. Respir Med, 2018, 137: 48-54. DOI: 10.1016/j.rmed.2018.02.010.
[4] ALVARO-LOZANO M, AKDIS C A, AKDIS M, et al. EAACI allergen immunotherapy user’s guide[J]. Pediatr Allergy Immunol, 2020, 31(Suppl 25): 1-101. DOI: 10.1111/pai.
13189.
[5] TABAR A I, ECHECHIPÍA S, GARCÍA B E, et al. Double-blind comparative study of cluster and conventional immunotherapy schedules with Dermatophagoides pteronyssinus[J]. J Allergy Clin Immunol, 2005, 116(1): 109-118. DOI: 10.1016/j.jaci.
2005.05.005.
[6] 罗志红, 李彬, 万浪, 等. 变应性鼻炎集群免疫治疗与常规免疫治疗的临床疗效及安全性对照研究[J]. 中华耳鼻咽喉头颈外科杂志, 2015, 50(2): 105-109. DOI: 10.3760/cma.j.issn.1673-0860.2015.02.004.
LUO Z H, LI B, WAN L, et al. Comparative study on cluster and conventional immunotherapy in patients with allergic rhinitis[J]. Chin J Otorhinolaryngol Head Neck Surg, 2015, 50(2): 105-109. DOI: 10.3760/cma.j.issn.1673-0860.2015.02.004.
[7] 王成硕, 张伟, 王向东, 等. 变应性鼻炎屋尘螨变应原集群免疫治疗与常规免疫治疗的对照研究[J]. 中华耳鼻咽喉头颈外科杂志, 2011, 46(12): 981-985. DOI: 10.3760/cma.j.issn.1673-0860.2011.12.004.
WANG C S, ZHANG W, WANG X D, et al. Comparative study on cluster and conventional immunotherapy with Dermatophagoides pteronyssinus in patients with allergic rhinitis[J]. Chin J Otorhinolaryngol Head Neck Surg, 2011, 46(12): 981-985. DOI: 10.3760/cma.j.issn.1673-0860.2011.12.004.
[8] 凡启军, 刘国钧, 刘学军, 等. 尘螨过敏的变应性鼻炎集群免疫与常规免疫治疗的疗效及安全性临床对照研究[J]. 医学研究杂志, 2013, 42(3): 123-127. DOI: 10.3969/j.issn.1673-548X.2013.03.038.
FAN Q J, LIU G J, LIU X J, et al. Comparative study on cluster and conventional immunotherapy in patients with allergic rhinitis[J].
J Med Res, 2013, 42(3): 123-127. DOI: 10.3969/j.issn.1673-548X.2013.03.038.
[9] SCHUBERT R, EICKMEIER O, GARN H, et al. Safety and immunogenicity of a cluster specific immunotherapy in children with bronchial asthma and mite allergy[J]. Int Arch Allergy Immunol, 2009, 148(3): 251-260. DOI: 10.1159/000161585.
[10] PFAAR O, MÖSGES R, HÖRMANN K, et al. Safety aspects of cluster immunotherapy with semi-depot allergen extracts in seasonal allergic rhinoconjunctivitis[J]. Eur Arch Otorhinolaryngol,
2010, 267(2): 245-250. DOI: 10.1007/s00405-009-1077-6.
[11] COLÁS C, MONZÓN S, VENTURINI M, et al. Double-blind, placebo-controlled study with a modified therapeutic vaccine of Salsola kali (Russian thistle) administered through use of a cluster schedule[J]. J Allergy Clin Immunol, 2006, 117(4): 810-816. DOI: 10.1016/j.jaci.2005.11.039.
[12] QUIRALTE J, JUSTICIA J L, CARDONA V, et al. Is faster safer? Cluster versus short conventional subcutaneous allergen immunotherapy[J]. Immunotherapy, 2013, 5(12): 1295-1303. DOI: 10.2217/imt.13.133.
[13] PARMIANI S, FERNÁNDEZ TÁVORA L, MORENO C, et al.
Clustered schedules in allergen-specific immunotherapy[J].
Allergol Immunopathol, 2002, 30(5): 283-291. DOI: 10.1016/s0301-0546(02)79138-6.
[14] PALATHUMPATTU B, PIEPER-FÜRST U, ACIKEL C, et al. Correlation of the combined symptom and medication score with quality of life, symptom severity and symptom control in allergic rhinoconjunctivitis[J]. Clin Transl Allergy, 2022, 12(10): e12191. DOI: 10.1002/clt2.12191.
[15] DAHL R, STENDER A, RAK S. Specific immunotherapy with SQ standardized grass allergen tablets in asthmatics with rhinoconjunctivitis[J]. Allergy, 2006, 61(2): 185-190. DOI: 10.1111/j.1398-9995.2005.00949.x.
[16] 吴谨准. 儿童哮喘控制测试及其临床应用价值[J]. 中国实用儿科杂志, 2009, 24(4): 261-263.
WU J Z. Application of asthma control test to children and its evaluation[J]. Chin J Pract Pediatr, 2009, 24(4): 261-263.
[17] 中华医学会呼吸病学分会哮喘学组. 支气管哮喘防治指南(2020年版)[J]. 中华结核和呼吸杂志, 2020, 43(12): 1023-1048. DOI: 10.3760/cma.j.cn112147-20200618-00721.
Asthma group of Chinese Throacic Society.Guidelines for bronchial asthma prevent and management(2020 edition) Asthma group of Chinese Throacic Society[J]. Chin J Tuberc Respir Dis, 2020, 43(12): 1023-1048. DOI: 10.3760/cma.j.cn112147-20200618-00721.
[18] JUNIPER E F, GUYATT G H, DOLOVICH J. Assessment of quality of life in adolescents with allergic rhinoconjunctivitis: development and testing of a questionnaire for clinical trials[J].
J Allerg3Bg8kxaCX6rJMV/DQoyCE99bZjJFqjDFhNQjO5IzKVM=y Clin Immunol, 1994, 93(2): 413-423. DOI: 10.1016/
0091-6749(94)90349-2.
[19] CARDONA V, ANSOTEGUI I J, EBISAWA M, et al. World allergy organization anaphylaxis guidance 2020[J]. World Allergy Organ J, 2020, 13(10): 100472. DOI: 10.1016/j.waojou.2020.100472.
[20] CARDONA-VILLA R, URIBE-GARCIA S, CALVO-BETANCUR V D, et al. Efficacy and safety of subcutaneous immunotherapy with a mixture of glutaraldehyde-modified extracts of Dermatophagoides pteronyssinus, Dermatophagoides farinae, and Blomia tropicalis[J]. World Allergy Organ J, 2022, 15(9): 100692. DOI: 10.1016/j.waojou.2022.100692.
[21] ROY S R, SIGMON J R, OLIVIER J, et al. Increased frequency of large local reactions among systemic reactors during subcutaneous allergen immunotherapy[J]. Ann Allergy Asthma Immunol, 2007, 99(1): 82-86. DOI: 10.1016/S1081-1206(10)60626-6.
[22] GREENBERG M A, KAUFMAN C R, GONZALEZ G E, et al. Late and immediate systemic-allergic reactions to inhalant allergen immunotherapy[J]. J Allergy Clin Immunol, 1986, 77(6):
865-870. DOI: 10.1016/0091-6749(86)90385-4.
[23] COPENHAVER C C, PARKER A, PATCH S. Systemic reactions with aeroallergen cluster immunotherapy in a clinical practice[J]. Ann Allergy Asthma Immunol, 2011, 107(5): 441-447. DOI: 10.1016/j.anai.2011.06.026.
[24] SERRANO P, JUSTICIA J L, SÁNCHEZ C, et al. Systemic tolerability of specific subcutaneous immunotherapy with index-of-reactivity-standardized allergen extracts administered using clustered regimens: a retrospective, observational, multicenter study[J]. Ann Allergy Asthma Immunol, 2009, 102(3): 247-252. DOI: 10.1016/S1081-1206(10)60088-9.
[25] COX L. Accelerated immunotherapy schedules: review of efficacy and safety[J]. Ann Allergy Asthma Immunol, 2006, 97(2): 126-137; quiz137-40, 202-202. DOI: 10.1016/S1081-1206(10)60003-8.
[26] STEWART G E 2nd, LOCKEY R F. Systemic reactions from allergen immunotherapy[J]. J Allergy Clin Immunol, 1992, 90(4 Pt 1): 567-578. DOI: 10.1016/0091-6749(92)90129-p.
[27] 冯淑仙, 褚玉会, 张智风. 安脱达屋尘螨变应原疫苗与低温等离子治疗变应性鼻炎的疗效比较[J]. 中国医药导刊, 2021, 23(4): 261-263. DOI: 10.3969/j.issn.1009-0959.2021.04.006.
FENG S X, CHU Y H, ZHANG Z F. Comparison of the curative effect of alutard house dust mite allergens vaccine and low-temperature plasma in the treatment of allergic rhinitis[J]. Chin J Med Guide, 2021, 23(4): 261-263. DOI: 10.3969/j.issn.1009-0959.2021.04.006.
[28] 上官秋苓. 标准化变应原疫苗安脱达治疗儿童变应性鼻炎合并哮喘30例疗效分析[J]. 系统医学, 2016, 1(11): 81-83. DOI: 10.19368/j.cnki.2096-1782.2016.11.081.
SHANGGUAN Q L. The effect observation of 30 children with allergic rhinitis and asthma by standardized allergen vaccine(antuoda) treatment[J]. Syst Med, 2016, 1(11): 81-83. DOI: 10.19368/j.cnki.2096-1782.2016.11.081.
[29] 杨雅琪, 杨永仕, 汪茵, 等. 安脱达特异性免疫治疗儿童变应性鼻炎伴/不伴哮喘的临床效果观察[J]. 检验医学与临床, 2018, 15(21): 3183-3185, 3190. DOI: 10.3969/j.issn.
1672-9455.2018.21.006.
YANG Y Q, YANG Y S, WANG Y, et al. ALK® house dust mite SCIT in children for allergic rhinitis with/without asthma[J]. Lab Med Clin, 2018, 15(21): 3183-3185, 3190. DOI: 10.3969/j.issn.1672-9455.2018.21.006.
[30] 王瑞云, 李群欢, 方向佳, 等. 标准化尘螨疫苗免疫治疗过敏性鼻炎的疗效[J]. 分子影像学杂志, 2016, 39(2): 197-199. DOI: 10.3969/j.issn.1674-4500.2016.02.37.
WANG R Y, LI Q H, FANG X J, et al. Observation and nursing of allergic rhinitis curative in treatment of standardized dust mites vaccine immune[J]. J Mol Imag, 2016, 39(2): 197-199. DOI: 10.3969/j.issn.1674-4500.2016.02.37.
[31] 易华容, 刘远华, 叶菁, 等. 标准化尘螨变应原制剂治疗变应性鼻炎的不良反应观察[J]. 临床耳鼻咽喉头颈外科杂志, 2014, 28(23): 1870-1872, 1876. DOI: 10.13201/j.issn.1001-
1781.2014.23.015.
YI H R, LIU Y H, YE J, et al. Clinical observation of the adverse effects of standardized dust mite allergen preparation in the treatment of allergic rhinitis[J]. J Clin Otorhinolaryngol Head Neck Surg, 2014, 28(23): 1870-1872, 1876. DOI: 10.13201/j.issn.1001-1781.2014.23.015.
[32] JENSEN-JAROLIM E, BACHMANN M F, BONINI S, et al.
State-of-the-art in marketed adjuvants and formulations in Allergen Immunotherapy: a position paper of the European Academy of Allergy and Clinical Immunology (EAACI)[J]. Allergy, 2020, 75(4): 746-760. DOI: 10.1111/all.14134.
(责任编辑:郑巧兰)
