阵发性心房颤动病人冷冻消融与射频消融术中镇痛药物使用剂量及有效性、安全性比较

摘要 目的:比较心房颤动冷冻消融与射频消融两种不同消融方式术中镇痛药物使用剂量及有效性、安全性。方法:纳入2021年1月—10月于首都医科大学附属北京安贞医院行经导管消融治疗的阵发性心房颤动病人60例,根据消融方式不同分为射频消融组及冷冻消融组,每组30例。比较两组术中使用镇痛药物枸橼酸芬太尼的总剂量、术中症状、手术时间、并发症等。结果:冷冻消融组使用枸橼酸芬太尼的总剂量更少(P<0.01),手术时间更短(P<0.01),且头痛、咳嗽的发生率高于射频消融组(P<0.05或P<0.01),均实现了肺静脉隔离,并发症方面差异无统计学意义(P>0.05)。结论:心房颤动冷冻消融术中使用镇静镇痛药物剂量较小,病人对冷冻消融产生的疼痛耐受程度更好。
关键词 心房颤动;冷冻消融;射频消融;芬太尼
doi:10.12102/j.issn.1672-1349.2024.20.022
作者单位 1.北京中医药大学第一临床医学院(北京中医药大学东直门医院)(北京 100700);2.首都医科大学附属北京安贞医院(北京 100029)
通讯作者 吴焕林,E-mail:wuhuanlinboshi@aliyun.com
引用信息 玄昌波,杨士伟,潘国忠,等.阵发性心房颤动病人冷冻消融与射频消融术中镇痛药物使用剂量及有效性、安全性比较[J].中西医结合心脑血管病杂志,2024,22(20):3767-3770.
心房颤动是临床最常见的快速性心律失常之一,目前心房颤动经导管消融治疗的有效性和安全性已被大量临床研究证实,在维持窦律、改善症状和生活质量方面显著优于药物治疗。心房颤动导管消融根据能源不同,目前在临床中应用最多的主要分为射频消融和冷冻消融,肺静脉隔离(pulmonary vein isolation,PVI)是心房颤动导管消融治疗的基石[1-2]。心房颤动射频消融及冷冻消融均对肺静脉前庭等心脏部位产生损伤,从而产生疼痛感[3],病人因疼痛可能导致身体位置的移动,从而影响心房颤动导管消融手术的有效性和安全性,因此,心房颤动导管消融术中常常需要镇痛镇静治疗[4-5]。为保证心房颤动导管消融的安全有效,目前国内较多中心在心房颤动消融术中采用静脉泵入枸橼酸芬太尼的方法镇痛镇静治疗,本研究总结了冷冻消融与射频消融治疗阵发性心房颤动病人术中应用枸橼酸芬太尼镇痛镇静病人的临床资料及术中、术后情况,比较两种消融方法使用镇痛药物的剂量以及两种消融方法的有效性及安全性。现报道如下。
1 资料与方法
1.1 研究对象
回顾性分析首都医科大学附属北京安贞医院2021年1月—10月经导管消融治疗的阵发性心房颤动病人60例,射频消融组及冷冻消融组各30例。纳入标准:阵发性心房颤动诊断标准参考《心房颤动:目前的认识和治疗建议(2021)》[2]。入选病人均为有症状的阵发性心房颤动病人,经抗心律失常药物治疗后效果不佳。排除标准:瓣膜性心房颤动、曾行心房颤动消融手术、先天性心脏病等或甲状腺功能亢进等疾病引起的继发性心房颤动病人。
1.2 方法
1.2.1 射频消融组
病人平卧于导管床,常规消毒、铺巾,穿刺双侧股静脉并成功置入冠状窦电极,经右股静脉置入8.5F Swartz鞘至右心房,送入房间隔穿刺针,成功穿刺房间隔后置Swartz鞘于左心房内,肝素化后在三维电生理标测系统指导下送入星形磁电双定位导管(Pentaray导管)至左心房,建立左心房模型。建模结束后,使用导航星56孔冷盐水灌注压力监测导管(ST-SF)行消融治疗。消融模式:上限功率35 W,上限温度43 ℃,冷盐水灌注17 mL/min。手术终点为双侧肺静脉传入及传出双向阻滞。术后根据指南及病人临床情况服用抗心律失常药物及抗凝药物等。
1.2.2 冷冻球囊消融组
病人平卧于导管床,常规消毒、铺巾,穿刺双侧股静脉并成功置入冠状窦电极及右心室电极,经右股静脉置入8.5F Swartz鞘至右心房,送入房间隔穿刺针,穿刺房间隔后置Swartz鞘于左心房内,肝素化后行双侧肺静脉造影。置换Swartz鞘为Flexcath鞘到左心房内,送Achieve电极先后至左上、左下、右下、右上肺静脉适当位置,记录肺静脉电位,28 mm冷冻球囊充气后贴靠肺静脉前庭,造影观察肺静脉开口封堵情况,确保封堵满意后开始冷冻消融治疗,消融左侧肺静脉起搏右心室电极防止迷走反射、消融右侧肺静脉时起搏膈神经预防膈神经损伤。手术终点为全部肺静脉隔离。术后根据指南及病人临床情况服用抗心律失常药物及抗凝药物等。
1.3 观察指标
两种消融方式术中均静脉使用枸橼酸芬太尼镇痛镇静治疗。使用方法:取0.5 mg用生理盐水稀释至50 mL,持续静脉泵入芬太尼1 μg /(kg·h),如果术中疼痛明显,增加芬太尼至2 μg/(kg·h),房间隔穿刺完毕后开始给药直至手术结束。术中备好呼吸机、简易呼吸器以及麻醉意外抢救药品。两组病人术后根据指南及临床情况给予相同抗凝、抗心律失常、预防左心房食道瘘等药物治疗方案。术中常规记录两种不同消融方式使用芬太尼的总剂量、手术时间、术中病人的症状表现等,术后常规复查心电图并心电血压监测24 h,观察有无心脏压塞、膈神经麻痹、假性动脉瘤、穿刺部位血肿、穿刺处动静脉瘘、左心房食道瘘、肺静脉狭窄等相关并发症。
1.4 统计学处理
采用SPSS 25.0统计软件进行数据分析。定量资料以均数±标准差(x±s)表示,符合正态分布采用独立样本t检验,不符合正态分布用两个独立样本的非参数检验;定性资料比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组临床资料比较
射频消融组,男21例,女9例;年龄39~75(60.4±9.8)岁;体重(70.67±5.99)kg。冷冻消融组,男20例,女10例;年龄42~76(61.4±9.2)岁;体重(71.77±7.36)kg。两组性别、体重、心房颤动时间、脑卒中风险评分(CHADS-VaSc评分)、左房前后径等临床资料比较,差异均无统计学意义(P>0.05)。详见表1。
2.2 两组术中使用枸橼酸芬太尼使用剂量比较
射频消融组芬太尼使用量为(0.27±0.31)mg,冷冻消融组芬太尼使用量为(0.11±0.30)mg,两组比较差异有统计学意义(P<0.01)。
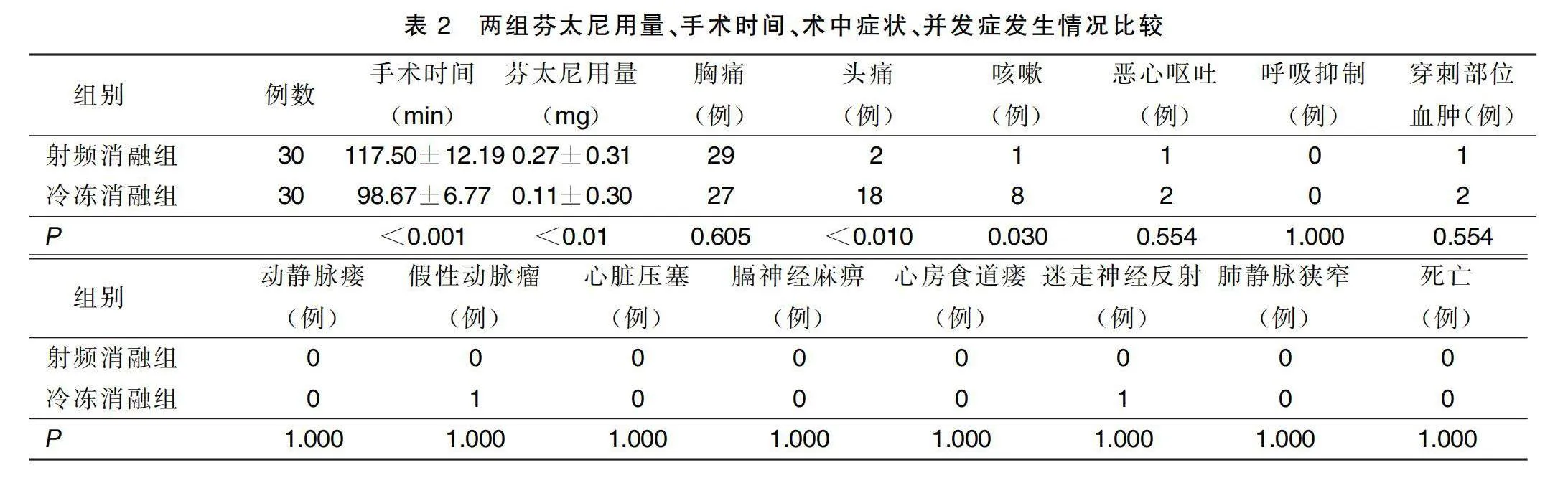
2.3 两组手术时间、并发症发生情况比较
两组病人均成功配合完成心房颤动消融手术,两种手术方式均实现肺静脉电隔离即刻成功。射频消融组平均手术时间长于冷冻消融组,差异有统计学意义(P<0.001);消融术中表现方面,两组病人均有不同程度的胸痛症状,差异无统计学意义(P>0.05),冷冻消融组头痛、咳嗽症状明显多于射频消融组,差异有统计学意义(P<0.05)。并发症方面,两组恶心呕吐、呼吸抑制、穿刺部位血肿、动静脉瘘、假性动脉瘤、膈神经麻痹、心脏压塞、心房食道瘘、迷走神经反射、肺静脉狭窄、死亡发生率比较差异均无统计学意义(P均>0.05)。两组发生穿刺部位血肿的病人经压迫等对症治疗后血肿逐渐自行吸收。冷冻消融组1例假性动脉瘤病人经压迫治疗后好转。
3 讨 论
心房颤动是临床常见的快速性心律失常之一,目前已经证实经导管消融治疗心房颤动可以减少心房颤动的负荷,延长维持窦律的时间,提高病人生活质量,降低脑卒中和死亡的发生率。肺静脉隔离是心房颤动导管消融治疗的基石[1-2]。心房颤动导管消融根据能源不同,目前主流的能量选择主要分为射频消融和冷冻消融,射频消融是利用射频能量在左心房肺静脉前庭部位进行一圈逐点的消融,从而实现肺静脉与左心房的电隔离。冷冻消融是通过冷冻球囊封堵肺静脉口,利用冷冻的方式使球囊贴靠的肺静脉前庭部位造成连续的带状损伤,从而达到肺静脉隔离[2]。经导管消融时病人需要保持身体平卧于手术台上,无论是射频消融还是冷冻消融均为心房部位的侵入性手术,因左心房分布大量的迷走神经,尤其以4个肺静脉口部及左房后壁分布最多,因此,两种消融方式均可产生疼痛感[6],疼痛可能导致消融术中病人身体位置发生移动,导致心房解剖结构的位置产生变化,从而影响到消融导管或球囊与消融灶之间的接触面积和作用时间,降低消融治疗的质量,延长消融时间和透视时间;病人身体位置移动也可能导致导管移位,增加并发症发生的可能性;另外术中疼痛也会显著增加病人的焦虑及不适感,增加相同部位的消融次数,影响单次消融的效果,从而影响消融的成功率[5]。因此,在心房颤动导管消融术中使用适当的镇静和镇痛药物十分必要,可以提高消融的成功率,降低消融相关并发症的发生风险。目前欧美国家多数中心主要在全身麻醉下完成心房颤动消融手术;在日本,大多数病人在清醒镇静麻醉或深度镇静麻醉下进行心房颤动导管消融,仅有0.5%的病人进行全身麻醉[5,7];在我国,由于手术量大以及麻醉科医师的短缺,全身麻醉未广泛应用[8]。既往有文献报道,心房颤动消融术前及术中如果出现过度镇静镇痛,可引起低氧血症、高碳酸血症、气道阻塞、严重肺动脉高压、冠状动脉痉挛等并发症以及增加左房食道瘘等严重并发症的风险[9-11]。目前国内较多中心在心房颤动消融术中采用清醒镇痛状态下行导管消融治疗,多采用芬太尼等阿片类镇痛药物。芬太尼为阿片受体激动剂,其镇痛效价为吗啡的100~180倍,哌替定的500~1 000倍,同时有拮抗药纳洛酮,但是芬太尼镇痛治疗有恶心呕吐、低血压、呼吸抑制等常见不良反应[12-13]。本研究主要比较心房颤动导管消融两种消融方式术中芬太尼的用量,因本研究样本量相对较少,未观察到芬太尼相关不良反应。本研究发现,冷冻消融组与射频消融组相比使用更小的枸橼酸芬太尼剂量,差异有统计学意义(P<0.01)。分析冷冻消融组芬太尼使用量少主要与以下几方面有关:首先,冷冻消融组消融时间更短,既往多个临床研究均发现,冷冻消融组手术总时间、左房内操作时间明显短于射频消融组[14],本研究结果显示,两组消融时间比较差异有明显统计学意义(P<0.001),冷冻消融组手术时间明显短于射频消融组。目前国内多数中心术中使用微量泵泵入芬太尼注射液镇静镇痛治疗,从这一方面看,手术时间越短,术中使用芬太尼等镇静镇痛药物的总剂量越少。其次,既往研究表明,病人对冷冻消融产生的疼痛有着更强的耐受性[15],两种消融方式比较发现冷冻消融的疼痛程度较射频消融更轻,推测这与两种消融方式的原理不同相关,射频消融是利用射频能量主要进行逐点的消融,通过点与点的连接形成线,从而实现肺静脉与左心房的电隔离,在每一点的消融过程中均可能有较强的疼痛感,尤其是在消融左房后壁迷走神经分布更多的区域时产生疼痛更加明显;冷冻消融是通过冷冻球囊封堵肺静脉口使得球囊贴靠的肺静脉前庭部位1次冷冻即可造成单根肺静脉连续的环形带状损伤,目前指南推荐,封堵良好的情况下,单根肺静脉隔离冷冻时间一般为180 s左右[3],冷冻消融过程中肺静脉前庭接触冷冻球囊的部位温度在较短时间内迅速下降,因此,冷冻消融产生疼痛的性质及时间与射频消融不同,病人对冷冻消融产生的疼痛具有更强的耐受性。本研究也发现冷冻消融组头痛、咳嗽的发生率高于射频消融组(P<0.05)。两种消融方式对病人因疼痛产生位置移动的要求可能不同,因为射频消融需要依靠使用三维标测系统建立左心房模型,消融导管在已经建立好的心房模型中进行操作,如果病人在术中因疼痛造成较大位置移动则会导致心房模型的失真,从而影响射频消融的有效性及安全性,因此,射频消融对术中疼痛的管理要求较高;而冷冻消融是在X线指导下实时观察冷冻球囊在心房中的位置,可以根据情况X线透视下随时调整导管的位置,病人因疼痛产生的位置移动对冷冻消融的效果及安全影响不大。本研究也有一定局限性,本研究为回顾性研究,病例入选方面可能存在偏倚,研究样本量相对较少,可能需要更多的样本量进一步总结规律。
综上所述,阵发性心房颤动病人无论使用射频消融方式还是冷冻消融的方式,术中均实现了肺静脉完全隔离,达到了手术治疗目的;心房颤动冷冻消融组比射频消融组使用的镇静镇痛药物更少;冷冻消融组病人头痛、咳嗽的发生率要高于射频消融组;而在并发症方面两组差异无统计学意义(P>0.05)。提示心房颤动冷冻消融术与射频消融术相比病人在术中具有更好的疼痛耐受性,心房颤动冷冻消融术可能需要更少的镇静镇痛药物,而镇静镇痛药物使用量的减少不会影响心房颤动冷冻消融术的有效性及安全性,可以避免大量镇静镇痛药物带来的不良反应。
参考文献:
[1] KOTALCZYK A,LIP G Y,CALKINS H.The 2020 ESC guidelines on the diagnosis and management of atrial fibrillation[J].Arrhythmia & Electrophysiology Review,2021,10(2):65-67.
[2] 中华医学会心电生理和起搏分会,中国医师协会心律学专业委员会,中国房颤中心联盟心房颤动防治专家工作委员会,等.心房颤动:目前的认识和治疗建议(2021)[J].中华心律失常学杂志,2022,26(1):15-88.
[3] 中华医学会心电生理和起搏分会中国医师协会心律学专业委员会.经冷冻球囊导管消融心房颤动中国专家共识[J].中国心脏起搏与心电生理杂志,2020,34(2):95-108.
[4] MORAVEC O,SKALA T,KLEMENTOVA O,et al.General anesthesia or conscious sedation in paroxysmal atrial fibrillation catheter ablation[J].Biomedical Papers of the Medical Faculty of the University Palacky,Olomouc,Czechoslovakia,2021,165(2):162-168.
[5] YAMAGUCHI T,SHIMAKAWA Y,MITSUMIZO S,et al.Feasibility of total intravenous anesthesia by cardiologists with the support of anesthesiologists during catheter ablation of atrial fibrillation[J].Journal of Cardiology,2018,72(1):19-25.
[6] CHEVALIER P,TABIB A,MEYRONNET D,et al.Quantitative study of nerves of the human left atrium[J].Heart Rhythm,2005,2(5):518-522.
[7] INOUE K,MURAKAWA Y,NOGAMI A,et al.Current status of catheter ablation for atrial fibrillation--updated summary of the Japanese Catheter Ablation Registry of Atrial Fibrillation(J-CARAF)[J].Circulation Journal,2014,78(5):1112-1120.
[8] TANG R B,DONG J Z,ZHAO W D,et al.Unconscious sedation/analgesia with propofol versus conscious sedation with fentanyl/midazolam for catheter ablation of atrial fibrillation:a prospective,randomized study[J].Chinese Medical Journal,2007,120(22):2036-2038.
[9] FURUI K,MORISHIMA I,KANZAKI Y,et al.Coronary vasospasm caused by intravenous infusion of dexmedetomidine:unrecognized pitfall of catheter ablation procedures of atrial fibrillation[J].Journal of Cardiology Cases,2019,20(6):221-224.
[10] HAMID A.Anesthesia for cardiac catheterization procedures[J]. Heart,Lung and Vessels,2014,6(4):225-231.
[11] DI BIASE L,SAENZ L C,BURKHARDT D J,et al.Esophageal capsule endoscopy after radiofrequency catheter ablation for atrial fibrillation: documented higher risk of luminal esophageal damage with general anesthesia as compared with conscious sedation[J].Circulation Arrhythmia and Electrophysiology,2009,2(2):108-112.
[12] 陈华艳,梁桦,龙宏杰,等.右美托咪啶与咪达唑仑联合芬太尼在房颤射频消融术中的镇静镇痛效果比较研究[J].临床合理用药杂志,2018,11(30):96-97.
[13] MANDEL J E,HUTCHINSON M D,MARCHLINSKI F E. Remifentanil-midazolam sedation provides hemodynamic stability and comfort during epicardial ablation of ventricular tachycardia[J].Journal of Cardiovascular Electrophysiology,2011,22(4):464-466.
[14] REISSMANN B,METZNER A,KUCK K H.Cryoballoon ablation versus radiofrequency ablation for atrial fibrillation[J]. Trends in Cardiovascular Medicine,2017,27(4):271-277.
[15] DEFAYE P,KANE A,JACON P,et al.Cryoballoon for pulmonary vein isolation:is it better tolerated than radiofrequency?Retrospective study comparing the use of analgesia and sedation in both ablation techniques[J].Archives of Cardiovascular Diseases,2010,103(6/7):388-393.
(收稿日期:2023-06-15)
(本文编辑 王丽)

