9例卵泡膜纤维瘤超声误诊探讨
施玉霞
福建中医药大学附属第二人民医院东二环院区超声科,福建 福州 350001
卵泡膜纤维瘤是一种良性肿瘤,发病率较低,约占卵巢肿瘤的0.5%~2.0%。该病好发于绝经期及绝经后妇女,主要来源于卵巢性索间质细胞,由间胚组织向卵泡膜细胞分化并合并纤维细胞,两种成分同时出现于同一肿瘤且互相移行,卵泡膜和成纤维分化的瘤细胞均具有内分泌功能,超声声像表现不一[1-2],易误诊为恶性肿瘤或子宫浆膜下肌瘤,因此探究卵泡膜纤维瘤的超声诊断方法显得十分必要。基于此,本研究回顾性分析2014 年1 月1 日—2022 年10 月30 日福建中医药大学附属第二人民医院误诊的9 例卵巢膜纤维瘤患者的超声声像特征,旨在提高诊断准确率,现将结果报告如下。
1 资料与方法
1.1 临床资料
收集福建中医药大学附属第二人民医院2014 年1 月1日—2022 年10 月30 日经手术病理证实为卵泡膜纤维瘤患者的临床资料,筛选出经超声检查误诊为其他肿物的患者9 例。所有患者年龄26~64 岁,平均年龄(55.11±15.66)岁;育龄期患者1 例,绝经后患者8 例;临床表现为阴道不规则出血2 例,腹部胀痛5 例,无明显症状体检发现附件区肿物2 例,CA125 升高3 例(参考值35 U/mL),均为单侧发病,合并腹水1例。
1.2 仪器与方法
使用PHILIPS EPIQ7、GE LOGIQ E9 等彩色多普勒超声诊断仪,经腹探头频率3.5~5.0 MHz,阴道超声探头6~8 MHz。患者采取平卧位,适度充盈膀胱,经腹部超声检查子宫双附件区,臀部铺妇检垫,采取膀胱截石位,探头套上探头套,经阴道超声检查,观察包块部位、大小、边界、形状、内部回声、血流Adler 分级[3]及血流阻力指数(RI)等,根据椭圆体积公式(V=4/3πabc)计算混合回声包块及包块内囊性部分体积,计算实性部分占比,并观察有无合并腹水等其他征象。
2 结果
2.1 病理及超声检查结果
9 例卵泡膜纤维瘤病理呈灰白色肿物,包膜完整,切面灰白色,质韧编织状或旋涡状,见高密度的梭形细胞,其中6例内见局部梗死,囊性变(66.7%),见图1。3例超声误诊为子宫浆膜下肌瘤(33.3%);6 例超声误诊为卵巢癌(66.7%)。
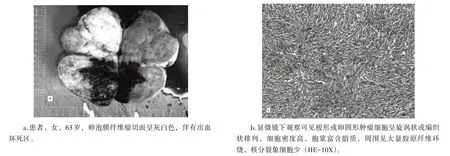
图1 病理及超声图像
2.2 超声声像图特征
病变以单发为主(100%)。其大小不一,最小约1.6 cm×0.6 cm,最 大 约17.0 cm×10.0 cm,平 均 大 小(7.76±4.89)cm×(6.32±3.30)cm。边界清晰,形态呈类圆形、类椭圆形,较大者呈分叶状。内部呈囊实性混合回声包块6 例(66.7%),实性占比在80%~97%之间;内部全部呈实性包块3 例(33.3%),其中1 例回声均匀(11.1%),1 例回声不均匀(11.1%);9 例中4 例后方出现回声稍增强(44.4%),1 例出现后方回声衰减(11.1%)。RI 为0.40~0.59,平均RI(0.46±0.06)。Adler 血流分级Ⅰ级6 例(66.7%)、Ⅱ级2 例(22.2%)、Ⅲ级1 例(11.1%),伴腹水1例(11.1%)。见表1、图2。
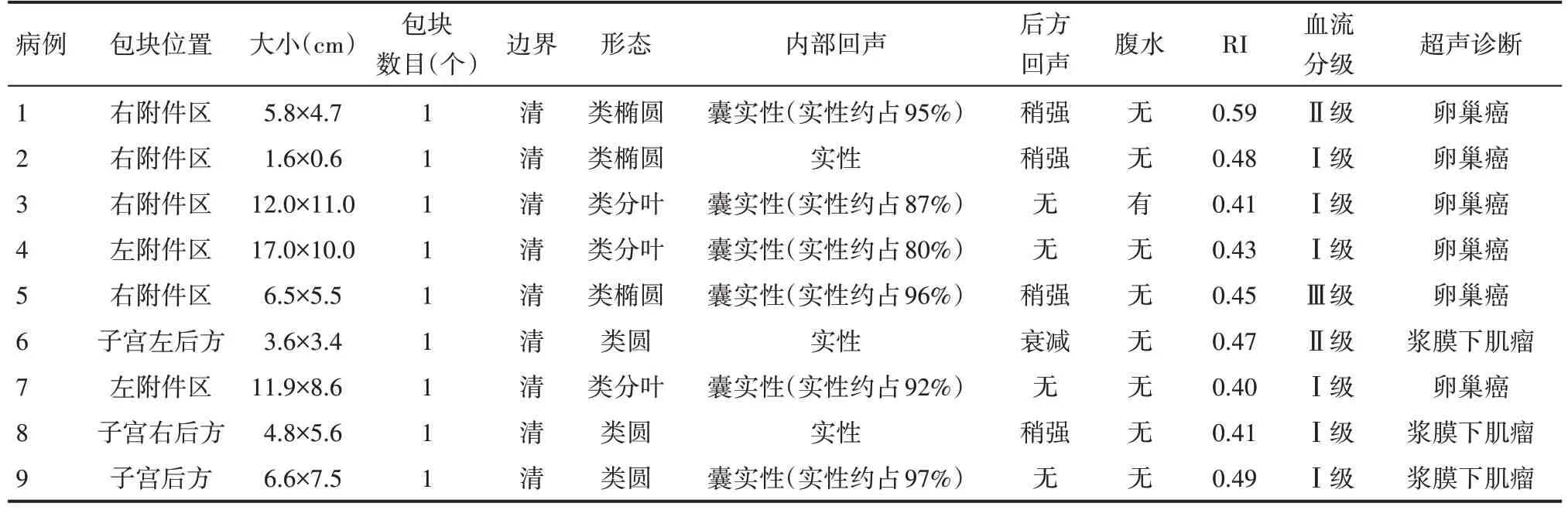
表1 9例卵泡膜纤维瘤声像图表现
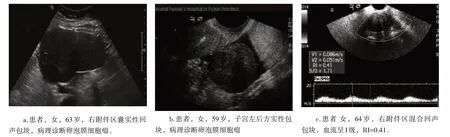
图2 不同患者超声征象情况
3 讨论
卵泡膜纤维瘤临床上多见于绝经期及更年期中老年女性,青春期女性罕见,发病率低,占卵巢良性肿瘤的2%[2]。本研究中,患者平均年龄(55.11±15.66)岁,仅有1例26岁患者,均为单侧发病。该肿瘤起源于卵巢性索间质的特殊间胚叶组织,肿瘤内含有纤维母细胞及黄体变性的卵泡膜细胞,因两者成分所占比不同及纤维结构含量不同而分为卵泡膜细胞瘤、卵泡膜纤维瘤、纤维瘤,肿瘤好发于单侧卵巢,双侧少见。绝大部分为良性,预后较好,恶变率约1%~5%[4]。临床表现与肿瘤大小及其分泌雌激素的多少有关,部分患者可无症状,往往经体检偶然发现[5]。当肿瘤细胞分泌雌激素较多时,患者可出现阴道不规则流血、月经紊乱等内分泌症状,部分患者还可伴有子宫内膜增生、子宫内膜癌及子宫肌瘤等雌激素相关性疾病,本研究中有2 例患者出现阴道不规则出血。当肿瘤较大邻近器官收到压迫时,患者可出现腹痛、腹胀等症状,妇检时可触及附件区包块,上述临床表现与本组病例基本相同。有报道[6]显示,约1%的患者可出现不明原因的腹水、胸水或胸腹水,即Meigs 综合征,手术切除肿瘤后胸腹水可自行消失。不少患者还合并血清CA125增高,可能与肿瘤持续刺激导致腹膜间皮细胞分泌增多有关[2],本研究中3 例患者呈CA125 阳性,1 例伴有腹水。肉眼观察病理,可见大部分呈类圆形、类椭圆或分叶状,包膜完整,切面呈灰白色或灰褐色,质韧或中等硬,体积较大时可发生梗死、囊性变。镜下观察可见梭形或卵圆形肿瘤细胞呈旋涡状或编织状排列,细胞密度高、胞浆富含脂质,周围见大量胶原纤维环绕,核分裂象细胞少。
病理特点决定超声表现特征。典型的卵泡膜纤维瘤超声特征以附件区类圆形、椭圆形或类分叶状肿物,边界清、包膜完整的实性低回声包块为主;肥胖短梭形的卵泡膜细胞呈旋涡状、编织状排列,细胞内胞浆因富含脂质而呈空泡状,纤维结蹄组织将细胞束分隔。当肿瘤内以卵泡膜细胞成分为主时,肿瘤切面以偏黄色多见,超声表现为实性低回声,可伴有后方回声稍增强。肿瘤内纤维组织主要由成纤维细胞束和交叉排列的胶原纤维组织带构成,梭形瘤细胞呈编织状排列,内含大量胶原纤维。因此以纤维组织为主时,肿瘤切面以灰白色多见,超声表现为实性低回声肿块,后方可伴有不同程度声衰减,而且含纤维成分多肿瘤质地较坚韧。卵巢门及周围淋巴管和血管在肿瘤较大时因受到压迫致回流受阻,腹膜间皮细胞因腹膜受到刺激而分泌增多产生腹水,合并腹水者手术后腹水可消失[7]。当肿瘤内血供较差发生机化时可出现钙化,声像图上可见不规则强回声的钙化灶。体积较大肿瘤出现梗死囊性变时,超声声像图以囊实性混合回声为特征。本研究结果显示,彩色多普勒血流可见包块内部及周边点条状血流,血流分级以Ⅰ级、Ⅱ级为主,也可见血流较丰富者;以0.4<RI<0.5 为主,血流情况显示除了与肿瘤自身血供情况有关外,还与仪器血流敏感度及操作者手法有关。
卵泡膜纤维瘤易误诊为浆膜下或阔韧带肌瘤,本研究3 例患者误诊为浆膜下子宫肌瘤,占33.3%,因此对浆膜下临床及超声诊断要点的掌握至关重要。(1)浆膜下子宫肌瘤与卵泡膜纤维瘤的临床鉴别点:①发病年龄,前者多在30~50 岁,而后者好发于绝经后;②发病部位,前者为子宫壁,部分或全部凸向浆膜外,后者为卵巢内性索间质;③病理组成,前者内为平滑肌纤维相互交叉形成旋涡状,内可含有不等量纤维结蹄组织,而后者内可见被纤维结缔组织分割的卵泡膜细胞束及梭状细胞;④血供来源,前者由子宫壁动脉供血,环绕瘤体并向内延伸,而后者来源于卵巢内,与子宫壁动脉无联系;⑤RI,前者为0.5 左右,后者约为0.4~0.5。(2)浆膜下子宫肌瘤与卵泡膜纤维瘤相同点如下:①前者完全外突时其部位与后者相似;②两个边界均清晰,内为实性团块,当前者发生囊性变或玻璃样变时,瘤内见大小不等不规则无回声区,而后者内出现出血坏死,瘤内也可见界清晰的液性区;③两者发生钙化时瘤体内均可出现强回声斑。(3)超声鉴别诊断要点:①子宫浆膜下肌瘤为子宫壁局部凸起或与子宫壁紧贴的肿块,其包膜与子宫浆膜层连续,按压时与子宫壁呈同向运动,彩色多普勒可显示来自子宫壁的供血血管,而卵泡膜纤维瘤肿块在按压时可与子宫壁分离,呈反向运动趋势,与子宫浆膜层无连续,彩色多普勒显示与子宫壁无血流相通,瘤体内部可显示散在分布的较微弱的血流信号;②子宫浆膜下肌瘤时双侧卵巢存在,而卵泡膜纤维瘤肿块同侧卵巢不显示。此外,阔韧带肌瘤同侧卵巢存在是与卵泡膜纤维瘤鉴别要点。
当肿瘤出血坏死呈现混合回声包块时易误诊为卵巢恶性肿瘤,本研究中6 例患者被误诊为卵巢癌,占66.7%,因此找到两者的鉴别点对临床诊疗方案选择具有价值。(1)卵巢恶性肿瘤与卵泡膜纤维瘤的临床鉴别点如下:①发病年龄,前者常见于儿童及青年妇女,后者绝经后多见;②临床表现,前者病程短、进展快、食欲下降,易较快出现消瘦、贫血等恶病质貌,主要表现为下腹胀、腹痛、月经不调或绝经后阴道出血等,后者病程长、进展缓慢,一般情况良好,偶因体检发现,当卵泡膜纤维瘤增大到中等大小时也可表现为下腹部胀痛,因卵泡膜细胞有分泌雌激素功能,部分患者可有内分泌紊乱或绝经后阴道不规则出血表现;③伴随症状,前者多伴有腹水,而少部分卵泡膜纤维患者伴有麦格综合征时可有胸、腹水;④腹水消失速度,前者一般在手术或放化疗后3~4 个月腹水减少消退,而后者术后胸腹水迅速消失,且CA125 下降。(2)卵巢恶性肿瘤与卵泡膜纤维瘤共同点:均发生与卵巢,均可伴有CA125增高。(3)卵巢恶性肿瘤与卵泡膜纤维瘤超声鉴别点如下[8]:①卵巢恶性肿瘤超声表现多样,主要表现为实体瘤,形态欠规则,未见完整包膜,常累及周边组织与周边组织分界不清,在实性肿块可见不规则液性区,伴随着盆腹腔积液,而后者呈圆形、类圆形或分叶状,包膜完整,肿瘤内出血坏死时,内见少许边界较清的液性暗区;②卵巢恶性肿瘤血流多为内部及周边存在不规则点状、条状血流,较丰富,呈枯树枝样分布,RI≤0.4,而卵泡膜纤维瘤血流不丰富,0.4<RI<0.5;③卵巢恶性肿瘤腹腔内常伴有游离积液,腹膜可见不规则增厚及其他脏器转移声像,而卵泡膜纤维瘤较少伴有腹腔游离积液,腹膜光滑,其他脏器无转移灶。
此外,还应与盆腔其他肿块,如畸胎瘤、小肠间质瘤及骶尾部神经纤维瘤等混合回声或实性回声为主的肿块,相区别,畸胎瘤一般以囊实性为主,好发于年轻女性,大部分可表现为脂液分层、面团征或瀑布征等,声像较容易鉴别,而小肠间质瘤及骶尾部神经纤维瘤以实性肿块为主,但是双侧卵巢声像无异常可以鉴别[9-11]。
综上所述,卵泡膜纤维瘤声像图以实性及以实性为主的囊实包块为主,有一定特点,但缺乏特异性,易误诊,其发病部位、内部回声、边界等特征有助于超声诊断与鉴别,为临床诊治提供更为客观的超声影像学依据。

