新交泰饮对2型糖尿病大鼠糖脂代谢的影响
罗 兰 张 镖 曹颖男 钟志勇 张素中*
糖尿病是一种由胰岛素分泌不足或外周组织对胰岛素不敏感而引起的以慢性高血糖为主要特征,蛋白质、脂肪和电解质等紊乱的终身性代谢性疾病。近年来,糖尿病的发病率显著上升,已成为危害人类健康的“第三大杀手”,严重影响着患者的生命质量[1]。因此对糖尿病的防治是医药学领域的重要研究课题之一。交泰丸是一首治疗心肾不交的著名中药方剂,组方源自《韩氏医通》,全方由黄连、肉桂(10∶1)两味中药组成。因其寒热并用,疗效突出,成为临床常用的方剂之一,在治疗失眠、抑郁和降低血糖、血脂方面取得了良好的效果[2-4]。但近年来有研究表明,黄连在临床应用中有较高的不良事件发生率与不良反应发生率[5-6]。可见,久服黄连降糖极有可能会对治疗效果产生不可忽视的影响。苦瓜在性味、归经及成分类别方面与黄连相似,有研究显示从苦瓜中分离出的苦瓜多肽-P(又称植物胰岛素),有显著的降糖降脂作用[7-8]。此外,苦瓜属于药食同源的中药,安全性方面比黄连高。本研究基于交泰丸的组方原则及其较好的临床疗效,采用苦瓜与肉桂配伍制备新交泰饮,探讨其对2型糖尿病大鼠的降糖降脂作用,也为糖尿病高血脂患者的日常饮食提供参考。
1 材料与方法
1.1 材料
1.1.1实验动物SPF级SD大鼠48只,体重120~150 g,雄性,由珠海百试通生物科技有限公司提供,许可证号:SCXK(粤)2020-0051,合格证号:44822700000115。饲养温度维持在20~26 ℃,相对湿度:40%~70%,采用12 h∶12 h昼夜间断照明。实验过程中动物处置均符合动物伦理标准(审批号:IAC202103030)。
1.1.2药品新交泰饮组成药物苦瓜(产地广东,批号:2009001)、肉桂(产地广西,批号:2010001)均购于岭南中药饮片有限公司;盐酸二甲双胍片(中美上海施贵宝制药有限公司,国药准字H20023370,批号:AA88543,规格:0.5 g/片);高脂高糖饲料(70.0%普通饲料+15.0%蔗糖+15.0%猪油)和普通饲料均由江苏美迪森生物医药有限公司提供。
1.1.3试剂链脲佐菌素(streptozotocin, STZ)(批号:X17O10L100226)由上海源叶生物科技有限公司提供;强生稳捷型血糖试纸(批号:3788423)由美国强生医疗器械有限公司提供;总胆固醇(total cholesterol, TC)测试盒(批号:20201011)、三酰甘油(triglyceride, TG)测试盒(批号:20201007)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)测试盒(批号:20201021)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol, HDL-C)测试盒(批号:20201021)、天冬氨酸转氨酶(aspartate aminotransferase, AST)测试盒(批号:20201015)、丙氨酸转氨酶(alanine aminotransferase, ALT)测试盒(批号:20201027),由南京建成生物工程研究所提供;大鼠肿瘤坏死因子-α(tumor necrosis factoralpha, TNF-α)检测试剂盒(批号:20201103)、白细胞介素6(interleukin 6, IL6)检测试剂盒(批号:20210122)和α-葡萄糖苷酶(a-glucosidase, α-GC)检测试剂盒(批号:20201228)由北京百奥莱博科技有限公司提供;胰岛素放射免疫分析试剂盒(批号:111220)由北京北方生物技术研究所提供;葡萄糖(分析纯)、柠檬酸(分析纯)等试剂由广州化学试剂厂提供。
1.1.4主要仪器分析天平(ME104E,瑞士梅特勒-托利多国际有限公司);血糖测量仪(OneTouch UltraEasy,美国强生医疗器械有限公司);全波长酶标仪(SpectraMax iD3,美国Molecular Devices公司);高速离心机(Sigma 3-30k,德国Sigma有限公司);恒温培养箱(CO2,上海幕斯实验设备有限公司)。
1.2 方法
1.2.1新交泰饮的制备按组方比例取苦瓜500 g,肉桂50 g,置于圆底烧瓶,加10倍量体积水浸泡30 min后,水煎煮约1 h,过滤,滤渣加8倍量体积水煎煮约0.5 h,过滤,合并2次滤液,煎煮过程中采用挥发油提取器提取挥发油。用旋转蒸发仪减压浓缩滤液,将挥发油加入所得浓缩液中,在70 ℃水浴中搅拌均匀,使得药液最终浓度约为1.4 g/ml,4 ℃冰箱储存备用。
1.2.2糖尿病大鼠的造模检疫结束后,所有大鼠普通饲料适应性喂养7 d后,随机分为正常组8只,继续给予普通饲料喂养;其他大鼠为造模组,给予高脂高糖饲料喂养2个月,造成肥胖模型。禁食12 h后,造模组一次性腹腔注射50 mg/kg STZ,注射后第5 天尾部采血,测定造模组大鼠在空腹状态下(禁食不禁水12 h)的血糖值,筛选血糖值>11.0 mmol/L者为糖尿病模型大鼠。
1.2.3分组与给药将造模成功的大鼠随机分为模型组、二甲双胍组、新交泰饮组(低、中、高剂量组),每组8只。具体分组及给药如下:正常组和模型组给予0.9%氯化钠注射液灌胃;二甲双胍组予以100 mg/(kg·d)二甲双胍溶液灌胃,该剂量以大鼠6倍于成人剂量(以60 kg成人1 g/d量)换算;新交泰饮低、中、高剂量组以5.94 g/(kg·d)、11.88 g/(kg·d)、17.82 g/(kg·d)灌服新交泰饮,分别相当于成人等效剂量的4倍、8倍和12倍(以60 kg成人计算)。各给药组每日定时以15 ml/kg剂量灌胃治疗,连续用药4周。实验期间每天观察大鼠体毛色泽、精神状态、行为状态、饮食饮水量、大便及尿量等指标,于每周末测量体重1次。
1.2.4 检测指标
1.2.4.1空腹血糖(fasting blood glucose,FGB)每周给药后,大鼠禁食不禁水12 h,尾静脉取血,用血糖测量仪检测各组大鼠FGB水平。
1.2.4.2葡萄糖耐量(glucose tolerance,OGTT)末次给药后,各组动物禁食不禁水12 h,灌胃给予2.0 g/kg葡萄糖,于灌胃后0、0.5、2 h尾静脉取血检测血糖值及计算血糖曲线下面积的变化。
血糖曲线下面积=[(0 h血糖+0.5 h血糖)×0.5+(2 h血糖+0.5 h血糖)×1.5]×0.5
1.2.4.3血清胰岛素(serum insulin,INS)、细胞因子及生化指标糖耐量实验结束,各组动物适应性喂养2 d后,禁食不禁水12 h,麻醉后腹主动脉采血,以3 000 r/min速度离心15 min取血清。采用放射免疫法检测INS、TNF-α、IL6,酶联免疫吸附试验法检测TC、TG、HDL-C、LDL-C、ALT、AST和α-GC活性,操作严格按试剂盒说明书进行。
1.3 统计学分析
采用SPSS 21.0统计软件进行数据分析,计量资料以±s表示,多组比较采用单因素方差分析,P<0.05为差异有统计学意义,P<0.01为差异有显著统计学意义。
2 结果
2.1 一般情况与体重
正常组大鼠毛色润泽,精神良好,行为活跃,生活正常;模型组大鼠毛色枯黄,精神状态差,喜扎堆,反应迟钝,饮食饮水量均增多,尿量也增多;各给药组大鼠毛色、精神状况、行为状态与模型组比较无明显差异,饮食饮水量、尿量较模型组有所减少,随着给药时间的延长,大鼠的一般状态有所改善。
造模前,与正常组比较,模型组大鼠体重显著增加(P<0.05);造模后,模型组和各给药组大鼠体重明显降低(P<0.05);给药期间,各给药组大鼠体重与模型组比较差异无统计学意义(P>0.05)。见图1。

图1 各组大鼠体重变化(±s)
2.2 FGB
给药前,模型组大鼠FGB水平高于正常组(P<0.01),各给药组与模型组FGB水平比较,差异无统计学意义(P>0.05);给药4周内,二甲双胍组、新交泰饮组(低、中、高剂量组)FGB水平与模型组比较,差异有统计学意义(P<0.05);给药1周后,新交泰饮中剂量组FGB水平明显低于二甲双胍组(P<0.05);给药2~3周,新交泰饮高剂量组FGB明显低于二甲双胍组(P<0.05);给药4周,二甲双胍组FGB水平低于新交泰饮组(低、中、高剂量组)(P<0.05)。见图2。
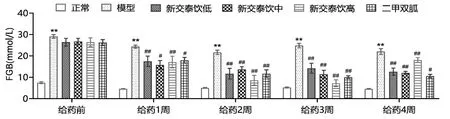
图2 各组大鼠FGB比较(±s)
2.3 OGTT
模型组大鼠各个时间点的血糖值及其血糖曲线下面积较正常组高,差异有统计学意义(P<0.01);二甲双胍组、新交泰饮组(低、中、高剂量组)各个时间点的血糖值及其血糖曲线下面积与模型组比较,差异有统计学意义(P<0.05);比较各时间点的血糖值和血糖曲线下面积发现,各给药组的疗效表现为二甲双胍组>新交泰饮中剂量组>新交泰饮低剂量组>新交泰饮高剂量组。见图3~4。
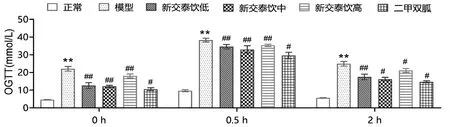
图3 各组大鼠OGTT比较(±s)

图4 各组大鼠血糖曲线下面积比较(±s)
2.4 IL6、TNF-α、INS和α-GC
模型组大鼠血清INS水平较正常组低,差异有统计学意义(P<0.01);二甲双胍组、新交泰饮组(低、中、高剂量组)大鼠血清INS水平高于模型组,差异有统计学意义(P<0.01);在增加胰岛素分泌方面,各给药组的疗效表现为:新交泰饮中剂量组>二甲双胍组>新交泰饮高剂量组>新交泰饮低剂量组;各组大鼠血清IL6、TNF-α和α-GC水平与正常组比较,差异无统计学意义(P>0.05)。见图5。

图5 各组大鼠血清IL6、TNF-α、INS和α-GC比较(±s)
2.5 对肝功能的影响
模型组大鼠血清ALT、AST水平较正常组升高,差异有统计学意义(P<0.05);各给药组ALT与AST水平与模型组比较,差异无统计学意义(P>0.05)。见图6。
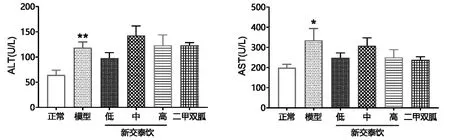
图6 各组大鼠血清ALT和AST水平比较(±s)
2.6 对血脂的影响
模型组TG、TC和LDL-C水平较正常组升高,差异有统计学意义(P<0.05);二甲双胍组、新交泰饮组(低、中、高剂量组)TG、TC和LDL-C水平与模型组比较,差异有统计学意义(P<0.05);各组HDL-C水平比较,差异无统计学意义(P>0.05)。在降低TG、TC水平方面,各给药组的疗效表现为:新交泰饮组中剂量组>新交泰饮低剂量组>二甲双胍组>新交泰饮高剂量组;在降低LDL-C水平方面,二甲双胍组>新交泰饮组中剂量组>新交泰饮低剂量组>新交泰饮高剂量组。见图7。

图7 各组大鼠血清TG、TC、HDL-C、LDL-C水平比较(±s)
3 讨论
糖尿病隶属于中医消渴范畴。中医认为,消渴病的基本病机是阴津亏损,燥热偏盛,而以阴虚为本,燥热为标。经典名方—交泰丸方中黄连苦寒,能泻心火;肉桂辛热,能补火助阳,同时又有引火归源之功[9]。两药相伍,一寒一热一清一补,使心肾相交、水火相济,正好符合糖尿病患者多久病及肾、阴损及阳、虚实夹杂、寒热交错的证候特点[10-11]。但黄连的大苦大寒之性使得其在糖尿病中广泛运用受到限制,长时间或大剂量服用会损伤脾胃,造成脾胃虚寒而出现一系列证候;此外,黄连为多基源品种,不同基源的黄连生物碱含量差异较大[12],极有可能会对治疗作用产生不可忽视的影响。苦瓜是我国传统的药用植物。《本草纲目》记载:苦瓜“苦、寒、无毒”,具有“清邪热、解劳乏”之功。现代医学研究表明,苦瓜中含有的甾体皂苷类、生物碱类和多肽类化学成分,均具有明显的降糖降脂作用[11]。肉桂为岭南道地药材,是临床常用的温里药,同时也是辛香食用调料的来源之一,其复方和单味药在预防和改善2型糖尿病及其并发症方面也具有一定的应用价值[12-13]。基于交泰丸寒热并用,配伍精当,比例悬殊及较好疗效的特点,选用药食同源的苦瓜和肉桂以10∶1配伍制备新交泰饮,并探讨其治疗2型糖尿病大鼠的降糖降脂作用机制,以期为开发降糖降脂保健食品提供理论依据。
二甲双胍能够提高患者机体对胰岛素的敏感性,缓解胰岛素抵抗症状,同时还能提高患者的血糖耐受程度,是治疗2型糖尿病的一线药物。本课题根据盐酸二甲双胍片的成人给药剂量1 g/d,以成人60 kg和大鼠千克体重剂量折算系数Kw=6.2计,大鼠的二甲双胍给药剂量约为100 mg/(kg·d)。有文献[14]报道,2型糖尿病大鼠服用人等效剂量的交泰丸药液时,降糖作用不明显,在服用人等效剂量4倍时有明显降糖作用,考虑到苦瓜的药性较黄连缓,因此本实验设计的最低给药剂量为人等效剂量的4倍。传统中医认为,复方中单味药物剂量的应用至关重要,其可能改变方剂的君臣佐使关系,从而影响方剂的治疗方向。因此,新交泰饮组方的不同配比与治疗效果的关系尚需进一步研究。本实验结果显示,新交泰饮组中剂量组在降低FGB和OGTT水平方面较二甲双胍组弱,但在增加胰岛素分泌和调控脂代谢方面较二甲双胍组强。
综上所述,新交泰饮可以降低2型糖尿病大鼠的血糖水平,其调控作用可能与维护糖耐量、促进胰岛素分泌和改善血脂代谢有关。对于交泰饮的具体作用机制及作用靶点还有待进一步探讨。

