百香果(Passiflora edulis)R2R3-MYB基因家族的结构和功能分析
张丹 郑平 邓彪 柴改凤 安昌 邓考 张文斌 陆宇明 卢翔宇 王小媚 秦源

收稿日期:2023-06-16 接受日期:2023-08-09
基金项目:广西自然科学基金面上项目(2022GXNSFAA035535);广西农业科学院基本科研业务专项(桂农科2021YT046);中国博士后科学基金(2022MD713731);平潭科技研究院科技创新项目(PT2021007,PT2021003)
作者简介:张丹,女,硕士,研究方向为植物遗传育种与生殖发育。E-mail:danzhang202110@163.com
*通信作者 Author for correspondence. E-mail:yuanqin@fafu.edu.cn;E-mail:wangxiaomei159@163.com
DOI:10.13925/j.cnki.gsxb.20230232
摘 要:【目的】探究R2R3-MYB转录因子在代谢、发育等多种生物学过程中发挥的调控作用。对百香果R2R3-MYB基因家族进行表达分析并探究其在花果发育过程中的调控机制,对深入研究R2R3-MYB转录因子在百香果中的生物学作用中具有重要意义。【方法】基于百香果全基因组数据,通过HMM搜索对R2R3-MYB家族成员进行筛选鉴定,并利用实时荧光定量PCR分析其在百香果花不同组织中的表达模式。【结果】从百香果基因组中鉴定出99个R2R3-MYB基因,根据系统进化分析将其分为36个亚组。99个R2R3-PeMYB基因随机分布在9条百香果染色体上。基序和基因结构分析表明,R2R3-PeMYB在同一亚组中具有相对保守的结构特征。共线性分析表明,片段复制事件促进了百香果R2R3-MYB家族的扩张。基于转录组数据和qRT-PCR分析,发现R2R3-PeMYB基因在百香果花的不同组织的不同发育阶段中表现出差异的表达模式,说明R2R3-PeMYB基因在花不同组织和果实的发育过程中发挥重要作用,尤其是PeMYB62和PeMYB63在百香果果皮转色期的高表达,说明其可能参与百香果花青素的合成。同时8个R2R3-PeMYB基因在非生物胁迫(冷、热、盐和渗透压)下也表现出不同的反应,说明R2R3-PeMYB基因还受到非生物胁迫的诱导。【结论】鉴定了99个R2R3-PeMYB基因家族成员,发现其在百香果花果发育和胁迫诱导方面发挥重要作用,为今后研究百香果R2R3-MYB基因在花果发育中的功能和进化提供了有价值的线索。
关键词:百香果;R2R3-MYB转录因子;系统发育分析;花果发育
中图分类号:S667.9 文献标志码:A 文章编号:1009-9980(2024)01-0012-18
Structure and function analysis of R2R3-MYB gene family from passion fruit (Passiflora edulis)
ZHANG Dan1, 2, ZHENG Ping1, 3, DENG Biao2, CHAI Gaifeng1, AN Chang 1, DENG Kao1, ZHANG Wenbin4, LU Yuming2, LU Xiangyu2, WANG Xiaomei1, 2*, QIN Yuan1, 3*
(1College of Life Sciences, Fujian Agriculture and Forestry University, Fuzhou 350002, Fujian, China; 2Horticultural Research Institute, Guangxi Academy of Agricultural Sciences, Nanning 530007, Guangxi, China; 3Haixia Institute of Science and Technology, Fujian Agriculture and Forestry University, Fuzhou 350000, Fujian, China; 4Fine Variety Breeding Farm in Xinluo District, Longyan 364000, Fujian, China)
Abstract: 【Objective】 The R2R3-MYB transcription factors (TFs) are widely involved in the regulation of various biological processes in plants, including primary and secondary metabolism, growth and development, and response to environmental factors and plant hormones. In this study, the expression of R2R3-MYB gene family in passion fruit was systematically analyzed and its regulatory mechanism during flower and fruit development was explored. 【Methods】 In this study, the hidden Markov Model profile (HMM) of the MYB binding domain (PF00249) was obtained from the Pfam database, which was used as the seed model for the HMMER search of candidate PeMYB genes from the passion fruit genome in TBtools. The redundant sequences were removed manually. The SMART and the NCBI-CDD database were used to cross-check the presence of the MYB domain in candidate sequences. The physicochemical features of the potential MYB protein sequences, including molecular weight, theoretical isoelectric point (pI), and the number of amino acids were further analyzed using ExPASy. The MYB protein sequences of Arabidopsis were downloaded from the Plant Transcription Factor Database. Based on the alignment of the R2R3-MYB protein sequence of passion fruit and Arabidopsis thaliana, a neighbor-joining phylogenetic tree was constructed by MEGA. The conserved motifs, gene structure and chromosome location were analyzed with TBtools. We also predicted the putative miRNA target sites of PeMYB genes by the online psRNATarget Server. Eight PeMYB genes clustered with Arabidopsis R2R3-MYB gene members from the above subgroups of phylogenetic trees were selected for qRT-PCR analysis under cold, heat, osmotic, and salt stress. In addition, the candidate PeMYB genes were analyzed by qRT-PCR analysis in the peel of passion fruit at different developmental stages after the pollination. 【Results】 A total of 99 R2R3-MYB genes were identified from passion fruit genome. The lengths of the protein sequences of PeMYB ranged from 113 (PeMYB78) to 1013 (PeMYB39) amino acids, and molecular weight (MWs) varied from 12.89 ku (PeMYB78) to 113.94 ku (PeMYB39). Moreover, the theoretical pI of PeMYBs was from 4.73 (PeMYB16) to 10.15 (PeMYB76). According to the topological structure of the phylogenetic tree and the classification of AtMYBs, the 99 R2R3-PeMYBs were divided into 36 groups (P1-P36). Most subgroups contained the R2R3-MYB members from both passion fruit and Arabidopsis, suggesting that they might be derived from a common ancestor. The structural analysis, including motifs and gene structure, illustrates that the R2R3-PeMYBs in the same subgroup have relative conserved structural features. The result showed that the number of exons varied from 1 to 13 in PeMYB genes. Most R2R3-PeMYB genes (53.3%) had similar distributions of three exons and two introns and a few R2R3-PeMYBs (PeMYB58, PeMYB60, PeMYB82) contained 12 or more exons. Motif 1, motif 2, and motif 3 were located in the N-terminal of almost all R2R3-PeMYB protein sequences, which contain conserved tryptophan residues and are related to R2 and R3 domains. The R2R3-PeMYB genes were randomly distributed on 9 passion fruit chromosomes. Most genes were located at the distal ends of the chromosomes. Chromosome 1 had the maximum number of R2R3-MYB genes (28 genes, 28.3%), followed by chromosome 6, which had 15 (15.2%) genes. The gene duplication event analysis revealed 37 pairs of segmentally duplicated genes and 7 pairs of tandemly duplicated genes were identified in R2R3-PeMYBs. The six tandem duplication events were on chromosomes 1, 2, 4, 5, and 6 and most segmental duplication events occurred on chromosome 1. Of the 99 genes, 54 (54.5%) produced 37 segmental duplication gene pairs suggesting that segmental duplication events contributed to the expansion of the R2R3-MYB family of passion fruit. Based on transcriptome data and qRT-PCR analysis, it was found that R2R3-PeMYB genes showed different expression patterns in different floral tissues at different developmental stages. Most of the R2R3-MYB genes (eg: PeMYB79 and PeMYB80) were expressed in the early development stage of floral tissues and showed a decreasing trend in the late development stages. A few genes showed high expression patterns throughout the development of different floral tissues. At all stages of ovule development, some R2R3-PeMYB genes, like PeMYB34 and PeMYB39, were highly expressed. In addition, the high expression of PeMYB62 and PeMYB63 in the peel color transformation period of passion fruit indicated that they may be involved in the anthocyanin synthesis pathway of passion fruit. Moreover, PeMYB62 and PeMYB63 genes were the targeted genes of Ped-miR828 family, and miR828 has been reported to be involved in the anthocyanin synthesis pathway. This further indicates that the two genes are likely to play an important role in the anthocyanin synthesis pathway. These results indicated that R2R3-PeMYB genes play an important role in the development of different floral tissues and fruit. At the same time, eight R2R3-PeMYB genes also showed different responses to abiotic stress (cold, heat, salt and osmotic stresses), these R2R3-PeMYB genes can be significantly regulated by at least two stress treatments. The result indicates that R2R3-PeMYB genes were also induced by various abiotic stress. 【Conclusion】 In this study, 99 R2R3-PeMYB gene family members were identified and found to play an important role in flower and fruit development and stress induction of passion fruit, which provided valuable clues for future research on the function and evolution of R2R3-MYB genes in flower and fruit development.
Key words: Passion fruit; R2R3-MYB transcription factors; Phylogenetic analysis; Flower and fruit development
百香果(Passiflora edulis)是西番莲科西番莲属的一种草质藤本植物,广泛分布于热带和亚热带地区[1]。百香果营养价值高,果实可供鲜食,也可加工成多种副产品,在鲜果消费和工业用途中备受青睐[2]。然而,目前国内百香果主栽品种均为外来引进品种,种植适应性较差,且百香果成花坐果易受到温度、光照、水分等环境因素的影响[3],难以实现丰产稳产,种植百香果高效益、高收益的特点未得到体现。因此,探索百香果的花果发育和环境应激响应的调控机制,对促进百香果的经济效益提升具有重要意义。
MYB(v-myb avian myeloblastosis viral oncogene homolog)转录因子家族是植物中最大和最有特点的转录因子家族之一,其定义为存在1~4个50~53个氨基酸的MYB重复序列,形成螺旋-转角-螺旋(helix-turn-helix,HTH)结构[4]。根据MYB结构域中不完全重复序列的数目,可以将其分为4个亚家族:1R-MYB、R2R3-MYB、R1R2R3-MYB和4R-MYB,其中R2R3-MYB是植物中最大且研究最深入的MYB转录因子亚家族[5]。R2R3-MYB转录因子广泛参与植物各种生物过程的调节,包括初级和次级代谢、生长发育以及对环境因素和植物激素的应答[6-8]。
目前,已经有许多研究人员对拟南芥和其他植物中R2R3-MYB基因进行了系统分析,明确了部分R2R3-MYB基因功能。在拟南芥中,若干R2R3-MYB转录因子被确认参与类黄酮的合成[9],其中AtMYB75/PAP1和AtMYB90/PAP2的过表达可以调节花青素的积累[10]。第7亚组中的AtMYB11/PFG1、AtMYB12/PFG1和AtMYB111/PFG可以调控黄酮醇的合成[11]。此外,不少R2R3-MYB转录因子参与调节花和果实的发育。例如,AtMYB98在参与雌配子体发育和花粉管引导过程中调节辅助细胞分化[12]。在梨中,PbMYB25和PbMYB52可能参与了果实发育过程中木质素生物合成的调节[13]。而且,大多数R2R3-MYB基因在植物对非生物胁迫的应答中也发挥着重要作用[9]。例如,AtMYB2、AtMYB44和AtMYB74增强了植物对盐胁迫的耐受性[14-16],而AtMYB73在响应盐胁迫中起负调控作用[17]。再则,AtMYB96不仅参与植物抗旱,还通过促进CBF(C-repeat binding transcription factors)的表达来抵抗低温[18]。而其他植物物种的MYB基因,如GhMYB73(Gossypium hirsutum L.)、TaMYB73(Triticum aestivum L.)和StMYB30(Solanum tuberosum L.),在转基因植株中增强了对盐胁迫的耐受性[19-21]。
作为植物中最大的一类转录因子,MYB转录因子群体的规模主要归因于R2R3-MYB亚家族的快速扩张[22]。对不同物种中R2R3-MYB基因的系统鉴定和研究将进一步加深读者对其进化和功能的理解,这已在许多作物和园艺植物中进行,如玉米、菠萝、大豆等[23-25]。近期,百香果基因组序列已公布[26-27],这为鉴定R2R3-MYB基因家族成员并探索其在百香果花果发育和胁迫响应中的潜在调控作用提供了良好的契机。
笔者在本研究中共鉴定了99个R2R3-MYB基因,并进行了一系列的系统分析,包括系统发育关系、基因组结构、染色体分布、保守基序和表达模式分析。此外,还进行了qRT-PCR实验以验证候选PeMYB基因的表达模式,为进一步研究百香果R2R3-MYB基因家族在花果发育方面的功能奠定了基础。
1 材料和方法
1.1 百香果中MYB基因家族的鉴定
百香果(P. edulis)基因组数据来自国家基因组数据中心(National Genomics Data Center,https://ngdc.cncb.ac.cn/)。从Pfam数据库(http://pfam.xfam.org/)[28]中下载MYB结合域(PF00249)的隐马尔科夫模型(Hidden Markov Model profile,HMM)。使用TBtools(v1.098745)中的Simple HMM Search[29],以PF00249为模型从百香果基因组中搜索出候选PeMYB基因,截止到E值为0.01。对冗余序列进行手动删除。使用SMART(http://smart.embl-heidelberg.de/)和CDD数据库(https://www.ncbi.nlm.nih.gov/cdd)用于交叉验证候选序列中MYB结构域的存在。使用ExPASy(https://www.expasy.org/)进一步分析潜在的MYB蛋白序列的物理化学特征,包括分子质量、理论等电点(pI)和氨基酸的数量等信息。此外,通过在线网站Cell PLoc 2.0(http://www.csbio.sjtu.edu.cn/bioinf/Cell-PLoc-2/)预测推断的PeMYB蛋白的亚细胞定位。
1.2 多序列比对与系统发育分析
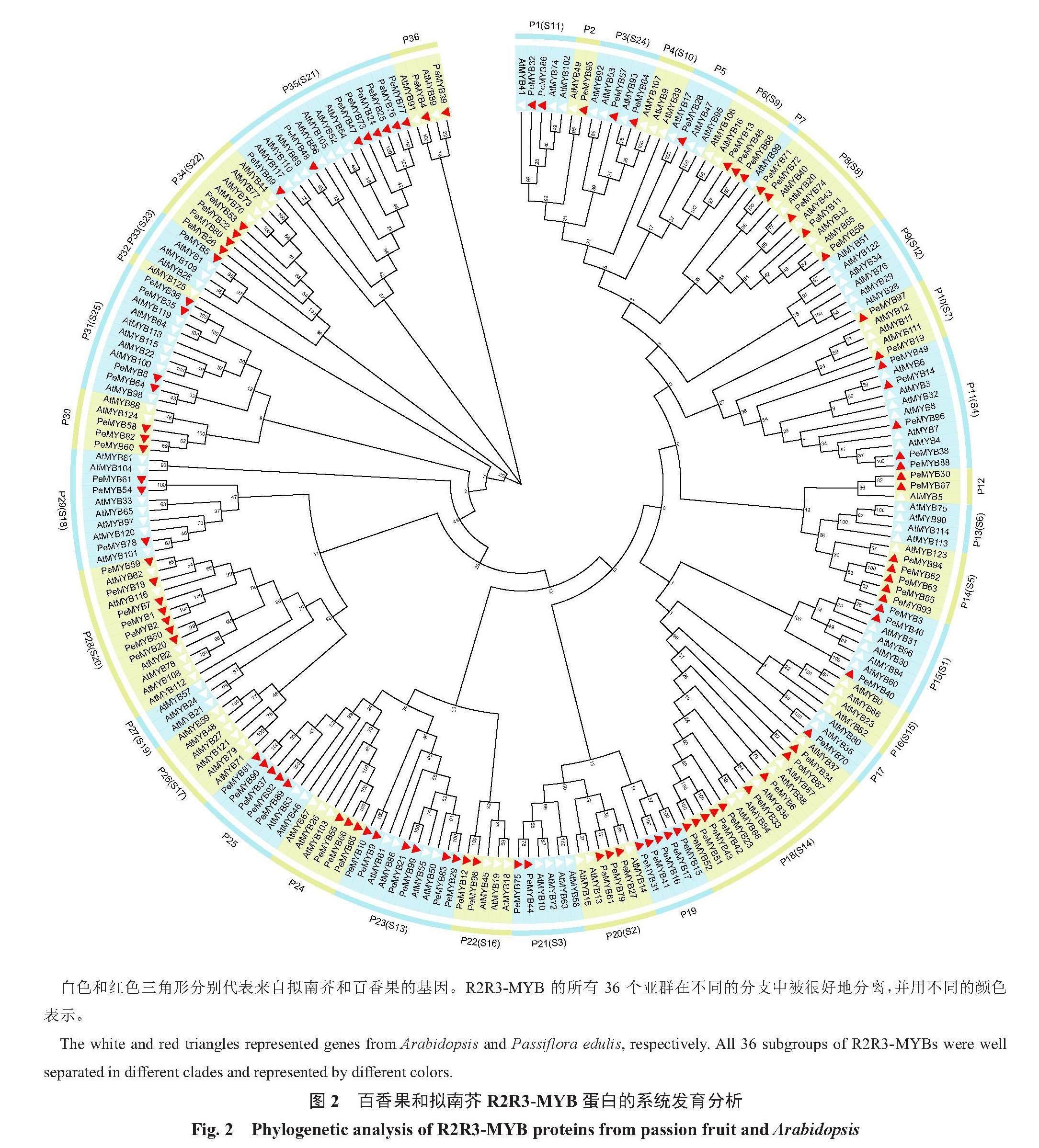
使用DNAMAN软件可视化R2和R3 MYB重复序列的分布,使用WebLogo生成保守基序Logos(http://weblogo.berkeley.edu/logo.cgi)。从Plant TFDB(http://planttfdb.gao-lab.org/index.php)[30]中下载拟南芥MYB蛋白序列。使用MEGA(version 11.0)中的MUCLE对百香果R2R3-PeMYB蛋白和拟南芥R2R3-MYB蛋白序列进行多序列比对。根据百香果和拟南芥的R2R3-MYB蛋白序列的比对,用MEGA(version 11.0)采用Neighbor-Joining(NJ)法构建系统发育树。利用在线网站Evolview v2 (https://www.evolgenius.info/evolview-v2/#login)[31]对进化树进行美化。根据拟南芥AtMYB蛋白的分类,最终将百香果PeMYB蛋白分为36个组(P1~P36)[32]。
1.3 基因结构、蛋白保守基序分析
从百香果基因组的GFF文件中获得PeMYB基因的外显子分布。使用MEME在线网站(https://meme-suite.org/meme/tools/meme)分析PeMYB蛋白的保守基序。使用Tbtools(v1.098745)[29]软件可视化R2R3-PeMYB的基因结构和蛋白保守基序。
1.4 百香果中PeMYB基因的染色体分布、基因复制分析
根据百香果基因组的GFF文件,使用TBtools软件(v1.098745)[29]可视化PeMYB基因的染色体分布信息。利用TBtools软件中的MCScanX分析R2R3-PeMYB基因的基因复制事件,并在TBtools的Advanced Circos中可视化结果。基于大于75%的同一性和超过75%基因长度的查询覆盖率的筛选标准,使用TBtools中的Simple Ka/Ks Calculator计算PeMYB基因的Ka(非同义替换)和Ks(同义替换)。
1.5 miRNA靶向PeMYB基因结合位点的预测
为了预测PeMYB基因中可能的miRNA靶位点,从已发表的数据中下载百香果成熟miRNA序列[33],使用在线网站psRNATarget (https://www.zhaolab.org/psRNATarget/)分析预测PeMYB基因中的miRNA靶位点。通过Cytoscape软件[34]构建和可视化PeMYB靶基因和预测的miRNA之间的网络相互作用。
1.6 R2R3?PeMYB基因表达分析
用于转录组分析的百香果(P. edulis Sims)种植于广西农业科学院园艺研究所品种试验园。苞片、萼片、花丝、花瓣、雄蕊、柱头和胚珠等不同组织的RNA测序数据来自中国国家基因库(CNGB)[35]。RNA-seq使用发育早期(原孢子细胞形成时)和发育晚期(胚珠完全分化时)的百香果花的不同组织[35](不同发育时期信息见https://pan.baidu.com/s/1LcC6pEZBS4vP72aaX1aNxA?pwd=PMYB)。此外,在果汁形成期[授粉后53 d(53 DAP)]、果汁转色期[授粉后60 d(60 DAP)]、果皮转色期[授粉后100 d(100 DAP)]和果实成熟期[授粉后128 d(128 DAP)]采集果实样品。
RNA提取和Illumina测序按照Chen等[36]的研究方法进行。简言之,使用RNAprep Pure Plant Kit(Tiangen,Beijing,China)试剂盒提取总RNA。计算R2R3?PeMYB基因在百香果花的8个发育阶段的TPM(Transcripts Per Kilobase Million)值。R2R3?PeMYB基因在不同发育阶段的表达谱通过其TPM值来测量,并且基于log2(TPM+0.01)的值使用R中的pheatmap包制作热图。TPM值大于50表示基因丰富,用“*”标记。
1.7 胁迫处理和实时定量PCR分析
采用规格一致的百香果无病毒健康嫁接苗,待生长3周后分别进行冷(4±2 ℃)、热(45±2 ℃)、渗透(200 mmol·L-1甘露醇)和盐(200 mmol·L-1 NaCl)胁迫处理[35]。在进行冷和热胁迫处理时,将健康的幼苗置于4 ℃或45 ℃的生长室中;在进行渗透和盐胁迫处理时,百香果幼苗先在1/2 MS液体培养基中培养7 d,然后转移到含有200 mmol·L-1甘露醇或200 mmol·L-1 NaCl的新鲜1/2 MS液体培养基中进行胁迫处理。在胁迫处理后0 h、24 h和48 h的时间点,收集至少3株植物的叶片,并收集未处理的植物样本作为对照,将所有采集的样品用液氮快速冷冻,在-80 ℃下保存,用于提取RNA。
qRT-PCR在Bio-Rad实时PCR系统(Foster City,CA,USA)中进行,使用SYBR Premix Ex Taq Ⅱ系统(TaKaRa Perfect Real Time),样品体积为20 μL(引物序列信息见https://pan.baidu.com/s/1LcC6pEZBS4vP72aaX1aNxA?pwd=PMYB)。每个样品3次技术重复,每个样品3次生物学重复。以EF1a基因作为内参基因,使mRNA水平正常化。使用2-ΔΔCT方法计算基因的倍数变化[37],误差条表示3个重复的标准偏差(SD)。
1.8 用qRT-PCR分析PeMYB基因在花青素生物合成中的表达
为了筛选与花青素合成相关的PeMYB基因,利用MEGA(version 11.0)构建了4个物种(拟南芥、番茄、葡萄和百香果)的R2R3-MYB基因系统发育树。然后,根据与花青素合成有关的MYB基因的分支,如VvMYBA1、SlMYB75、AtMYB75、AtMYB90、AtMYB113和AtMYB114,筛选出候选PeMYB基因。然后对授粉后不同发育阶段(G:青皮期,授粉后第60天;T:果皮颜色转化期,授粉后第110天;P:紫皮成熟期,授粉后第130天)的百香果果皮中的候选PeMYB基因进行qRT-PCR分析。
2 结果与分析
2.1 百香果中MYB基因的鉴定
根据MYB结构域的HMM模型,从百香果基因组数据库中初步筛选具有典型MYB结构域的候选基因。在去除冗余序列后,总共确定了99个R2R3-MYB基因(基因信息见https://pan.baidu.com/s/1LcC6pEZBS4vP72aaX1aNxA?pwd=PMYB)。根据基因在染色体上的位置将R2R3-MYB基因命名为PeMYB1至PeMYB99。PeMYB蛋白序列长度从113(PeMYB78)到1013(PeMYB39)个氨基酸不等,分子质量从12.89 ku(PeMYB78)到113.94 ku(PeMYB39)不等。此外,PeMYB的理论pI值从4.73(PeMYB16)到10.15(PeMYB76)不等。所有PeMYB蛋白的亚细胞定位被预测为在细胞核中表达,这与PeMYB作为转录因子的功能和特性一致。
2.2 百香果R2R3-MYB基因的多序列比对及系统发育分析
为了进一步分析和鉴定R2R3-PeMYB蛋白中R2和R3 MYB重复序列的特征,笔者进行了Web Logo和多序列比对(图1)。R2和R3的基本结构分别为[-W-(X19)-W-(X19)-W-]和[-F-(X18)-W-(X18)-W-],它们包含约52个氨基酸残基。如图1所示,PeMYB蛋白的R2和R3结构域有大量的保守氨基酸,特别是色氨酸残基(W)。R2重复序列包含3个保守的色氨酸残基(W),它们形成MYB转录因子的螺旋-转角-螺旋结构。R3重复序列的第二个和第三个色氨酸残基(W)高度保守,而第一个保守的色氨酸残基大部分被苯丙氨酸(F)取代,少数被异亮氨酸(I)和亮氨酸(L)取代。此外,R2重复序列中的E-10、D-11、L-14、G-22、R-37、K-40、R-43、R-45和L-50残基和R3重复序列中的E-10、G-22、A-29、R-35、T-36、N-38、K-41和N-42残基,在大多数MYB蛋白序列中都是一致的(图1-A)。
为了分析R2R3-PeMYB的系统发育关系和基因功能,利用MEGA软件构建了包含99个百香果R2R3-PeMYB蛋白和126个拟南芥AtMYB蛋白的系统发育树(图2)。根据之前的研究,拟南芥中的R2R3-MYB蛋白成员被分为25个亚组(S1~S25)[32]。根据树的拓扑结构和AtMYB蛋白的分类,99个R2R3-PeMYB蛋白可以分为36组(P1~P36),用不同的颜色绘制(图2)。其中百香果和拟南芥聚为27个分支,亚组P35(S21)含有最多的R2R3-MYB蛋白成员,有7个AtMYB蛋白和8个PeMYB蛋白。同时,第1分支和第8分支分别是拟南芥和百香果的物种特异性分支。聚在同一亚群中的PeMYB蛋白和AtMYB蛋白成员数量的差异表明两个物种之间MYB基因家族存在明显的种间差异。
2.3 R2R3-PeMYB的基因结构和蛋白保守基序分析
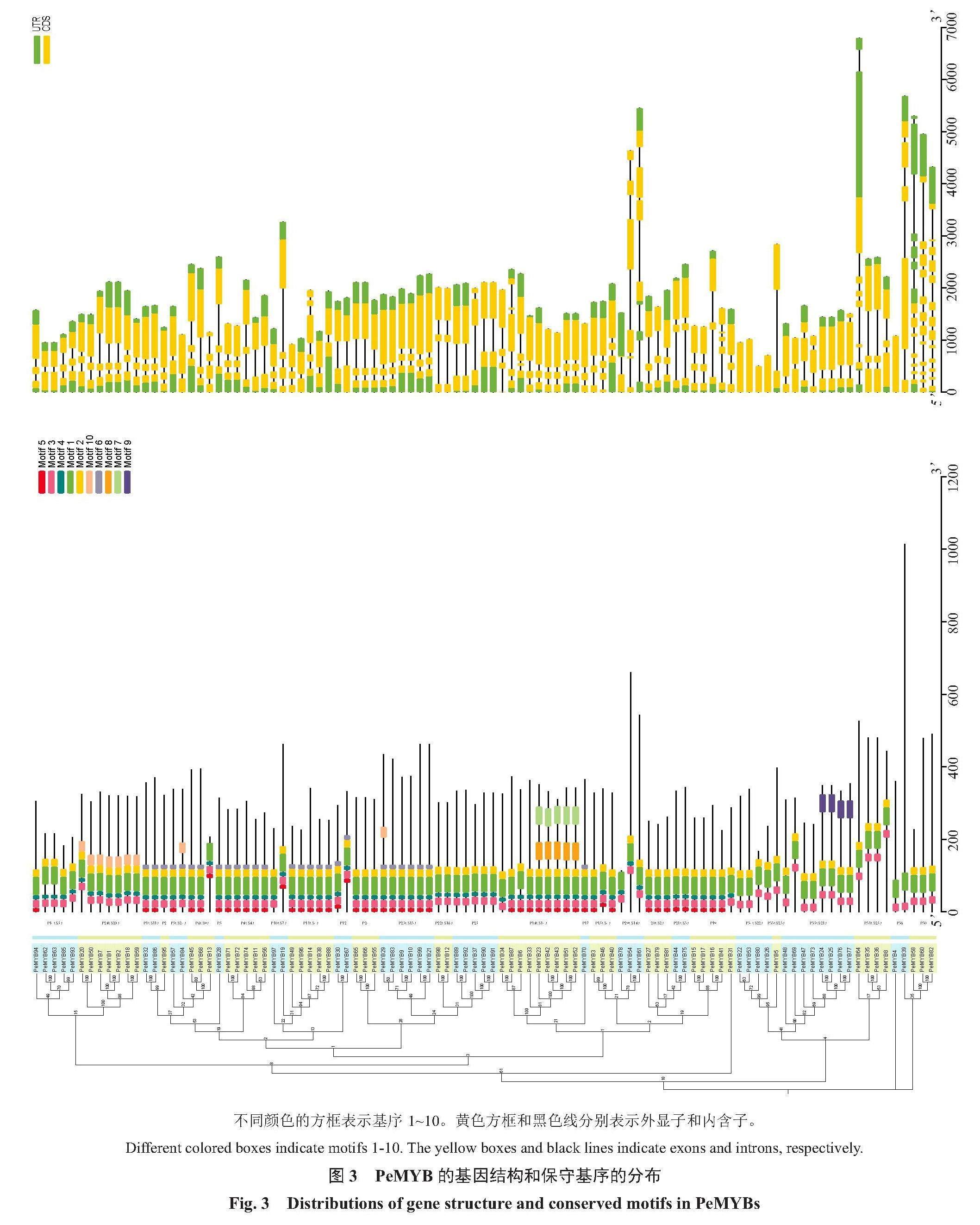
为了解PeMYB基因的结构和遗传多样性,使用TBtools软件对外显子-内含子结构进行了分析和可视化(图3)。结果表明,PeMYB基因的外显子数目从1到13不等。大部分R2R3-PeMYB基因(53.3%)具有相似的外显子-内含子分布(含有3个外显子和2个内含子),少数R2R3-PeMYB基因含有12个或更多的外显子(PeMYB58、PeMYB60、PeMYB82)。此外,具有相似外显子-内含子结构的基因,特别是在内含子数量方面,倾向于在系统发育树中聚集在同一亚组中。例如,P34(S22)亚组中的两个基因都缺乏内含子,而P38(S20)亚组的基因都有两个内含子(图3)。
使用MEME在线网站预测了99个R2R3-PeMYB蛋白的10个保守基序(图3,各基序的长度和保守序列见https://pan.baidu.com/s/1LcC6pEZBS4vP72aaX1aNxA?pwd=PMYB)。结果表明,基序1、基序2和基序3位于几乎所有R2R3-PeMYB蛋白序列的N端,且这些序列含有保守的色氨酸残基,并与R2和R3结构域相关。总体而言,同一亚组内的基因表现出相似的基序组成,但亚组间存在明显差异,表明基序模式可能与PeMYB蛋白的功能有关。有趣的是,基序7和基序8只出现在P18(S14)亚组中,可能P18(S14)亚组中的一些基因在进化过程中发生了变化。PeMYB蛋白的基序分析显示,同一亚组下的成员高度保守,进一步证明了它们在系统发育树中进化关系的接近性。
2.4 R2R3-PeMYB基因的染色体定位和基因复制
为了研究百香果R2R3-MYB基因家族的遗传差异,分析了R2R3-PeMYB基因的染色体定位(图4)。结果显示,95个R2R3-PeMYB基因被不均匀地定位在9条染色体上,4个R2R3-PeMYB基因分布在未组装的支架上。大多数R2R3-PeMYB基因位于染色体的末端。1号染色体上的R2R3-PeMYB基因数量最多(28个,28.3%),其次是6号染色体,包含15个(15.2%)基因。其余的染色体上有3到11个基因,表明染色体和基因数量之间没有相关性。
基因重复事件分析显示,在R2R3-PeMYB基因中鉴定出37对片段重复基因和7对串联重复基因(图4,基因对信息见https://pan.baidu.com/s/1LcC6pEZBS4vP72aaX1aNxA?pwd=PMYB)。6次串联重复事件发生在1、2、4、5和6号染色体上,大部分片段重复事件发生在1号染色体上。在99个基因中,54个(54.5%)产生了37个片段重复基因对,表明基因重复事件(串联重复和片段重复)对PeMYB基因的多样性和进化有重要贡献。Ka和Ks的比例可以反映生物进化过程中的选择压力。因此,为了探索选择压力在MYB基因家族进化中的作用,获得了同源基因的Ka/Ks比率(Ka/Ks比率信息见https://pan.baidu.com/s/1LcC6pEZBS4vP72aaX1aNxA?pwd=PMYB)。几乎所有R2R3-PeMYB基因对的Ka/Ks比值均小于1,表明这些PeMYB基因进化过程可能受到纯化选择。
2.5 MicroRNA靶向R2R3-PeMYB基因的预测
MicroRNAs(miRNA)是一类长度约22 nt的小型非编码RNA,参与动物和植物的转录后基因表达调控。因此,为了更好地了解miRNA参与PeMYB基因的调控机制,利用已发表的miRNA序列在psRNATarget网站上预测miRNA靶向PeMYB基因的结合位点。PeMYB基因中miRNA靶向位点的网络相互作用和示意图如图5-A和图5-B所示,鉴定的11个miRNA靶向17个PeMYB基因,结果显示ped-miR828b靶向最多的7个PeMYB基因(PeMYB3、PeMYB30、PeMYB46、PeMYB62、PeMYB63、PeMYB85和PeMYB93);ped-miR319p靶向3个PeMYB基因(PeMYB32、PeMYB54、PeMYB61),其余9个miRNA分别靶向至少1个PeMYB基因。通过比较靶基因,PeMYB54和PeMYB61被三个miRNA靶向,即ped-miR319b、ped-miR319l和ped-miR319p;PeMYB32被两个miRNA靶向,分别为ped-miR319p和ped-miR171k-5p(图5,详情信息见https://pan.baidu.com/s/1LcC6pEZBS4vP72aaX1aNxA?pwd=PMYB)。总之,ped-miR828b和ped-miR319p是主要的miRNA,而PeMYB32、PeMYB54和PeMYB61是可能发挥重要作用并需要进一步对其功能进行研究的主要靶基因。
2.6 基于转录组数据的R2R3-PeMYB基因表达分析
为了探索R2R3-PeMYB基因的潜在功能,使用RNA-seq数据对99个R2R3-PeMYB基因在百香果花的不同组织的不同发育阶段和果实中的表达谱进行了表征(图6)。在所有样本中具有低表达水平的基因被过滤掉。
根据不同花发育阶段PeMYB基因表达的模式,观察到PeMYB基因在百香果花的不同组织发育阶段的表达变化(图6)。大部分PeMYB基因(如PeMYB79和PeMYB80)在百香果花的不同组织发育中早期表达,但在发育后期呈下降趋势。较少基因在百香果花的不同组织的发育过程中表现出高表达模式。在胚珠发育的各个阶段,一些PeMYB基因,如PeMYB34和PeMYB39,都表现出高表达模式。
笔者在本研究中还分析了PeMYB基因在授粉后不同发育时期的表达模式(图6)。随着授粉后时间的延长,PeMYB40和PeMYB93的表达水平持续下降。此外,一些PeMYB基因,如PeMYB22、PeMYB59、PeMYB82和PeMYB83,仅在果汁形成过程(53 DAP)中表达。此外,PeMYB30、PeMYB75和PeMYB76在果汁转色期(60 DAP)、果皮转色期(100 DAP)和果实成熟期(128 DAP)均呈现高表达模式。这些结果表明,不同的PeMYB基因在百香果发育的不同阶段发挥着重要作用。
为了验证PeMYB基因在百香果花的不同组织发育中的表达情况,利用qRT-PCR研究了6个代表性PeMYB基因(PeMYB11,PeMYB34,PeMYB39,PeMYB69,PeMYB79和PeMYB88)在同一花组织中的表达谱(图7)。总体而言,6个PeMYB基因的qRT-PCR趋势与RNA-seq分析结果一致。PeMYB11在雄蕊发育早期高表达,同时PeMYB88在雄蕊发育晚期高表达。PeMYB34、PeMYB39和PeMYB69在胚珠发育过程中优先表达,而PeMYB79在百香果花的不同组织的发育早期显著高表达。
2.7 R2R3-PeMYB基因响应非生物胁迫的表达模式
据报道,拟南芥R2R3-MYB基因家族S1、S2、S11、S20和S22亚组的成员与各种应激反应有关[32]。已知与一亚组中的同源基因可能具有相似的生物学功能。为了进一步探索R2R3-PeMYB基因可能的生物学功能,在冷、热、渗透和盐胁迫下,选择了上述系统发育树亚群中与拟南芥R2R3-MYB基因成员聚集的8个PeMYB基因进行qRT-PCR分析(图8)。在低温处理下,4个基因(PeMYB27、PeMYB40,PeMYB46和PeMYB79)具有相似的表达模式,且随着处理时间的延长呈现持续增加的趋势。PeMYB53、PeMYB80和PeMYB86的相对表达水平随着处理时间的推移先升高后降低。而在热处理条件下,只有PeMYB27和PeMYB80的表达量显著上调,其他PeMYB基因(PeMYB46,PeMYB50,PeMYB53,PeMYB79和PeMYB86)呈现波动表达模式。在盐胁迫处理下,4个PeMYB基因(PeMYB40、PeMYB46、PeMYB80和PeMYB86)的表达水平与0 h相比均上升,而PeMYB27、PeMYB50和PeMYB53的表达水平显著下调。在渗透处理过程中,PeMYB27、PeMYB50、PeMYB53和PeMYB80呈现波动的表达模式,而4个基因(PeMYB40、PeMYB46、PeMYB79和PeMYB86)的表达水平呈现极显著上调。有趣的是,PeMYB40在除热胁迫外的所有胁迫下都表现出显著上调的表达水平。PeMYB27仅在低温和高温处理下表达量呈增加趋势,而PeMYB86的表达量仅在渗透和盐胁迫条件下增加。
2.8 R2R3-PeMYB基因在花青素生物合成中的表达分析
为了更好地探索PeMYB基因在花青素生物合成中的表达模式,构建了多个物种(拟南芥、番茄、葡萄和百香果)中R2R3-MYB基因的系统发育树(系统发育树信息见https://pan.baidu.com/s/1LcC6pEZBS4vP72aaX1aNxA?pwd=PMYB),然后在其他不同物种中与花青素合成相关的R2R3-MYB基因(VvMYBA1、SlMYB75、AtMYB75、AtMYB90、AtMYB113和AtMYB114)的分支中筛选候选的PeMYB基因。候选PeMYB基因以百香果果实不同发育时期的果皮来进行qRT-PCR分析(图9)。qRT-PCR结果显示,PeMYB62和PeMYB63的表达量在果皮颜色转化期(T)显著增加,表明PeMYB62和PeMYB63可能参与调节百香果果皮中花青素的积累。
3 讨 论
在百香果基因组中共鉴定到99个R2R3-PeMYB基因。在系统发育分析时,根据以往研究提出的分类学和拓扑结构,将百香果和拟南芥的R2R3-MYB基因分为36个亚组[32]。大多数亚组包含来自百香果和拟南芥的R2R3-MYB成员,暗示它们可能来源于共同的祖先。然而,少数亚组只来自百香果或拟南芥的R2R3-MYB成员,这表明R2R3-MYB基因家族在分离后可能经历了物种特异性分化。
聚集在同一亚组的成员具有相似的外显子-内含子结构、基序组成和分布顺序[32]。与其他植物一样,大多数R2R3-PeMYB基因表现出3个外显子和2个内含子的常规剪接模式,这可能表明它们在不同物种中的保守功能。基序1、基序2和基序3在大多数R2R3-PeMYB蛋白中高度保守,并作为MYB保守结构域的组成部分,这对转录因子的功能特异性至关重要[38]。不同亚组的R2R3-MYB结构差异很大。例如,亚组P18(S14)和P35(S21)具有与其他亚组显著不同的基序组成,而基序7和基序8是亚组P18(S14)所特有的基序,表明P18(S14)亚组的PeMYB基因可能经历了不同的进化发展,具有特定的功能。R2R3-PeMYB基因在P18(S14)亚组中的表达谱不同。例如,PeMYB33在雄蕊发育后期高表达,而PeMYB42在雄蕊发育早期高表达。此外,P35(S21)亚组的PeMYB基因在胚珠发育的不同时期均低表达或不表达。因此,不同亚组间的结构多样性可能有助于R2R3-PeMYB基因家族的功能多样性。
基因复制事件在基因家族成员的扩展中起着重要作用,片段复制和串联复制是基因家族在基因组中扩展的主要原因[38]。在百香果R2R3-MYB基因家族中,鉴定出7对串联重复和37对片段重复基因,表明片段重复事件是百香果R2R3-MYB基因家族扩增的主要来源。在这些基因对中,只有一对片段重复基因(PeMYB15-PeMYB17)的Ka/Ks值大于1,表明这对基因在进化过程中经历正向选择。然而,这两个基因在本研究中的不同组织中都没有显示出任何特殊的表达谱,这表明它们可能只在其他特定的发育阶段或某些条件下表达。有些重复基因表现出相似的表达模式,聚集在同一个亚家族中,如来自同一亚组(P30)的PeMYB58和PeMYB60均在花丝、雄蕊、柱头和胚珠发育的早期阶段高表达,表明它们可能存在功能冗余。然而,大多数基因对表现出不同的表达模式,这表明百香果R2R3-MYB基因家族的成员存在功能分化的现象。例如,尽管PeMYB6和PeMYB34属于同一亚组(P18/S14),但它们显示出完全不同的表达模式。PeMYB34在胚珠发育阶段具有高水平表达,而PeMYB6在萼片、胚珠的早期发育阶段以及苞片和花瓣的后期发育阶段高度表达。此外,PeMYB79和PeMYB81基因对的表达模式也不同。PeMYB79在果汁颜色转化期(60 DAP)表达,而PeMYB81主要在果皮颜色转化期(100 DAP)表达。这些基因对表达模式的差异表明了PeMYB基因的功能多样性。
百香果作为广受欢迎的水果和观赏作物,探究其代谢过程、花和果实发育的调控机制具有重要意义。大多数R2R3-PeMYB基因的生物学功能仍不清楚,鉴定不同物种中的同源基因将为探究这些基因的功能提供有价值的参考。前人研究表明AtMYB117/LOF1在花器官发育和胚珠生长等多种发育过程中建立边界区域[39]。同源的PeMYB48和PeMYB69在胚珠发育过程中表现出高表达模式,并与AtMYB117/LOF1聚类,表明PeMYB48和PeMYB69在调节胚珠发育中可能具有类似的功能。P29(S18)亚组的基因,包括AtMYB33、AtMYB65和AtMYB101,在花的发育,特别是花粉发育中发挥重要作用[40]。同一亚组中的PeMYB54和PeMYB61在雄蕊发育早期特异性高表达,说明其可能在雄蕊发育中具有相似的功能。已有研究表明R2R3-MYB基因在果实发育过程中也具有调控功能。基于R2R3-PeMYB基因在不同组织中的表达谱的层次聚类,建立了一个具有8个基因表达的果实特殊表达块,这些基因在果实发育的某些阶段丰富。大部分丰富基因在果汁转色期(60 DAP)和果皮转色期(100 DAP)的表达量最高。已知植物中许多R2R3-MYB基因在黄酮醇生物合成中发挥作用[11]。例如,MdMYB1是苹果中花青素生物合成的一个调节器[41]。PalMYB90可通过调节关键类黄酮途径提高杨树花青素水平[42]。说明在果汁转色期和果实转色期均高表达的R2R3-PeMYB基因可能参与了果实发育过程中黄酮醇或花青苷的代谢。
花青素是植物中重要的次生代谢产物,主要积累在花、果、叶等组织中。它们通过色彩丰富的颜色吸引昆虫等传粉者,帮助植物完成生命过程[43]。目前,与花青素合成有关的R2R3-MYB基因已在多个物种中被发现,包括拟南芥[9]、葡萄[44]、番茄[45]等。AtMYB75、AtMYB90、AtMYB113和AtMYB114控制拟南芥组织中花青素的生物合成[14]。葡萄(Vitis vinifera L.)的VvMybA1基因调节花青素生物合成的最后代谢步骤[44]。笔者在本研究中用拟南芥、葡萄和番茄的R2R3-MYB基因构建了一个系统发育树,以筛选与花青素合成相关的候选PeMYB基因,并对候选PeMYB基因进行了qRT-PCR分析。结果表明,PeMYB62和PeMYB63基因在果皮颜色转化中高度表达,表明PeMYB62和PeMYB63基因可能参与花青素的合成。此外,PeMYB62和PeMYB63基因是Ped-miR828家族的靶基因,并且miR828已被报道参与花青苷合成途径[46]。这进一步表明,PeMYB62和PeMYB63基因很可能在花青素合成途径中发挥重要作用,未来可以进一步研究。
百香果的生长发育易受光照、温度和水分等环境因素的影响[3]。R2R3-MYB基因已被证明与响应非生物胁迫有关[9]。笔者在本研究中设置冷、热、渗透和盐胁迫4种非生物胁迫条件,通过qRT-PCR分析了8个R2R3-PeMYB基因的表达水平。有趣的是,这些R2R3-PeMYB基因显著响应至少两种应激处理。AtMYB41能够影响细胞壁发育,响应ABA、干旱和盐胁迫[47],其同源基因PeMYB86也对干旱和盐胁迫最敏感且诱导程度高。此外,与拟南芥的情况类似[18],P15(S1)亚组的基因包括PeMYB40和PeMYB46在干旱、盐和冷胁迫下也被高度诱导。ped-miR166h-5p靶向的PeMYB79也参与响应多种胁迫,进一步说明了PeMYB79在参与百香果抗逆方面具有重要作用。同时,这些响应胁迫的PeMYB基因中的大多数也在特定发育阶段的某些组织中优先表达。例如,亚组P20(S2)中的PeMYB27在高温和低温胁迫下被高度诱导,并且在萼片和苞叶及柱头的发育晚期也高表达。对这些基因功能的进一步研究有助于揭示PeMYB基因在不同条件下对百香果生长和发育的调控机制。
4 结 论
在百香果(P. edulis)基因组中总共鉴定出99个R2R3-MYB基因。基于系统发育关系,99个R2R3-PeMYB基因分为36个亚组。R2R3-PeMYB基因随机分布在9条百香果染色体上。基因结构分析表明,同一亚组中内含子的剪接模式在MYB结构域中高度保守。共线性分析表明,片段复制事件促进了百香果R2R3-MYB家族的扩张。PeMYB基因在不同发育阶段的花组织中表现出不同的表达模式,8个R2R3-PeMYB在各种非生物胁迫(冷、热、盐和渗透压)下也表现出不同的反应。此外,PeMYB62和PeMYB63可能参与百香果花青素的合成。本研究为后续研究和验证R2R3-MYB基因在百香果花果发育中的潜在功能奠定了基础。
参考文献 References:
[1] DHAWAN K,DHAWAN S,SHARMA A. Passiflora:A review update[J]. Journal of Ethnopharmacology,2004,94(1):1-23.
[2] DAS B K,AL-AMIN M M,RUSSEL S M,KABIR S,BHATTACHERJEE R,HANNAN J M A. Phytochemical screening and evaluation of analgesic activity of Oroxylum indicum[J]. Indian Journal of Pharmaceutical Sciences,2014,76(6):571-575.
[3] FALEIRO F G,JUNQUEIRA N T V,JUNGHANS T G,DE JESUS O N,MIRANDA D,OTONI W C. Advances in passion fruit (Passiflora spp.) propagation[J]. Revista Brasileira De Fruticultura,2019,41(2):e-155.
[4] KLEMPNAUER K H,SIPPEL A E. The highly conserved amino-terminal region of the protein encoded by the v-myb oncogene functions as a DNA-binding domain[J]. The EMBO Journal,1987,6(9):2719-2725.
[5] MARTIN C,PAZ-ARES J. MYB transcription factors in plants[J]. Trends in Genetics,1997,13(2):67-73.
[6] RAHIM M A,RESENTINI F,DALLA V F,TRAINOTTI L. Effects on plant growth and reproduction of a peach R2R3-MYB transcription factor overexpressed in tobacco[J]. Frontiers in Plant Science,2019,10:1143.
[7] ZHANG Z Y,LIU X,WANG X D,ZHOU M P,ZHOU X Y,YE X G,WEI X N. An R2R3 MYB transcription factor in wheat,TaPIMP1,mediates host resistance to Bipolaris sorokiniana and drought stresses through regulation of defense-and stress-related genes[J]. New Phytologist,2012,196(4):1155-1170.
[8] JIANG W H,LIU T X,NAN W Z,JEEWANI D C,NIU Y L,LI C L,WANG Y,SHI X,WANG C,WANG J H,LI Y,GAO X,WANG Z H. Two transcription factors TaPpm1 and TaPpb1 co-regulate anthocyanin biosynthesis in purple pericarps of wheat[J]. Journal of Experimental Botany,2018,69(10):2555-2567.
[9] DUBOS C,STRACKE R,GROTEWOLD E,WEISSHAAR B,MARTIN C,LEPINIEC L. MYB transcription factors in Arabidopsis[J]. Trends in Plant Science,2010,15(10):573-581.
[10] GONZALEZ A,ZHAO M Z,LEAVITT J M,LLOYD A M. Regulation of the anthocyanin biosynthetic pathway by the TTG1/bHLH/Myb transcriptional complex in Arabidopsis seedlings[J]. The Plant Journal,2008,53(5):814-827.
[11] STRACKE R,ISHIHARA H,HUEP G,BARSCH A,MEHRTENS F,NIEHAUS K,WEISSHAAR B. Differential regulation of closely related R2R3-MYB transcription factors controls flavonol accumulation in different parts of the Arabidopsis thaliana seedling[J]. The Plant Journal,2007,50(4):660-677.
[12] PUNWANI J A,RABIGER D S,LLOYD A,DREWS G N. The MYB98 subcircuit of the synergid gene regulatory network includes genes directly and indirectly regulated by MYB98[J]. The Plant Journal,2008,55(3):406-414.
[13] CAO Y P,HAN Y H,LI D H,LIN Y,CAI Y P. MYB transcription factors in Chinese pear (Pyrus bretschneideri Rehd.):Genome-wide identification,classification,and expression profiling during fruit development[J]. Frontiers in Plant Science,2016,7:577.
[14] YOO J H,PARK C Y,KIM J C,DO HEO W,CHEONG M S,PARK H C,KIM M C,MOON B C,CHOI M S,KANG Y H,LEE J H,KIM H S,LEE S M,YOON H W,LIM C O,YUN D J,LEE S Y,CHUNG W S,CHO M J. Direct interaction of a divergent CaM isoform and the transcription factor,MYB2,enhances salt tolerance in Arabidopsis[J]. Journal of Biological Chemistry,2005,280(5):3697-3706.
[15] JUNG C,SEO J S,HAN S W,KOO Y J,KIM C H,SONG S I,NAHM B H,DO CHOI Y,CHEONG J J. Overexpression of AtMYB44 enhances stomatal closure to confer abiotic stress tolerance in transgenic Arabidopsis[J]. Plant Physiology,2008,146(2):623-635.
[16] XU R,WANG Y H,ZHENG H,LU W,WU C G,HUANG J G,YAN K,YANG G D,ZHENG C C. Salt-induced transcription factor MYB74 is regulated by the RNA-directed DNA methylation pathway in Arabidopsis[J]. Journal of Experimental Botany,2015,66(19):5997-6008.
[17] KIM J H,NGUYEN N H,JEONG C Y,NGUYEN N T,HONG S W,LEE H. Loss of the R2R3 MYB,AtMyb73,causes hyper-induction of the SOS1 and SOS3 genes in response to high salinity in Arabidopsis[J]. Journal of Plant Physiology,2013,170(16):1461-1465.
[18] LEE H G,SEO P J. The MYB96-HHP module integrates cold and abscisic acid signaling to activate the CBF-COR pathway in Arabidopsis[J]. The Plant Journal,2015,82(6):962-977.
[19] ZHAO Y Y,YANG Z E,DING Y P,LIU L S,HAN X,ZHAN J J,WEI X,DIAO Y Y,QIN W Q,WANG P,LIU P P,SAJJAD M,ZHANG X L,GE X Y. Over-expression of an R2R3 MYB Gene,GhMYB73,increases tolerance to salt stress in transgenic Arabidopsis[J]. Plant Science,2019,286:28-36.
[20] HE Y N,LI W,LV J,JIA Y B,WANG M C,XIA G M. Ectopic expression of a wheat MYB transcription factor gene,TaMYB73,improves salinity stress tolerance in Arabidopsis thaliana[J]. Journal of Experimental Botany,2012,63(3):1511-1522.
[21] LI X X,GUO C,AHMAD S,WANG Q,YU J,LIU C,GUO Y F. Systematic analysis of MYB family genes in potato and their multiple roles in development and stress responses[J]. Biomolecules,2019,9(8):317.
[22] RIECHMANN J L,RATCLIFFE O J. A genomic perspective on plant transcription factors[J]. Current Opinion in Plant Biology,2000,3(5):423-434.
[23] DU H,FENG B R,YANG S S,HUANG Y B,TANG Y X. The R2R3-MYB transcription factor gene family in maize[J]. PLoS One,2012,7(6):e37463.
[24] SALIH H,GONG W F,HE S P,SUN G F,SUN J L,DU X M. Genome-wide characterization and expression analysis of MYB transcription factors in Gossypium hirsutum[J]. BMC Genetics,2016,17(1):129.
[25] LIU C Y,XIE T,CHEN C J,LUAN A P,LONG J M,LI C H,DING Y Q,HE Y H. Genome-wide organization and expression profiling of the R2R3-MYB transcription factor family in pineapple (Ananas comosus)[J]. BMC Genomics,2017,18(1):503.
[26] MA D N,DONG S S,ZHANG S C,WEI X Q,XIE Q J,DING Q S,XIA R,ZHANG X T. Chromosome-level reference genome assembly provides insights into aroma biosynthesis in passion fruit (Passiflora edulis)[J]. Molecular Ecology Resources,2021,21(3):955-968.
[27] XIA Z Q,HUANG D M,ZHANG S K,WANG W Q,MA F N,WU B,XU Y,XU B Q,CHEN D,ZOU M L,XU H Y,ZHOU X C,ZHAN R L,SONG S. Chromosome-scale genome assembly provides insights into the evolution and flavor synthesis of passion fruit (Passiflora edulis Sims)[J]. Horticulture Research,2021,8:14.
[28] FINN R D,COGGILL P,EBERHARDT R Y,EDDY S R,MISTRY J,MITCHELL A L,POTTER S C,PUNTA M,QURESHI M,SANGRADOR-VEGAS A,SALAZAR G A,TATE J,BATEMAN A. The Pfam protein families database:Towards a more sustainable future[J]. Nucleic Acids Research,2016,44(D1):D279-D285.
[29] CHEN C J,CHEN H,ZHANG Y,THOMAS H R,FRANK M H,HE Y H,XIA R. TBtools:An integrative toolkit developed for interactive analyses of big biological data[J]. Molecular Plant,2020,13(8):1194-1202.
[30] JIN J P,TIAN F,YANG D C,MENG Y Q,KONG L,LUO J C,GAO G. PlantTFDB 4.0:Toward a central hub for transcription factors and regulatory interactions in plants[J]. Nucleic Acids Research,2017,45(D1):D1040-D1045.
[31] HE Z L,ZHANG H K,GAO S H,LERCHER M J,CHEN W H,HU S N. Evolview v2:An online visualization and management tool for customized and annotated phylogenetic trees[J]. Nucleic Acids Research,2016,44(W1):W236-W241.
[32] STRACKE R,WERBER M,WEISSHAAR B. The R2R3-MYB gene family in Arabidopsis thaliana[J]. Current Opinion in Plant Biology,2001,4(5):447-456.
[33] PAUL S,DE LA FUENTE-JIM?NEZ J L,MANRIQUEZ C G,SHARMA A. Identification,characterization and expression analysis of passion fruit (Passiflora edulis) microRNAs[J]. 3 Biotech,2020,10(1):25.
[34] KOHL M,WIESE S,WARSCHEID B. Cytoscape:Software for visualization and analysis of biological networks[J]. Methods in Molecular Biology,2011,696:291-303.
[35] LIANG J X,FANG Y Y,AN C,YAO Y B,WANG X M,ZHANG W B,LIU R Y,WANG L L,ASLAM M,CHENG Y,QIN Y,ZHENG P. Genome-wide identification and expression analysis of the bHLH gene family in passion fruit (Passiflora edulis) and its response to abiotic stress[J]. International Journal of Biological Macromolecules,2023,225:389-403.
[36] CHEN P J,LI Y,ZHAO L H,HOU Z M,YAN M K,HU B Y,LIU Y H,AZAM S M,ZHANG Z Y,RAHMAN Z U,LIU L P,QIN Y A. Genome-wide identification and expression profiling of ATP-binding cassette (ABC) transporter gene family in pineapple [Ananas comosus (L.) Merr.] reveal the role of AcABCG38 in pollen development[J]. Frontiers in Plant Science,2017,8:2150.
[37] WU Y Y,TIAN Q L,HUANG W H,LIU J Y,XIA X Z,YANG X H,MOU H F. Identification and evaluation of reference genes for quantitative real-time PCR analysis in Passiflora edulis under stem rot condition[J]. Molecular Biology Reports,2020,47(4):2951-2962.
[38] FELLER A,MACHEMER K,BRAUN E L,GROTEWOLD E. Evolutionary and comparative analysis of MYB and bHLH plant transcription factors[J]. The Plant Journal,2011,66(1):94-116.
[39] GOMEZ M D,URBEZ C,PEREZ-AMADOR M A,CARBONELL J. Characterization of constricted fruit (ctf) mutant uncovers a role for AtMYB117/LOF1 in ovule and fruit development in Arabidopsis thaliana[J]. PLoS One,2011,6(4):e18760.
[40] GOCAL G F,SHELDON C C,GUBLER F,MORITZ T,BAGNALL D J,MACMILLAN C P,LI S F,PARISH R W,DENNIS E S,WEIGEL D,KING R W. GAMYB-like genes,flowering,and gibberellin signaling in Arabidopsis[J]. Plant Physiology,2001,127(4):1682-1693.
[41] HU D G,SUN C H,MA Q J,YOU C X,CHENG L L,HAO Y J. MdMYB1 regulates anthocyanin and malate accumulation by directly facilitating their transport into vacuoles in apples[J]. Plant Physiology,2016,170(3):1315-1330.
[42] BAI Q X,DUAN B B,MA J C,FEN Y N,SUN S J,LONG Q M,LV J J,WAN D S. Coexpression of PalbHLH1 and PalMYB90 genes from Populus alba enhances pathogen resistance in poplar by increasing the flavonoid content[J]. Frontiers in Plant Science,2020,10:1772.
[43] DAVIES K M,ALBERT N W,SCHWINN K E. From landing lights to mimicry:The molecular regulation of flower colouration and mechanisms for pigmentation patterning[J]. Functional Plant Biology,2012,39(8):619-638.
[44] WONG D C J,SCHLECHTER R,VANNOZZI A,H?LL J,HMMAM I,BOGS J,TORNIELLI G B,CASTELLARIN S D,MATUS J T. A systems-oriented analysis of the grapevine R2R3-MYB transcription factor family uncovers new insights into the regulation of stilbene accumulation[J]. DNA Research,2016,23(5):451-466.
[45] SUN C L,DENG L,DU M M,ZHAO J H,CHEN Q,HUANG T T,JIANG H L,LI C B,LI C Y. A transcriptional network promotes anthocyanin biosynthesis in tomato flesh[J]. Molecular Plant,2020,13(1):42-58.
[46] BONAR N,LINEY M,ZHANG R X,AUSTIN C,DESSOLY J,DAVIDSON D,STEPHENS J,MCDOUGALL G,TAYLOR M,BRYAN G J,HORNYIK C. Potato miR828 is associated with purple Tuber skin and flesh color[J]. Frontiers in Plant Science,2018,9:1742.
[47] LIPPOLD F,SANCHEZ D H,MUSIALAK M,SCHLERETH A,SCHEIBLE W R,HINCHA D K,UDVARDI M K. AtMyb41 regulates transcriptional and metabolic responses to osmotic stress in Arabidopsis[J]. Plant Physiology,2009,149(4):1761-1772.

