保留肾单位手术治疗巨大肾错构瘤的疗效观察
侯亚坤, 周星宇, 拜合提亚·阿扎提, 木拉提·热夏提, 王玉杰, 王文光
作者单位:新疆医科大学第一附属医院泌尿外科中心,乌鲁木齐 830054
肾血管平滑肌脂肪瘤(renal angiomyolipoma,RAML)又称肾错构瘤,是肾脏最常见的良性肿瘤,其发病率低,多见于女性[1]。对于巨大肾错构瘤(≥8 cm)患者来说[2],以双侧多发较为常见。由于肿瘤巨大,丢肾的风险高,术后长期肾功能丢失带来的问题不容忽视,因此行保留肾单位手术意义重大。现将新疆医科大学第一附属医院泌尿外科中心2015年1月至2022年6月收治的35例巨大肾错构瘤行保留肾单位手术经验总结报告如下。
1 资料与方法
1.1临床资料 回顾性收集新疆医科大学第一附属医院泌尿外科中心2015年1月至2022年6月收治35例肾错构瘤患者的资料。纳入标准:(1)经肾脏增强CT确诊为肾错构瘤。(2)肿瘤直径较大且行手术治疗。排除标准:(1)结节性硬化症(tuberous sclerosis complex,TSC)相关的肾错构瘤。(2)合并其他肿瘤及并发症。(3)合并急性出血。35例患者中男7例,女28例;年龄18~78岁,平均43.6岁。10例在体检时发现,无明显症状,腰痛21例,腹痛1例,血尿2例,尿路刺激症状4例。右肾12例(肾上极2例,肾中上极2例,肾中部3例,肾中下极3例,肾下极2例),根据影像学特点将肿瘤分为3类:部分外凸(肿瘤突出肾脏表面<50%,见图1ⓐ)3例,大部分外凸(肿瘤突出肾脏表面50%~70%,见图1ⓑ)7例,完全外凸(肿瘤突出肾脏表面>70%,见图1ⓒ)2例。左肾23例(肾上极5例,肾中上极5例,肾中部2例,肾中下极6例,肾下极5例),其中部分外凸5例,大部分外凸14例,完全外凸4例。左侧多发3例,右侧多发4例,双侧多发9例。35例肿瘤直径8~24.5 cm,平均11.34 cm,其中8~<10 cm 16例,≥10~12 cm 9例,>12 cm 10例。所有患者术前完善超声及泌尿系CT增强检查,临床诊断为巨大肾错构瘤。术前血肌酐为37.52~104.75(61.80±13.75)μmol/L。术前24例行肾脏发射计算机断层扫描(emission computed tomography,ECT)分肾功能测定检查,患侧肾脏肾小球滤过率(glomerular filtration rate,GFR)为32.7~62.9(51.60±5.70)mL·min-1·(1.73 m2)-1。经腹途径开放保留肾单位手术22例,经腹途径腹腔镜保留肾单位手术13例。所有研究对象知情同意。
1.2治疗方法
1.2.1 经腹途径开放保留肾单位手术 患者全麻后取平卧位,根据肿瘤大小和位置,取肋缘下切口或患侧“L”型切口。逐层切开进入腹腔完全显露肿瘤和肾脏,右侧将十二指肠后腹膜部分游离牵开防止损伤。肿瘤附近一般有比较粗大的异常静脉,要仔细结扎防止出血。游离肾动静脉备用,分离输尿管,牵引吊起。小心游离右侧腔静脉及生殖静脉防止损伤。若肿瘤位于肾门附近,要明确肿瘤和肾血管的解剖关系,防止肾门部位大血管损伤。阻断肾蒂血管,将肿瘤大部分切除,使用吸引器去除创面残留的肾错构瘤组织。仔细检查基底部是否有集合系统损伤以及明显的出血血管。对于肾门肿瘤或部分外凸型肿瘤,一定仔细检查肾窦内是否有供应肿瘤的血管,仔细结扎,防止漏扎引起术后出血。若发现肾窦内较大的动静脉损伤,应使用适当滑线给予精准缝合,并使用100 W电刀喷凝处理肾脏实质以减少出血,之后使用2-0倒刺线连续缝合肾实质创面。若肿瘤位于肾门附近,不易缝合创面或肿瘤主体完全位于肾窦内,将肾脏完全分成两部分,肿瘤切除后创面不能完全对合,可采用肾实质边缘连续锁边缝合,使创面敞开。创面缝合无误后,清除积血,松开阻断钳,观察是否有出血,若发现出血给予缝合止血,确定无误后放置引流管,手术完成。
1.2.2 经腹途径腹腔镜保留肾单位手术 全麻健侧半卧位(60°~70°)。采用Harson技术放置第一个Trocar,在脐旁经腹直肌纵行切口约5 cm,逐步切开皮下组织、腹直肌外鞘,钝性分离腹直肌直达后鞘,在后鞘上做荷包缝合,在荷包中央打开后鞘及腹膜,置入10 mm Trocar并固定防止漏气。在腹腔镜监视下,以肾脏和肿瘤为中心,在患侧锁骨中线肋缘下2 cm处置入10 mm Trocar 1个,在腋前线水平髂前上棘上2 cm处置入10 mm Trocar 1个。根据需要可以增加第4个5 mm Trocar ,用于挑起肝脏和牵开肠道以增加显露。游离肾下极及输尿管,若肿瘤位于肾脏下极,应同时游离肿瘤。若肿瘤位于上极或背侧,要将肾脏完全游离旋转,使肿瘤充分暴露于术野中;若肿瘤位于下极或腹侧易暴露位置,可仅游离肿瘤及其周围足够缝合的肾实质范围。其余处理同经腹途径开放保留肾单位手术,若术中发现肾表面多发小肿瘤,同期处理。
1.3观察指标 手术时间、出血量、开放手术冷缺血时间、腹腔镜手术热缺血时间、术后3~5 d血肌酐、术后拔管时间、术后住院时间、术后并发症及预后情况等。
1.4随访方式 门诊或住院定期复查,术后3个月第一次随访,之后每6~12个月复查一次。随访内容:肾功能、血常规、尿常规、泌尿系B超。B超肾功能异常时需复查泌尿系CT及肾脏GFR。
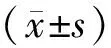
2 结果
本组35例手术均顺利完成,腹腔镜手术者无中转开放手术,无破裂出血。手术时间为65~265(139.82±54.94)min,出血量为20~1 100(279.72±310.42)mL。22例开放手术冷缺血时间为15~65(36.43±13.92)min,13例腹腔镜手术热缺血时间为20~40(26.47±4.96)min。术后3~5 d内复查血肌酐为36~110(69.99±17.54)μmol/L。术后拔管时间为3~11(4.84±1.63)d,术后住院时间为4~12(6.71±1.73)d。术后随访3~87(46.16±26.97)个月,肾功能均正常且未见肿瘤复发。术后18例行肾脏ECT分肾功能检查,患侧肾脏GFR为28.7~57.6(37.38±8.15)mL·min-1·(1.73 m2)-1,见表1。3例开放手术发生创面上较大静脉出血(>1 000 mL),经缝合、使用止血胶后止血,给予输血处理;2例术后因感染发热,体温最高39.5 ℃,经抗感染、补液等对症治疗后治愈。其余患者术后恢复良好。
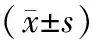
表1 35例患者手术资料
3 讨论
3.1肾错构瘤是肾脏良性肿瘤最常见的类型[3]。保留肾单位手术是肾错构瘤首选术式[4-5]。一侧肾切除1年后对侧肾功能约下降33%。Laguna[6]经过6.7年随访发现一侧肾切除术后对侧肾发生肾功能不全[估算肾小球滤过率(estimated glomerular filtration rate,eGFR)<60 mL·min-1·(1.73 m2)-1]的比例为85.7%,eGFR<30 mL·min-1·(1.73 m2)-1比例为10.0%。多项研究表明肾功能不全患者会增加非癌症特异性死亡率及心血管疾病发生率[7]。因此,保留肾单位手术对良性肾错构瘤患者来说意义重大。
3.2根据笔者经验总结,巨大肾错构瘤保留肾单位手术具有以下适应证:(1)肿瘤属于大部分外凸或完全外凸型,肿瘤基底部较宽位置表浅,与周围组织结构清晰利于操作。若肿瘤属于部分外凸型,则需要术前仔细评估术后患者残余肾实质发生肾功能不全或肾萎缩的概率。Ochoa-Arvizo等[8]研究发现肾部分切除术后患者发生肾功能不全的概率为64.7%。Thompson等[9]发现肾部分切除术后残余肾实质每增加5%,术后患者发生4期慢性肾脏病的风险减少17%。(2)肿瘤位于肾上极、下极、腹侧等较易处理的位置,未侵犯肾门大血管。(3)双侧多发肿瘤。双肾功能已受到不同程度的影响,且患者年龄年轻,随着时间推移,对侧肾肿瘤有逐渐增大、再次手术的风险。(4)孤立肾或对侧肾功能低下是保留肾单位手术的绝对适应证。
3.3近年来研究发现,对于经验丰富的医师来说,腹腔镜手术方式可取得不错的效果[10-11]。对于完全外凸型及部分、大部分外凸型相对较小的肿瘤,若肿瘤位于肾脏腹侧及腹侧外侧缘且容易分离,可以选择经腹途径腹腔镜保留肾单位手术。随着机器人辅助腹腔镜手术发展迅速,其在巨大肾错构瘤手术中占有重要地位[12-13]。术前通过血管造影(computed tomography angiography,CTA)明确肿瘤血供及解剖位置,腹腔镜下高选择性肾动脉阻断肾部分切除术亦可以取得较好的结果[14]。此外,热缺血时间亦是一个不容忽视的指标,一般认为热缺血时间>30 min则会影响患者预后[15]。根据自身腹腔镜手术的熟练程度及术前影像、检验资料估计术中热缺血时间,若<30 min则考虑选用腹腔镜手术。本组13例接受经腹途径腹腔镜保留肾单位手术,肿瘤直径平均为9.8 cm,部分外凸3例,大部分外凸6例,完全外凸4例。位于腹侧7例,外侧3例,肾门腹侧3例。术前血肌酐为(60.84±10.62)μmol/L,术后血肌酐为(66.63±9.22)μmol/L,热缺血时间为(26.47±4.96)min,均取得较好结果。
3.4经腹开放手术适用于肿瘤直径相对较大、与周围组织器官密切相关或肿瘤侵入肾实质较多的肿瘤,面对术中各种突发状况更易应对。对于开放手术而言,其优势是可以采用冷缺血技术。有研究表明,肾脏冷缺血时间<60 min行保留肾单位手术能最大限度地降低对残肾肾功能的影响[16]。本组22例接受开放保留肾单位手术患者的肿瘤直径平均为12.4 cm。部分外凸5例,大部分外凸15例,完全外凸2例。其中8例肿瘤凸入肾门、突出肾包膜外,肿瘤切除后将肾脏分为两部分。位于腹侧9例,外侧5例,背侧2例,肾门侧6例。其中位于肾门侧2例和腹侧1例与周围组织粘连较严重。术前血肌酐为(62.36±15.26)μmol/L,术后血肌酐为(71.98±20.70)μmol/L,均在正常范围,冷缺血时间为(36.43±13.92)min。开放保留肾单位手术效果良好。
3.5巨大肾错构瘤保留肾单位手术技巧也是关键的一环:(1)分离出肾动静脉备用,因肿瘤体积大,术中难免对瘤体造成挤压导致破裂出血,影响手术视野,延长手术时间。若发现出血较多,及时阻断肾门血管。(2)若肿瘤位于背侧肾门或不易显露的位置,应先完全游离肾脏使其可以随意旋转达到易操作部位。若肿瘤位于易显露位置则只需暴露部分正常肾实质用于切除后的缝合。(3)若肿瘤与肾主干血管关系密切,应使用小组织剪沿肾主干血管向肾窦内小心分离,避免损伤。(4)肾血管阻断后,快速将肿瘤从正常肾实质表面切除,靠近肾窦的位置应尽量采用吸引器吸除肿瘤。(5)肿瘤吸除后创面往往有小动脉出血,应使用单层肾实质缝合充分止血。除此之外,结合文献学习,笔者认为还需要注意以下几点:(1)Trocar的放置要尽量远离肿瘤,同时在建立手术空间时不要注入过多空气,以防止压迫肿瘤出血。(2)在肾动脉旁放置一条纱布作标识,利于肿瘤破裂出血时及时找到肾动脉并夹闭止血。(3)手术过程中若发生破裂出血,切勿在破口处反复止血,否则可能导致破口增大,应及时阻断肾动脉,迅速清除瘤体[5]。(4)肾门部肿瘤毛细血管更为丰富,操作空间也更小,不宜缝合止血,使用止血棉填塞止血最佳。
3.6腹腔镜保留肾单位术后并发症发生率为10%~25%[17],主要表现为出血、尿瘘、急性肾衰及感染等。腹腔镜保留肾单位手术中转根治性肾切除术发生率为0~0.03%[18]。开放保留肾单位手术术后并发症发生率为10%~13%,较腹腔镜手术低。本组35例患者中,3例开放手术发生术中大出血(>1 000 mL),经缝合、输血后患者好转;2例术后因感染发热,体温最高39.5 ℃,经抗感染、补液等对症治疗后治愈。其余患者术后恢复良好。研究发现手术切缘沿错构瘤包膜进行,对肾功能起到极大的保护作用[11],因此,对巨大肾错构瘤更应开展保留肾单位手术。
综上所述,巨大肾错构瘤保留肾单位手术在技术成熟的中心是安全可行的。术者应根据患者术前资料、术者经验选择合适的手术方案,运用得当的手术技巧可为患者带来巨大收益。

