甲维盐@海藻酸纳米颗粒制备及缓控释性能研究
侯晓君, 马林*, 邹沛禹, 陈利标, 卢瑞, 张敏
(1.广西大学 化学化工学院, 广西 南宁 530004;2.广西田园生化股份有限公司, 广西 南宁 530007)
0 引言
粮食安全是社会稳定、经济发展和国家安全的基石。随着世界各国经济的发展,人口增加和耕地减少的事实迫使人们大量使用各种农药来提高农作物单产,以缓解粮食安全与资源短缺之间的矛盾,但是农药广泛用于防治病虫草害的同时,也带来了污染、残毒及抗药性等严重问题[1-3]。传统的施药方式造成的农药流失和分解十分严重,研究显示,杀虫剂在实际应用中仅有不到0.1%的有效成分可以到达靶点害虫[4-5]。
农药缓控释是减少农药用量及其环境影响的重要策略。在过去的十几年中,纳米材料的应用极大推动了农药缓控释技术的发展。纳米材料尺寸小、比表面积大的特点有助于增强农药的分散性、可湿性以及与靶点害虫的亲和力,减少使用有机溶剂的风险。把农药活性成分负载于纳米载体不仅可以保护农药活性成分免受高温和光照的影响,增强其化学稳定性,而且纳米颗粒易于通过胞吞作用进入细胞,纳米农药剂型具有比传统剂型更高的药效[6-8]。同时,根据农药的作用机制和应用要求选择结构性质不同的载体材料构建刺激响应型(如pH敏感、温度敏感)剂型,可以实现农药的可控释放,对减少农药的用量及其对环境的影响非常有利[9-14]。
把农药活性成分包埋于高分子基材是最重要的农药缓控释制剂制备技术。海藻酸(alginate,Alg)是由D-甘露糖醛酸和L-古罗糖醛酸结构单元构成的天然高分子多糖,来源丰富,价格低廉,并具有良好的生物相容性和可降解性。海藻酸易于通过Ca2+、Mg2+等二价金属离子的交联作用形成凝胶,非常适合于敏感药物包封,并且羧基的电离作用具有pH敏感性,是当前研究最广泛的缓释剂基材之一[15-16]。
甲氨基阿维菌素苯甲酸盐(甲维盐,emamectin benzoate,EB)是阿维菌素的衍生物,是一种高效、低毒和高选择性抗生素类杀虫、杀螨剂,但其大环内酯结构在紫外光照射下易于发生分解,为了延长持效期而重复施药,不仅需要增加使用成本,而且对作物生长和环境安全造成影响。利用木质素[9]、壳聚糖[10]、玉米醇溶蛋白[11]、纤维素[12]等天然高分子材料和聚多巴胺[13]、聚琥珀酰亚胺[14]等合成高分子制备纳米颗粒,不仅可延缓甲维盐的释放,而且可减少光解,对于减少甲维盐用量和延长持效期非常有利,但是目前国内外制备纳米制剂过程中普遍大量使用各种助剂和有机溶剂,并采用高速剪切、超声波、超高速离心分离等高能耗辅助技术,对纳米农药的规模化生产和应用造成了较大的制约。
本研究工作利用甲维盐在水和甲醇中溶解性的差异、以溶剂扩散法制备甲维盐纳米颗粒,并包裹海藻酸制备纳米缓释剂,应用动态光散射技术(dynamic light scattering, DLS)、ζ-电位测定和透射电镜(transmission electron microscope, TEM)分析海藻酸浓度、交联剂CaCl2浓度等工艺条件对甲维盐@海藻酸纳米颗粒的粒径Dh、ζ-电位、甲维盐包封率PEE和载药率PLE的影响,研究纳米颗粒的结构形貌、介质pH对甲维盐释放行为的影响和机制,为甲维盐纳米缓释剂型的开发和应用提供理论和实验依据。
1 实验
1.1 试剂和仪器
实验用试剂包括:海藻酸,中黏度,Sigma公司;甲维盐原药,广西田园生化股份有限公司;无水氯化钙、甲醇,AR,广东光华科技股份有限公司;实验所用水为去离子水。
实验用仪器包括:傅里叶变换红外光谱仪FTIR(Nicolet iS10型,Thermo Fisher Scientific Inc.公司);粒度电位测定仪(Malvern Zetasizer ZSE型,帕纳利塔尔有限公司);高分辨透射电镜TEM(F200型,日本电子株式会社);紫外-可见分光光度计(UV-2600型,Shimadzu公司)。
1.2 方法
1.2.1 制备甲维盐纳米颗粒
甲维盐溶于甲醇配置系列质量浓度为5~200 mg/mL的溶液,取1 mL混合溶液搅拌条件下缓慢加入到49 mL水中(甲维盐最终质量浓度为0.1~4.0 mg/mL),继续搅拌30 min,得到甲维盐纳米颗粒。为了了解甲醇对甲维盐纳米颗粒的影响,取1 mL质量浓度为5 mg/mL的甲维盐溶液,搅拌条件下缓慢加入到49 mL甲醇-水混合溶剂中(甲醇与水体积比分别为1∶48、 2∶47、 4∶45)。
1.2.2 制备甲维盐@海藻酸纳米颗粒
取1 mL质量浓度为5 mg/mL的甲维盐甲醇溶液,搅拌条件下缓慢加入到44 mL海藻酸溶液后,缓慢加入5 mL CaCl2溶液,继续搅拌30 min,得到甲维盐@海藻酸纳米颗粒分散液。空白海藻酸纳米颗粒按类似方法制备,具体工艺条件见表1。所得空白海藻酸纳米颗粒和甲维盐@海藻酸纳米颗粒分别命名为AlgxCay、EB@AlgxCay,x、y分别为制备时溶液中海藻酸、CaCl2的终质量浓度。
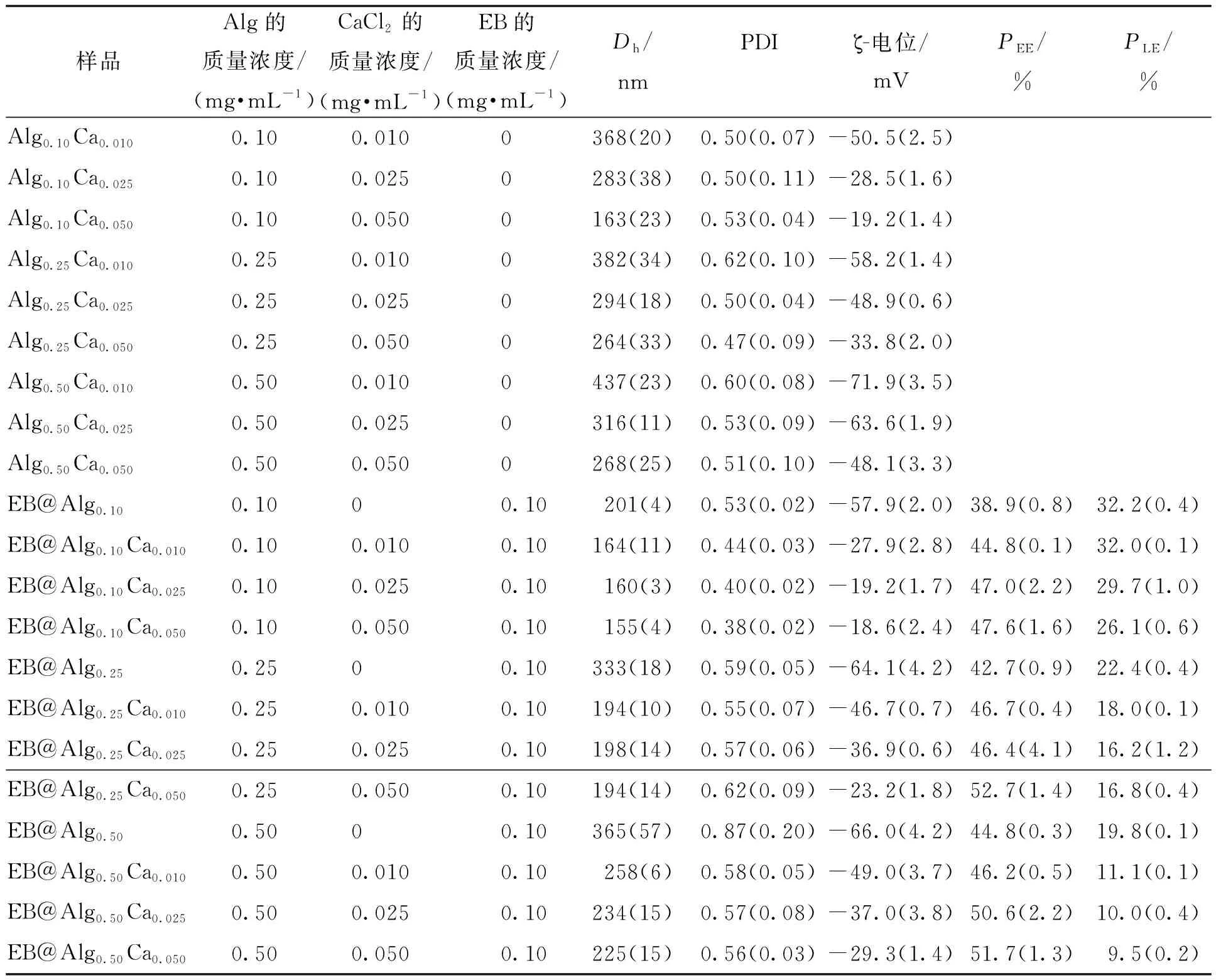
表1 空白海藻酸纳米颗粒和甲维盐@海藻酸纳米颗粒制备条件和Dh、多分散性指数(polydispersity index, PDI)、ζ-电位、PEE和PLETab.1 Formulations and hydrodynamic diameter Dh, polydispersity index PDI, ζ-potential, encapsulation efficiency PEE and loading efficiency PLE of Alg nanoparticles with and without EB
1.2.3 FTIR
空白海藻酸纳米颗粒和甲维盐@海藻酸纳米颗粒分散液取样在转速为50 000 r/min条件下离心40 min,去除上清液,所得固体重新分散在少量的水后冷冻干燥,所得纳米颗粒与KBr按质量比约2∶100混合均匀、研磨后压片,利用傅里叶变换红外光谱仪测定FTIR,波数扫描范围为500~4 000 cm-1,分辨率为4 cm-1。
1.2.4Dh和ζ-电位测定
采用粒度电位测定仪测定甲维盐纳米颗粒、空白海藻酸纳米颗粒和甲维盐@海藻酸纳米颗粒的Dh和ζ-电位。每个样品在相同条件下重复测定5次,分别计算Dh、ζ-电位和PDI的平均值。
1.2.5 TEM
甲维盐纳米颗粒、空白海藻酸纳米颗粒和甲维盐@海藻酸纳米颗粒分散液稀释后利用磷钨酸染色10 min,取少量样品滴在铜网上,于空气中干燥后利用高分辨透射电镜观察颗粒表观形貌。
1.2.6 甲维盐浓度测定
利用紫外-可见分光光度计测定溶液中甲维盐在245 nm的吸光度,标准工作曲线法确定溶液中甲维盐的含量。
1.2.7PEE与PLE的测定
称取一定量的甲维盐@海藻酸纳米颗粒分散液,于转速50 000 r/min条件下离心40 min,收集上清液,固体颗粒冷冻干燥后称重。利用紫外-可见分光光度计测定245 nm处上清液的吸光度,计算溶液中未包封甲维盐的含量mF、PEE和PLE:
PEE=(mT-mF)/mT×100%,
(1)
PLE=(mT-mF)/mN×100%,
(2)
式中:mT为甲维盐的投药量;mN为制备所得甲维盐@海藻酸纳米颗粒总质量。
1.2.8 甲维盐释放
量取5 mL甲维盐@海藻酸纳米颗粒分散液装入透析袋(截留分子质量为14 000 Da)中,浸没在体积分数为10%甲醇-水混合溶剂中,磁力搅拌下进行释放。在设定的时间点取5 mL释放介质,同时补加等体积的介质。利用紫外-可见分光光度计测定样品中甲维盐含量,计算得到甲维盐累积释放曲线。
2 结果与讨论
2.1 甲维盐纳米颗粒制备和表征
溶剂扩散法是制备纳米颗粒的常用方法。甲维盐在水中的溶解度较低,但是在甲醇中具有较好的溶解度,因此,把甲维盐预溶于甲醇,利用甲醇在水中的扩散稀释制备纳米颗粒。实验发现,搅拌速率对甲维盐纳米颗粒的制备无明显作用,强烈搅拌反而使溶液中产生大量泡沫,因此,本文采取在低速磁力搅拌条件下,研究甲维盐质量浓度、溶剂中甲醇的质量浓度对Dh、ζ-电位的影响,不同质量浓度的EB、甲醇-水混合溶剂制备所得EB纳米颗粒的Dh、ζ-电位和PDI分别见表2、表3。不同质量浓度的EB制备所得纳米颗粒的粒径分布如图1所示。从表2和图1可见,低浓度(ρEB≤1.00 mg/mL)甲维盐在水中形成粒径分布均匀的纳米颗粒(PDI≤0.22),粒径约为68 nm,ζ-电位为20.5~30.7 mV,甲维盐质量浓度的增大对平均粒径无明显影响,而ζ-电位略有增大。随着EB质量浓度的进一步增大,甲维盐纳米颗粒粒径分布在约25 nm和90 nm附近呈双峰特征,平均粒径急剧减小,PDI显著增大。从表3可见,在实验所采取的甲醇体积分数范围内(2%~8%),利用溶剂扩散法都可以形成粒径均匀的甲维盐纳米颗粒,其PDI<0.20,甲醇体积分数增大对甲维盐纳米颗粒粒径影响不大,但是ζ-电位略有增大,说明溶剂中添加少量的甲醇促进了甲维盐的电离。

表2 不同质量浓度EB制备所得纳米颗粒的Dh、ζ-电位和PDITab.2 Hydrodynamic diameter Dh, ζ-potential and PDI of EB nanoparticles prepared at different concentrations

表3 不同用量甲醇-水混合溶剂中制备所得EB纳米颗粒的Dh、ζ-电位和PDITab.3 Hydrodynamic diameter Dh, ζ-potential and PDI of EB nanoparticles prepared in methanol-water mixtures with different methanol concentrations
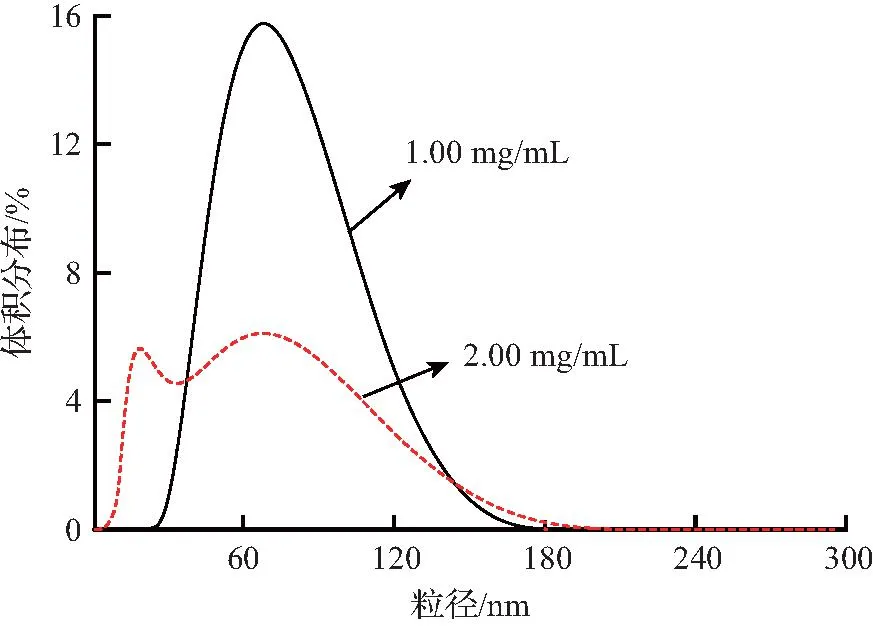
图1 不同质量浓度的EB制备所得纳米颗粒的粒径分布Fig.1 Size distribution of EB nanoparticles prepared at different concentrations
2.2 甲维盐@海藻酸纳米颗粒制备和表征
从表2、表3可见,由于甲维盐纳米颗粒表面分子的电离而带正电荷,而海藻酸分子链上的羧基在水中部分电离而带负电荷,因此可以通过静电作用与海藻酸形成复合纳米颗粒。根据表2和表3实验结果和甲维盐的实际使用量(1~2 g/km2,以10~20 L水溶解稀释后叶面喷施),本文采取甲维盐最终质量浓度为0.10 mg/mL的条件下利用溶剂扩散法在海藻酸溶液中制备甲维盐@海藻酸纳米颗粒,研究海藻酸和交联剂CaCl2浓度对纳米颗粒结构和甲维盐释放的影响。
2.2.1Dh和ζ-电位分析
甲维盐@海藻酸纳米颗粒的Dh和ζ-电位结果见表1,为方便比较,表1中同时给出了相同条件下制备的空白海藻酸纳米凝胶颗粒的测定结果。从表1中可以看出,在无交联剂CaCl2的条件下,海藻酸溶液中检测不到颗粒或聚集体的存在。与甲维盐纳米颗粒相比,甲维盐@海藻酸纳米颗粒的Dh明显增大,ζ-电位转变为负值,并且Dh和ζ-电位负值随着海藻酸质量浓度的增加而增大,说明海藻酸分子与甲维盐纳米颗粒形成静电结合。
海藻酸分子链易于通过L-古罗糖醛酸结构单元上的羧基与二价金属离子(如Ca2+和Mg2+)交联形成凝胶或者聚集形成颗粒[15]。由表1可以看到,空白海藻酸纳米颗粒的Dh和ζ-电位的负值随着CaCl2质量浓度的增大而逐步减小;在CaCl2质量浓度相同的情况下,海藻酸纳米颗粒的Dh和ζ-电位的负值随着溶液中海藻酸浓度的增大而增大。甲维盐@海藻酸纳米颗粒的Dh和ζ-电位也有相类似的变化规律,但是,CaCl2质量浓度相同的甲维盐@海藻酸纳米颗粒的Dh和ζ-电位负值与空白海藻酸纳米颗粒相比明显减小,说明甲维盐@海藻酸纳米颗粒表面的海藻酸分子链由于Ca2+的交联作用形成更紧密的结构。
2.2.2 FTIR分析

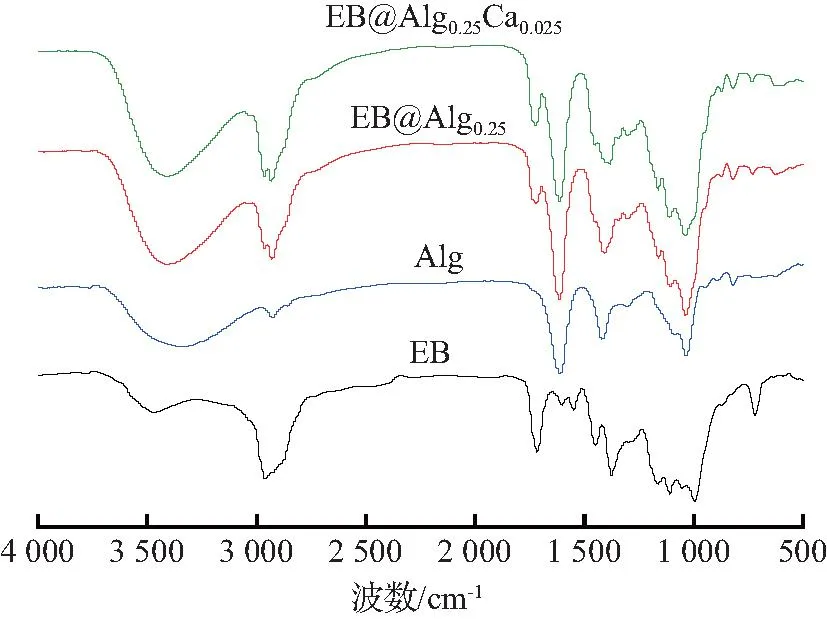
图2 EB纳米颗粒、Alg纳米颗粒和EB@Alg纳米颗粒FTIR谱图Fig.2 FTIR Spectra of EB, Alg and EB@Alg nanoparticle
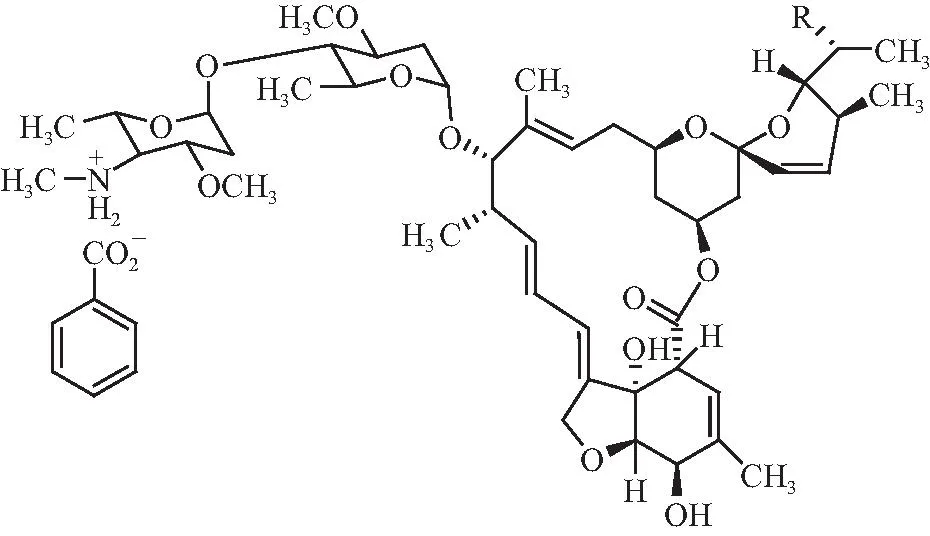
图3 甲维盐分子结构Fig.3 Chemical structure of EB
2.2.3 TEM分析
利用TEM分析了甲维盐纳米颗粒、空白海藻酸纳米颗粒、交联和未交联的甲维盐@海藻酸纳米颗粒的表观形貌。纳米颗粒典型TEM图像如图4所示。由图4可见,利用溶剂扩散法可以在水中制备得到分散良好的甲维盐纳米颗粒,其粒径为50~90 nm,与DLS分析结果吻合。甲维盐纳米颗粒在海藻酸溶液中发生不同程度的聚集,较好地解释了甲维盐@海藻酸纳米颗粒与甲维盐纳米颗粒相比粒径和PDI增大的现象(表1)。甲维盐@海藻酸纳米颗粒在CaCl2溶液中形成聚集体,其边缘处清晰可见粒径约为60 nm的颗粒,与海藻酸分子在CaCl2溶液中形成的无规则团聚体具有明显区别,说明甲维盐@海藻酸纳米颗粒表面吸附的海藻酸分子通过Ca2+的交联作用产生团聚。

(a) EB

(b) EB@Alg0.025

(c) Alg0.25Ca0.025

(d) EB@Alg0.25Ca0.025图4 纳米颗粒典型TEM图像Fig.4 Typical TEM images of nanoparticles
2.3 PEE和PLE测定结果分析
从表1可见,在实验所采用的工艺条件下制备纳米颗粒,甲维盐的PEE较小,在未交联的情况,甲维盐的PEE为38.9%~44.8%,所得纳米颗粒中甲维盐PLE为32.2%~19.8%。这一情况与甲维盐在水中的溶解以及海藻酸对甲维盐的吸附有关,分析结果显示,室温下甲维盐在水中形成饱和溶液时质量浓度约为42 mg/L。同时,海藻酸分子链在甲维盐纳米颗粒表面的结合是动态的平衡过程,溶液中游离的海藻酸分子链通过静电作用与甲维盐形成的复合物难以通过离心进行分离,从而使得甲维盐的PEE减小。
海藻酸用量对甲维盐的PEE、PLE具有双重影响。在无交联的情况下,海藻酸质量浓度的增大将使得溶液中游离海藻酸的增加,不利于甲维盐PEE的提高,但是,表1结果显示,增加海藻酸质量浓度使得甲维盐的PEE略有增大,这一结果可能与以下2方面的原因有关:①海藻酸分子在甲维盐纳米颗粒表面的吸附量增加,增加了甲维盐在颗粒表面海藻酸分子上的吸附量;②海藻酸分子链上的羟基和羧基与水分子的氢键作用弱化了甲维盐的水化作用及减小了其在水中的溶解度。与PEE的变化相反,甲维盐在纳米颗粒中的PLE随着海藻酸质量浓度的增大而逐步减小,说明甲维盐@海藻酸纳米颗粒壳层的海藻酸分子的增加与PLE的变化相比更为明显。
Ca2+的交联对甲维盐的PEE、PLE也有明显影响。由TEM分析可知,海藻酸分子链易于通过Ca2+的交联形成聚集体,使得分子链上吸附的甲维盐在离心操作中得以分离,甲维盐的PEE增大;然而,Ca2+与海藻酸分子上羧基的结合与甲维盐形成吸附竞争,因此,由表1结果可见,甲维盐的PLE随着CaCl2的质量浓度增大而减小。
2.4 释放动力学
甲维盐在水中的溶解度较小,为了更好地体现甲维盐@海藻酸纳米颗粒的释放性能,本文中在体积分数为10%的甲醇-水混合溶剂中测定甲维盐的累积释放曲线,同时给出了空白甲维盐纳米颗粒在相同条件下的溶解动力学曲线。海藻酸质量浓度对甲维盐从未交联和交联甲维盐@海藻酸纳米颗粒的释放动力学的影响分别如图5、图6所示。从图5可见,空白甲维盐纳米颗粒在甲醇-水混合溶剂中快速释放,36 h累积释放率达到74.7%。海藻酸包覆显著延缓了甲维盐的释放,海藻酸质量浓度分别为0.10、0.25、0.50 mg/mL时,甲维盐36 h的累积释放率分别为43.8%、35.1%、24.8%。

图5 EB从未交联Alg纳米颗粒的释放动力学Fig.5 Release kinetics of EB from Alg-based nanoparticles without crosslinking

图6 EB从CaCl2交联Alg纳米颗粒的释放动力学Fig.6 Release kinetics of EB from CaCl2 crosslinked Alg-based nanoparticles
药物或者农药从海藻酸基材的释放一般为扩散释放机制,与基材的通透性及其与活性分子的相互作用有关,基材通透性下降和相互作用增强有利于获得更强的缓释性能[17-18]。海藻酸分子通过Ca2+和Mg2+交联形成三维网络结构,有利于降低基材的通透性[15-16]。由动态光散射结果可知,甲维盐@海藻酸纳米颗粒经Ca2+交联后粒径减小(表1),说明海藻酸分子在纳米颗粒表面形成更紧密的结构。然而,从图6可见,Ca2+交联实际上加快了甲维盐从纳米颗粒的释放,海藻酸质量浓度分别为0.10、0.25、0.50 mg/mL的甲维盐@海藻酸纳米颗粒分散液中加入0.025 mg/mL的CaCl2时,甲维盐36 h的累计释放率分别为67.4%、59.9%、34.2%。
为了分析甲维盐的释放机制,进一步比较了经不同浓度的CaCl2交联后的甲维盐@海藻酸纳米颗粒的释放动力学,CaCl2用量对EB从Alg纳米颗粒释放动力学的影响如图7所示。从图7可见,甲维盐的释放随着溶液中CaCl2质量浓度的增大而逐渐加快,说明Ca2+与海藻酸羧基的静电结合与甲维盐形成竞争,削弱了甲维盐与海藻酸的相互作用,从而加快了甲维盐的扩散释放。
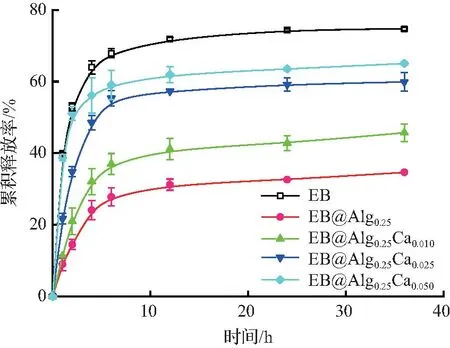
图7 CaCl2用量对EB从Alg纳米颗粒释放动力学的影响Fig.7 Influence of CaCl2 on EB release from Alg-based nanoparticles.
海藻酸分子中的羧基基团在水中部分解离,其解离度与介质的pH值有关,使得海藻酸材料的药物释放性能表现出一定的pH值敏感性。为了研究pH值对甲维盐从纳米颗粒释放的影响,本文中测定了未交联甲维盐@海藻酸纳米颗粒在不同pH值的NaH2PO4-柠檬酸钠缓冲溶液中的释放动力学,结果如图8所示。
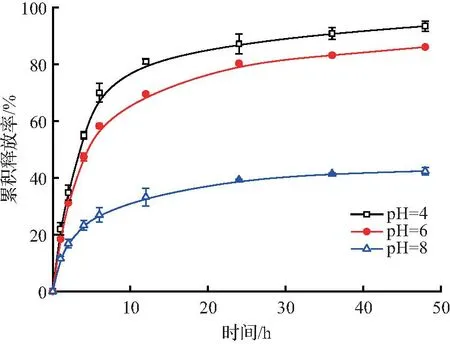
图8 介质pH值对EB从Alg纳米颗粒的释放动力学的影响Fig.8 Influence of pH of the medium on EB release from Alg-based nanoparticles
海藻酸分子的羧基在碱性介质中解离度增大,不仅提高海藻酸分子的水化程度,而且增强了分子链之间的静电排斥作用,因此,介质pH值的增大通常导致海藻酸基材通透性的增强和药物释放的加快[19-20],然而,图8结果显示,介质pH值的增大延缓了甲维盐的释放,pH值为4、6、8时,甲维盐48 h的累积释放率分别为93.5%、86.1%、42.4%,说明甲维盐从海藻酸纳米颗粒的释放主要受活性分子与基材之间的相互作用的影响,在碱性介质中,海藻酸分子与甲维盐之间的相互作用因羧基解离度的增加而增强,从而获得更好的缓释性能。甲维盐的作用方式以胃毒为主,而胃液呈酸性,甲维盐@海藻酸纳米颗粒在酸性环境中释放加快,对提高农药药效、减少用量是非常有利。
3 结论
甲维盐在甲醇中具有良好的溶解度,预溶于甲醇的甲维盐在水中通过溶剂扩散分散形成粒径分布均匀的纳米颗粒。由于甲维盐纳米颗粒表面的分子发生电离而带正电荷,通过静电作用非常容易地与海藻酸形成复合纳米颗粒,其粒径和ζ-电位负值随着海藻酸质量浓度的增大而增大,但是因Ca2+的交联作用而减小。甲维盐在纳米颗粒中的负载与海藻酸、CaCl2质量浓度有关,增大海藻酸和CaCl2的质量浓度有利于提高甲维盐的PEE,但是减小了纳米颗粒中甲维盐的PLE。未交联的情况下,海藻酸质量浓度为0.10、0.25、0.50 mg/mL时,甲维盐的PEE分别为38.9%、42.7%、44.8%。
海藻酸包覆延缓了甲维盐的释放,甲维盐从甲维盐@海藻酸纳米颗粒的释放主要受到活性分子与基材的相互作用的影响,增加海藻酸质量浓度显著延缓了甲维盐的释放,海藻酸质量浓度分别为0.10、0.25、0.50 mg/mL时,甲维盐36 h的累积释放率分别为空白甲维盐纳米颗粒的58.6%、47.0%、33.2%,但是Ca2+与海藻酸羧基的静电结合与甲维盐形成竞争,削弱了甲维盐与海藻酸的相互作用,从而加快了甲维盐的扩散释放。甲维盐从海藻酸纳米颗粒的释放具有明显的pH敏感性,碱性介质中海藻酸分子与甲维盐之间的相互作用因羧基解离度的增大而增强,具有更好的缓释性能。

