奥希替尼序贯和吉非替尼治疗EGFR突变型晚期非小细胞肺癌近期生存获益的临床研究
张彭辉,边静,李佳佳
河南科技大学第一附属医院药品调剂科,洛阳 471003
肺癌是指起源于肺部支气管黏膜或腺体的恶性肿瘤,其发病率和死亡率高。据调查显示[1],非小细胞肺癌(non-small cell lung cancer,NSCLC)约占肺癌的80%。与小细胞肺癌相比,NSCLC 癌细胞生长分裂较慢,故扩散转移相对较晚,大多数患者就诊时已处于中晚期,错失早期手术根治机会,且患者放化疗效果不佳,导致其5 年生存率较低[2]。表皮生长因子受体(epidermal growth factor receptor,EGFR)突变为导致NSCLC 最主要的驱动因素[3-4],EGFR突变可激活EGFR信号通路,使肿瘤细胞不断增殖。现阶段,对于NSCLC 的治疗已转为针对驱动基因的精准化分子靶向治疗[5]。在分子靶向药物中,表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitors,EGFRTKIs)的临床应用最为广泛[6],其中代表药物为第一代靶向药吉非替尼。在晚期NSCLC 患者的临床治疗中,吉非替尼被推荐为一线治疗药物[7]。临床研究结果显示[8],NSCLC 患者在应用吉非替尼治疗6~12 个月后出现耐药现象,临床疗效随之降低,最终导致晚期NSCLC 进展。目前对EGFR突变型晚期NSCLC 患者尚未明确统一的标准化药物治疗方案。近年来,第三代EGFR-TKIs 奥希替尼已逐渐用于治疗NSCLC 患者。研究表明[9],奥希替尼可通过阻断EGFR活化突变和T790M突变,延长患者生存期和提高患者生活质量。但目前关于奥希替尼治疗吉非替尼耐药后EGFR突变型晚期NSCLC 患者的临床研究较少。基于此,本研究通过回顾性收集奥希替尼序贯治疗吉非替尼耐药后EGFR突变型晚期NSCLC 患者的临床资料,探讨其对临床疗效、生存质量等的影响,以期为临床治疗NSCLC 提供参考。现报道如下。
1 资料与方法
1.1 一般资料
回顾性收集2017 年7 月~2022 年7 月期间某院收治的150 例吉非替尼耐药后EGFR突变型晚期NSCLC 患者作为研究对象,在充分告知药物可能带来的获益、风险及药物治疗费用基础上,根据治疗方式不同将使用奥希替尼序贯治疗的患者纳入序贯组(n=78),使用吉非替尼治疗的患者纳入对照组(n=72)。序贯组:男性42 例,女性36 例;年龄45~78 岁,平均年龄(63.24±5.17)岁;体重指数(body mass index,BMI)19.6~27.4kg/m2,平均BMI(23.46±0.85)kg/m2;病程0.5~5 年,平均病程(2.73±0.45)年。对照组:男性39 例,女性33 例;年龄44~80 岁,平均年龄(63.95±5.24)岁;BMI 19.7~27.5kg/m2,平均BMI(23.39±0.74)kg/m2;病程0.7~5 年,平均病程(2.68±0.49)年。两组患者一般资料比较无统计学差异(P>0.05),具有可比性。本研究经医院伦理委员会审批通过,所有患者及家属对本研究均知情同意。
纳入标准:①符合《中华医学会肿瘤学分会肺癌临床诊疗指南》(2021 版)[10]中晚期NSCLC 诊断标准者。②经影像学及病理学检查评估,均为ⅢB或Ⅳ期NSCLC 者。③经基因检测,均为EGFR突变型者。④均已接受吉非替尼常规治疗,且出现耐药现象者。⑤年龄≥18 岁者。⑥临床资料完整者。
排除标准:①生存期<3 个月者。②同时接受其他放疗或免疫治疗方案者。③合并有其他恶性肿瘤者。④心、肝、肾功能障碍者。⑤存在认知障碍或精神类疾病,不能配合者。⑥对本研究中使用药物过敏,或不能耐受者。⑦因各种不明原因中途退出者。
1.2 研究方法
对照组患者予以吉非替尼片(Kagamiishi Plant,Nipro Pharma Corporation, 国药准字HJ20171297,规格0.25g)加量治疗:口服,初始剂量为250mg/次,qd,随后根据患者病情变化调整用量,每日最大剂量不超过1000mg。3 周为1 个疗程,连续治疗3 个疗程。序贯组患者予以甲磺酸奥希替尼片[AstraZeneca AB,国药准字HJ20170167,规格80mg(按C28H33N7O2计)]序贯治疗:口服,80mg/次,qd。3 周为1 个疗程,连续治疗3 个疗程。
1.3 观察指标
(1)临床疗效。根据RECIST 1.1 版[11]中的实体瘤评价标准评估两组患者的临床疗效:①完全缓解(complete response,CR):肿瘤病灶消失。②部分缓解(partial response,PR):肿瘤体积缩小≥50%。③疾病稳定(stable disease,SD):肿瘤体积缩小<50%或增大≤25%。④疾病进展(progressive disease,PD):肿瘤体积增大>25%或出现新病灶。治疗总有效率(%)=(CR+PR)例数/每组总例数×100%;生存获益率(%)=(CR+PR+SD)例数/每组总例数×100%。
(2)肿瘤标志物。分别于治疗前后采集患者清晨空腹肘静脉血3ml,采用M3250 台式低速离心机(长沙综仪生物科技有限公司,r=10cm),以3000r/min(4℃)离心 10min,留取上清液待检。采用酶联免疫吸附法检测两组患者血清癌胚抗原(carcinoembryonic antigen,CEA)、糖类抗原125(carbohydrate antigen 125,CA125)、糖类抗原199(carbohydrate antigen 199,CA199),严格按照试剂盒说明书操作。试剂盒购自瑞士罗氏公司。
(3)生存质量。分别于治疗前后使用生存质量核心问卷(quality of life core questionnaire-30,QLQ-C30)[12]评估两组患者的生存质量。QLQ-C30共有30 个条目,由功能量表和症状量表2 部分构成,2 个量表均为100 分。功能量表评分与生存质量呈正相关,即评分越高,表示患者的生存质量越高;症状量表评分与生存质量呈负相关,即评分越高,表示患者的生存质量越差。
(4)不良反应发生情况。观察记录两组患者治疗期间不良反应的发生情况,主要包括脱发、白细胞减少、胃肠道症状(包括恶心、呕吐、腹泻等症状)和肝肾功能异常等。
1.4 统计学方法
应用SPSS 21.0 软件对数据处理分析。计量资料以±s表示,采用t检验;计数资料以n(%)表示,采用χ2检验。P<0.05 为具有统计学差异。
2 结果
2.1 基线资料
两组患者性别、年龄、BMI、病程、卡诺夫斯凯计分(Karnofsky performance score,KPS)评分、病理分期、病理类型等基线资料比较均无统计学差异(P>0.05),具有可比性(表1)。
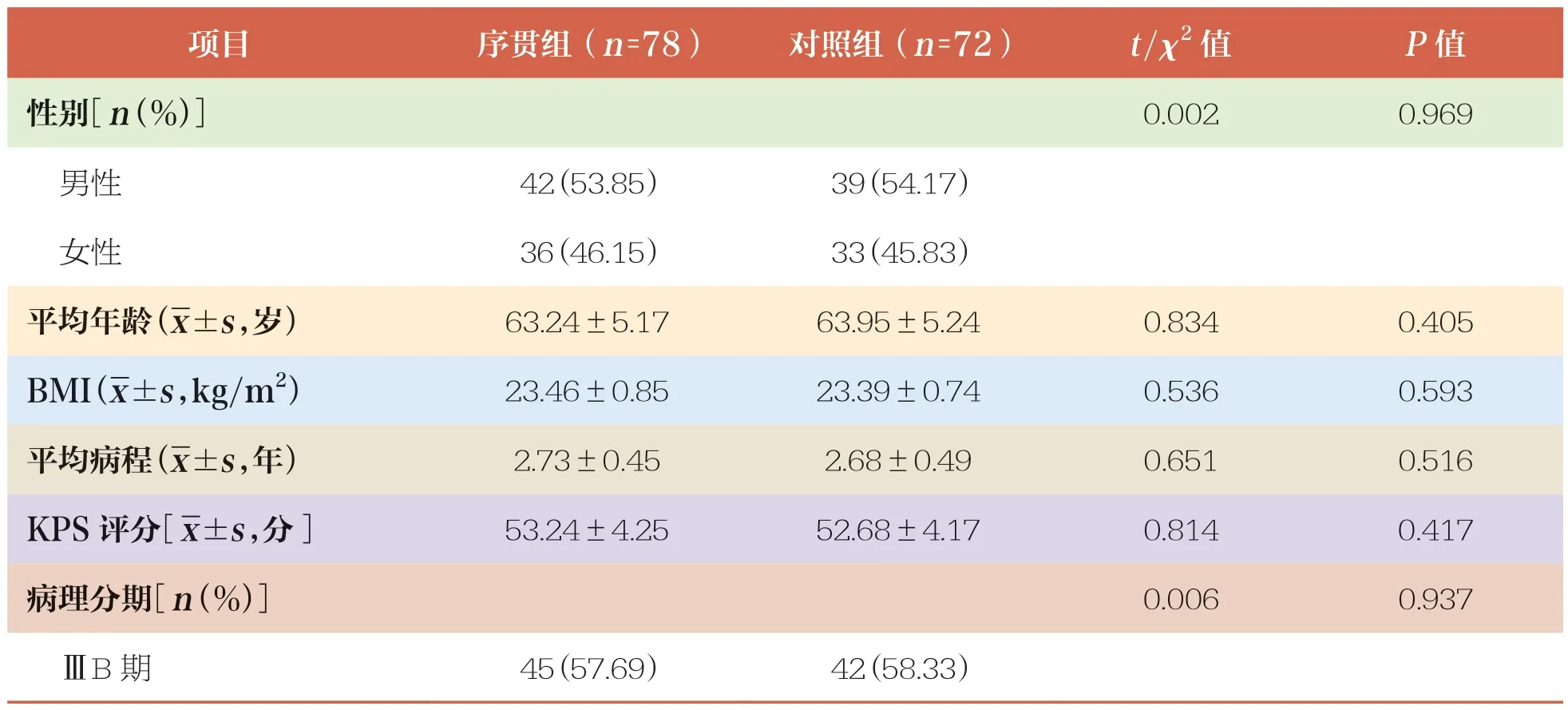
表1 两组基线资料比较
2.2 临床疗效
治疗后,序贯组治疗总有效率及生存获益率均高于对照组(P<0.05)(表2)。
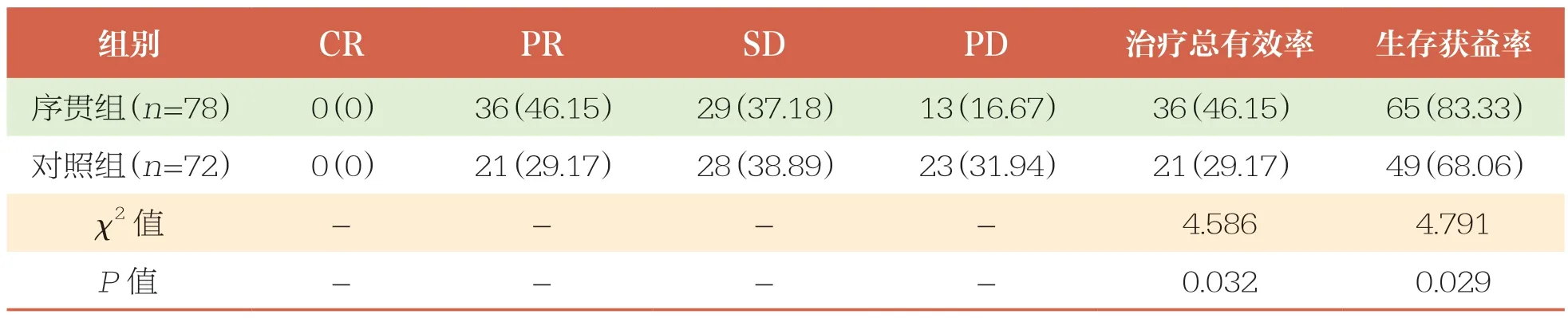
表2 两组临床疗效比较 n(%)
2.3 肿瘤标志物
治疗前,两组血清肿瘤标志物水平比较均无统计学差异(P>0.05)。治疗后,两组血清CEA、CA125、CA199 水平均降低(P<0.05),且序贯组低于对照组(P<0.05)(表3)。
表3 两组血清肿瘤标志物水平比较 ±s
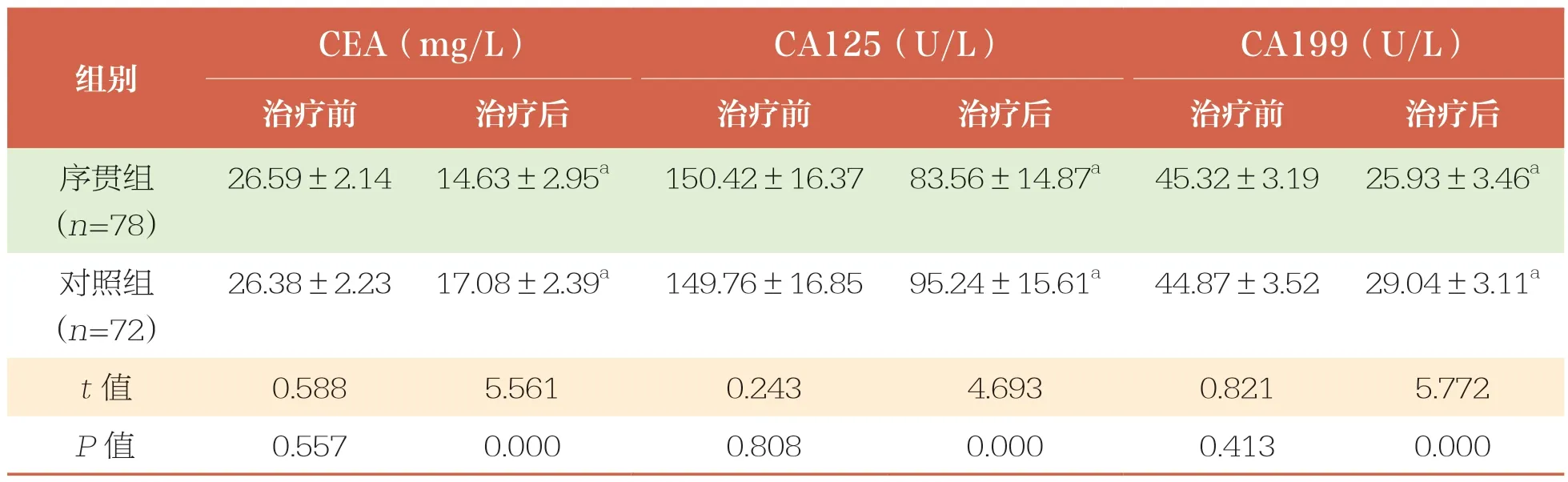
表3 两组血清肿瘤标志物水平比较 ±s
CEA:癌胚抗原;CA125:糖类抗原125;CA199:糖类抗原199;与同组治疗前比较,a:P<0.05。下同
CEA(mg/L)CA125(U/L)CA199(U/L)治疗前治疗后治疗前治疗后治疗前治疗后序贯组(n=78)组别26.59±2.14 14.63±2.95a150.42±16.37 83.56±14.87a45.32±3.19 25.93±3.46a对照组(n=72)26.38±2.23 17.08±2.39a149.76±16.85 95.24±15.61a44.87±3.52 29.04±3.11a t 值0.5885.5610.2434.6930.8215.772 P 值0.5570.0000.8080.0000.4130.000
2.4 QLQ-C30 评分
治疗前,两组QLQ-C30 评分比较无统计学差异(P>0.05)。治疗后,两组QLQ-C30 功能评分均升高(P<0.05),且序贯组高于对照组(P<0.05);两组QLQ-C30 症状评分均降低(P<0.05),且序贯组低于对照组(P<0.05)(表4)。
表4 两组QLQ-C30 评分比较 ±s,分
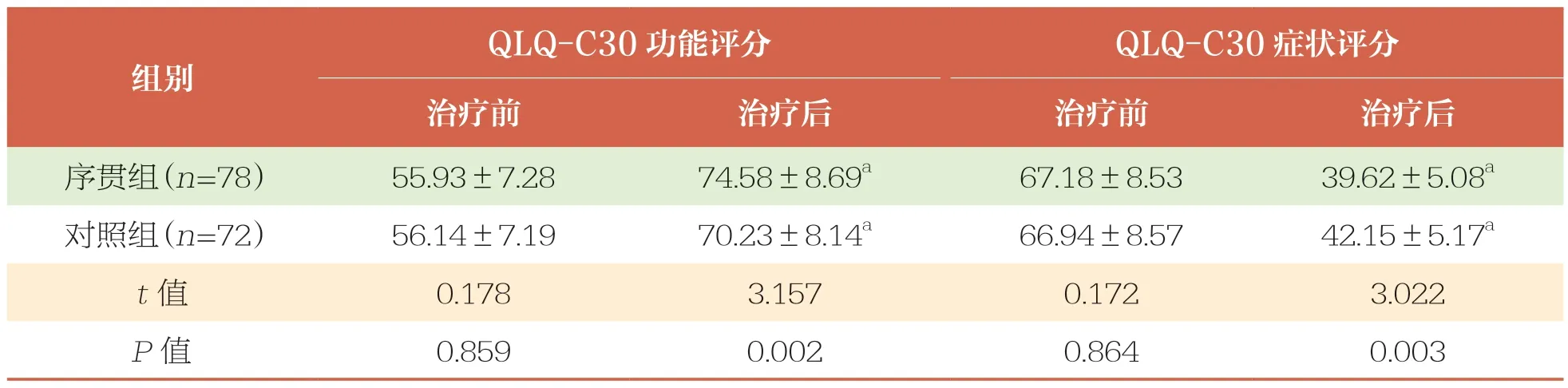
表4 两组QLQ-C30 评分比较 ±s,分
QLQ-C30:生存质量核心问卷
QLQ-C30 功能评分QLQ-C30 症状评分治疗前治疗后治疗前治疗后序贯组(n=78)55.93±7.2874.58±8.69a67.18±8.5339.62±5.08a对照组(n=72)56.14±7.1970.23±8.14a66.94±8.5742.15±5.17a t 值0.1783.1570.1723.022 P 值0.8590.0020.8640.003组别
2.5 不良反应发生情况
两组患者脱发、白细胞减少、胃肠道症状和肝肾功能异常等不良反应的发生率比较均无统计学差异(P>0.05)(表5)。
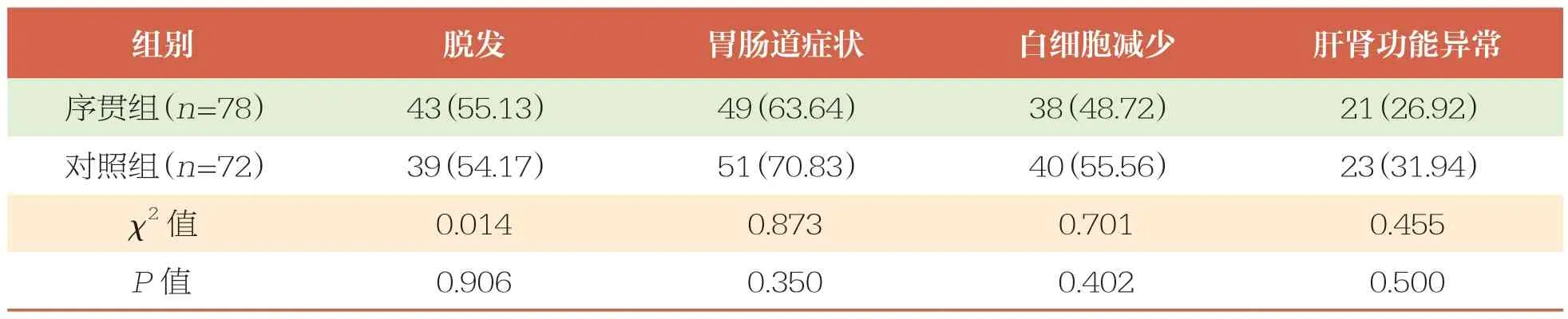
表5 两组不良反应发生情况比较 n(%)
3 讨论
目前,全球肺癌人数呈逐年上升趋势[13],且死亡率高,因此亟需预防和尽早治疗,以提高患者生存率及改善患者生存质量。随着医学技术和药物研发的不断进步,生物靶向治疗现已成为治疗晚期NSCLC 患者的优先推荐方案[14],可有效提高晚期NSCLC 患者的生存质量。研究证实[15],以EGFR作为治疗靶点受体选择药物可使EGFR突变型晚期NSCLC 患者明显获益。EGFR表达于正常细胞表面,其过表达提示肿瘤细胞可能转移、浸润,EGFR可通过Ras-Raf-MAPK 通路传递信号,促使机体组织内血管生成、细胞增殖及凋亡[16]。EGFR突变不仅可加速肿瘤细胞的生长及增殖,还可促使大量Treg 细胞聚集在肿瘤微环境(tumor microenvironment,TME)中,最终导致肿瘤细胞免疫逃逸[17]。以EGFR为治疗靶点受体的EGFRTKIs 可有效抑制EGFR结构域的活性,使广大NSCLC 患者受益。然而,使用第一代EGFR-TKIs(如吉非替尼)治疗后,多数患者在1~2 年后难以避免出现耐药现象,推测与T790M突变引起耐药有关[18]。
针对第一、二代EGFR-TKIs 耐药问题,现已研发出第三代EGFR-TKIs(如奥希替尼)并应用于临床。研究证实[19],奥希替尼可强效抑制T790M基因突变细胞系磷酸化,中断激酶催化引起的下游信号转导,抑制细胞增殖,促使细胞凋亡,可应用在T790M阳性的EGFR突变型晚期NSCLC 患者治疗中。李双双等[20]研究指出,使用奥希替尼治疗对第一代EGFR-TKIs 已经产生耐药的T790M阳性晚期肺腺癌患者临床疗效确切,可使患者明显获益。娄安琦等[21]利用数据挖掘进行奥希替尼疗效和安全性的Meta 分析时发现,给予EGFR突变型晚期NSCLC 患者奥希替尼治疗时,不仅可有效提高患者中位无进展生存期(progression free survival,PFS)和生存获益,还可降低3 级及以上不良事件(adverse event,AE)的发生率。吴皓等[22]研究提示,给予晚期NSCLC 患者奥希替尼并联合放化疗,不仅可有效抑制肿瘤生长、降低血清肿瘤因子水平,还能显著降低不良反应的发生风险。胡良峰[23]研究发现,给予NSCLC 患者甲磺酸奥希替尼片治疗时,临床疗效确切,可有效降低多项肿瘤标志物水平,减少不良反应。本研究结果提示,经治疗后,序贯组治疗总有效率及生存获益率均高于对照组(P<0.05);两组QLQ-C30 功能评分均升高(P<0.05),且序贯组高于对照组(P<0.05);两组QLQ-C30 症状评分均降低(P<0.05),且序贯组低于对照组(P<0.05),提示奥希替尼序贯治疗吉非替尼耐药后EGFR突变型晚期NSCLC 患者可获得较好的治疗效果,提高患者生存获益,改善患者生存质量。
CEA、CA125、CA199 为诊断恶性肿瘤的重要标志物[23]。CEA 作为富含多糖的蛋白复合物,属于广谱性肿瘤标志物,在肺癌、胃癌、乳腺癌等恶性肿瘤中水平升高;CA125 为一种大分子多聚糖蛋白,当机体出现恶性肿瘤后,其水平异常升高;CA199 为一种黏蛋白型的糖类蛋白肿瘤标志物,在恶性肿瘤患者中呈高表达[24-25]。本研究结果显示,经治疗后,两组血清CEA、CA125、CA199 水平均降低(P<0.05),且序贯组低于对照组(P<0.05),提示奥希替尼序贯治疗可有效降低患者血清肿瘤标志物水平。此外,本研究中,两组患者脱发、白细胞减少、胃肠道症状和肝肾功能异常等不良反应的发生率比较均无统计学差异(P>0.05),与胡良峰[23]研究结果不一致,这可能与纳入病例的个体差异有关,也可能与胡良峰[23]中奥希替尼用于起始治疗,而本研究中奥希替尼用于吉非替尼耐药后EGFR突变型晚期NSCLC 序贯治疗有关。
综上所述,使用奥希替尼序贯治疗吉非替尼耐药后EGFR突变型晚期NSCLC 患者临床疗效确切,可有效降低血清肿瘤标志物水平,改善患者生存质量。然而,本研究仍存在一定局限性,如本研究为基于现有临床资料的回顾性分析,样本量偏少,且观察时间较短,今后仍需进行大样本的多中心研究以进一步验证。

