虚拟现实联合跑台训练对脑卒中患者平衡功能和步行能力的效果
于春洋, 刘然, 赵依双, 郭帅, 周亚楠, 李丽, 张皓
1.首都医科大学康复医学院,北京市 100068;2.首都医科大学附属北京天坛医院,北京市 100070;3.中国康复研究中心北京博爱医院,北京市 100068;4.康复大学,山东青岛市 266071;5.山东大学齐鲁医学院,山东济南市 250063
0 引言
脑卒中是一种常见的脑血管疾病,其发病率、死亡率和致残率不断升高,被认为是全球第二大常见死因之一[1]。2019 年,全球范围内脑卒中患者总人数达1 亿[2],其中约70%行走功能受到不同程度损害,不仅使得他们参与家庭、社区活动的能力受到限制,而且极大地影响他们的生活质量,也使得患者、家庭和社会承受巨大的生理和心理负担[3]。恢复行走能力被视为脑卒中患者最重要和最普遍的康复目标之一[4]。
平衡功能障碍是影响脑卒中患者行走的主要因素之一,可增加摔倒的风险,不仅引发各种不良事件,而且影响患者的康复进程[5-6]。由于害怕摔倒,脑卒中患者的步行速度和效率会降低,根据任务目标和环境调整步行方式的能力会下降,在进行远距离行走、爬台阶、楼梯或斜坡,躲避障碍时会遇到困难[7]。
在脑卒中患者的步行康复方法中,跑台训练作为强制诱导运动方法被证明是一种有效的康复手段,通过进行密集和重复的练习,在平衡、运动功能、心血管参数方面都有改善,深受大家的认可[8]。但是,有些患者在跑台上行走并没有真正提高他们的社区步行能力,面对复杂的生活环境,他们仍然寸步难行。随着科技的进步,为解决这一难题,科学家利用计算机模拟个性化丰富的、可操控性的训练环境,多任务的互动反馈,在脑卒中康复领域中应用越来越广泛[9-10]。有研究发现,在跑台中增加非沉浸式虚拟现实组件,可以改善老年人平衡功能,降低跌倒发生率[11]。但一些相关研究存在试验方法的缺陷,试验组比对照组获得额外虚拟现实跑台的练习时间,对照组没有受到同等时间的训练,很难确定差异是由虚拟现实干预本身还是由在治疗中花费的额外时间产生的[12]。
本试验采用主动控制干预的治疗(即单独进行跑台训练),使试验更加严谨,探讨虚拟现实跑台对脑卒中患者平衡姿势控制以及步行能力的影响。
1 资料与方法
1.1 一般资料
2022 年3 月至2023 年3 月首都医科大学附属北京天坛医院康复科脑卒中住院患者40例,均符合《中国急性缺血性脑卒中诊治指南2018》卒中的诊断标准[13],且经头颅CT或MRI影像学检查确诊。
纳入标准:①年龄≥ 18 岁;②首次脑卒中,且存在一侧肢体功能障碍;③发病时间为1~6 个月;④Brunnstrom 分期下肢分期≥ 4 期,在独立、1 人帮助或扶拐的情况下,能站立并辅助步行超过12 m。
排除标准:①生命体征不稳定;②听力障碍、视力障碍、无法配合康复评定和治疗;③认知功能障碍,蒙特利尔认知评估量表(Montreal Cognitive Assessmen, MoCA)评分≤ 22 分;④由周围神经病变或颅脑外伤引起下肢步行功能障碍或有下肢骨折等影响下肢功能恢复的神经肌肉骨骼病变,或既往有颅脑疾病遗留下肢步行功能障碍。
脱落标准:①训练时患者出现不适,不能完成虚拟现实跑台训练;②因不可抗力导致数据记录不完整,资料不准确;③依从性差,不愿意参与试验;④未完成2周康复训练。
采用随机数字表法分为对照组和试验组,每组20例。两组基线资料比较均无显著性差异(P> 0.05)。见表1。本研究经首都医科大学附属北京天坛医院医学伦理委员会审核批准(No.KY2021-195-02),所有受试者均知情并签署知情同意书。
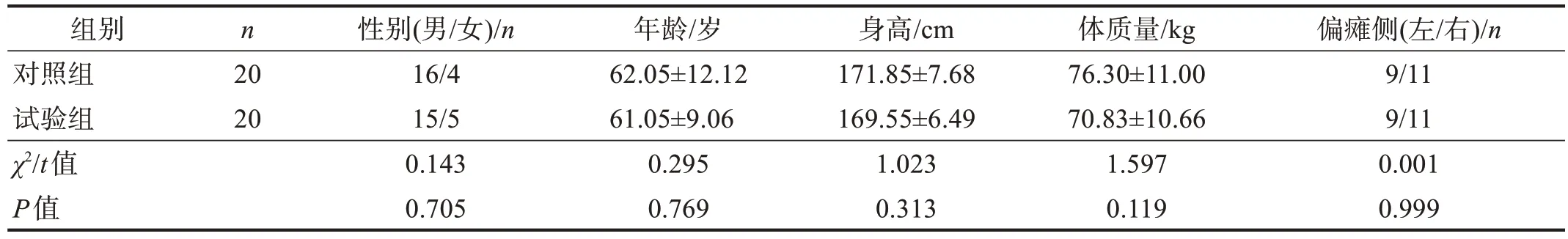
表1 两组基线资料比较Table 1 Comparison of baseline data between two groups
1.2 方法
两组均接受常规康复治疗。对照组辅以普通跑台步行训练,试验组辅以虚拟现实跑台步行训练。每天2次,每周5 d,连续2周。
1.2.1 常规康复训练
包括神经发育治疗,肌力、平衡功能、负重、上肢功能和日常生活活动能力等训练,每次40 min。
1.2.2 普通跑台训练
采用PHYSIORUN 普通跑台(德国PHYSIOMED公司)进行训练。使用跑台时,电视屏幕处于关闭状态。初始速度为0.6 km/h,根据患者情况,逐渐增加跑台速度,最高不超过2.0 km/h,每次20 min。
1.2.3 虚拟现实跑台训练
采用虚拟现实软件系统(德国ZEBRIS 公司),惠普电视屏幕和惠普笔记本电脑将虚拟现实的场景展现在跑台前面。使用跑台时,打开跑台前放置的虚拟现实系统,屏幕上会出现患者的脚印;启动跑台,患者行走在跑台上,其中的风景跟随其前进而变化。患者与情景进行互动,根据情况作出反馈,调整身体姿势、平衡。初始速度为0.6 km/h,根据患者情况,逐渐增加跑台速度,最高不超过2.0 km/h,每次20 min。
所有患者在训练过程中,穿着不支持任何体重的安全带。此外安装紧急停止装置,提升受试者的安全性。
1.3 评定方法
治疗前和治疗2 周后,分别进行以下评估。评估由2 位对分组不知情的物理治疗师进行,并且在试验开始前对评估标准统一性进行培训。
1.3.1 Berg平衡量表(Berg Balance Scale, BBS)
BBS 包括14 项评估动作,每项动作0~4 分,满分56分。< 40分,平衡功能有障碍,有跌倒风险[14]。
1.3.2 计时起立-行走测试(Timed "Up and Go" Test,TUGT)
患者坐在有扶手带靠背的椅子上,双手放在扶手上。测试者发出开始指令,患者起身,开始计时。测试中,不能给予额外的肢体帮助,向前行走3 m 后,围绕事先做好的标志物,转一圈后走回椅子,臀部接触椅面时停止计时。计算所用时间[15]。
1.3.3 平衡功能测试
采用Physiorun 虚拟现实跑台(德国PHYSIOMED公司)进行测试。患者站在测试平台上,目视前方,适应30 s后,收集患者睁眼站立10 s的足底压力数据。计算压力中心(center of pressure, COP)包络椭圆面积[16]和运动平均速度[17]。
1.3.4 步态参数
采用Zebris 步态系统测量。患者立于跑台上,跟随跑台步行,跑步机速度增加至患者舒适速度时,继续步行30 s。记录步长、步幅和步宽等参数。
1.4 统计学分析
采用SPSS 23.0 进行统计学分析。计量资料符合正态分布,以(±s)表示,组内比较采用配对样本t检验,组间比较采用独立样本t检验。显著性水平α= 0.05。
2 结果
所有患者均完成试验,治疗期间没有发生不良反应。
2.1 BBS评分
治疗前,两组BBS 评分均无显著性差异(P>0.05);治疗后,两组BBS 评分均明显增加(P< 0.01),且试验组明显优于对照组(P< 0.01)。见表2。
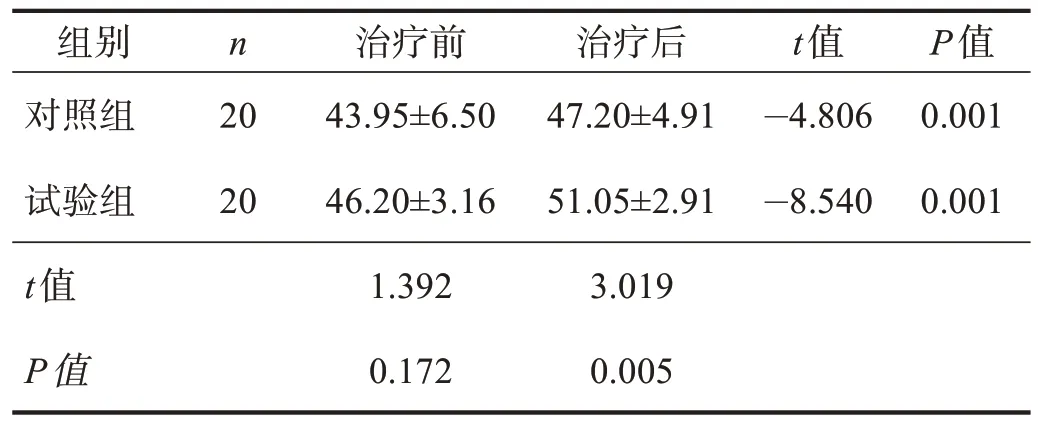
表2 两组治疗前后BBS评分比较Table 2 Comparison of BBS score between two groups pre and post treatment
2.2 TUGT时间
治疗前,两组TUGT 时间均无显著性差异(P>0.05);治疗后,两组TUGT 时间均明显缩短(P<0.01),且试验组明显短于对照组(P< 0.01)。见表3。
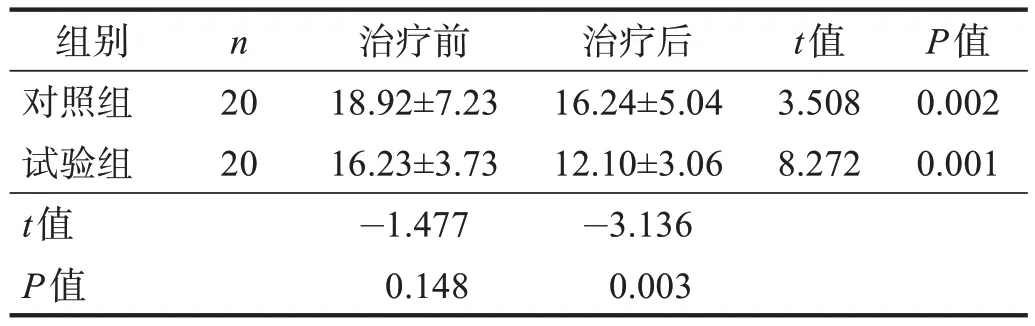
表3 两组治疗前后TUGT时间比较Table 3 Comparison of TUGT time between two groups pre and post treatment 单位:s
2.3 包络椭圆面积
治疗前后,两组包络椭圆面积均无显著性差异(P> 0.05)。见表4。
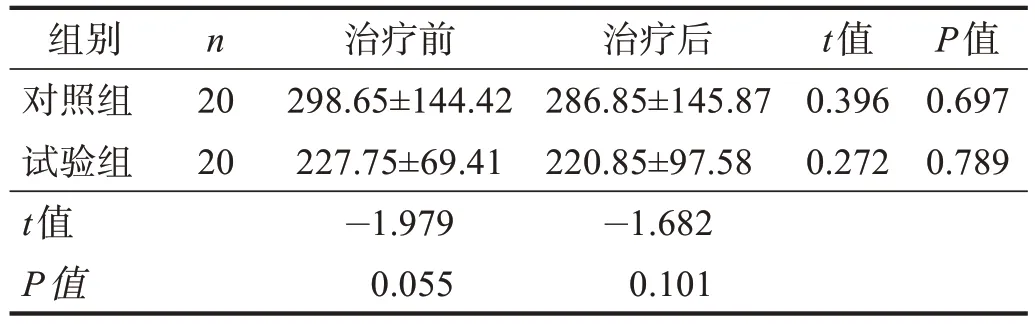
表4 两组治疗前后包络椭圆面积比较Table 4 Comparison of enveloping ellipse area between two groups pre and post treatment 单位:mm2
2.4 COP运动平均速度
治疗前后,两组COP运动平均速度均无显著性差异(P> 0.05)。见表5。
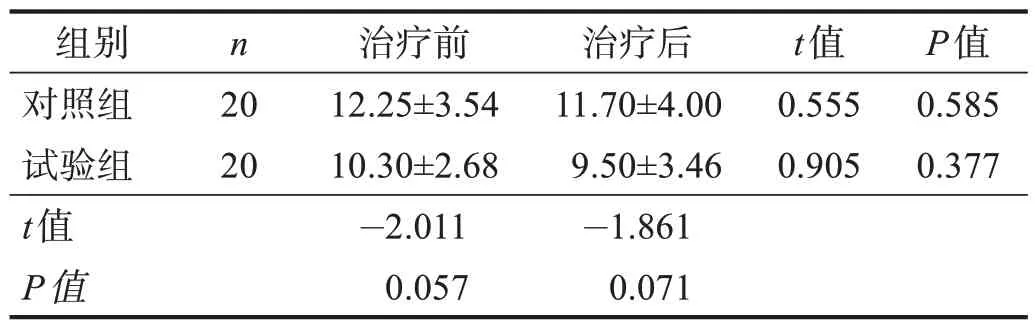
表5 两组治疗前后COP运动平均速度比较Table 5 Comparison of mean velocity of COP between two groups pre and post treatment 单位:mm/s
2.5 步态参数
治疗前,两组步长和步幅均无显著性差异(P>0.05);治疗后,试验组步长和步幅明显改善(P<0.01),但两组间比较均无显著性差异(P> 0.05)。治疗前后两组步宽均无显著性差异(P> 0.05)。见表6~表8。
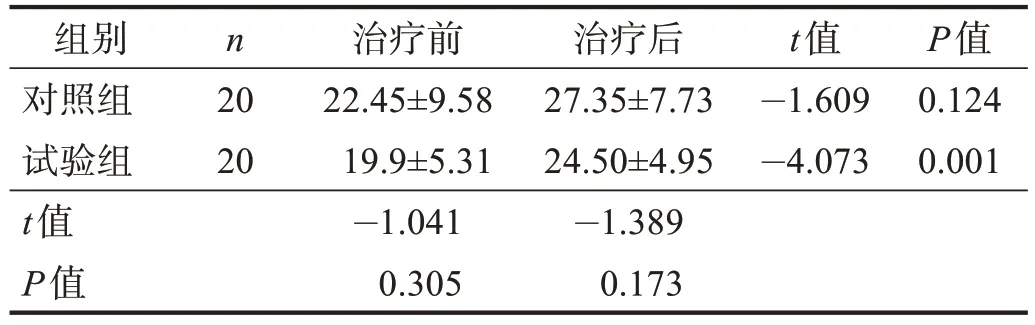
表6 两组治疗前后步长比较Table 6 Comparison of step length between two groups pre and post treatment 单位:cm
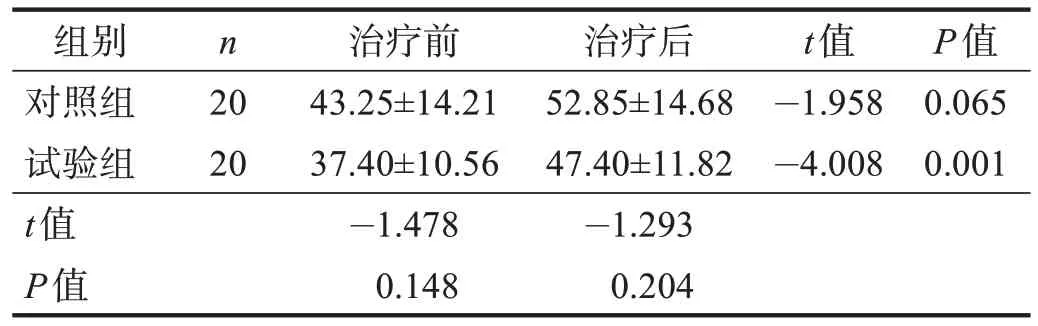
表7 两组治疗前后步幅比较Table 7 Comparison of stride length between two groups pre and post treatment 单位:cm
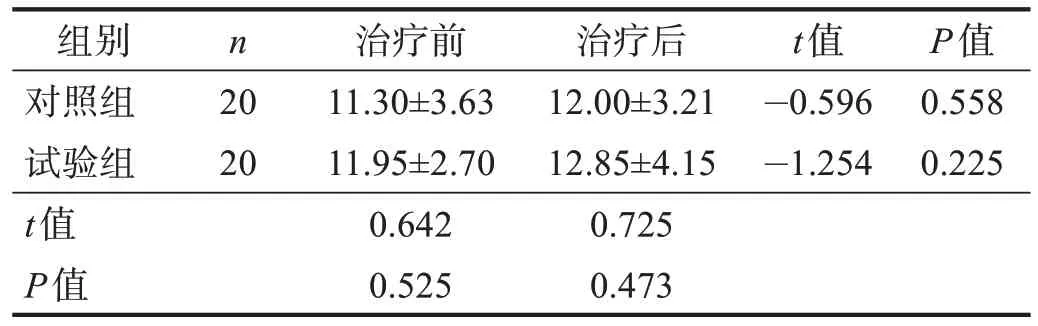
表8 两组治疗前后步宽比较Table 8 Comparison of stride width between two groups pre and post treatment 单位:cm
3 讨论
本研究显示,虚拟现实联合跑台训练后,患者平衡功能提高,这与既往研究报道结果一致。Zhang等[18]指出,虚拟现实治疗在提高患者平衡测试上有优势。虚拟现实与传统疗法结合可以改善脑卒中患者平衡和步态质量[19]。动态虚拟现实环境对受试者平衡稳定性产生干扰,从而影响姿势控制,是由视觉与本体感觉和前庭感觉之间产生感觉冲突所导致[20]。虚拟现实可以更大程度上刺激患者,获得维持平衡和姿势的新的运动和感觉能力,这是应对不断变化的环境所必需的能力,这种训练可以直接提高稳定性和平衡功能[21]。
本研究中,关于站立位静态平衡的相关数据(包络椭圆面积、COP 运动平均速度),两组之间均无显著性差异。Yang等[22]也发现,动态平衡学习的姿势控制技能对维持静态平衡作用不明显。但也可能是由于本研究训练时间较短导致。
本研究显示,虚拟现实联合跑台训练后,患者步长,步幅改善明显。再次验证Kim 等[23]提出的平衡功能以及功能性移动与步态方面是正相关的理论,平衡功能的提高也会有助于步态的改善。Galperin 等[24]也发现,虚拟现实跑台训练可以提高多发性硬化患者步行能力。Mirelman 等[25]指出,在实验室和社区中,使用机器人设备结合虚拟现实对慢性偏瘫患者进行训练,比单独使用机器人训练更好,能够大幅度提高行走能力,在虚拟环境中的步行训练比单纯重复运动效果更好。
虚拟现实是利用计算机生成的三维虚拟环境,具有成本低、趣味性强、便捷和安全等优点,其沉浸式的体验,可提高患者的参与度和积极性[3,26]。虚拟现实跑台基于运动学习和神经可塑性的理论,提供以目标为导向的、重复的、多样化的练习,并根据患者的能力进行调整。虚拟现实跑台训练可提高缺血性脑卒中患者运动能力、平衡功能、步行能力和日常生活活动能 力[27-28]。Slobounov 等[29]利用脑电图研 究2D 与3D 虚拟现实环境中的大脑皮质活动机制,发现患者在执行认知运动的双任务期间,处在完全沉浸式的虚拟环境中,需要更多的大脑和感官资源。Gavgani 等[30]利用经颅多普勒和近红外光谱评估正常人乘坐虚拟现实过山车对脑血流动力的影响,发现经过虚拟现实干预后两侧大脑半球顶颞区一些通道的氧合血红蛋白浓度显著增加,部分皮质区域的血流灌注增加。丰富环境能够多方面促进突触可塑性,从而有利于神经再生:促进与突触可塑性相关的蛋白(包括突触前膜和突触后膜的支架蛋白)充分表达;上调神经营养因子;通过影响N-甲基-D-天冬氨酸受体通道的开放性,加快海马CA3 区学习依赖性长时程增强过程[31-32]。Xiao 等[33]利用功能磁共振,研究亚急性期脑卒中患者接受虚拟现实增强跑步机训练后的皮质重组,发现治疗后损伤半球的初级感觉运动皮质和双侧辅助运动区激活增加,受损半球初级感觉运动皮质的变化与10 m步行时间的改善显著相关。综上所述,增加皮质区域的募集和激活,可能是虚拟现实联合跑台训练诱导脑卒中患者步态功能恢复的机制之一[34]。
本研究还存在一些局限性。首先,单中心试验,样本量较小,随机性较差,本研究结论需要在更大的样本范围内进一步验证。其次,本研究的训练时间仅为2 周,未来需要更长时间的随访,以评估虚拟现实联合跑台训练的长期效果。
4 结论
虚拟现实联合跑台训练有助于提高脑卒中患者的平衡功能和步行能力。
利益冲突声明:所有作者声明不存在利益冲突。

