ALK突变晚期非小细胞肺癌靶向治疗耐药后帕博利珠单抗治疗的新探索
程琳 魏亚兰 田霞
西安高新医院呼吸与危重症医学科,西安 710000
超过85%的肺癌为非小细胞肺癌(non-small cell lung cancer,NSCLC),该病早期发病隐匿,大部分患者就诊时已为晚期,5 年生存率<15%[1]。铂类为基础的化疗药物,常用于治疗晚期NSCLC 患者,然而长期用药会出现大量药物不良反应,临床疗效有限[2]。近年来,随着分子靶向治疗与基因检测的发展,治疗模式也在发生改变。相关指南推荐,间变性淋巴瘤激酶-酪氨酸激酶抑制剂(anaplastic lymphoma kinase-tyrosine kinase inhibitors,ALK-TKI)为ALK 突变晚期NSCLC患者的一线标准治疗方案[3],克唑替尼是全球第一个小分子ALK双靶点口服抑制剂,但多数患者在克唑替尼使用1年后出现耐药。相比于克唑替尼,阿来替尼对多种ALK耐药突变和ALK 阳性细胞具有更强的抑制力[4]。阿来替尼对接受克唑替尼治疗后耐药或进展的ALK突变NSCLC患者具有良好的抗肿瘤作用[5]。帕博利珠单抗作为一种程序性死亡受体1(programmed death-1,PD-1)单克隆抗体,可通过激发患者自身免疫达到抗肿瘤效果[6]。本研究者旨在探讨ALK 突变晚期NSCLC 靶向治疗耐药后患者采用阿来替尼联合帕博利珠单抗的有效性与安全性。
资料与方法
1.一般资料
本方案采用前瞻性、对照、单中心、随机、单盲临床研究方法设计。选择2020年3月至2022年7月在西安高新医院就诊的ALK 突变晚期NSCLC 靶向治疗耐药后患者,共筛选167 例患者,95 例入组,按随机数字表法分为试验组(48 例)和对照组(47例)。(1)入选标准:①临床诊断为NSCLC[7];②经癌组织基因型检测确认携带ALK 突变;③年龄≥18 岁;④临床分期ⅢB 或Ⅳ期;⑤均为克唑替尼治疗后耐药患者;⑥患者及家属均签署知情同意书。(2)排除标准:①合并其他类型恶性肿瘤患者;②伴有巨细胞病毒等感染性疾病患者;③处于哺乳期或妊娠期女性;④重度肝肾功能不全患者;⑤对本研究药物过敏;⑥有大咯血风险或中央型肺鳞癌。
本研究经西安高新医院医学伦理委员会审批通过(伦理编号:2020第003)。
2.治疗方法
对照组每次口服600 mg 阿来替尼(规格:每粒150 mg,批号20151211,注册证号H20180047,德国Excella GmbH &Co.KG公司),每天2次。试验组每次口服600 mg阿来替尼,每天2 次+第1 天静脉滴注200 mg 帕博利珠单抗(规格:每瓶100 mg,批号EV6371,注册证号S20180019,德国 Merck Sharp & Dohme Corp公司)。21 d为1个周期,两组治疗时间均为3个周期。
3.观察指标与疗效判定
(1)患者治疗前、后分别采集4 ml 外周静脉血,离心分离血清(时间:10 min,转速:3 000 r/min,半径:10 cm),通过酶联免疫吸附法测定血清细胞角蛋白19 片段抗原21-1(cytokeratin 19 fragment antigen 21-1,CYFRA21-1)、神经元特异性烯醇化酶(neuron-specific enolase,NSE)、糖类抗原9(carbohydrate antigen 9,CA9)、内皮抑素(endostatin,ES)、基质金属蛋白酶-9(matrix metalloproteinase-9,MMP-9)水平,通过化学发光法测定血清血管内皮生长因子(vascular endothelial growth factor,VEGF)水平。酶联免疫吸附试剂盒由上海机纯实业有限公司提供,化学发光法试剂盒由上海语纯生物科技有限公司提供。(2)分别于患者治疗前后采集5 ml 外周静脉血,CD4+、CD8+、自然杀伤(natural killer,NK)细胞水平均通过流式细胞仪检测。CD4+、CD8+、NK 流式细胞抗体购自艾柏森流式抗体公司。FACSCantoⅡ型流式细胞仪,美国BD公司产品;PerkinElmer型多功能酶标仪,上海美仪生物科技有限公司。(3)观察并记录两组治疗期间药物不良反应。(4)参照参考文献[8]对两组临床疗效进行评价,包括疾病进展、疾病稳定、部分缓解及完全缓解。(疾病稳定例数+部分缓解例数+完全缓解例数)/总病例数×100%=总有效率。(5)随访1年,以电话、门诊系统等形式进行随访,每3 个月随访1 次,记录两组患者生存情况。患者从治疗开始到癌因死亡或随访截止的时间为总生存期(overall survival,OS)。
4.统计学方法
应用统计学软件SPSS 25.0 行数据处理。符合正态分布的计量资料以均数±标准差()表示,组内比较行配对t检验,组间比较行独立样本t检验;计数资料用率(%)表示,行χ2检验。Kaplan-Meier 法绘制生存曲线,行Log-rankχ2检验,P<0.05为差异有统计学意义。
结果
1.一般资料(表1)

表1 两组间变性淋巴瘤激酶突变晚期非小细胞肺癌靶向治疗耐药后患者一般资料比较
试验组48 例患者中2 例因私自停药脱落,最终纳入46例;对照组47例患者中2例因主动退出研究脱落,最终纳入45例。两组一般资料比较差异均无统计学意义(均P>0.05)。
2.免疫功能、VEGF及肿瘤标志物对比(表2)
表2 两组间变性淋巴瘤激酶突变晚期非小细胞肺癌靶向治疗耐药后患者治疗前后肿瘤标志物、VEGF及免疫功能水平比较()
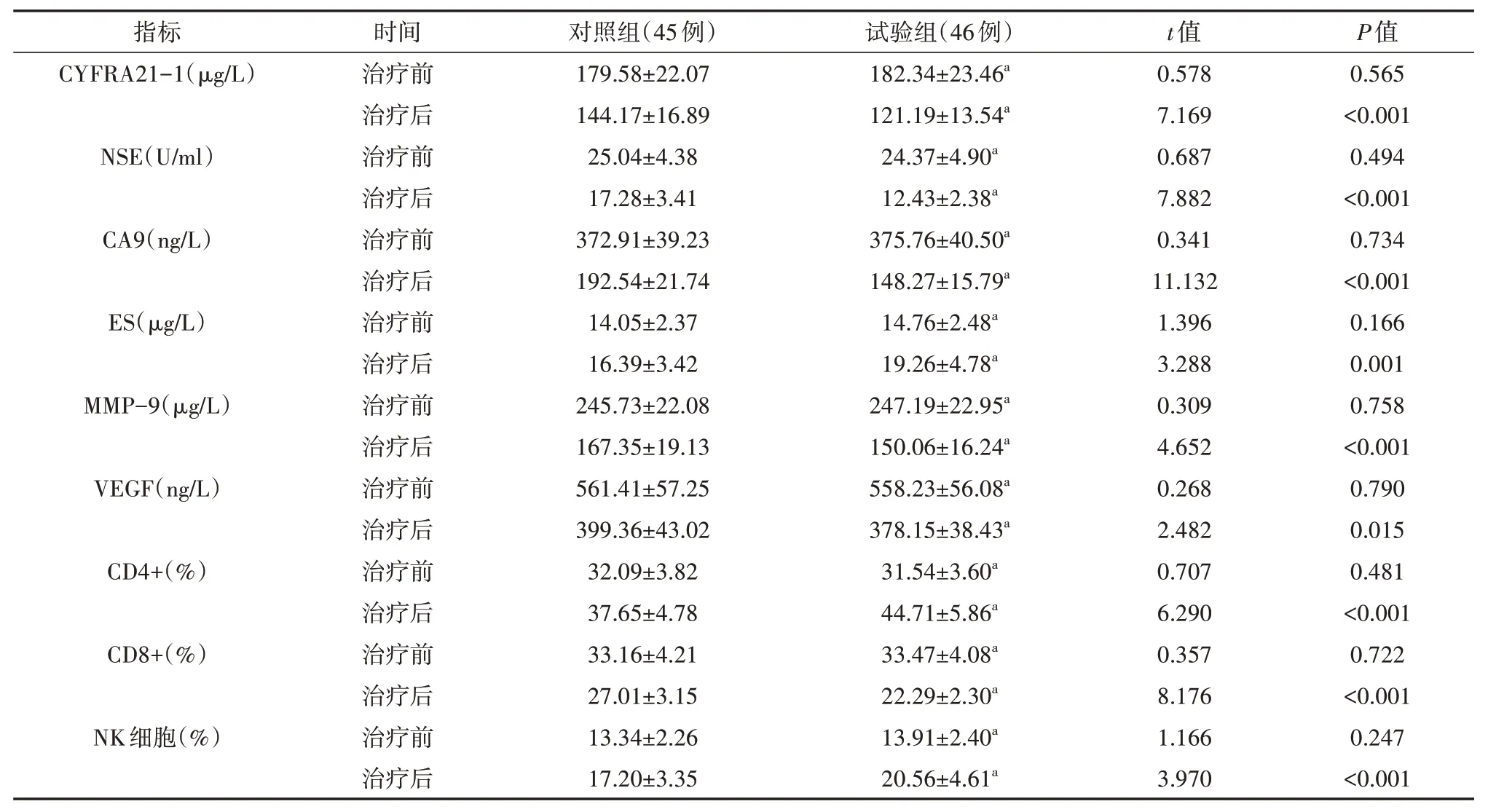
表2 两组间变性淋巴瘤激酶突变晚期非小细胞肺癌靶向治疗耐药后患者治疗前后肿瘤标志物、VEGF及免疫功能水平比较()
注:对照组行阿来替尼治疗,试验组在对照组基础上联合帕博利珠单抗治疗;CYFRA21-1为细胞角蛋白19片段抗原21-1,NSE 为神经元特异性烯醇化酶,CA9为糖类蛋白9,ES为内皮抑素,MMP-9为基质金属蛋白酶-9,VEGF为血管内皮生长因子,NK细胞为自然杀伤细胞;与同组治疗前比较,aP<0.05
?
与治疗前比较,治疗后两组CYFRA21-1、NSE、CA9、MMP-9、VEGF、CD8+水平均降低,ES、CD4+、NK 细胞水平均升高(均P<0.05);治疗后,试验组CYFRA21-1、NSE、CA9、MMP-9、VEGF、CD8+水平均低于对照组,ES、CD4+、NK细胞水平均高于对照组(均P<0.05)。
3.临床疗效比较(表3)

表3 两组间变性淋巴瘤激酶突变晚期非小细胞肺癌靶向治疗耐药后患者临床疗效比较[例(%)]
治疗后,试验组的总有效率(78.26%)高于对照组(57.78%),差异有统计学意义(χ2=4.396,P=0.036)。
4.安全性比较
治疗期间,试验组患者发生口腔黏膜炎2例、头晕2例、皮疹3例、发热1例、蛋白尿3例、恶心呕吐4例,对照组患者发生口腔黏膜炎1例、头晕2例、皮疹3例、发热1例、蛋白尿2 例、恶心呕吐3 例;试验组药物不良反应总发生率为32.61%(15/46),对照组为26.67%(12/45),两组药物不良反应总发生率比较差异无统计学意义(χ2=0.385,P=0.535)。
5.两组患者生存率比较(图1)

图1 两组间变性淋巴瘤激酶突变晚期非小细胞肺癌靶向治疗耐药后患者总生存期曲线比较
随访1 年,试验组失访1 例,对照组失访2 例,随访率为97.70%。试验组的1 年总生存率为55.56%(25/45),对照组的1 年总生存率为34.88%(15/43)。两组患者OS 曲线比较差异有统计学意义(Log-rankχ2=7.805,P=0.005)。
讨论
ALK 发生基因突变后会引起ALK 信号通路失调,细胞异常增殖与转移,增加恶性肿瘤发生风险。近年来,随着靶向药物的不断创新与发展,针对ALK 突变晚期NSCLC 患者的治疗方案已经从铂类化疗逐渐转向靶向药物作为一线治疗选择[3]。大部分患者在ALK-TKI 使用后1 年内会出现耐药造成疾病进展,以获得性耐药较为常见,患者起初对ALK-TKI 有反应而后出现疾病进展,其机制分为ALK 非依赖性/依赖性耐药[9]。阿来替尼是一种高选择性的ALK-TKI药物,能够通过抑制ALK 活性,阻断下游信号通路激活,诱导肿瘤细胞凋亡,可用于ALK 突变晚期NLCLC 靶向治疗后耐药患者[5]。Bodor 等[10]研究表明,ALK 突变晚期NSCLC 患者采用ALK-TKI药物联合PD-1抑制剂治疗的生存率更高。
本研究结果显示,试验组和对照组总有效率分别为78.26%和57.78%,与Eisenhauer等[8]研究报道相似。分析原因:帕博利珠单抗可通过阻断程序性死亡受体配体1(PD-L1)结合PD-1,抑制免疫逃逸,并重启免疫应答,有助于T 细胞的识别能力及杀伤活性的恢复,抑制肿瘤细胞的生长[11]。阿来替尼进入肿瘤细胞,能够直接作用于ALK 的胞内催化区,对肿瘤细胞的侵袭、迁移等过程进行抑制,从而发挥抗肿瘤作用[5]。肿瘤标志物在判断癌症患者预后及反映治疗效果中具有重要价值。Li等[12]报道,当支气管上皮恶变时,肺癌患者血清CYFRA21-1 异常增加。Mehta 等[13]发现CA9 及NSE 与NSCLC 患者癌细胞增殖过程关系密切,经相关抗肿瘤治疗后,CA9 及NSE 水平显著降低。本研究结果显示,相比于对照组,试验组治疗后的CA9、NSE、CYFRA21-1 水平均更低,可能原因为二者联合使用利于抑制TKI 信号通路,从而降低肿瘤标志物水平。临床研究发现,免疫功能降低会促进癌症发展,减少药物耐受能力[14]。Zhu 等[15]研究证实,NSCLC 患者CD8+水平较高,而NK 细胞与CD4+水平较低,在采用PD-1抑制剂治疗后,其水平会明显改善,与本研究报道相符。血管形成与肿瘤的发生及发展关系密切,阻碍肿瘤血管形成可对肿瘤增殖进行有效抑制[16]。王学中等[17]研究表明,采用PC 方案(培美曲塞+顺铂)联合帕博利珠单抗治疗晚期食管鳞癌患者的MMP-9、VEGF 水平均明显降低。帕博利珠单抗联合培美曲塞加铂类化疗治疗转移性非鳞状NSCLC 患者,结果表明患者2 年生存率为94.6%[18],明显高于本研究,可能与本研究患者病情严重、样本量较少等有关。本研究中,帕博利珠单抗联合阿来替尼可提高患者总体生存率,改善血管生成调节因子水平,与上述报道相符。帕博利珠单抗能够抑制PD-1/PD-L1途径的负向免疫调节机制,调节相关炎症因子的表达,有助于改善肿瘤微环境,增强免疫系统检出肿瘤细胞的突变蛋白能力,并可有效抑制肿瘤细胞增殖与肿瘤组织扩张,从而降低VEGF、MMP-9水平[3]。本研究两组患者药物不良反应总发生率对比无明显差异,提示帕博利珠单抗联合阿来替尼不会明显增加药物不良反应发生率。
综上所述,帕博利珠单抗治疗ALK 突变晚期NSCLC 靶向治疗耐药后患者疗效显著,可改善免疫功能,降低肿瘤标志物水平,提高生存率,改善血管生成调节因子水平,且不会明显增加药物不良反应的发生率。
利益冲突所有作者均声明不存在利益冲突
作者贡献声明程琳:酝酿和设计试验,实施研究,分析/解释数据,起草文章,统计分析;魏亚兰:采集数据,行政、技术或材料支持,支持性贡献;田霞:对文章的知识性内容作批评性审阅,指导

