发酵乳杆菌对灭菌豆浆中晚期糖化终末产物形成的影响
张霖,肖柯,王文悦,易弛,余帆,肖俊峰,樊鑫,朱晓青,李琴,周梦舟,穆杨
(湖北工业大学 生物工程与食品学院,湖北 武汉 430068)
随着社会的进步,人们越来越关注饮食健康。晚期糖化终末产物(advanced giycation end products,AGEs)是一组在蛋白质、脂肪酸或核酸的氨基基团与还原糖的醛基之间发生非酶性糖基化反应(又称美拉德反应)所形成的一系列具有高度活性终产物的总称,其结构具有高度异质性[1]。然而,AGEs 容易积聚在机体的不同组织纤维、器官和循环系统中,对机体造成氧化损伤,进而引发糖尿病、阿尔茨海默病、动脉粥样硬化等疾病。当在饮食中摄入过多的精细碳水或糖类物质后,体内会保持一个高糖的环境,进而在一系列复杂的酶代谢反应中形成内源性AGEs,其反应条件相对温和且形成周期较长。已有研究表明,内源性AGEs 是一种强毒性分子,可加速细胞死亡,从而导致器官损伤[2]。外源性AGEs(dietary advanced glycation end products,dAGEs)是食物中的AGEs 通过胃肠道消化吸收进入人体,学术界普遍认为摄入dAGEs 会增加血液中AGEs 的含量[3]。
豆浆是大豆的水提取物,外观与牛奶相似,豆浆含有优质蛋白质、必需脂肪酸和大量维生素,以蔗糖、毛蕊花糖等为代表的碳水化合物,不含胆固醇和乳糖。在食品加工过程中,豆浆蛋白可能发生降解、聚集和交联等构象和结构的变化,影响蛋白的功能性[4]。豆浆作为发酵食品的良好底物,可以通过发酵提高豆浆的品质。近几年,有不少研究发现经乳酸菌发酵后得到的化合物,在体外蛋白非酶糖化模型中具有较好的抗AGEs 能力。Zhou 等[5]发现发酵豆浆具有较好的延缓氧化、老化的作用,对D-半乳糖诱导衰老小鼠具有抗氧化作用,Peng 等[6]在研究中认为,混合菌发酵显著改变了豆浆的黏性、弹性等流变特性,丰富了发酵豆浆的口感,显著提高了发酵豆浆的营养特性和抗氧化能力。基于此,本文利用发酵乳杆菌制备发酵豆浆,以豆浆和灭菌豆浆作为对照,进行抗AGEs 能力、抗氧化特性、感官品质及营养价值等质量标准和蛋白结构变化的研究,以期提高豆浆的品质。
1 材料与方法
1.1 材料与试剂
黄豆(食品级):市售;三羟甲基氨基甲烷盐酸盐[tris(hydroxymethyl)aminomethane hydrochloride,Tris-HCl)]、异黄酮、二辛可宁酸(bicinchoninic acid,BCA)蛋白浓度测定试剂盒(均为分析纯):中国医药集团有限公司;发酵乳杆菌(L.fermentum):保藏于湖北工业大学湖北省食品发酵工程技术研究中心。
1.2 仪器与设备
L18-Y31 豆浆机:九阳股份有限公司;ZWYR-2102恒温振荡培养器:上海智城分析仪器制造有限公司;CT15RE 高速冷冻离心机:日本工机株式会社;DVB/CRA/PDMS 固相微萃取头:美国Supelco 公司;1260 高效液相色谱、7890B-5977B 气相色谱-质谱联用仪:安捷伦科技有限公司;UV-1601 紫外可见分光光度计:北京瑞丽分析仪器有限公司;84-1A 磁力搅拌器:上海司乐仪器有限公司;Nexus470 傅里叶变换红外光谱仪:美国Nicolet 仪器;HH.W21-Cr600 电热恒温水浴锅:北京长安科学仪器厂。
1.3 试验方法
1.3.1 发酵豆浆的制备
称取一定量的黄豆,洗涤,按料液比1∶5(g/mL)用去离子水于4 ℃浸泡12 h。将黄豆捞出沥干,水∶干豆=8∶1(质量比)用豆浆机榨汁并煮熟。煮熟的豆浆通过40 目筛过滤,分装至已灭菌的容器中。豆浆:4 ℃冰箱保存;灭菌豆浆:高温灭菌(121 ℃杀菌15 min)[7];发酵豆浆:冷却后,加入发酵乳杆菌(豆浆与乳酸菌的质量比为100∶1),置于37 ℃恒温振荡培养器中发酵24 h,4 ℃冰箱保存备用。
1.3.2 荧光AGEs 的测定
将豆浆组、灭菌豆浆组和发酵豆浆组分别取一部分进行离心(8 000 r/min,30 min),以除掉大分子蛋白,取上述上清液200µL 加入到黑色96 塑料微孔板,每组保持3 个平行,使用紫外可见分光光度计,在激发/发射波长分别为370 nm/440 nm 和335 nm/385 nm,激发和发射带宽均为5 nm 的条件下,测量每组反应溶液中荧光AGEs 和戊糖素的形成含量[8]。AGEs 或戊糖素形成的抑制率(R,%)的计算公式如下。
R=[1-(F试验组-F试验空白组)/(F对照组-F对照空白组)]×100
式中:F试验组为阳性对照[氨基胍(amino guanidine,AG)+牛血清白蛋白(bovine serum albumin,BSA)+葡萄糖(glucose,Glu)]或试验组[乳酸菌(lactic acid bacteria,LAB)+BSA+Glu]的荧光值;F试验空白组为阳性对照[AG+BSA+磷酸盐缓冲液(phosphate buffered salin,PBS)]或试验组(LAB+BSA+PBS)的荧光值;F对照组为BSA+Glu的荧光值;F对照空白组为BSA+PBS 的荧光值。
1.3.3 抗氧化活性和总酚含量的测定
参考Li 等[9]的方法,用无水乙醇配制0.2 mmol/L的1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)溶液,样品溶液与DPPH 溶液等体积涡旋混合,在室温下避光反应30 min,在517 nm 波长下测量吸光度A1。将等量的样品溶液与无水乙醇混合,在517 nm 波长下测量吸光度A2。将相同体积的DPPH 溶液与纯水混合,在517 nm 波长下测量吸光度A3。DPPH 自由基清除率(Q,%)的计算公式如下。
Q=[1-(A1-A2)/A3]× 100
用福林酚法测定总酚含量[10],取1 mL 样品溶液与0.5 mL 福林酚试剂混合均匀,反应5 min 后加入1.5 mL 7.5% Na2CO3溶液,用超纯水定容至6 mL,摇匀,室温下避光反应30 min,在760 nm 处测量吸光度。按上述方法分别取2、4、6、8、10µg/mL 没食子酸标准溶液测量吸光度,绘制没食子酸标准曲线(0~10µg/mL)。
1.3.4 发酵豆浆蛋白的提取
参照夏佳恒[11]的方法并稍作修改。将豆浆pH 值调至8.0,与Tris-HCl 溶液以料液比1∶1(g/mL)混合,再加入等体积的正己烷溶液,置于磁力搅拌器上4 ℃充分混匀4 h,再经过8 000 r/min 离心30 min,取中间澄清溶液,记为豆浆蛋白溶液,用BCA 蛋白浓度测定试剂盒测定蛋白浓度,收集的溶液在-20 ℃保存,备用。
1.3.5 发酵豆浆蛋白结构表征
将孵育后的样品上清溶液放入8 000 Da 透析袋,在PBS 溶液中充分透析24 h 以去除游离葡萄糖。透析完成后,将样品冷冻干燥成厚度均匀的干片,用傅里叶变换红外光谱(Fourier transform infrared,FTIR)仪测量,并将干片放在FTIR 附件上扫描。采用OMNIC 软件记录红外光谱:测量范围为4 000~400 cm-1,波长精度为0.01 cm-1,分辨率为4 cm-1,扫描次数为32,环境温度为25 ℃。利用傅里叶反褶积、二阶导数求导和高斯曲线对1 700~1 600 cm-1的峰进行拟合,根据拟合结果,利用峰面积计算蛋白质各二级结构的相对含量[12]。
1.3.6 表面疏水性的测定
采用8-苯氨基-1-萘磺酸(8-anilino-1-naphthalenesulfonic acid,ANS)荧光探针法监测豆浆发酵前后对表面疏水性的影响。称取适量ANS,完全溶解于二甲基甲酰胺溶液中,制得浓度为30µmol/mL 的ANS 溶液。样品与ANS 溶液等体积混合,在25 ℃避光条件中反应30 min。扫描记录荧光激发波长为380 nm,发射波长为390~650 nm,激发和发射狭缝宽度为5 nm。所得的测量光谱被调整为空白值。
1.3.7 大豆异黄酮成分分离和含量测定
豆浆中大豆异黄酮的分离和定量采用高效液相色谱检测法[13]。采集的豆浆样品冻干至粉末状,精确称量0.1 g 粉末,溶于6 mL 80%甲醇溶液,超声提取异黄酮2 h,然后13 000 r/min 离心5 min,上清液用0.22µm微孔滤膜过滤。采用梯度洗脱的方式对异黄酮进行定量检测。检测条件:进样量20µL;流速1 mL/min;选用YMC-PackODS-AMC18(250 mm×4.6 mm×5µm,12 nm)色谱柱;柱温25 ℃;二极管阵列检测器(diode array detector,DAD)检测波长254 nm;流动相0.1%乙酸和0.1%乙酸乙腈。按照GB/T 26626—2011《动植物油脂水分含量测定卡尔费休法(无吡啶)》设置梯度洗脱条件。
标准曲线的建立:准确称取大豆苷、染料木苷、黄豆黄苷、大豆苷元、染料木素、黄豆黄素标准品各1 mg,分别溶于甲醇溶液,定容至10 mL,即为标准液,储存在4 ℃备用。取适量的大豆异黄酮标准液,用甲醇按梯度稀释,制作不同浓度的标准工作液,上机进行检测分析。用每种标准品的质量浓度(x)和峰面积(y)绘制线性方程,并进行回归分析。
1.3.8 挥发性风味成分的测定
采用顶空固相微萃取-气相色谱-质谱(head sead solid phase microextractions-gas chromatography-mass spectormetry,HS-SPME-GC-MS)测定挥发物。准确称取豆浆20 mL、5 g 氯化钠置于40 mL 顶空进样瓶,加入一颗搅拌子,用带有橡胶隔垫的瓶盖密封。将其放在45 ℃的电热恒温水浴锅中,预热10 min,平衡20 min,用50/30µm DVB/CAR/PDMS 纤维针插入顶空瓶中,距离液面1 cm,萃取风味化合物30 min。随后,将针头缓慢插入注射口,250 ℃下解吸5 min。
参考冯笑笑[14]的方法设置GC-MS 分析条件:色谱柱HP-5MS(30 m×250µm×0.25µm)。升温程序:起始温度40 ℃保持3 min,以6 ℃/min 升温至100 ℃,再以10 ℃/min 升温至230 ℃,保持7 min。载气:氦气,流速1.3 mL/min;不分流。MS 条件:电子电离(electron impact,EI);离子源温度230 ℃;电子轰击能量70 eV;离子扫描范围m/z 33~500;全扫描模式。
挥发性风味物质定性定量分析:经美国国家标准技术研究所(National Institute of Standards and Technology,NIST)11 标准质谱库进行检索、定性定量,采用峰面积进行相对定量。
1.4 数据处理
所有试验均重复3 次,结果以平均值±标准差表示,数据采用SPSSv21.0 分析,在P<0.05 时认为差异有统计学意义。利用OrigionPro 8.0 绘图。
2 结果与分析
2.1 豆浆中AGEs 含量变化
热加工是豆浆生产过程中必不可少的环节,商业豆浆在生豆浆包装前或包装后还需经过巴氏杀菌或超高温处理。高温处理用于杀死病原体和变性抗营养因子,如胰蛋白酶抑制剂和脂氧合酶,可以确保微生物安全、提高消化率并延长产品的保质期[15]。热处理会促进还原糖与蛋白质之间的糖基化反应,产生糖基化产物和AGEs。AGEs 可通过阻断赖氨酸残基、改变消化率、掩盖或产生过敏原而降低蛋白质的营养价值[16]。豆浆中AGEs 含量如图1 所示。
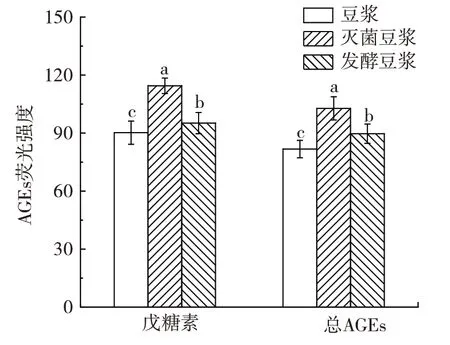
图1 豆浆中AGEs 含量Fig.1 AGE content in soybean milk
由图1 可知,与豆浆相比,灭菌豆浆的AGEs 荧光强度均升高,戊糖素与总AGEs 均增长了25%。再经发酵乳杆菌发酵后,发酵豆浆AGEs 的荧光强度较灭菌豆浆降低了12%~17%,相较于豆浆增长了5%~9%。
2.2 发酵对豆浆蛋白结构的影响
2.2.1 二级结构
豆浆蛋白的二级结构对其物理化学性质和功能具有重要影响。α-螺旋结构是豆浆蛋白主要的二级结构之一,其稳定性和可消化性高。β-折叠具有良好的乳化、发泡和凝胶性质,豆浆蛋白的二级结构与酸碱度、温度、蛋白浓度等因素有关[17]。豆浆经灭菌、发酵后的蛋白二级结构如图2、表1 所示。

表1 豆浆蛋白二级结构含量Table 1 Secondary structure content of soybean milk protein%
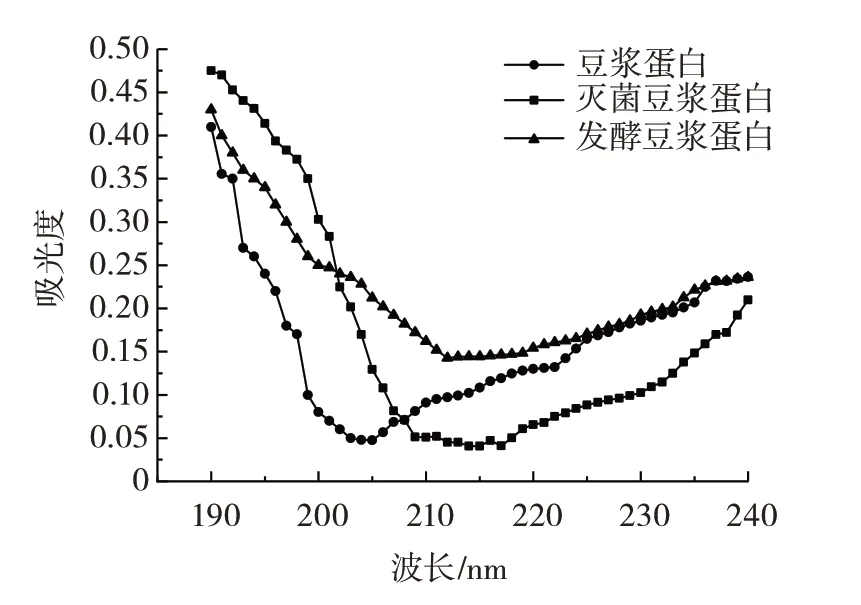
图2 豆浆蛋白的红外光谱Fig.2 Infrared spectrometry of soybean milk protein
由图2、表1 可知,与豆浆蛋白相比,经灭菌处理后的豆浆蛋白二级结构均发生显著变化,其中α-螺旋和β-折叠主要被破坏。β-转角呈现细微上升的趋势,无规卷曲呈现细微下降的趋势。发酵豆浆蛋白中的β-转角呈现细微下降的趋势,无规卷曲呈现细微上升的趋势。结果表明,灭菌豆浆经发酵后,减少了对蛋白二级结构的破坏,增长的α-螺旋转变成β-折叠和无规卷曲,使蛋白结构发生改变,变得更加灵活和松散。
2.2.2 表面疏水性
ANS 是一种用于蛋白质研究的荧光染料,已广泛用于监测暴露的蛋白质疏水斑块及其折叠中间体、蛋白质错误折叠和表面疏水基团的存在[18]。ANS 结合到蛋白质表面或膜的非极性区域时,流动性受到限制,导致荧光发射最大值的蓝移和荧光强度的增加。豆浆蛋白的表面疏水性主要取决于蛋白质表面的氨基酸残基的组成和分布。具体而言,富含疏水性氨基酸残基(如烷基、苯环等)的蛋白表面通常具有较高的疏水性。相反,富含亲水性氨基酸残基(如羟基、羧基等)的蛋白表面通常具有较高的亲水性。豆浆蛋白表面的疏水性对其在食品加工中的乳化、稳定、发泡等性质有着重要的影响。除了影响豆浆蛋白的物理化学性质外,豆浆蛋白表面疏水性还对其生物活性和免疫学特性产生影响。近年来的研究表明,豆浆蛋白表面的疏水性能够影响豆浆蛋白与消化酶的相互作用,从而影响豆浆蛋白的消化和生物利用率[19]。豆浆经灭菌、发酵后的表面疏水性如图3 所示。
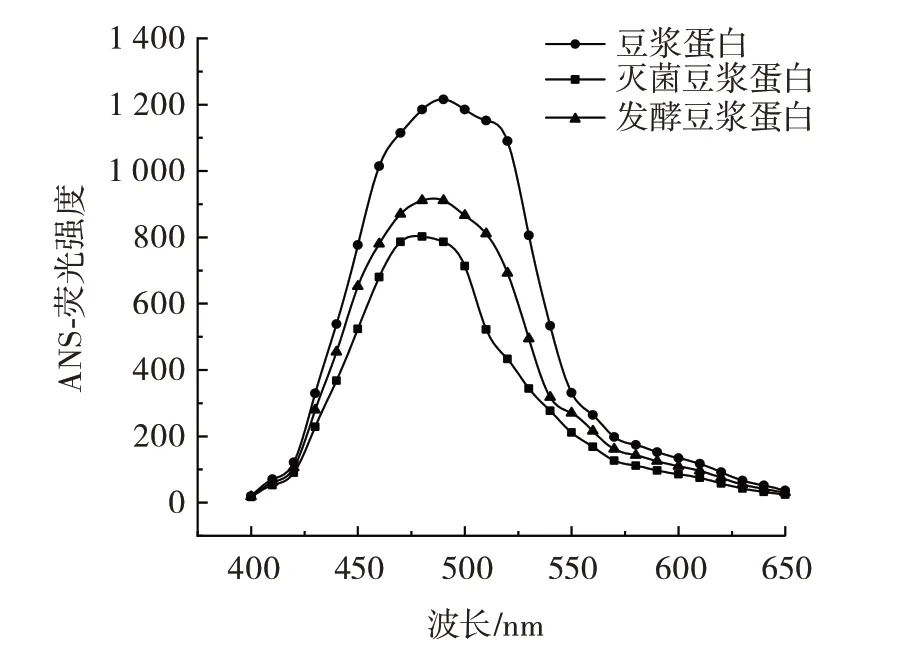
图3 豆浆蛋白的表面疏水性测定Fig.3 Determination of surface hydrophobicity of soybean milk protein
由图3 可知,豆浆经灭菌后的表面疏水性明显升高,这可能是因为豆浆蛋白受热后发生聚集,结构展开,内部的疏水性基团被暴露,与ANS 结合的程度升高,使得荧光强度升高。经发酵后,荧光强度明显降低,聚集的蛋白被酶水解、疏水基团被保护或隐藏。但是,发酵豆浆蛋白的表面疏水性比豆浆蛋白的表面疏水性高,可能是因为发酵形成新的疏水肽,这与Rui等[20]的研究结果一致。
2.3 发酵对豆浆功能性质的影响
2.3.1 抗氧化特性
各样品组的DPPH 自由基清除能力和总酚的含量如图4 所示。

图4 豆浆的抗氧化活性Fig.4 Antioxidant activity of soybean milk
由图4 可知,灭菌豆浆的抗氧化性最好,清除DPPH 自由基的能力达到66.86%,比发酵豆浆高8.75%,比豆浆高11.22%。灭菌豆浆的总酚含量较高,这可能与豆浆高温灭菌中因发生美拉德反应而产生的棕色类黑素有关,而美拉德反应是抗氧化性增强的原因。发酵乳杆菌发酵豆浆后降低了灭菌豆浆中的抗氧化活性,另外Mirlohi 等[21]证明豆浆发酵过程中生育酚的破坏是发酵后大豆产品抗氧化能力降低的主要原因。
2.3.2 异黄酮的生物转化
在大豆的不同生物活性成分中,异黄酮是重要成分之一。研究已验证它们具有抗氧化、抗炎、抗糖尿病和植物雌激素的特性。异黄酮的种类很多,其中结合型的糖苷包括黄豆苷、染料木苷和大豆苷,游离型的苷元为豆黄素、染料木素和大豆素。据报道,糖苷和苷元都具有重要的生理活性,但苷元由于分子量较低,疏水性较高,容易在小肠中被吸收,在医学研究中的治疗效果最好[22]。豆浆异黄酮含量见图5。
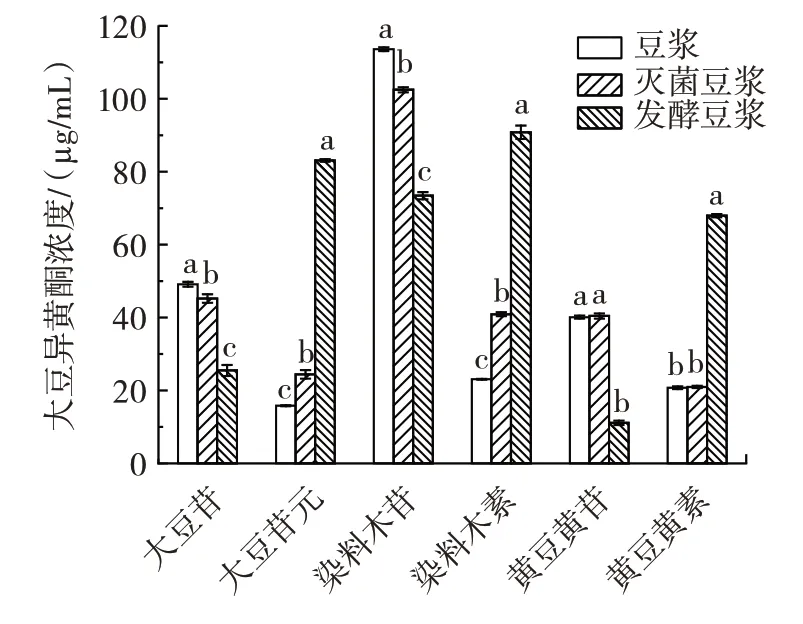
图5 豆浆异黄酮含量Fig.5 Isoflavone content of soybean milk
由图5 可知,豆浆中异黄酮含量为262.38µg/mL,其中糖苷总含量为202.81 µg/mL(染料木苷含量为113.60 µg/mL),苷元总含量为59.57 µg/mL(大豆苷元含量为15.78 µg/mL,染料木素含量为23.05 µg/mL)。灭菌后,豆浆中异黄酮含量发生了细微的变化,含量为274.43 µg/mL,其中糖苷总含量为188.15 µg/mL(染料木苷含量为102.48 µg/mL),较豆浆中含量显著降低(P<0.05),苷元总含量为86.28 µg/mL(大豆苷元含量为24.41 µg/mL,染料木素含量为40.91 µg/mL),较豆浆中含量显著升高(P<0.05)。发酵后异黄酮含量明显升高,总含量为351.83 µg/mL,苷元总含量显著增加,为241.80 µg/mL(P<0.05),糖苷和苷元分别占异黄酮含量的31.27% 和68.73%,苷元型异黄酮比例增大。结果表明,加热引起的糖基化反应导致了异黄酮类型向苷元型转化,发酵对豆浆的异黄酮生物转化、抗氧化活性有明显的提升作用。
2.4 发酵对豆浆挥发性风味物质的影响
豆浆含有70 种以上挥发性风味成分,不同的风味成分具有不同的风味特征[23]。影响豆浆接受度的主要属性之一是其独特的风味,主要表现为青草味、油脂味、果味、黄瓜味等。为了探究发酵对豆浆中豆类挥发性风味物质含量的影响,通过HS-SPME-GC-MS 从豆浆中定性定量鉴定出15 种典型的风味化合物,具体如表2 所示。

表2 典型风味化合物含量Table 2 Content of typical flavor compound
由表2 可知,1-辛烯-3-醇、正己醛、辛醛、苯甲醛等挥发性化合物,在豆浆、灭菌豆浆和发酵豆浆中的风味含量中存在明显差异。
实际制作出来的豆浆风味清淡,还有一些黄豆的香气,再结合上述15 种化合物的气味含量和气味特征,分别绘制了3 种豆浆中气味活性成分的分布雷达图,如图6 所示。

图6 豆浆风味特征Fig.6 Flavor features of soybean milk
由图6 可知,青草味在3 种豆浆中所占比例均最高。其中,豆浆中青草味风味特征最明显,壬醇所呈现的果味微乎其微,其他风味占比较均匀;灭菌豆浆中青草味的强度明显弱于豆浆,美拉德反应促使豆浆的焦糖味和油脂味明显增加,还出现微量香甜的果味;发酵豆浆会产生有机酸,从而导致其青草味也明显减弱[25]。
3 结论
以豆浆为基质,将乳酸菌掺入豆浆后,低聚糖发酵产生的大量短链脂肪酸不仅可以作为乳酸菌的能量来源,还可以提高产品营养价值。结果表明,发酵乳杆菌对灭菌豆浆进行发酵后,显著减少了由加热造成的美拉德反应(或蛋白非酶糖化反应)生成的AGEs 含量,最高可降低17% 的AGEs;高温灭菌造成豆浆蛋白质的结构展开,蛋白质二级结构中的无规卷曲和β-折叠向α-螺旋和β-转角转变,蛋白质三级结构中的疏水基团被暴露。然而,经发酵后的豆浆蛋白质结构变得更加舒展,α-螺旋向无规卷曲和β-折叠转变,疏水性降低37%;发酵的豆浆表现出较好的DPPH 自由基清除能力和较高的总酚含量,这是由于发酵豆浆中异黄酮含量增加和异黄酮类型向苷元型转化,其中,异黄酮含量较发酵豆浆增加了77.40µg/mL,苷元型异黄酮比例从22.70%增加到68.73%。本研究结果可为乳酸菌在豆浆中的应用提供参考。

