布拉氏酵母菌散联合蒙脱石散在腹泻患儿中的应用
陈迎春
(河南省郑州市第九人民医院 郑州 451191)
腹泻为小儿高发病,因感染病原体所致,临床检查显示多见病毒感染,少部分为细菌感染。病毒感染以轮状病毒为主,该病毒属于双链核糖核酸病毒,口、粪为重要传播途径,一旦肠道黏膜出产生肠毒素,胃肠道炎症反应极易导致腹泻,严重影响患儿身体健康[1]。目前,临床针对轮状病毒感染的腹泻患儿多采取抗病毒、补液、补盐、抗感染等方法进行治疗。蒙脱石散属于黏膜保护剂,主要作用机制为分解后结合黏液蛋白,形成黏膜修复层,减轻屏障损伤程度,从而预防病菌侵袭[2]。但本病极易复发,单一药物治疗无法完全控制病情进展,临床使用中多联合其他药物治疗。微生态制剂在消化道疾病中备受青睐,以布拉氏酵母菌散较为常用,在调节消化道菌群失衡方面效果显著,可有效降低复发率[3]。但布拉氏酵母菌散多被用于成人胃肠道疾病治疗中,有关其在小儿腹泻中研究数据有限。本研究制定布拉氏酵母菌散联合蒙脱石散方案进行治疗。现报道如下:
1 资料与方法
1.1 一般资料 按随机数字表法将2021 年3 月至2023 年3 月医院收治的110 例腹泻患儿分为对照组与观察组,各55 例。对照组女29 例,男26 例;年龄1~5 岁,平均(2.89±1.05)岁;病程1~8 d,平均(3.42±1.47)d;脱水程度:轻度11 例,中度30 例,重度14 例。观察组女31 例,男24 例;年龄1~6 岁,平均(2.93±1.08)岁;病程1~7 d,平均(3.30±1.40)d;脱水程度:轻度12 例,中度32 例,重度11 例。两组一般资料均衡可比(P>0.05)。本研究经医院医学伦理委员会批准(伦理审批号:2020000115)。
1.2 入组标准 纳入标准:符合西医相关诊断标准[4];轮状病毒检测阳性;大便频率>4 次/d;粪便常规检测白细胞≤4 个/Hp;大便为黄色稀水样/蛋花汤样;服药依从性良好;患儿家属自愿签署知情同意书。排除标准:消化道畸形;先天性心脏病;呕吐严重;对本研究药物过敏;先天性免疫缺陷;肝、肾功能严重损伤;呼吸道感染;合并其他影响炎症因子水平的疾病。
1.3 治疗方法 两组均行常规治疗,如抗炎、补液、补盐等。对照组给予蒙脱石散(国药准字H19990307)治疗,1.5 g/次,3 次/d,温水冲服。观察组在对照组基础上加用布拉氏酵母菌散(国药准字SJ20150051)治疗,年龄<3 岁,0.25 g/次,1 次/d;年龄≥3 岁,每日增加1 次,温水冲服。两组均根据病情程度治疗3~5 d。
1.4 观察指标 (1)疗效。显效:粪便形态恢复正常,排便次数1~2 次/d;有效:粪便形态相比治疗前有所好转,排便次数减少;无效:粪便形态相比治疗前无改变,排便次数>4 次/d,甚至更多。总有效=显效+有效。(2)症状缓解时间。比较两组腹痛、呕吐、腹泻缓解时间。(3)炎症反应。抽取两组治疗前、治疗结束后空腹静脉血3 ml,离心处理后取其清液,采用ELISA 测定血清肿瘤坏死因子-α(TNF-α)、白介素-6(IL-6)、干扰素-γ(INF-γ)、超敏C 反应蛋白(hs-CRP)水平。(4)肠道黏膜屏障功能。抽取两组治疗前、治疗结束后空腹静脉血3 ml,离心处理后取其清液,采用分光光度法检测内毒素(ET)、二胺氧化酶(DAO)、D-乳酸(D-LAC)水平。(5)不良反应。观察两组口干、便秘、皮肤过敏等发生情况。
1.5 统计学方法 采用SPSS23.0 软件进行数据处理。计量资料以(±s)表示,行t检验;计数资料以%表示,行χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组疗效对比 观察组总有效率高于对照组(P<0.05)。见表1。
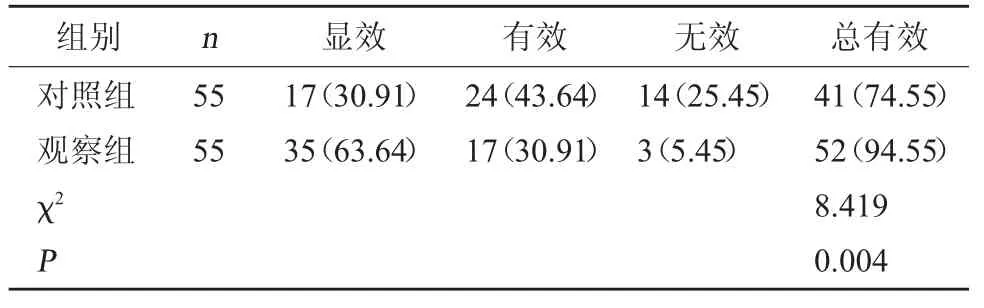
表1 两组疗效对比[例(%)]
2.2 两组炎症反应对比 治疗后,两组各指标水平均低于治疗前,且观察组更低(P<0.05)。见表2。
表2 两组炎症反应对比(±s)
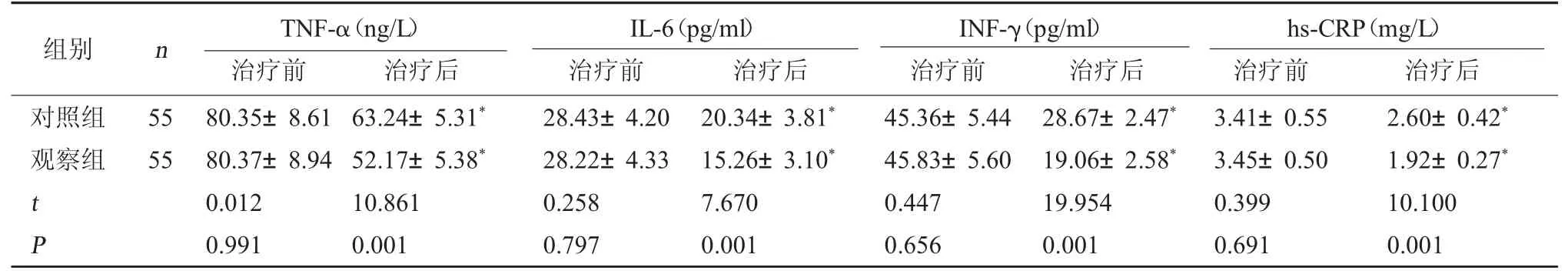
表2 两组炎症反应对比(±s)
注:与本组治疗前相比,*P<0.05。
hs-CRP(mg/L)治疗前治疗后对照组观察组组别nTNF-α(ng/L)治疗前治疗后IL-6(pg/ml)治疗前治疗后INF-γ(pg/ml)治疗前治疗后55 55 t P 80.35±8.61 80.37±8.94 0.012 0.991 63.24±5.31*52.17±5.38*10.861 0.001 28.43±4.20 28.22±4.33 0.258 0.797 20.34±3.81*15.26±3.10*7.670 0.001 45.36±5.44 45.83±5.60 0.447 0.656 28.67±2.47*19.06±2.58*19.954 0.001 3.41±0.55 3.45±0.50 0.399 0.691 2.60±0.42*1.92±0.27*10.100 0.001
2.3 两组肠道黏膜屏障功能对比 治疗前两组肠道黏膜屏障功能对比,差异无统计学意义(P>0.05);治疗后,两组ET、DAO、D-LAC 水平均低于治疗前,且观察组更低(P<0.05)。见表3。
表3 两组肠道黏膜屏障功能对比(±s)

表3 两组肠道黏膜屏障功能对比(±s)
注:与本组治疗前相比,*P<0.05。
D-LAC(mg/L)治疗前治疗后对照组观察组组别nET(pg/ml)治疗前治疗后DAO(U/L)治疗前治疗后55 55 t P 0.93±0.15 0.91±0.17 0.654 0.514 0.72±0.13*0.50±0.11*9.581 0.000 12.74±2.67 12.80±2.44 0.123 0.902 10.25±1.36*8.27±2.03*6.010 0.000 9.68±2.01 9.73±2.14 0.126 0.900 7.94±1.12*6.03±1.02*9.351 0.001
2.4 两组症状缓解时间对比 观察组腹痛缓解时间、呕吐缓解时间、止泻时间均短于对照组(P<0.05)。见表4。
表4 两组症状缓解时间对比(d,±s)
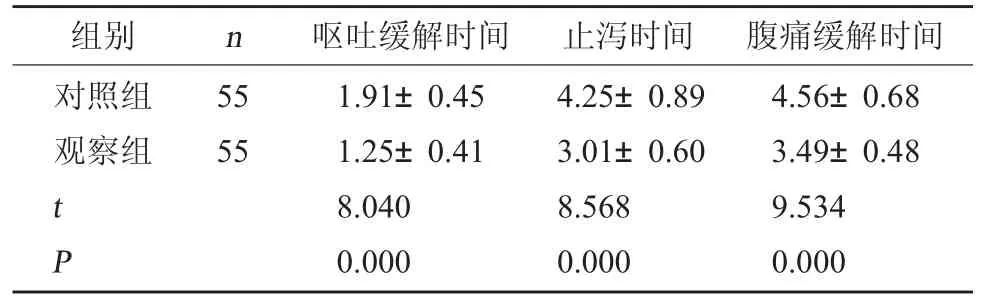
表4 两组症状缓解时间对比(d,±s)
组别n呕吐缓解时间止泻时间腹痛缓解时间对照组观察组55 55 t P 1.91±0.45 1.25±0.41 8.040 0.000 4.25±0.89 3.01±0.60 8.568 0.000 4.56±0.68 3.49±0.48 9.534 0.000
2.5 两组安全性对比 两组不良反应发生率对比,差异无统计学意义(P>0.05)。见表5。
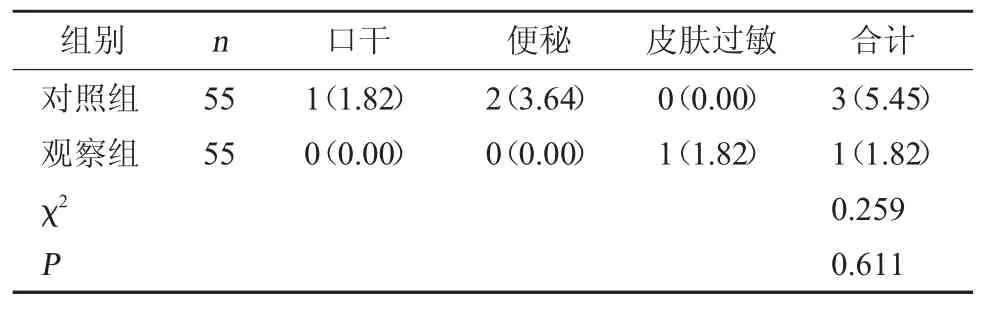
表5 两组安全性对比[例(%)]
3 讨论
腹泻为小儿发病率较高的一种急性胃肠道反应,具有一定的传染性。经流行病学调查显示,约80%患儿感染轮状病毒,极易诱发肝炎、胃肠功能障碍等并发症,甚至导致急性肾衰竭,已成为导致患儿病死的重要原因[5]。机体一旦感染轮状病毒,可定植在肠道内,刺激小肠上皮细胞,首先促进多种血管活性分子释放,导致肠道吸收水钠功能衰退,最终引起腹泻;同时还会使大部分钙离子聚集,氯离子通道随之开放,导致肠道内外氯离子浓度不平衡,小肠绒毛顶端细胞发生脱落、坏死现象,最终引发腹泻[6]。另外,该病具有发病迅速、进展快、复发风险高等特征,药物治疗首要目的为止泻。但迄今为止,尚未研究出标准化治疗方案,多予以微生态制剂、抗感染、补液盐等措施。因此,如何制定有效且安全的方案治疗腹泻患儿一直以来都是临床研究热点。
蒙脱石散是有镁铝自然合成的一种硅酸盐,因具有明显的吸附作用,已被广泛用于治疗胃肠道疾病。该药物是主要结构为层纹状,可借助吸附作用清楚肠道内多种致病菌及其释放的有害物质,从而缓解肠道刺激,修复肠内黏膜损伤[7]。该药物还可快速结合黏液蛋白,在肠内形成保护膜,抑制黏液溶解,促进结肠黏蛋白合成,进而快速修读肠道黏膜屏障功能[8]。但仅采用蒙脱石散单独治疗腹泻效果不够理想。布拉氏酵母菌散属于真菌类微生物制剂,为目前临床唯一一个被作为益生菌使用的药物,具有抗炎、抗病毒、肠营养等作用。本研究将其与蒙脱石散联用,结果显示观察组总有效率高于对照组,腹痛缓解时间、呕吐缓解时间及止泻时间均短于对照组,表明两种药物配合治疗腹泻患儿可显著提高疗效,缓解临床症状。与李泽等[9]研究结果基本一致。分析其原因为,布拉氏酵母菌散作为止泻性药物,具有纠正胃肠道微生态系统紊乱作用,可有效清除病原微生物及其分泌物,减轻肠道黏膜损伤,减轻症状[10]。且有研究指出,该药物能够提升多胺类物质水平,有助于促进上皮细胞成熟,缓解腹泻[11]。
病原菌损伤肠道黏膜后,会大量释放ET,刺激肠黏膜下淋巴系统,导致炎症细胞因子分泌,诱发或加重炎症反应,而炎症反应又会反作用于肠道黏膜,加重损伤,导致肿胀、充血,病情不断恶性循环[12]。TNF-α、IL-6、INF-γ、hs-CRP 均属于促炎因子,其中TNF-α、IL-6 可共作用,激发炎症级联效应,INF-γ 为具有广泛免疫调节作用的淋巴因子,hs-CRP 属于急性时相反应蛋白,出现炎症反应时,上述因子均会显著增加[13]。本研究结果发现,治疗后两组TNF-α、IL-6、INF-γ、hs-CRP、ET、DAO、D-LAC 水平均低于治疗前,且观察组更低,提示布拉氏酵母菌散联合蒙脱石散治疗腹泻患儿可明显抑制炎症因子表达,提高肠道黏膜屏障功能。另外,服用后该药物成分中的酵母菌可迅速结合上皮细胞,借助细胞壁中甘露聚糖黏附病原菌,进而抑制病毒损伤肠道黏膜,有助于提高肠道黏膜屏障功能[14]。在治疗安全性中,本研究结果发现,对照组、观察组副作用均较少,组间比较无明显差异,表明该方案在临床治疗中具有良好的安全性,与相关文献研究结果相似[15]。

