地热水中硼与碳酸盐类矿物吸附过程的实验研究
刘家千琳,正安婷,望尧瑶,陈子豪,谭天畅
(长江大学 资源与环境学院,湖北 武汉 430100)
0 引言
硼是自然界中普遍存在的一种元素,也是各种生命体生长发育不可或缺的一种元素,但当硼摄入过量时,就会在环境介质中具有很大的危害效应[1],世界卫生组织规定,人体饮用水中硼的含量应小于0.5 mg/L,植被灌溉水中硼含量应小于1 mg/L[2]。过量摄入会造成人体慢性中毒,伴随腹泻、头痛、恶心等一系列症状,严重时可使肝脏造成损害,脑和肺出现水肿甚至导致死亡,植物则会产生叶片枯黄、脱落,光合作用能力降低等影响,致使植物生长受阻[3]。地热资源是一种用途广泛、绿色环保、运营成本低的可再生清洁能源,合理开发利用地热资源可以获得很大的经济效益。但高温地热流体中硼含量很高往往很高[4],当高温地热流体从泉口或地热井口直接排放时会对环境造成破坏,尤其是当大规模开发利用时,排放到环境中的硼总量会更大,造成更加严峻的地热区周边环境的硼污染问题。
高温地热系统中,在地热流体从地层深处上升到地表的运动过程中,由于所处地层温度及压力的降低,以及二氧化碳的逸出,在地热流体泉口经常会形成碳酸盐类矿物层(钙华)。相关研究指出,碳酸盐类矿物表面较为活跃的羟基官能团能与硼产生配位体交换反映,从而硼通过化学反应被吸附到固相沉积物中。碳酸盐类矿物的这种吸附作用可以在一定程度上减少地热流体中的硼直接排放到环境后所造成的危害。本文通过人工模拟富硼地热水中碳酸盐类矿物的形成过程以及硼的被吸附过程,对实际地热水环境中,硼与碳酸盐类矿物相互作用的微观机理展开讨论研究,并分析在不同反应条件对该过程的影响,为我国地热资源开发利用中的环境污染防治问题提供理论依据。
1 材料与方法
1.1 实验仪器与样品配置
FD-1A-50冷冻干燥机、UPT-Ⅱ-20T超纯水机、UV-5500紫外分光光度计、10 mm比色皿、容量瓶、烧杯若干。
制备氯化钙标准贮备溶液:称取22.2 g 氯化钙(CaCl2)于烧杯中,将其充分溶于去离子水后转入1 000 ml容量瓶中并定容到标线。
制备乙酸铵贮备溶液:称取50 g乙酸铵置于烧杯中,将其充分溶于去离子水后转入100 ml容量瓶中并定容到标线。
制备500 mg/L的硼标准贮备溶液:称取2.82 g硼酸(H3BO3)于烧杯中,将其充分溶于去离子水后转入1 000 ml容量瓶中并定容至标线。
制备人工地热水:取已经制备完成的500 mg/L硼标准贮备溶液160 ml、乙酸铵贮备溶液20 ml和氯化钙标准贮备溶液100 ml于2 000 ml容量瓶中,在容量瓶中定容,随后转入烧杯,通入适量氨气或CO2气体以达到调节溶液pH的作用,将pH调至8.0±0.1后即可得到2 L硼含量为40 mg/L,pH=8的人工地热水。
1.2 硼与碳酸盐类矿物吸附实验
1.2.1 反应动力学实验
准备72个100 ml聚乙烯瓶,分别加入制备好的碳酸钙沉淀固体1.000 0 g,平均分为三组,每组分别加入的硼的标准储备溶液的浓度为40 mg/L、100 mg/L、500 mg/L,然后一起放入恒温振荡器中振荡,设置恒温振荡器的温度为25℃,转速为150 r/min,控制时间分别为1 h、2 h、3 h、5 h、8 h、1 d、2 d、5 d。为了减小误差,每个变量设置了三个平行样,到了规定的时间后一起拿出,分离上清液与沉淀,将沉淀进行超声润洗五次后,放入冰箱冷冻,在冷冻干燥机中至少干燥24 h以上,取0.5 g碳酸钙沉淀固体样品进行测试,用甲亚胺-H 酸分光光度法测定沉淀样品中硼的含量,同时做标准样品的测定,观察测定结果,找出碳酸钙吸附硼的平衡时间。
1.2.2 等温吸附实验
准备27个100 ml聚乙烯瓶,分别加入制备好的碳酸钙沉淀固体1.000 0 g,平均分为三组,每组的加入的硼标准储备溶液的浓度分别是0、20、40、60、100、200、300、400、500 mg/L,并将混合液置于恒温振荡器中振荡,设置恒温振荡器的温度为25℃,转速为150 r/min,反应时间为5 h。为了减小误差,每个变量设置了三个平行样,到了规定的时间后一起拿出,分离上清液与沉淀,将沉淀进行超声润洗五次后,放入冰箱冷冻,在冷冻干燥机中至少干燥24 h以上,取0.5 g碳酸钙沉淀固体样品进行测试,用甲亚胺-H酸分光光度法测定沉淀样品中硼和上清液中硼的含量,同时测定吸附平衡5 h时的pH值,观察测定结果。
1.2.3 影响因素实验
1)不同B浓度影响实验
设置浓度梯度为0、20、40、60、100、200、300、400、500 mg/L的硼溶液,每个变量设置2个平行样,准备72个100 ml聚乙烯瓶,分别加入制备好的碳酸钙沉淀固体1.000 0 g,将混合液放入恒温振荡器中振荡,设置恒温振荡器的温度为25℃,转速为150 r/min,反应时间为1 h、2 h、4 h、5 h。为了减小误差,每个变量设置了2个平行样,到了规定的时间后一起拿出,分离上清液与沉淀,将沉淀进行超声润洗五次后,放入冰箱冷冻,在冷冻干燥机中至少干燥24 h以上,取0.5 g碳酸钙沉淀固体样品进行测试,用甲亚胺-H酸分光光度法测定沉淀样品中硼和上清液中硼的含量,同时测定吸附平衡5h时的pH值,观察测定结果。
2)不同温度影响实验
设置温度梯度为25℃、45℃、65℃、85℃的硼溶液,每个变量设置2个平行样,准备32个100 ml聚乙烯瓶,分别加入制备好的碳酸钙沉淀固体1.000 0 g,将装有混合液的聚乙烯瓶放入恒温振荡器中进行振荡,设置恒温振荡器的温度为25℃,转速为150 r/min,反应时间分别为1 h,2 h,4 h,5 h。为了减小误差,每个变量设置了三个平行样,到了规定的时间后一起拿出,分离上清液与沉淀,将沉淀进行超声润洗五次后,放入冰箱冷冻,在冷冻干燥机中至少干燥24 h以上,取0.5 g碳酸钙沉淀固体样品进行测试,用甲亚胺-H 酸分光光度法测定沉淀样品中硼和上清液中硼的含量,同时测定吸附平衡5h时的pH值,观察测定结果。
3)不同pH值影响实验
设置pH梯度为7.5、8、8.5、9、9.5、10的硼溶液,每个变量设置2个平行样,准备48个100 ml聚乙烯瓶,分别加入制备好的碳酸钙沉淀固体1.000 0 g,放入恒温振荡器中振荡,设置恒温振荡器的温度为25℃,转速为150 r/min,反应时间为1 h,2 h,4 h,5 h。为了减小误差,每个变量设置了三个平行样,到了规定的时间后一起拿出,分离上清液与沉淀,将沉淀进行超声润洗五次后,放入冰箱冷冻,在冷冻干燥机中至少干燥24 h以上,取0.5 g碳酸钙沉淀固体样品进行测试,用甲亚胺-H酸分光光度法测定沉淀样品中硼和上清液中硼的含量,同时测定吸附平衡5h时的pH值,观察测定结果。
1.3 硼的测定
本次研究采取的对水样中的硼浓度的测定方法为甲亚胺-H酸光度法,经由此方法测定水样中的硼浓度为0.03 mg/L,测定上限为5.0 mg/L(相当于10.0 mg/L HBO2)。
该方法的原理为:硼与甲亚胺-H酸在pH=5.2的盐酸和乙酸铵缓冲溶液中,可生成溶于水的甲亚胺H-硼酸棕黄色化合物,且该化合物的最大吸收波长在410~420 nm处。甲亚胺H-硼酸棕黄色化合物的显色速度缓慢,可在6 h后发色完全,30 h内趋于稳定(其摩尔吸光系数 ε=6×103)。
1.3.1 样品测定
1.3.2 测量
将比色管静置于避光处6 h后,用10 mm比色皿,于420 nm波长处,使用空白试验溶液作对照,测定吸光度。
1.3.3 校准曲线的绘制
分别准确移取每毫升含0.010 mg HBO2的标准溶液0、0.50、1.00、3.00、5.00、7.00、11.00、15.00、20.00、25.00 ml于50 ml比色管中,用去离子水稀释至25 ml,以下按样品测定步骤进行显色和测量[5]。
2 实验过程与结果分析
本实验研究在刘明亮(2018)[4]对藏南典型高温高硼地热区地热水样的分析基础上展开研究讨论, 人工模拟的室内地热水中的硼含量为40 mg/L、温度为25℃、pH=8.0,并在其原有的实验方案基础上进行改进和完善。为了更好地模拟方解石在自然环境中的形成过程,本次研究采用CaCl2和Li2CO3反应生成碳酸钙,Li2CO3具有可溶但不易溶于水的特点,因此采用该材料产生方解石沉淀的过程更为缓慢,与方解石在自然条件下的产生过程更加接近,可以得出更符合实际情况的结果。
2.1 反应动力学实验
为了确定方解石吸附硼达到平衡所需的时间进行反应动力学实验研究,分别设置初始硼浓度为40 mg/L、100 mg/L、500 mg/L时测定方解石吸附硼达到平衡时所需要的时间,对反应后沉淀样品进行检测,得出方解石与硼的吸附反应在5 h左右达到平衡。对上述3种情况下的反应动力学过程用Lagergren准二级动力模型进行拟合有较好的相关性,数据拟合结果见于图1~图3。

图1 初始硼浓度为40 mg/L吸附过程的Lagergren模型

图3 初始硼浓度为500 mg/L吸附过程的Lagergren模型
2.2 等温吸附实验
方解石吸附硼的等温吸附实验数据及参数见表1和表2,随着初始硼浓度的增加方解石对硼的吸附量也增加。当初始硼浓度为500 mg/L时方解石对硼的吸附量大1.62 mg/g。将方解石对硼的吸附过程用Freundlich等温吸附模型拟合有较好的相关性,结果见图4。R2=0.937 8,表明方解石对硼的吸附以层间离子交换为主,且在一定硼浓度范围内有较好的吸附效果。

表1 方解石吸附硼的等温吸附数据

表2 等温吸附实验模型参数

图4 Freundlich模型模拟方解石对硼的吸附过程
2.3 初始溶液中硼浓度对固相中硼浓度的影响
初始溶液中硼浓度不同时控制反应温度与pH不变时方解石吸附硼达到平衡时的测试结果见表3所示,绘制关系曲线见图5。从图5中可以得出结论,在初始溶液中硼浓度在0~100 mg/L时方解石对硼的吸附率随着硼浓度的增大显著提高,在硼浓度为100 mg/L时超过了90%,在初始硼浓度超过100 mg/L之后吸附率继续增大,但受硼浓度影响不再明显。本结果与刘明亮(2018)[4]所得结果相近,但与Duygu Kavak研究所得结果不同[7]。其原因可能有以下两点,一方面溶解态的硼能够被一些反应表面积较大的矿物所吸附,如铁锰氧化物、粘土矿物和碳酸盐类矿物等[9]而Duygu Kavak的研究对象为粉煤灰成分复杂其反应表面积不如方解石从而导致对硼的吸附效果远不如方解石;另一方面Duygu Kavak实验时所研究的初始溶液中的硼浓度范围很大,最高初始硼浓度达到了1 600 mg/L,而本实验研究范围较小最大硼浓度仅为500 mg/L,因此所得出的结果存在一定差异。
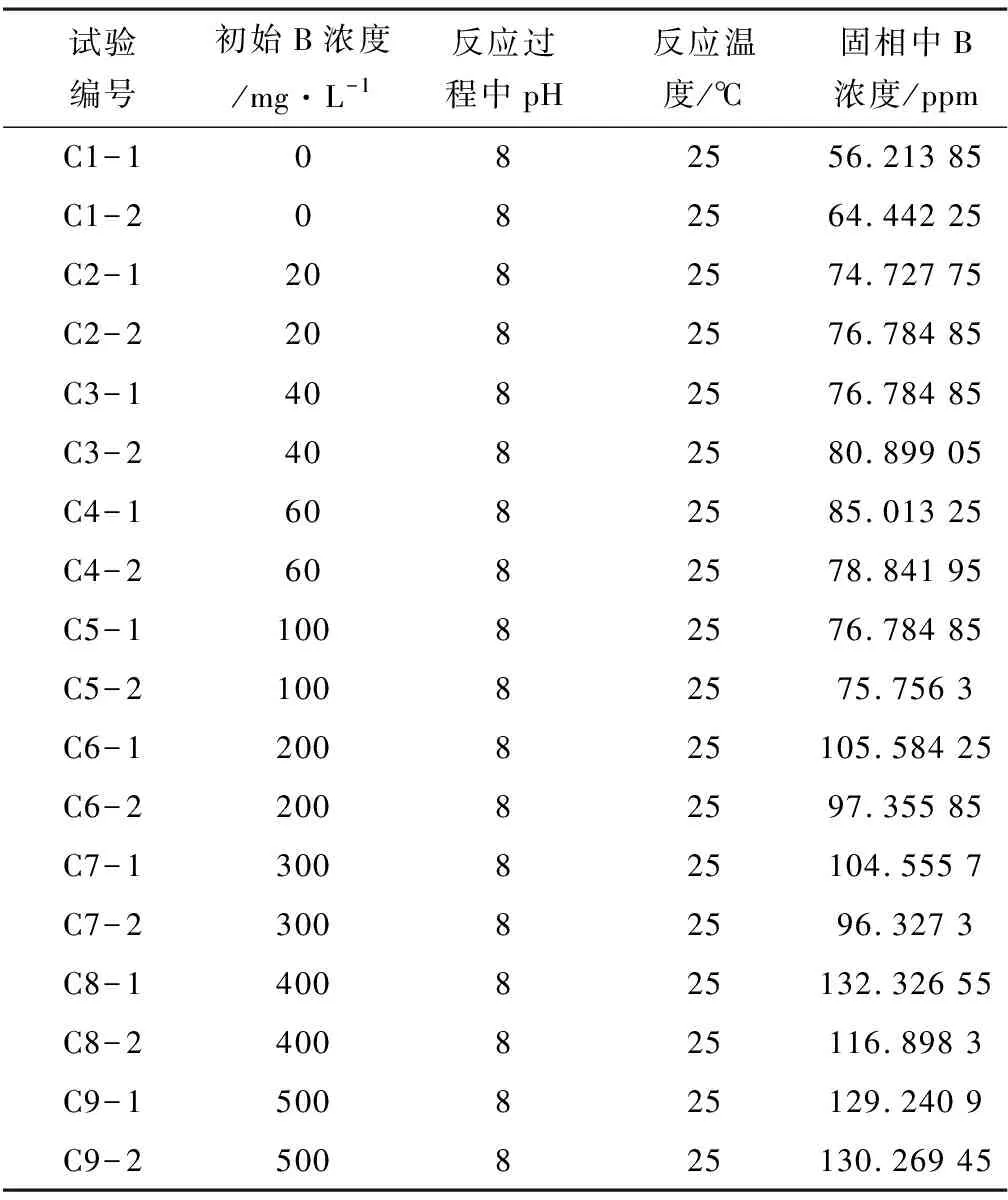
表3 初始溶液中硼浓度对固相中硼浓度的影响

图5 方解石对硼的吸附率随初始硼浓度变化
2.4 不同反应温度的影响
初始溶液中硼浓度40 mg/L,pH不变反应温度发生变化时方解石吸附硼的实验结果见表4,吸附量与温度变化关系见图6。由图6中可以看出当温度在25℃~65℃时,固相中的硼浓度明显升高,说明在此温度范围内温度升高对方解石吸附硼有着很强的促进作用,温度在80℃以上后虽然固相中硼浓度变化不大,方解石吸附硼的能力仍有所增加,但随着温度的继续升高,温度对方解石吸附硼的影响逐渐减小。此结果与Majidi A等在研究硼在钙质土壤中的吸附研究所得结果相似类似[4][10][11-12],当温度达到85℃时固相中的硼浓度达到250 ppm,可以看出高温有利于方解石吸附硼。程东升等研究认为,方解石与硼的吸附反应是一个吸热过程[12],所以当反应温度升高时方解石对硼的吸附量会增大。

表4 反应温度对固相中硼浓度的影响

图6 固相中硼浓度随反应温度的变化
2.5 不同pH的影响
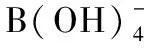

表5 pH对固相中硼浓度的影响

图7 固相中硼浓度随pH的变化
3 结语
通过利用Li2CO3的可溶但不易溶于水的特性,模拟自然条件下高温热泉口方解石对硼的吸附过程所得结论如下:
(1)当硼浓度在一定范围内时,随着初始硼浓度的增大方解石对硼的吸附率也逐渐增大。
(2)当温度升高时,方解石对硼的吸附能力也随之增强,当温度达到65℃以上时方解石的吸附效果最佳。
(3)pH升高时,固相中的硼浓度也逐渐升高,当pH在9左右时方解石吸附能力最佳,但本次研究尚无法解释该现象,仍需进一步研究。

