咪达唑仑、地佐辛复合瑞芬太尼在肝癌患者射频消融术中的应用效果观察Δ
王略伟,程建军,洪 伟,王文耀
(西安交通大学医学部附属三二〇一医院麻醉科,陕西 汉中 723000)
射频消融术是一种微创外科治疗方法,其原理是借助射频电极针使局部组织核心温度达到90 ℃以上,从而使肿瘤细胞坏死[1]。在肝癌射频消融术中,最主要的疼痛来源于刺痛、皮肤灼烧和内脏痛,除镇痛外,在一些特定部位病灶消融过程中还需患者能够被唤醒并配合治疗,对术中麻醉管理要求高,因此,提高患者舒适度及配合度对保证手术顺利进行具有重要影响[2-3]。瑞芬太尼以其半衰期短、起效迅速以及无蓄积特点在临床麻醉中得到了广泛应用,但瑞芬太尼可能会引起痛觉过敏,在停止输注后,患者会出现明显的疼痛感,影响患者术后恢复,降低患者术后舒适度,且瑞芬太尼大剂量使用时可引起剂量相关性呼吸抑制[4]。咪达唑仑具有作用时间短、起效快和毒性低等优点,并有抗肌肉松弛和抗焦虑等作用,对呼吸循环影响较小[5]。地佐辛具备激动κ受体和拮抗μ受体双重功能,镇静镇痛效果良好,对呼吸抑制影响较小,具有较高的安全性,研究结果表明地佐辛可以在一定程度上对瑞芬太尼产生的痛觉过敏进行抑制[6]。基于此,本研究比较了咪达唑仑与地佐辛分别复合瑞芬太尼在肝癌患者射频消融术中的应用效果及安全性,现报告如下。
1 资料与方法
1.1 资料来源
选取2019年12月至2022年12月我院收治的行射频消融术的肝癌患者97例进入研究。纳入标准:符合肝癌诊断标准[7];具有射频消融术适应证;美国麻醉医师协会分级标准为Ⅰ—Ⅱ级;知情同意。排除标准:长期使用阿片类药物者;具有其他恶性肿瘤者;具有心脏、肝肾功能衰竭者;意识障碍者;凝血功能异常者。本研究经我院医学伦理委员会审批。将所有患者按随机数字表法分为咪达唑仑组48例和地佐辛组49例,两组患者的一般资料具有可比性,见表1。
1.2 方法
两组患者术前常规禁饮禁食。开放静脉通路,严密监测心率(HR)、血氧饱和度(SpO2)和平均动脉压(MAP),鼻导管输氧。地佐辛组患者静脉给予地佐辛注射液(规格:1 mL∶5 mg)负荷量0.8 mg/kg,溶解于0.9%氯化钠注射液中,稀释至20 mL,注射10 min。咪达唑仑组患者静脉给予咪达唑仑注射液(规格:1 mL∶5 mg)50 mg,溶解于0.9%氯化钠注射液中,稀释至50 mL,按负荷量0.05 mg/kg剂量进行静脉注射。
两组患者均给予注射用盐酸瑞芬太尼(规格:1 mg),使用0.9%氯化钠注射液稀释至100 mL,以0.05 μg/(kg·min)维持麻醉。在超声指引下,应用CTRF-220型射频消融系统,靶温度设置在90 ℃,将电极刺入病灶进行消融。如果发生呼吸抑制,及时给予辅助通气等。
1.3 观察指标
(1)围手术期HR、SpO2和MAP:观察两组患者在入室时(T0)、消融开始时(T1)、消融开始后10 min(T2)和术毕时(T3)的HR、SpO2和MAP水平变化。(2)记录两组患者术中并发症(恶心呕吐、呼吸抑制、心动过缓及血压升高或降低)发生情况。(3)Ramsay镇静评分:记录两组患者在T0、T1、T2和T3时的Ramsay镇静评分[8]。(4)疼痛的视觉模拟评分(VAS)[9]:记录两组患者术毕、术后2 h和术后4 h的VAS评分,0分表示无痛,1~3分表示轻微疼痛,4~6分表示中度疼痛,7~10分表示重度疼痛。(5)记录两组患者术后不良反应发生情况。
1.4 统计学方法
2 结果
2.1 两组患者术中血流动力学指标比较
两组患者各时间点的HR、MAP和SpO2水平比较,差异均无统计学意义(P>0.05),见表2。
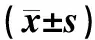
表2 两组患者术中HR、SpO2和MAP水平比较
2.2 两组患者术中并发症发生情况比较
地佐辛组患者术中并发症发生率低于咪达唑仑组,差异有统计学意义(P<0.05),见表3。

表3 两组患者术中并发症发生情况比较
2.3 两组患者不同时间Ramsay镇静评分比较
T1、T2和T3时,两组患者Ramsay镇静评分的差异均无统计学意义(P>0.05),见表4。
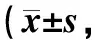
表4 两组患者不同时间Ramsay镇静评分比较分)
2.4 两组患者术后VAS评分比较
地佐辛组患者术后2、4 h时的VAS评分显著低于咪达唑仑组,差异均有统计学意义(P<0.05),见表5。
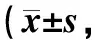
表5 两组患者术后VAS评分比较分)
2.5 两组患者不良反应发生情况比较
两组患者不良反应总发生率的差异无统计学意义(P>0.05),见表6。

表6 两组患者不良反应发生情况比较[例(%)]
3 讨论
肝癌射频消融术是一种使用电极针,经过皮肤、肝脏穿刺进入肿瘤内部,利用产热原理杀灭肿瘤,从而实现肿瘤治疗的临床治疗方法[10]。随着近年来射频消融术应用范围扩大,其风险也在不断升高,对于某些特殊部位病灶的治疗,患者的密切配合尤为关键。如在近心包病灶进行穿刺时,患者需屏住呼吸,以防止肝脏因呼吸运动而移位,在消融过程中,患者必须保持静止,任何身体动作都会增加心包损伤的风险;另外,在肝脏Ⅱ、Ⅶ、Ⅷ段术中,由于病灶被右下肺和剑突遮挡,手术过程中要求患者积极配合执行深吸气和屏气,以便使膈肌下移,更好地显示病灶。因此,射频消融术安全、有效的麻醉管理是值得讨论的重要问题,该问题的关键在于如何让患者更好地配合手术,同时减轻痛苦。
与芬太尼相比,地佐辛引起恶心呕吐、头痛头晕等不良反应的发生率明显较低,因此,可以选择给予患者小剂量地佐辛来达到有效镇痛目的。咪达唑仑是常用的镇静药,可用于射频消融术镇静,可以单独使用或与其他药物联合应用,咪达唑仑注射静脉,起效时间为65~100 s,剂量增加则起效迅速,镇静效果与剂量有关,0.3 mg/kg剂量的镇静作用较差,无法满足临床需求;0.05 mg/kg剂量即可获得良好的镇静效果。基于此,本研究设置地佐辛负荷量0.8 mg/kg、咪达唑仑负荷量0.05 mg/kg分别联合瑞芬太尼用于肝癌患者射频消融术中,结果显示,两组患者术中血流动力学指标和各时间点Ramsay镇静评分比较,差异均无统计学意义(P>0.05)。当Ramsay镇静评分为1~2分时,患者舒适度较低;而当镇静评分为5~6分时,患者很难被及时唤醒,且患者醒来后的配合程度较低[11]。本研究中,两组患者的Ramsay镇静评分均在3~4分,表明患者术中易唤醒,能较好地配合手术医师,咪达唑仑和地佐辛均可迅速镇静,且血流动力学稳定。
瑞芬太尼药效持续时间短,长期输注不会蓄积,但有研究结果表明瑞芬太尼可触发痛觉过敏,在停药后患者会有剧烈痛觉,必要时需追加其他镇痛药,对术后恢复不利[12-13]。而且,与镇静药共同使用的镇痛药可能会增加瑞芬太尼引起的呼吸抑制的发生风险[14]。本研究结果显示,地佐辛组患者术后2、4 h的VAS评分显著低于咪达唑仑组,术中并发症发生率显著低于咪达唑仑组,表明地佐辛可以明显减轻瑞芬太尼触发痛觉过敏,降低术中并发症发生率,与张宜林等[15]的研究结果一致。地佐辛主要激动κ和δ受体,对于μ受体也有一定的拮抗作用,因此不会形成典型的μ受体依赖性[16-17]。与其他阿片类药物相比,地佐辛具有更强的镇痛效果,还能使胃肠平滑肌松弛,从而减少恶心呕吐等不良反应的发生[18];地佐辛通过对μ受体的激动-拮抗作用,可以有效降低呼吸抑制情况,且对患者意识几乎不会产生影响[19-20]。
综上所述,肝癌射频消融术中咪达唑仑、地佐辛联合瑞芬太尼均可实现良好的清醒镇痛;地佐辛可以进一步降低患者术中并发症发生率,减轻触发痛觉过敏。

