替格瑞洛递减联合尼可地尔对老年急性冠脉综合征PCI术后干预的有效性和安全性
邵翔,卞宁,王鸿燕,田海涛,华参,吴超联,朱北星,陈睿,李俊侠,李田昌,马路*
1解放军医学院,北京 100853;2解放军总医院第六医学中心老年医学科,北京 100048;3北京朝阳中西医结合急诊抢救医院心内科,北京 100022;4解放军总医院第七医学中心心内科,北京 100700;5解放军总医院第六医学中心心内科,北京 100048
急性冠脉综合征(acute coronary syndromes,ACS)是临床常见的心血管疾病,具有起病急骤、病情复杂多变、病死率高的特点,是致死致残的重要原因,给人类的健康造成了巨大负担[1‐3]。随着老年人口不断增长,ACS 的发病率也逐年增高,每年全球约有超过700万人被诊断为ACS[4]。由于动脉粥样硬化斑块的增加及其解剖学的复杂性,加之与年龄相关的心血管和非心血管并发症,老年ACS 患者的预后更差。经皮冠状动脉介入(percutaneous coronary intervention,PCI)是目前治疗该病的主要方法,可通过恢复心外膜相关动脉的通畅性,实现血流再灌注,控制心肌损伤程度[5]。对于ACS接受PCI治疗的患者,指南推荐联合运用阿司匹林+P2Y12 抑制剂抗血小板治疗1年[6‐7]。强效P2Y12抑制剂在带来缺血获益的同时可能增加出血风险。老年患者更易发生出血事件,因此,本研究观察老年ACS 患者PCI 术后替格瑞洛的降阶梯治疗联合尼可地尔干预的有效性及安全性,旨在探索如何降低老年ACS 患者PCI 术后出血事件的发生风险,且不增高缺血事件发生率的方法。
1 资料与方法
1.1 研究对象 选择2016年11月-2019年6月于解放军总医院第六、第七医学中心及北京朝阳中西医结合急诊抢救医院诊治的符合条件的PCI 术后老年ACS 患者300 例,其中,男153 例,女147 例,年龄65.0~88.0(73.3±5.6)岁。根据疾病特征将所有受试者分 为ST 段 抬 高 型 心 肌 梗 死(ST elevation myocardial infarction,STEMI)、非ST 段抬高型心肌梗死(non‐ST elevation myocardial infarction,NSTEMI)和不稳定性心绞痛(unstable angina,UA)三个区组(block)。由各参研单位根据入组受试者的疾病特征将其分别分配至STEMI、NSTEMI 或UA 区组,上报研究中心,指派专人将各参研单位上报患者进行统一编号,然后利用随机数字表再在区组内将受试者随机分为替格瑞洛递减+尼可地尔组(n=154)与替格瑞洛组(n=146),并告知参研单位进行相应的干预措施。其中,替格瑞洛组有急性STEMI 55 例、急性NSTEMI 73例及UA 18例;替格瑞洛递减+尼可地尔组有急性STEMI 58 例、急性NSTEMI 77 例及UA 19 例。本研究获北京朝阳中西医结合急诊抢救医院伦理委员会审批(2022伦审第4号)。
1.2 诊断标准
1.2.1 STEMI 诊断标准 符合中华医学会心血管病学分会《急性ST 段抬高型心肌梗死诊断和治疗指南》(2015版)[8]的诊断标准:(1)超过10~20 min的胸骨后或心前区剧烈压榨性疼痛(应排除主动脉夹层、气胸、急性肺栓塞等引起的胸痛),或伴放射痛,或伴有大汗、恶心、呼吸困难等,含服硝酸甘油无法缓解;(2)查体可见皮肤湿冷、面色苍白、颈静脉怒张等;(3)听诊可闻及肺部啰音、心脏杂音和奔马律等;(4)心电图可见急性心肌梗死心电图改变;(5)血清心肌损伤标记物升高且动态变化;(6)影像学检查提示室壁运动异常或新的存活心肌丧失。
1.2.2 NSTEMI及UA诊断标准 符合中华医学会心血管病学分会《非ST段抬高型急性冠状动脉综合征诊断和治疗指南》(2016 版)[9]的诊断标准:(1)临床表现为典型或不典型的心绞痛,如长时间(>20 min)静息性心绞痛,或新发心绞痛,近1 个月内症状加重的稳定性心绞痛,并具有至少加拿大心血管学会(Canadian Cardiovascular Society,CCS)Ⅲ级的特点,或于心肌梗死后1 个月内出现心绞痛;(2)查体可闻及新出现的肺部啰音、第三心音等非特异性体征;(3)心电图可见ST 段下移或T 波异常改变;(4)生物标志物高敏肌钙蛋白(high‐sensitivity cardiac troponin,hs‐cTn)水平升高;(5)无创药物或运动负荷检查可诱导缺血发作。
1.3 纳入及排除标准 纳入标准:(1)入院诊断为STEMI、NSTEMI及UA,包括发病12 h内或发病12~24 h仍伴有胸痛,或持续性ST段抬高,或新发左束支阻滞;(2)双联抗血小板治疗(dual antiplatelet therapy, DAPT) 评 分≥2 分, 新 型DAPT 评 分(PRECISE‐DAPT)≥25分的老年患者;(3)年龄>65岁;(4)符合《中国经皮冠状动脉介入治疗指南(2016)》中的适应证,患者接受PCI 治疗[10];(5)严格遵医嘱规律服用所有口服药物。排除标准:(1)STEMI患者近2 周进行过溶栓治疗,或长期应用抗凝药物;(2)近1 个月内有活动性出血,有严重外伤或行外科大手术;(3)血小板计数<100×109/L,存在出血倾向,或有凝血功能障碍;(4)合并严重的肝、肾、神经系统和血液系统病变、恶性肿瘤等全身疾病,或预计寿命不足1年;(5)合并主动脉夹层、肺栓塞及气胸;(6)对替格瑞洛、尼可地尔或造影剂过敏。
1.4 治疗方法 两组均给予阿司匹林、他汀、ACEI、β 阻滞剂等药物治疗,此外,替格瑞洛组给予替格瑞洛180 mg 负荷剂量后行PCI,术后给予替格瑞洛90 mg bid,服用至少12 个月;替格瑞洛递减+尼可地尔组给予替格瑞洛180 mg 负荷剂量后PCI,术后给予替格瑞洛90 mg bid+尼可地尔5 mg tid,6 个月后改为替格瑞洛60 mg bid+尼可地尔5 mg tid,服用至少12个月。对所有患者进行随访,时间为住院期间及出院后随访1、3、6、12个月。
1.5 观察指标
1.5.1 基本资料 记录所有患者的性别、年龄、体重指数(BMI)、既往病史[有无高血压、糖尿病、心肌梗死、PCI 及冠状动脉旁路移植术(coronary artery bypass grafting,CABG)史]、病变长度、手术入路、支架数目和主动脉球囊反搏(intra‐aortic balloon pump,IABP)例数等基本资料。
1.5.2 主要终点及定义 研究的主要终点为PCI 术后1~12个月的心血管死亡、心肌梗死、缺血性卒中的复合终点,血小板抑制和患者后果结局研究(platelet inhibition and patient outcomes,PLATO)定义的轻微出血、次要出血、其他主要出血和主要致命/危及生命的出血的复合终点,以及心血管死亡、心肌梗死、缺血性卒中与PLATO研究定义出血的复合终点。PLATO研究的出血定义[11]:(1)主要致命或危及生命的出血、致命性或颅内出血、伴有心包填塞的心包内出血、出血所导致的低血容量休克或严重低血压需要升压药或手术;(2)其他主要出血:出血致明显功能丧失(如眼内出血伴永久性失明)、出血有关的血红蛋白(HGB)下降(30~50 g/L)、因出血而输血2~3 U(全血或浓集红细胞)等;(3)次要出血:需要医学干预止血或治疗的出血(如需到医院进行填塞治疗的鼻出血);(4)轻微出血:其他如擦伤、牙龈出血等不需干预或治疗的出血事件。
1.5.3 超声心动图测量左室心肌重量(left ventricular mass,LVM)及左室心肌重量指数(left ventricular mass index,LVMI) 采用美国GE Vingmed 公司System‐Five 型彩色多普勒超声显像系统进行检测,探头频率2.5 MHz。用M 型超声时按ISFC/WHO 推荐的标准检测,所得数据均重复2或3次,并取几次测量近似值的平均值作为本次检查的结果。按Devereux 公式[12]计算出LVM 及LVMI:LVM(g)=1.04×[(LVEDd+LVPWT+IVST)3-LVEDd3]-13.6;LVMI(g/m2)=LVM/体表面积(BSA)。
1.5.4 实验室检测 采用化学发光免疫法检测脑钠肽(brain natriuretic peptide,BNP),免疫层析法检测氨基末端‐脑钠肽前体(N terminal pro‐brain natriuretic peptide,NT‐proBNP),均使用雅培公司i2000化学发光仪及试剂测定,试剂盒均由武汉明德生物科技股份有限公司提供。采用全自动生化分析仪、化学发光仪、荧光免疫定量分析仪等进行肌钙蛋白I(cardiac troponin I, cTnI)、 HGB、 血 小 板 浓 度(platelet,PLT)、血清肌酐浓度(creatinine,Cr)、高敏C反应蛋白(high sensitivity C‐reactive protein,hs‐CRP)等指标检测。
1.6 指标分析 收集并比较两组患者性别、年龄、体重指数(BMI)、吸烟史、既往病史、cTnI、HGB、PLT、Cr、hs‐CRP、病变长度、LVMI、BNP、NT‐proBNP、手术入路、支架数目和IABP等基线资料的差异。比较PCI 术后1~12 个月缺血、出血及复合终点事件累积发生率的差异,并绘制生存曲线。
1.7 统计学处理 采用SPSS 23.0 软件进行统计分析。计量资料行正态性检验,呈正态分布者以x±s表示,组间比较采用t检验;呈偏态分布者以M(Q1,Q3)表示,组间比较采用Mann‐WhitneyU检验。计数资料以例(%)表示,组间比较采用χ2检验或Fisher确切概率法。患者置入支架数目的组间比较采用等级资料的秩和检验。绘制生存曲线,采用Kaplan‐Meier 法 进 行 生 存 分 析 并 行Log‐rank 检 验。P<0.05为差异有统计学意义。
2 结 果
2.1 两组一般资料比较 两组患者的性别、年龄、体重指数(BMI)、吸烟史、糖尿病及高血压等一般资料,以及术前既往病史(心肌梗死、PCI 及CABG)、cTnI、HGB、PLT、Cr、hs‐CRP、病变长度、LVMI、BNP、NT‐proBNP、手术入路、支架数目和IABP 等差异均无统计学意义(P>0.05),具有可比性(表1)。
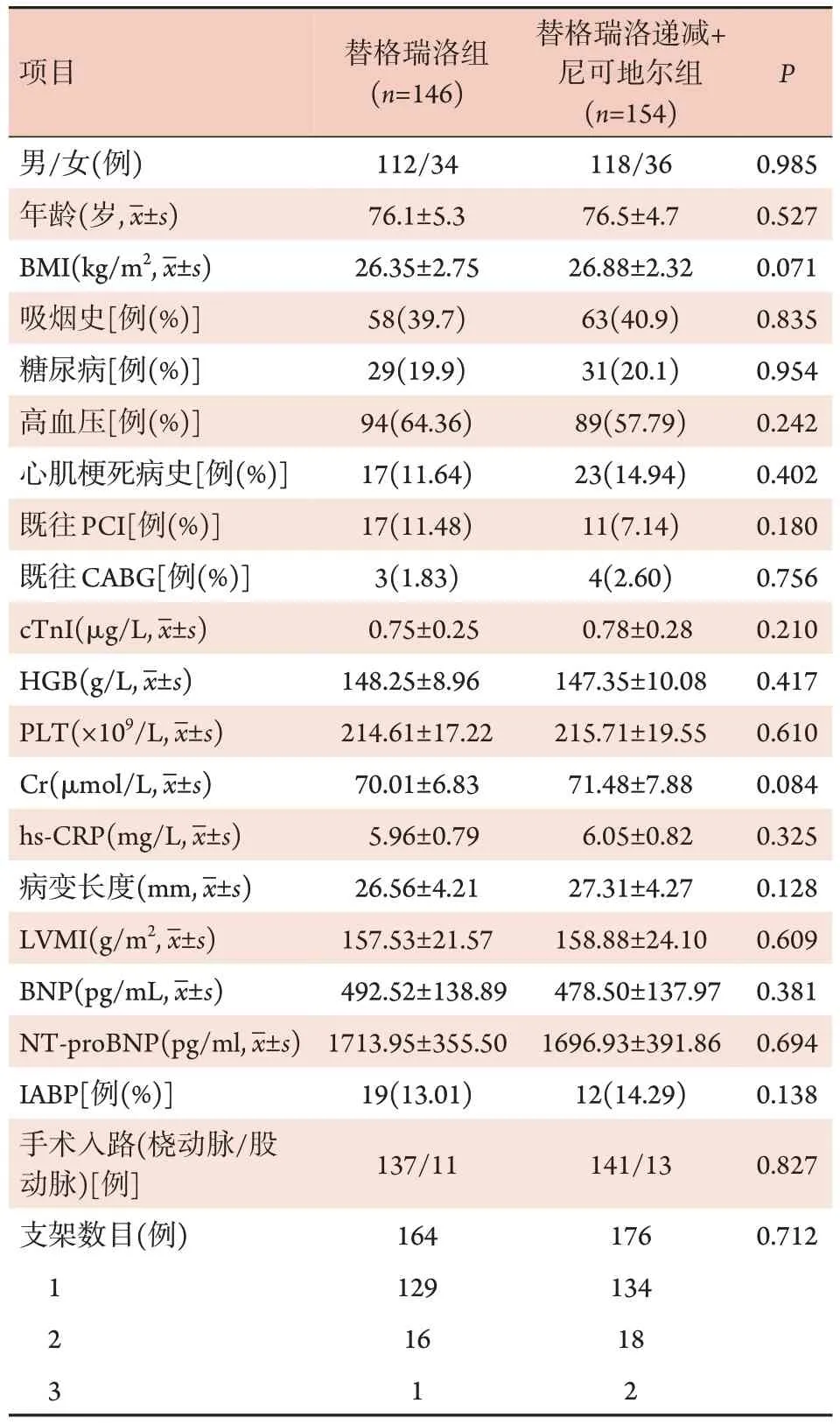
表1 两组老年ACS患者基线资料比较Tab.1 Comparison of baseline information between the two groups of elderly patients with ACS
2.2 两组主要终点及出血事件的比较 替格瑞洛递减联合尼可地尔组心血管死亡1 例、缺血性卒中2 例、再发心肌梗死3 例;替格瑞洛组心血管死亡2 例、缺血性卒中1 例、再发心肌梗死3 例。两组缺血性(心血管死亡、心肌梗死、缺血性卒中)复合终点事件的发生率分别为3.90%和4.11%,差异无统计学意义(χ2=0.015,P=0.903)。两组出血事件方面,替格瑞洛递减联合尼可地尔组轻微出血3 例、次要出血0例、其他主要出血0例和主要致命或危及生命的出血0 例;替格瑞洛组分别为8 例、4 例、0 例和1例,两组出血类别差异无统计学意义(P=0.215)。替格瑞洛递减联合尼可地尔组出血事件累积发生率明显低于替格瑞洛组(χ2=6.077,P=0.014)。两组心血管死亡、心肌梗死、缺血性卒中与PLATO定义出血的复合终点事件的发生率分别为5.84%和13.01%,复合终点事件累积发生率差异有统计学意义(χ2=4.456,P<0.05,图1)。
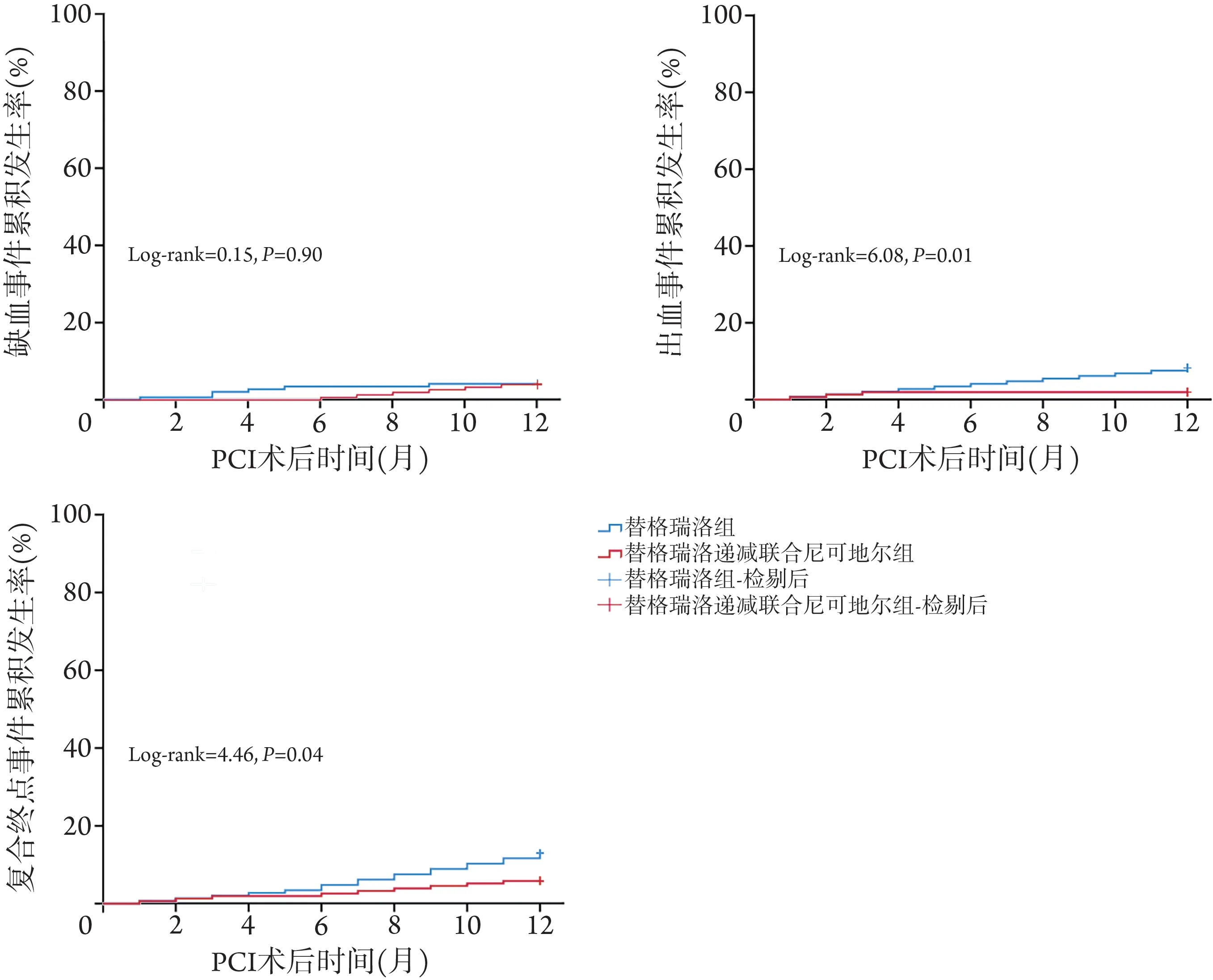
图1 两组老年ACS患者主要终点及出血事件累积发生率的比较Fig.1 Comparison of cumulative incidence of ischemic events, hemorrhagic events and composite end point events between the two groups of elderly patients with ACS
3 讨 论
近年来,尽管PCI 技术在不断优化,但多数ACS 患者PCI 术后仍存在较高的缺血风险[13],尤其对于复杂性ACS 冠状动脉病变和糖尿病患者[14]。目前,以阿司匹林和P2Y12 抑制剂为代表的DAPT 是ACS 患者PCI 支架植入术后药物治疗的基础和核心环节[15],旨在减少术后血栓并发症和缺血事件的发生。PCI 术后早期血栓形成风险高,随着患者病情稳定,血栓形成风险有所下降[16],而出血风险随之增加,尤其是在使用强效P2Y12抑制剂时[17]。此时,如何平衡术后缺血和出血,以及如何选择最佳的抗血小板方案等是临床医师重点关注的问题。
既往的多项研究探索了短期DAPT 方案的疗效和安全性,如Yin 等[18]发现,短期DAPT 与标准期DAPT 的疗效和安全性相似,大多数放置药物洗脱支架的PCI 术后患者可考虑短期DAPT。NIPPON 研究发现,PCI术后6个月的短期DAPT与18个月的长期DAPT 相比,不良临床事件和脑血管事件(net adverse clinical and cerebrovascular events,NACCE)的发生率差异无统计学意义,短期DAPT 具有非劣效性[19]。而SMART DATE研究结果显示,6个月DAPT组心肌梗死发生率明显高于≥12 个月或更长时间的DAPT组[20]。由此可见,短期DAPT方案的疗效与安全性仍有待充分验证,在这种情况下,抗血小板治疗的降级策略成为一种颇具吸引力的选择,且在临床中经常被选用,既往的TWILIGHT、TOPIC、TROPICAL‐ACS 试验[21‐23]均对使用单一抗血小板药物或更换P2Y12抑制剂来实现降级进行了探索。
有研究证实,对于PCI 术后病情稳定的急性心肌梗死患者,降级策略可通过减少出血事件降低长达12 个月的净临床事件风险[16]。在接受PCI 联合阿司匹林和普拉格雷抗血小板治疗的ACS 患者中,1个月后减少1/2普拉格雷剂量可使净不良临床事件的风险降低[24]。对于接受替格瑞洛治疗的患者,在最大缺血风险期渡过后,可考虑降级[25]。相关研究均显示,抗血小板降级治疗在减少缺血事件方面并不亚于传统治疗,但是出血率方面大多数研究在降级治疗中均有下降。因此,在减少出血而不增加缺血事件方面,降级策略是较为安全、有效的策略[26]。
PCI 可通过解除心外膜下冠状动脉的梗阻以实现心肌的血运重建,恢复缺血心肌的血流。但有研究发现,由于心肌层面未达到有效灌注,部分PCI术后心外膜大血管达到心肌梗死溶栓治疗(thrombolysis in myocardial infarction,TIMI) 3 级血流的患者临床疗效并不乐观[27]。目前仍未明确PCI 术后发生心肌灌注不足的原因,有研究认为与微血管阻塞(microvascular obstruction,MVO)、缺血/再灌注损伤、高血小板活性和血栓负担,以及个体差异等密切相关[28‐30]。其中,MVO 被认为是发生心肌灌注不足的重要原因,急诊冠状动脉介入操作对于心血管本身是一种外源性刺激,因而原位血栓或微血栓的脱落可造成微血管阻塞,因此,强化抗血小板治疗成为预防和治疗心肌灌注不足的可行方法[31‐32]。
替格瑞洛是一种高效、新型的口服抗血小板药物,相较于氯吡格雷,不需经肝药酶代谢激活,可选择性抑制二磷酸腺苷(adenosine diphosphate,ADP)与血小板P2Y12 受体结合,抗血小板聚集作用更明显,且患者发生氯吡格雷抵抗后服用替格瑞洛仍有效[33]。尼可地尔是ATP 敏感性钾通道开放剂,同时具有扩张冠状动脉微循环及阻力血管的硝酸酯类作用[34],既能改善微循环,也能扩张大冠状动脉。因此,替格瑞洛联合尼可地尔干预,可能进一步减少ACS 的缺血事件发生,而当血栓形成风险降低时,减少替格瑞洛用量又可降低出血事件的发生率。本研究意图使“冠状动脉树”全面开放以抗缺血,在出血成为主要风险时替代抗血小板药物的抗缺血作用,以减少缺血事件的发生。本试验观察到老年ACS 患者PCI 术后以替格瑞洛+尼可地尔干预6 个月后替格瑞洛减量随访12个月,PLATO研究定义的主要致命/危及生命出血、其他主要出血、次要出血和轻微出血的复合终点事件累积发生率低于替格瑞洛组,差异有统计学意义(P<0.05)。本研究还发现,两组心血管死亡、心肌梗死、缺血性卒中的复合终点比较差异无统计学意义(P>0.05),而心血管死亡、心肌梗死、缺血性卒中与PLATO定义出血的复合终点比较则差异有统计学意义(P<0.05),提示替格瑞洛递减联合尼可地尔干预后,缺血事件发生率与常规替格瑞洛治疗相比未见增高,而出血发生率明显降低,与以上研究结果类似。
综上所述,对于老年ACS 患者PCI 术后,替格瑞洛递减联合尼可地尔干预有可能减少出血且不增加缺血事件的发生。通过对替格瑞洛递减联合尼可地尔干预的抗血小板治疗降级策略的研究,可对临床决策起参考作用。但本研究仍存在一定的局限性,如本研究属于探索性研究、样本量小、事件发生率低等。今后应开展更大规模的随机对照研究,以进一步探讨替格瑞洛递减联合尼可地尔干预的抗血小板治疗降级策略问题。

