探讨奥卡西平联合左乙拉西坦治疗小儿癫痫的效果及对患儿认知功能的影响
李彩云 徐成 许青国 黄瑞
临床中, 癫痫属于常见疾病之一, 归属于慢性神经系统疾病类型, 其发生率较高, 患者多存在认知功能障碍, 疾病往往会对患者沟通能力、记忆能力、执行功能产生损害, 继而严重损害患者的生活质量[1-3]。癫痫在小儿群体中较为常见, 其临床症状多表现为情感异常、意识模糊、感觉异常、肌肉抽搐等, 待患儿长期保持癫痫持续状态, 极易危害到患儿生命安全[4]。相关研究提示, 针对癫痫并发认知功能障碍的患儿实施治疗时, 药物可发挥显著突出作用, 对癫痫具有良好的控制作用[5]。然而, 通常单独用药所得疗效有限[6]。鉴于此, 本研究于2021 年3 月~2022 年11 月期间, 从本院选取60 例癫痫患儿作为研究对象, 分析联合奥卡西平与左乙拉西坦治疗的效果以及对患儿认知功能的影响。
1 资料与方法
1.1 一般资料 2021 年3 月~2022 年11 月, 使用随机数字表法将60 例癫痫患儿分为观察组及对照组, 均30 例。对照组内, 包括12 例男性, 18 例女性;年龄3~10 岁, 平均年龄(5.24±1.76)岁;病程10 d~3 年,平均病程(2.13±0.52)年。观察组内, 包括13 例男性,17 例女性;年龄3~11 岁, 平均年龄(5.19±1.96)岁;病程10 d~4 年, 平均病程(2.24±0.59)年。两组患儿的一般资料比较, 差异无统计学意义(P>0.05), 资料可比。见表1。
表1 两组患儿一般资料比较[n(%), ±s]

表1 两组患儿一般资料比较[n(%), ±s]
注:两组比较, P>0.05
组别 例数 性别 平均年龄(岁) 平均病程(年)男女对照组 30 12(40.00) 18(60.00) 5.24±1.76 2.13±0.52观察组 30 13(43.33) 17(56.67) 5.19±1.96 2.24±0.59 χ2/t 0.069 0.104 0.766 P 0.793 0.918 0.447
1.2 纳入及排除标准
1.2.1 纳入标准 ①属于特发性癫痫;②年龄为3~11 岁;③接受治疗前蒙特利尔认知评估量表(MoCA)总分<20 分;④患儿或(及)其家长了解具体研究方案,签署自愿参与书, 且通过本院伦理委员会批准;⑤患儿满足相关诊断标准[7]。
1.2.2 排除标准 ①伴发恶性肿瘤疾病;②对此次研究涉及药物存在过敏问题;③伴发严重脑外伤;④存在颅脑手术史;⑤不配合本次研究以及基本资料欠缺患儿。
1.3 方法
1.3.1 对照组 予以奥卡西平(商品名:曲莱, Novartis Farma S.p.A., 北京诺华制药有限公司分装, 国药准字HJ20171032)单独治疗, 口服, 首次用量为:10 mg/(kg·d), 结合患儿病情调整药物用量, 最大用药剂量为48 mg/(kg·d)。持续治疗16 周。
1.3.2 观察组 联合奥卡西平与左乙拉西坦治疗, 奥卡西平用法用量和对照组保持一致, 口服应用左乙拉西坦[商品名:开浦兰, UCB PharmaS.A., 优时比(珠海)制药有限公司分装, 国药准字HJ20160254], 首次用量为:5~10 mg/(kg·d), 结合患儿病情调整药物用量,最大用药剂量为60 mg/(kg·d)。持续治疗16 周。
1.4 观察指标及判定标准
1.4.1 比较两组患儿的治疗效果 治疗后, 患儿癫痫持续状态停止, 且48 h 内未出现发作情况, 即显效;治疗后, 患儿癫痫持续状态未立即停止, 但也逐渐停止, 且48 h 内无复发现象, 即有效;治疗后, 患儿癫痫持续状态未停止, 且48 h 内再次发作, 即无效。治疗总有效率=显效率+有效率[8]。
1.4.2 比较两组患儿的免疫功能 分别于治疗前和治疗16 周后评价两组患儿的免疫功能, 采集空腹静脉血5 ml, 以3000 r/min, 半径10 cm, 离心处理10 min, 分离血清, 应用免疫比浊法测定IgA、IgM、IgG, 应用流式细胞仪检测CD3+、CD4+。
1.4.3 比较两组患儿的认知功能 分别于治疗前和治疗16 周后评价两组患儿的认知功能, 应用韦氏儿童智力量表进行测定, 测定指标包括FIQ、PIQ、VIQ[9]。
1.4.4 比较两组患儿的不良反应发生情况 包括轻度皮疹、头晕、嗜睡、胃肠道反应, 不良反应发生率=不良反应发生例数/总例数×100.00%。
1.4.5 比较两组患儿的症状改善指标 包括临床症状好转时间、癫痫持续时间以及癫痫发作次数。
1.5 统计学方法 此次研究全部数据均经SPSS23.0软件统计。应用均数±标准差(±s)表示计量资料,并应用t 检验;应用[n(%)]表示计数资料, 采用χ2检验。当P<0.05 时, 提示具备统计学差异。
2 结果
2.1 两组患儿的治疗效果比较 和对照组进行比较, 观察组治疗总有效率显著较高, 其中对照组治疗 总 有 效 率 为73.33%, 观 察 组 为93.33%(χ2=4.320,P=0.038<0.05)。见表2。
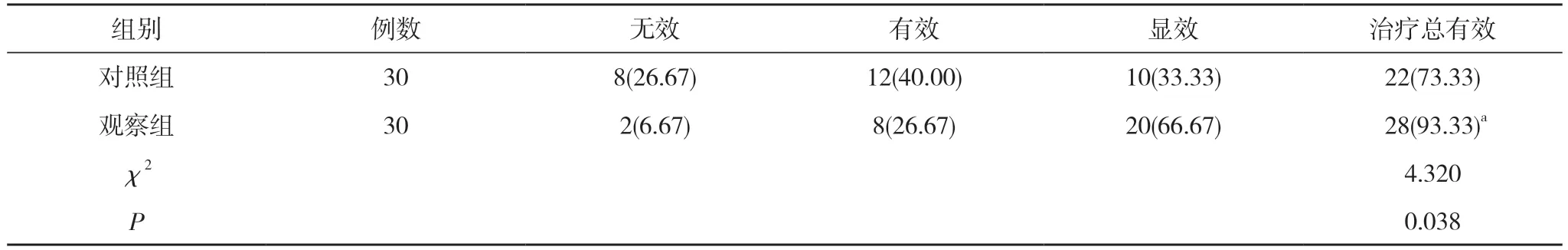
表2 两组患儿的治疗效果比较[n(%)]
2.2 两组患儿的免疫功能改善情况比较 两组患儿的IgA、IgM、IgG、CD3+、CD4+水平治疗前比较无统计学差异(P>0.05);治疗后, 两组患儿的IgA、IgM、IgG、CD3+、CD4+水平均升高, 且观察组高于对照组,差异显著(P<0.05)。见表3。
表3 两组患儿的免疫功能改善情况比较( ±s)

表3 两组患儿的免疫功能改善情况比较( ±s)
注:与本组治疗前比较, aP<0.05;与对照组治疗后比较, bP<0.05
组别 例数 IgA(g/L) IgM(g/L) IgG(g/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 30 0.77±0.39 1.08±0.16a 0.69±0.52 1.03±0.30a 7.40±3.08 12.32±1.60a观察组 30 0.80±0.42 1.26±0.12ab 0.74±0.55 1.34±0.29ab 7.69±3.19 14.48±1.22ab t 0.287 4.930 0.362 4.069 0.358 5.880 P 0.775 0.000 0.719 0.000 0.721 0.000组别 例数 CD3+(%) CD4+(%)治疗前 治疗后 治疗前 治疗后对照组 30 51.36±8.53 64.26±9.08a 27.34±7.12 45.23±7.52a观察组 30 50.29±7.94 72.02±9.36ab 26.59±7.22 50.30±7.12ab t 0.503 3.259 0.405 2.682 P 0.617 0.002 0.687 0.010
2.3 两组患儿的认知功能改善情况比较 两组患儿的FIQ、PIQ、VIQ 水平治疗前比较无统计学差异(P>0.05);治疗后, 两组患儿的FIQ、PIQ、VIQ 水平均升高, 且观察组均高于对照组, 差异显著(P<0.05)。见表4。
表4 两组患儿的认知功能改善情况比较( ±s, 分)

表4 两组患儿的认知功能改善情况比较( ±s, 分)
注:与本组治疗前比较, aP<0.05;与对照组治疗后比较, bP<0.05
组别 例数 FIQ PIQ VIQ治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 30 96.19±1.94 98.05±1.13a 94.34±2.88 96.29±1.29a 94.02±2.92 96.32±1.78a观察组 38 96.25±2.02 99.26±1.04ab 94.28±2.96 98.25±1.18ab 93.97±2.89 98.39±1.94ab t 0.117 4.315 0.080 6.141 0.067 4.306 P 0.907 0.000 0.937 0.000 0.947 0.000
2.4 两组患儿的不良反应发生情况比较 对照组和观察组患儿的不良反应发生率比较, 无统计学差异(P>0.05)。见表5。

表5 两组患儿的不良反应发生情况比较[n(%)]
2.5 两组患儿的症状改善指标比较 观察组患儿的临床症状好转时间、癫痫持续时间短于对照组, 癫痫发作次数少于对照组, 差异显著(P<0.05)。见表6。
表6 两组患儿的症状改善指标比较( ±s)
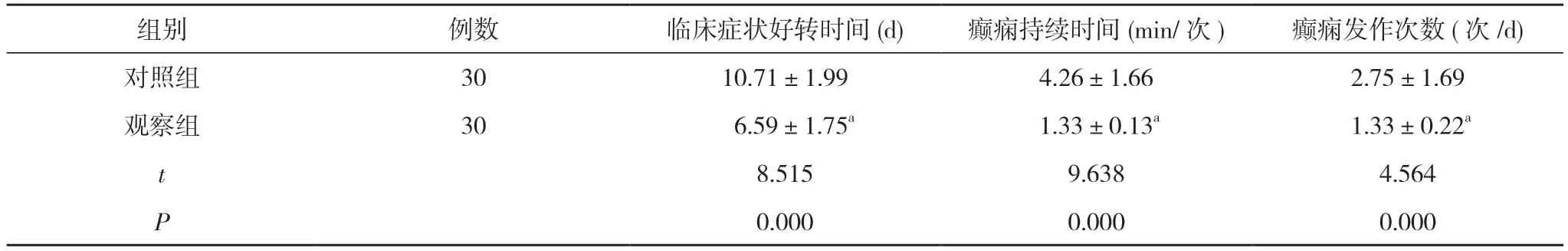
表6 两组患儿的症状改善指标比较( ±s)
注:与对照组比较, aP<0.05
组别 例数 临床症状好转时间(d) 癫痫持续时间(min/次) 癫痫发作次数(次/d)对照组 30 10.71±1.99 4.26±1.66 2.75±1.69观察组 30 6.59±1.75a 1.33±0.13a 1.33±0.22a t 8.515 9.638 4.564 P 0.000 0.000 0.000
3 讨论
癫痫是比较常见的一种慢性神经系统疾病, 具有较高的发病率, 患儿通常伴随一定程度的认知功能障碍, 影响记忆、语言表达、定向力以及视空间与执行功能等, 造成患儿生活质量下降[10-12]。患儿在发病后,会出现意识不清晰的症状, 而且患儿四肢出现抽搐, 从病症特点上看, 癫痫发病较为突然, 而且会导致患儿反复发作, 使患儿的生活受到严重影响, 治疗难度较高[13,14]。在临床治疗中, 能够通过多种药物使患儿的病症得到缓解, 但是在常规药物治疗中, 患儿的治疗效果并没有达到预期, 而且药物副作用也会对患儿造成较大的影响, 导致患儿出现多种不良反应。因此, 积极采用联合治疗方案具有十分重要的价值[15,16]。
此次研究结果提示, 和对照组进行比较, 观察组治疗总有效率显著较高, 其中对照组治疗总有效率为73.33%, 观察组为93.33%;经相应治疗后, 两组IgA、IgM、IgG、CD3+、CD4+水平均升高, 且观察组高于对照组;治疗后, 两组患儿FIQ、PIQ、VIQ 水平均升高,且观察组均高于对照组。由此可知, 癫痫患儿联合应用奥卡西平与左乙拉西坦治疗能够发挥突出效果, 不仅能够改善患儿免疫功能, 而且可改善患儿的认知功能, 利于患儿病情康复, 分析原因:奥卡西平属于新型抗癫痫药物之一, 包含了治疗癫痫的主要活性成分, 人体代谢时间较长, 药效时间持续久, 安全性高, 其作用机制主要通过对电压敏感性钠离子通道产生阻滞, 抑制谷氨酸能兴奋性突触后电位, 能够促使谷氨酸释放减少[17,18]。与此同时, 奥卡西平能够提升钾离子传导性, 调节电压, 从而激活钙离子通道, 减弱谷氨酸能的传导, 最终发挥抗癫痫价值。虽然奥卡西平较为安全,但是该药物仍然可能诱发头晕、嗜睡等不良反应, 尤其是在10-羟基卡马西平浓度超过35 mg/L 的情况[19]。左乙拉西坦属于新型抗癫痫药物, 是乙酰吡咯烷化合物, 既具备提升γ-氨基丁酸(GABA)活性的作用, 而且对低激活钙电流具有抑制作用, 具体作用机制主要是对脑内神经递质释放具有调节作用, 抑制了神经元的异常放电, 最终起到了抗癫痫的作用[20]。奥卡西平联合左乙拉西坦治疗可发挥协同作用, 提升患儿的治疗效果。
综上所述, 癫痫患儿联合应用奥卡西平与左乙拉西坦治疗能够发挥突出效果, 不仅能够改善患儿的免疫功能, 而且可改善患儿的认知功能, 利于患儿病情康复, 值得推广应用。

