胰高血糖素样肽-1受体激动剂在儿童患者中的临床应用进展Δ
王月玥,卢金淼,朱 琳,王 艺3#,李智平#
(1.国家儿童医学中心/复旦大学附属儿科医院临床药学部,上海 201102; 2.复旦大学附属儿科医院启东分院/启东市妇幼保健院药学部,江苏 启东 226200; 3.国家儿童医学中心/复旦大学附属儿科医院神经内科,上海 201102)
胰高血糖素样肽-1受体激动剂(glucagon-like peptide-1 receptor agonist,GLP-1RA)是一类新型药物,其能模拟人体内自然产生的胰高血糖素样肽-1(GLP-1)激素,刺激胰岛素分泌和减缓胃肠道排空速度。该类药物已被广泛用于成人2型糖尿病的治疗,并取得了良好的临床效果。自从GLP-1被发现有降糖效果之后,GLP-1RA的开发便受到广泛关注。迄今为止,包括已经停用的阿必鲁肽在内,全球已有9款GLP-1RA类药物获批上市。此外,还有Tirzepatide,其是全球首个GLP-1受体和葡萄糖依赖性促胰岛素多肽(GIP)受体双重激动剂,在临床试验中展现了优异的降低血糖和糖化血红蛋白、减轻体重、改善血脂等作用[1]。同时,国内外多款GLP-1创新药也在研发过程中。随着儿童和青少年肥胖率、2型糖尿病发病率不断升高,越来越多的研究开始探讨GLP-1RA在儿童中的应用。研究发现,GLP-1RA在2型糖尿病患儿中耐受性良好,且被认为可能是治疗儿童和青少年2型糖尿病的有效替代药物[2-3]。本文将介绍GLP-1RA在儿童中除2型糖尿病外的其他应用研究进展,并探讨该类药物在儿童中的潜在治疗作用,同时讨论目前在该领域面临的挑战和未来的发展方向,以期为该领域的研究提供参考和借鉴。
1 部分GLP-1RA在儿童中的使用和研发进程
目前,国内外部分GLP-1RA在儿童中的使用和研发进程情况见图1。
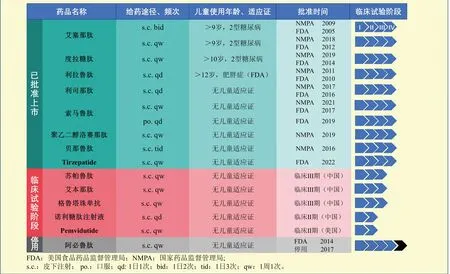
图1 国内外部分GLP-1RA在儿童中的使用和研发情况
2 用于青少年肥胖的治疗
目前,青少年肥胖问题是一个全球性的健康挑战,涉及许多心血管代谢合并症和生化改变。解决该问题需要从多个层面采取干预措施,包括政府、教育、医疗保健、食品行业等各领域共同努力。新兴的青少年减肥疗法包括数字技术、新型 GLP-1RA和内窥镜手术等[4]。生活方式干预是推荐的治疗方法,但现实世界数据显示,大多数青少年不能坚持生活方式干预实现长期减肥。减肥手术是另一种有效方法,但风险包括需要额外的腹部手术和特定的微量营养素缺乏症。故除生活方式干预和减肥手术之外,新的药物治疗可为肥胖儿童和青少年提供更多的机会[5-6]。
研究发现,GLP-1RA治疗青少年肥胖可帮助减少临床、社会和经济负担,这是一个非常令人鼓舞的发现。尽管该类药物已在成人中得到广泛应用,但儿童和青少年的生理特点、药物代谢过程与成人不同,需要进一步的研究来确定GLP-1RA在儿童中的安全性和有效性。
目前用于青少年肥胖治疗的GLP-1RA主要涉及利拉鲁肽和艾塞那肽[7-8]。2021年,欧洲药品管理局批准了利拉鲁肽用于治疗12~17岁的青少年肥胖。该药在临床研究中表现出良好的有效性和安全性,可在一定程度上帮助青少年减轻体重。缓释艾塞那肽治疗青少年重度肥胖一般耐受性良好,可使体重指数(BMI)适度降低,葡萄糖耐量和胆固醇改善[9]。由于经验有限,一般建议优先考虑长效而不是短效GLP-1RA。在未来的研究中,需要更多的高等级证据,包括新的GLP-1RA迭代和长期随访的儿科人群[10]。
GLP-1RA用于青少年肥胖具有以下优势:(1)改善胰岛素敏感性。青少年肥胖患者往往伴随着胰岛素抵抗的发生,而GLP-1RA可增加胰岛素敏感性,改善胰岛素抵抗。(2)减轻体重。GLP-1RA可抑制胃肠道运动,减少进食,从而减轻体重。(3)降低血压。青少年肥胖患者常伴随着高血压的发生,而GLP-1RA可通过减轻体重、改善胰岛素敏感性等多种方式降低血压。(4)减少代谢综合征发生风险。青少年肥胖患者往往伴随着代谢综合征的发生,而GLP-1RA可通过改善胰岛素敏感性、减轻体重等多种方式降低代谢综合征的发生风险。总之,GLP-1RA能通过多种方式改善青少年肥胖患者的代谢异常和心血管疾病风险,在青少年肥胖的治疗中具有广泛的应用前景。
就相关临床研究进展而言,1项在10~26岁(中位数为16岁)的青年人群中的研究结果显示,艾塞那肽可减少青少年食物摄入总量和增加能量消耗,进而减轻体重[11]。GLP-1RA是改善或稳定儿童和青少年下丘脑肥胖症的一种有前途且安全的治疗方法,对临床肥胖儿童和青少年适度减轻体重、BMI、糖化血红蛋白 和心脏收缩压方面是安全、有效的[12-13]。GLP-1RA在治疗儿童肥胖方面的效应大小与成年人相当[14-15]。1项针对利拉鲁肽短期治疗肥胖儿童(7~11岁)的临床研究发现,利拉鲁肽短期治疗儿童肥胖的安全性和耐受性与成人和青少年肥胖的研究相似,且未发现新的安全问题[16]。GLP-1RA作为一种治疗小儿肥胖的新疗法,对心血管和代谢参数产生积极影响的潜力令人兴奋,未来对儿科GLP-1RA使用的研究将继续推进儿科肥胖领域,并为一些受影响的儿童提供有希望的选择[17]。
3 用于儿童短肠综合征(short bowel syndrome,SBS)的治疗
SBS是由于疾病或胃肠道手术导致肠道长度缩短而引起的营养吸收障碍。儿童SBS的最常见病因包括坏死性小肠结肠炎、腹裂、肠闭锁、肠扭转等。约80%的儿童SBS发生在新生儿期。坏死性小肠结肠炎是新生儿SBS的最常见病因。由于肠道长度缩短,吸收黏膜表面积减少,患儿通常需要靠静脉营养支持来维持生命。但静脉营养支持可能会引发许多并发症,如感染、肝功能异常和骨质疏松等。患儿小肠的消化吸收功能除维持生存所需营养外,还要满足生长发育的需要,长期依赖肠外营养支持可严重降低患儿的生活质量,且患儿可能死于肠外营养相关并发症。
由肠道L细胞分泌的GLP-1和胰高血糖素样肽-2(GLP-2)是调节肠道运输、分泌、吸收和黏膜生长的关键激素,对肠功能衰竭患儿的肠道适应性具有调节作用[18]。目前,注射用替度鲁肽是全球首款也是唯一获批应用于SBS的GLP-2类似物[19]。2019年,美国批准该药用于1岁以上儿童SBS患者。GLP-2已明确能刺激肠黏膜隐窝细胞增殖,从而增加绒毛高度、肠道长度和表面积,促进肠黏膜的修复和适应性生长,有益于SBS患者[20-22]。但GLP-2不是唯一在SBS患者预后中起作用的肠道激素。GLP-1也是一种关键激素,可调节近端肠道运输[23]。目前已有证据证明,GLP-1RA在成人SBS的治疗中具有良好的疗效和安全性。1项GLP-1RA艾塞那肽治疗SBS的回顾性研究共纳入5例SBS患者,使用艾塞那肽治疗后所有患者的排便频率和排便形式立即改善,且全部成功停止了全肠外营养支持,疗效显著[24]。艾塞那肽可以作为SBS的一种新型且安全的治疗选择。另外,Hvistendahl 等[25]利用代谢平衡研究了利拉鲁肽对SBS患者空肠造口输出量的影响,发现利拉鲁肽治疗使造口湿重输出量减少,肠湿重和能量吸收增加。
对回肠切除患者而言,GLP-1和 GLP-2浓度升高可能有助于保留结肠对肠运动和功能的适应作用[26]。正常情况下,GLP-1和 GLP-2同时等比例分泌。生理 GLP-1的半衰期很短(≤2 min),而GLP-1RA具有极长的半衰期(6~24 h),剂量也远超GLP-1生理剂量。GLP-1RA通过增加肠道收缩和减少胃肠道运动,减缓食物在肠道中的通过速度,增加肠道对养分的吸收。艾塞那肽在SBS患者中的成功治疗证明其可以改善SBS患者的预后,可能是由于其对胃肠道转运的影响以及其鲜为人知的促进肠道生长的作用,可改善SBS患者的排便习惯,减少肠外营养和小肠移植的需要,显著改善患者的生活质量[24,27-29]。
1项比较连续输注GLP-1、GLP-2以及GLP-1+GLP-2组合治疗SBS的随机对照研究结果提示,GLP-1和GLP-2均可减少腹泻和粪便排泄,GLP-1+GLP-2的组合显示出加和效应,并倾向于改善单独输注GLP-1时的恶心和食欲减退等不利影响[30]。故GLP-1与GLP-2共同治疗可能存在协同效应。由于GLP-1RA的半衰期较长,长期存在的 GLP-1RA 可能会促进内源性GLP-2分泌增加,可进一步促进小肠、结肠绒毛和隐窝的生长,增加小肠的长度,促进肠道适应和吸收,减少粪便流失,减少甚至消除肠外支持的需要,将有助于SBS患者的肠道康复[31]。GLP-1和GLP-2的组合突出了双重激动剂的潜力,不仅比单一疗法更有效地改善吸收,减少初始所需剂量,还可减轻 GLP-1的剂量依赖性不良反应[27,30]。此外,SBS患儿易出现小肠细菌过度生长的情况,GLP-1和GLP-2作为代谢和炎症信号的传感器,通过与微生物群和免疫系统相互通信的复杂网络,在维持肠道健康和代谢方面也发挥着协调作用[32]。故GLP-1和GLP-2可能通过恢复和利用正常的反馈机制和潜在的协同效应,进一步促进肠道适应,为SBS患儿带来更有效的治疗[27,33]。
总之,由于SBS病因和病情的复杂性,GLP-1RA的应用仍需进一步的临床研究和验证。
4 可能存在的安全性风险
目前,GLP-1RA被广泛用于成人2型糖尿病的治疗,且在青少年肥胖和SBS的治疗中也逐步开始使用。该类药物虽在临床应用中具有显著的疗效,但也存在一些潜在的安全性风险,目前已知的风险因素包括低血糖(特别是与胰岛素或磺酰脲类药物合用时)、恶心和呕吐等胃肠道反应、胰腺炎(尤其是有胰腺炎既往史或存在其他胰腺炎的危险因素的患者)、甲状腺癌(长期使用GLP-1RA可能会增加甲状腺癌的风险)[34]。1项在10~18岁患有2型糖尿病的青少年中进行的随机对照试验结果显示,利拉鲁肽组胃肠道不良事件发生率高于安慰剂组,安全性与成人报告一致[35]。相关Meta分析也提出,GLP-1RA治疗儿童及青少年肥胖会导致低血糖发生率升高,结果也与成人报告相似[36]。
GLP-1RA改善人类肠道适应性的效果已经显现,但长期使用也会带来相应的不良反应,GLP-1RA对胃肠道蠕动的长期抑制可能会使肠梗阻风险增加[37]。鉴于肥胖的慢性和复发性,必然需要长期治疗,青少年和成人患者停药后体重反弹已在临床研究中得到证实[38-39]。1项GLP-1RA索马鲁肽用于成人肥胖患者的Ⅲ期临床研究中,停药后患者出现体重反弹[38]。目前对GLP-1RA在青少年或成人中长期应用的安全性知之甚少,而这对处于大脑发育重要时期的儿童患者尤为重要[40]。故除上述已知的不良反应外,对于儿童和青少年患者,还需考虑GLP-1RA对生长发育可能产生的影响。不能仅重视GLP-1RA的多重短期益处,而忽略其可能存在的长期安全性问题。
5 小结
综上,GLP-1RA在儿童肥胖和SBS的治疗中具有良好的应用前景。但肠道疾病患者更关注胃肠道相关不良反应,且处于生长发育期的儿童和青少年对GLP-1RA的反应和耐受程度不同于成人。在尝试采用GLP-1RA治疗时,应缓慢调整剂量,合理选择短效与长效制剂,以满足患儿的个体需求。这将在平衡不良反应与疗效方面带来挑战,故需要开展更加系统和深入的研究。目前,GLP-1RA在儿童和青少年人群中尚未广泛应用,在使用的同时需要重视其长期安全性问题。

