功能性二尖瓣反流在二叶式主动脉瓣重度狭窄患者经导管主动脉瓣置换术后的转归分析
林大卫 翁梓珑 张 峰 潘文志 周达新△
(1复旦大学附属中山医院心内科 上海 200032; 2上海市心血管病研究所 上海 200032)
先天性二叶式主动脉瓣(bicuspid aortic valves,BAV)是导致主动脉功能异常的主要原因之一[1-2]。由于BAV 狭窄具有瓣膜不规则增厚、瓣叶对称性差、主动脉根部增宽等解剖结构与病理表现上的特殊性,经导管主动脉瓣置换(transcatheter aortic valve replacement,TAVR)术后更易引起瓣周漏等并发症,因此BAV 狭窄在国外临床试验中被列为排除标准[3-4]。不同于其他国家1%~2%的BAV 患病率,在我国接受TAVR 的患者中BAV 占比高达40%~50%[5]。因此深入研究TAVR 治疗BAV 瓣狭窄的预后十分必要。
因主动脉瓣重度狭窄接受TAVR 手术的患者常伴有二尖瓣反流(mitral regurgitation,MR)[6]。MR分为原发性MR 与继发性MR,继发性MR 又称功能性MR(functional mitral regurgitation,FMR),相比于TAV 患者,BAV 患者中FMR 占比更高,而主动脉瓣狭窄患者伴有FMR 可显著增加左心系统的负荷,对患者预后造成严重影响。临床已证实部分FMR 在TAVR 术后会有所改善,但是否同期治疗FMR 存在争议,且目前尚无针对BAV 狭窄合并FMR 患者接受TAVR 的研究[7-9]。本研究通过回顾复旦大学附属中山医院的病例资料,探讨FMR 在BAV 重度狭窄患者TAVR 术后的转归,并分析其预测因素。
资 料 和 方 法
研究对象回顾性分析2018 年6 月至2022 年9月在复旦大学附属中山医院接受TAVR(Venus-A瓣膜,杭州启明医疗器械有限公司)的患者。纳入标准:(1)确诊主动脉瓣重度狭窄合并功能性MR,经综合评估后,不适合外科瓣膜置换术,且经过主动脉根部CT 评估确诊为BAV 畸形;(2)随访时间≥1月,并且接受心超检查。排除标准:(1)术前多排螺旋CT(multi-detector spiral computer tomography,MDCT)显示主动脉瓣狭窄患者为三叶瓣;(2)器质性二尖瓣病变;(3)合并肥厚型梗阻性心肌病;(4)合并左心室内血栓或感染性心内膜炎。
分组及数据收集生理条件下3 个半月形且大小一致的瓣叶(左、右和无冠瓣)组成主动脉瓣,称三叶瓣。与之不同,BAV 通常由大小不同的两个瓣叶组成。Sievers-Schmidtke[10]分型法依据嵴的数量将BAV 分为:0 型(无嵴)、1 型(有1 条嵴)、2 型(有2 条嵴)。我们对患者进行术前MDCT 检查,通过Fluro-CT 软件对收缩期影像进行三维重建,根据CT 结果将研究对象分为0 型二叶瓣组(n=49)及1 型二叶瓣组(n=51)(图1)。本研究无2 型二叶瓣狭窄病例。

图1 不同二叶主动脉瓣类型患者接受TAVR 术后二尖瓣反流的改善程度Fig 1 The improvement of mitral regurgitation in patients with different types of aortic valve post-TAVR
根据患者病历资料及导管室信息系统采集患者临床信息,并进行回顾性分析。从病历资料中记录患者的基线信息,包括术前是否合并高血压、糖尿病、肺动脉高压、心房颤动、心力衰竭、肾功能不全等疾病。患者术前均经过MDCT 及超声心动图检查,术后复查超声心动图。记录升主动脉宽度、钙化体积、左室射血分数、左心房及左心室内径、主动脉瓣反流程度、主动脉瓣平均跨瓣压等关键参数。根据超声心动图获得的二尖瓣反流束面积(mitral regurgitation area,MRA)结果对FMR 程度进行评估分级:0 级,无反流;1 级,轻微反流,反流量1+;2 级,轻度反流,MRA<4 cm2,反流量2+;3 级,中度反流,MRA 为4~8 cm2,反流量3+;4 级:重度反流,MRA>8 cm2,反流量4+。
治疗及随访所有患者均在静脉麻醉下由中山医院心内科结构性心脏病手术团队行TAVR 手术。经MDCT 评估后选择股动脉或颈静脉途径,根据术前MDCT 检查、术中主动脉根部造影结果,酌情确定是否行球囊预扩张。根据检查结果选择人工瓣膜型并置换Venus-A 瓣膜。嘱患者术后30 天门诊随访,并行超声检查。记录超声检查结果及根据瓣膜学术研究联盟-3 (VARC-3)标准的临床结局发生情况[11]。
统计学分析采用STATA 15.1 软件进行数据的统计学分析。正态分布的计量资料以表示,计数资料以n(%)表示,分别采用独立样本t检验和χ2检验进行组间比较。若频数<5,则采用Fisher 精确概率法进行组间比较。采用双侧检验,P<0.05为差异有统计学意义。为进一步分析影响FMR 改善的因素,依据术后1 个月FMR 与术前相比是否改善为标准,将纳入的患者病例分为FMR 改善组与FMR 非改善组。采用多元Logistic 回归分析影响BAV 患者接受TAVR 术后FMR 的因素。
结 果
患者总体特征共纳入100 例行TAVR 的患者,其中二叶瓣0 型49 例,二叶瓣1 型51 例,平均年龄为(74.9±7.60)岁,男性60 例,女性40 例。纳入患者均随访至术后30 天,未发现患者死亡、再入院及心衰、致残性卒中等严重不良事件发生。
BAV 分组患者的基线资料与影像学资料比较在临床信息方面,相比二叶瓣1 型患者,二叶瓣0 型患者年龄较小[(72.78±6.09)岁vs.(77.00±8.35)岁,P=0.050],男性比例偏低(47%vs. 73%,P=0.009),BMI 偏高[(23.19±2.62)kg/m2vs.(21.99±3.13)kg/m2,P=0.041],两组的高血脂、高血压病、心功能Ⅲ~Ⅳ级、糖尿病、肺动脉高压、房室传导阻滞相比较,差异均无统计学意义。
影像学方面,二叶瓣0 型组主动脉瓣关闭不全反流发生率较低(69%vs. 92%,P=0.040)。其他CTA 与超声方面的比较,包括瓣环面积、有效瓣口面积、钙化体积、升主动脉直径、左室舒张期末内径、平均跨瓣压差、瓣口最大流速、左室EF、左室后壁厚度等,差异无统计学意义(表1)。
表1 BAV 分型的临床与影像学特征比较Tab 1 Comparison of clinical and imaging features in different BAV classifications [ or n(%)]
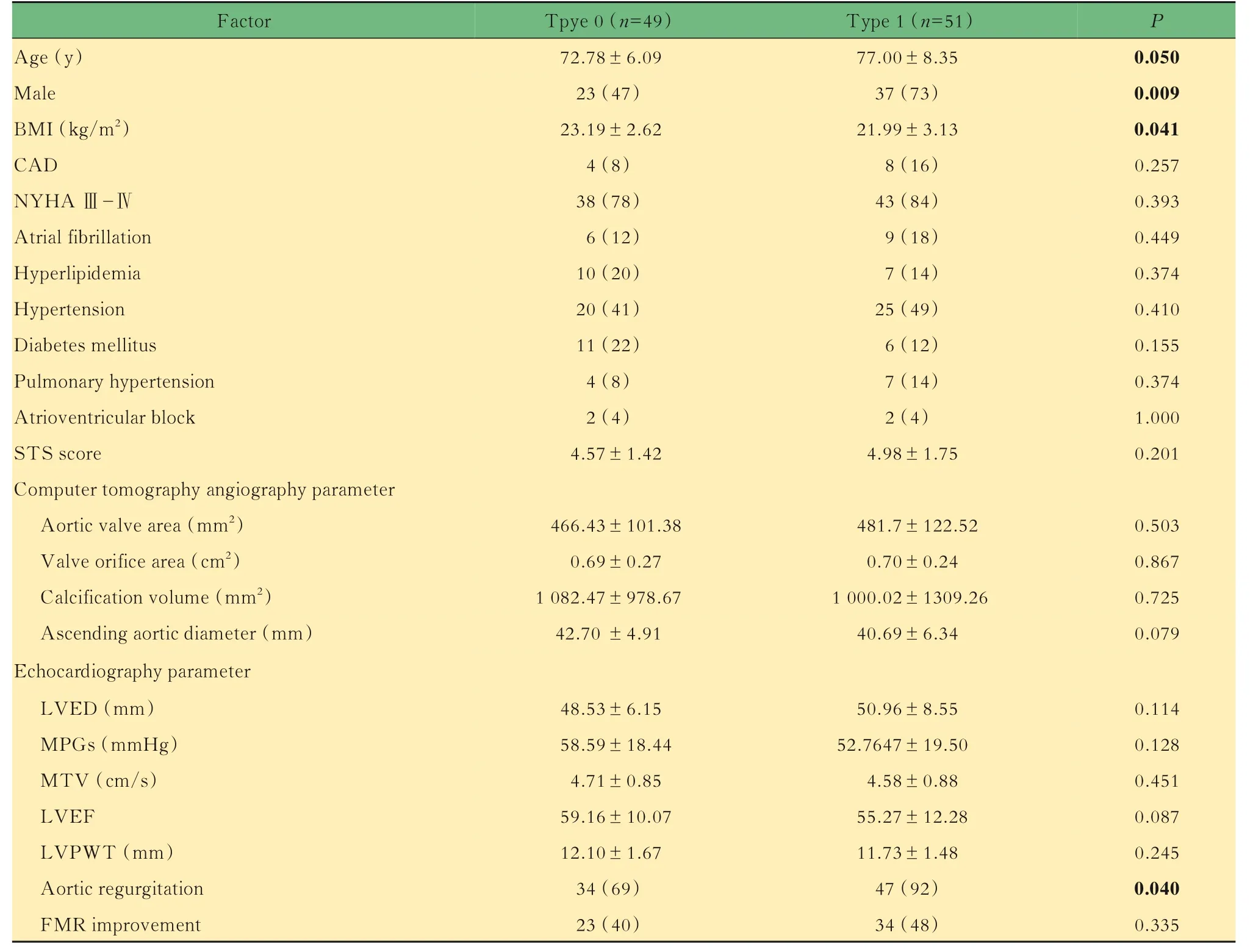
表1 BAV 分型的临床与影像学特征比较Tab 1 Comparison of clinical and imaging features in different BAV classifications [ or n(%)]
BMI:Body mass index;CAD:Coronary artery disease;STS scores:Society of thoracic surgeons;LVED:Left ventricular end-diastolic diameter;MPGs:Transvalvular mean pressure gradients;MTV:Maximum transvalvular velocity;LVEF:Left ventricular ejection fraction; LVPWT:Left ventricular posterior wall thickness. 1 mmHg=0.133 kPa.
?
BAV 分组患者术前与术后MR 情况比较术后1 个月随访超声结果显示,二叶瓣0 型组和1 型组患者的FMR 分级与术前相比显著改善,两组术前与术后FMR 改善率差异无统计学意义(40%vs.48%,P=0.335),详见图1。
FMR 改善组与非改善组临床资料与影像学资料比较临床方面,相比非改善组,改善组有更低的冠心病发病率(5%vs.18%,P=0.042),以及更高的肺动脉高压发病率(20%vs. 2%,P=0.007)。比较两组的高血脂、高血压病、心功能3~4 级、糖尿病、房室传导阻滞相,差异均无统计学意义。影像学方面,改善组左室舒张末期内径较大[(51.98±6.74) mmvs. (48.04±7.72) mm,P=0.009],主动脉瓣口最大流速更高[(4.86±0.95)cm/svs. (4.47±0.75)cm/s,P=0.023]。其他CTA与超声方面的比较,包括瓣环面积、有效瓣口面积、钙化体积、升主动脉直径、左室舒张期末内径、平均跨瓣压差、瓣口最大流速、左室射血分数、左室后壁厚度等,差异均无统计学意义。将上述的差异因素作为因变量纳入Logistic 回归分析,得出结果:术前肺动脉高压、左室舒张期末内径和瓣口最大流速是BAV 患者接受TAVR 术后FMR 改善的相关因素(表2)。
表2 转归组与非转归组的临床与影像学特征比较Tab 2 Comparison of clinical and imaging features between FMR improvement group and non-improvement group[ or n(%)]
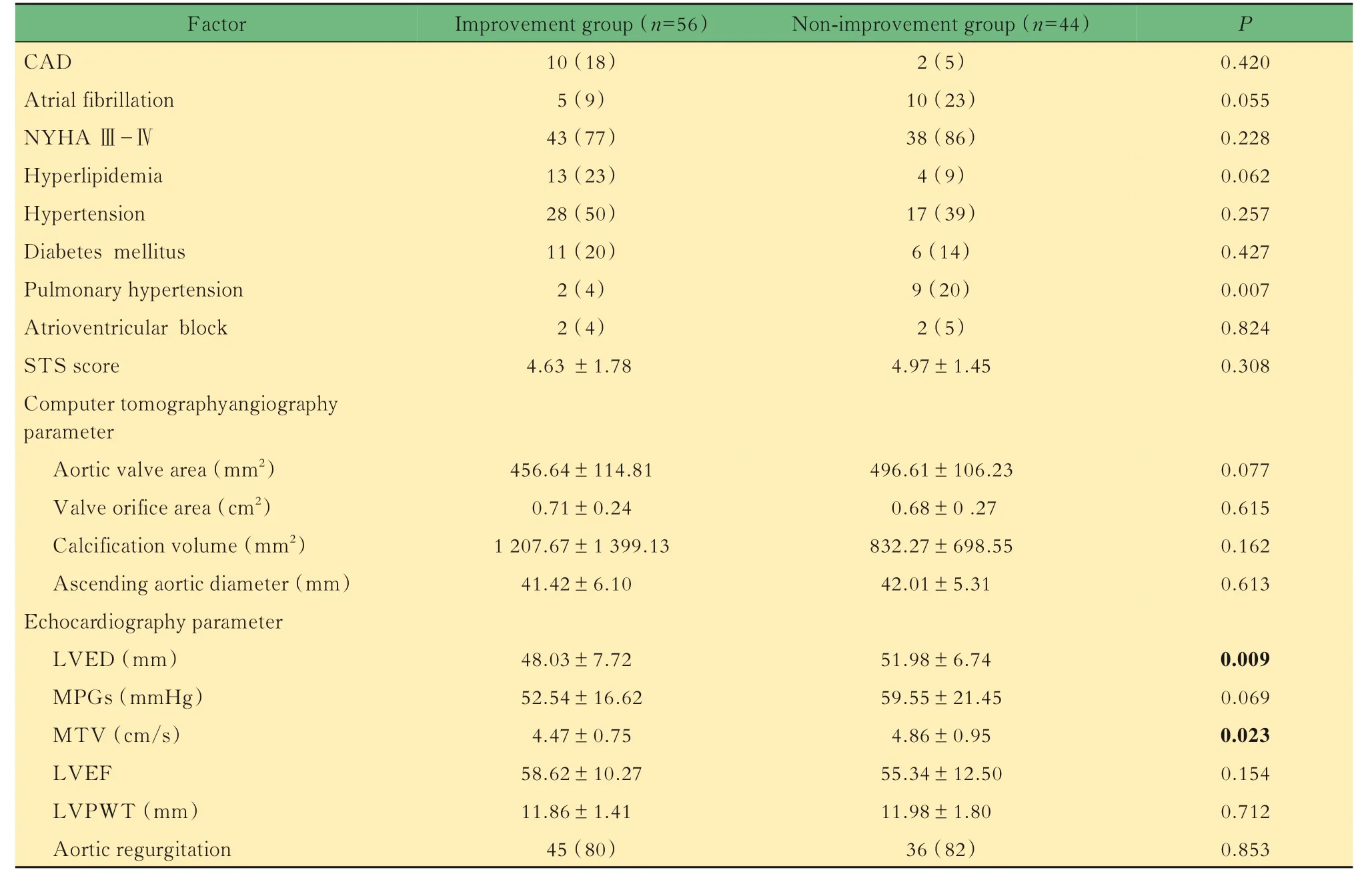
表2 转归组与非转归组的临床与影像学特征比较Tab 2 Comparison of clinical and imaging features between FMR improvement group and non-improvement group[ or n(%)]
CAD: Coronary artery disease; STS scores: Society of Thoracic Surgeons scores; LVED: Left ventricular end-diastolic diameter; MPGs:Transvalvular mean pressure gradients; MTV: Maximum transvalvular velocity; LVEF: Left ventricular ejection fraction; LVPWT: Left ventricular posterior wall thickness.
?

表3 多元Logistic 分析TAVR 术后FMR 改善影响因素Tab 3 Multivariate Logistic analysis was used to analyze the factors influencing the improvement of FMR after TAVR
讨 论
BAV 狭窄患者常伴有FMR。研究发现,60%主动脉瓣狭窄伴有FMR[12],尤其是重度主动脉瓣狭窄,FMR 常作为其病理特征之一。其原因为主动脉瓣狭窄时左心室射血阻力增加,射血分数下降,左心室压力负荷增大。在长期的负荷下,左心室肌细胞并联增生、肥大,导致左心室壁增厚,射血做功增加。重度主动脉瓣狭窄将导致向心性肥厚,产生较高的左心室舒张末压力,在该情况下,左心房需要增加收缩力才能维持足够的心室充盈血量。在长期的左心房高负荷下,左心房代偿性增大,牵拉二尖瓣后瓣,导致二尖瓣环扩张,且腱索及乳头肌支撑力不够,随之二尖瓣关闭不全,FMR 发生。进一步由于高心室舒张末期压力,即使轻微的二尖瓣反流也可以显著减少向前搏出量,从而导致MR 进行性加重[13]。BAV 独特的解剖学特征使其具有更高的FMR 发生率[14]。BAV 瓣膜不规则增厚,瓣叶不对称性钙化,易导致主动脉瓣狭窄,且常伴有主动脉根部的疾病,促进左心功能障碍的发生,从而引起FMR。本研究中重度FMR 患者接受TAVR 术后改善率较高(均超过80%),推测其与较低的房颤率(分别为12%与18%)合并率相关,因房性FMR率少,而室性FMR 多由AS 所致,当AS 改善时,中重度FMR 可得到缓解。然而本研究中重度FMR病例数少,该结论需长期大规模临床研究进一步证实。
FMR 在BAV 狭窄患者经TAVR 术后明显改善。原因为TAVR 术后主动脉狭窄得到纠正,左心室腔的压力迅速下降,二尖瓣后负荷下降,二尖瓣压力梯度明显下降,从而使FMR 明显改善。在本研究中,二叶瓣0 型组FMR 术后改善率为40%,二叶瓣1 型改善率为48%,两组间差异无统计学意义。与本研究结果相似,经典的TAVR 研究Edwards SAPIEN、CoreValve 注册中心研究及PARTNER队列研究发现,分别有55%、58%和38%的患者在TAVR 术后MR 得到改善[15-17]。本研究中有4 位患者在术后1 个月随访时FMR 加重,均有冠心病病史,因此FMR 加重的可能原因为动脉疾病或术中缺血。对于合并有冠心病的重度二尖瓣狭窄患者,可同期行PCI 手术,改善冠脉血流、乳头肌及室壁的供血恢复有利于心脏收缩协调,有利于FMR 改善。此外,有研究发现,术后FMR 显著升高与患者的短期和长期死亡率相关,并建议同期纠正FMR[18]。
本研究通过Logistic 回归进一步对影响FMR在BAV 狭窄患者术后改善的因素进行分析,结果发现瓣口最大流速、肺高压及左心舒张末期内径可作为术后FMR 改善的预测因素。这些因素影响术后FMR 改善程度的原因可能为主动脉瓣狭窄引起的瓣口面积减小,瓣口最大流速更高,会导致左室的重构,心室负荷增大,从而导致心室内径增大。长期的高负荷使得左心房充盈压升高,左房容积增大,从而导致二尖瓣关闭不全。肺动脉高压及左心室舒张末期内径的增大也标志着心房的高负荷,也与更高程度的FMR 分级相关。根据研究[19]报道,FMR 分级越高,TAVR 术后改善的占比越大,而轻微及轻度FMR 术后改善效果不明显,因此主动脉瓣有效瓣口面积越小、肺高压发生率越高及左心舒张末期内径越大,则TAVR 术后FMR 改善的可能性越大。目前国内外暂无针对BAV 狭窄TAVR 术后FMR 转归的研究。国外对包含二叶瓣、三叶瓣TAVR 术后FMR 转归的研究分析发现,平均主动脉跨瓣压≥40 mmHg、无房颤和肺动脉压小于60 mmHg 是术后FMR 改善的预测因素[19]。
对于是否应该同期行TAVR 和经导管缘对缘修复(transcatheter edge to edge repair,TEER)两项手术尚未有明确证据。我们研究表明,对于因BAV狭窄接受TAVR 手术的FMR 患者,术后有40%以上的MR 可以得到改善,对于有肺高压、左室舒张末期内径较大、瓣口最大流速更高的患者,FMR 改善率更高。而与之相比,大部分轻度反流患者术后二尖瓣反流维持现状。且有研究发现,同期行TAVR及TEER 术围手术期死亡率比单纯的TAVR 高。因此,对于合并有FMR 的BAV 患者同期行双瓣手术缺乏证据支持。对于合并有冠心病的患者,术后二尖瓣反流程度加重,建议行经皮冠状动脉介入治疗手术。本研究主要局限为回顾性、单中心、小样本、因检查时间不一所致的超声医师及机器差异,可能使数据有潜在的偏差。本研究对于FMR 严重程度的评估为半定量评估,缺乏长期随访数据等。
综上,重度BAV 狭窄患者常合并FMR,二叶瓣0 型与二叶瓣1 型患者TAVR 术后FMR 改善率无显著差异。肺高压、左室舒张末期内径较大、以及瓣口最大流速更快与更高的FMR 改善率相关。
作者贡献声明林大卫,翁梓珑 论文构思和撰写。张峰 数据收集。潘文志 论文修订。周达新 研究指导,论文修订。
利益冲突声明所有作者均声明不存在利益冲突。

