两种尿蝶呤谱检测方法的比较及在高苯丙氨酸血症中的应用*
谢汛杰,江剑辉,曾伟宏△
1南方医科大学珠江医院检验医学部(广东广州 510220); 2广东省妇幼保健院(广东广州 511400)
高苯丙氨酸血症(HPA)常见于苯丙氨酸羟化酶(PAH)缺乏症导致的苯丙酮尿症(PKU)或四氢生物蝶呤(BH4)辅酶缺乏导致的四氢生物蝶呤缺乏症(BH4D);两者血中苯丙氨酸(Phe)或Phe/Tyr均明显升高,除了BH4D会出现肌张力异常外,两者其余表现相似,临床上容易误诊,检测尿液中的新蝶呤和生物蝶呤有助于PKU和BH4D的鉴别诊断[1-4]。高效液相色谱-荧光检测法(HPLC-RF)是检测尿液中的新蝶呤(N)和生物蝶常(B)用方法。国内现用于HPLC检测尿蝶呤谱的前处理方法主要有碘(I2)氧化法[5]和二氧化锰(MnO2)氧化法[1]。本文通过比较I2氧化法及与MnO2氧化法的两种前处理方法对尿液中的新蝶呤和生物蝶呤定量检测,寻找一种合适的尿蝶呤谱前处理方法。
1 资料与方法
1.1 一般资料 抽取55例健康人群和10例确诊PKU或BH4D患者新鲜尿液标本,年龄在1月到1岁区间(中位数为4个月),其中男39例,女26例。研究经过广东省妇幼保健院医学伦理委员会审查通过(广东省妇幼保健院医伦第[202301311]号)。
1.2 试剂 新蝶呤标准品(M.W.253.2阿拉丁公司),生物蝶呤标准品(M.W.237.2西格玛公司),HPLC级甲醇(默克公司),37%浓盐酸(广州化学试剂厂),500 g碘化钾(CNW公司),500 g抗坏血酸(CNW公司),100 g碘片(阿拉丁公司),二氧化锰(广州化学试剂厂)。
1.3 仪器设备 sartorius公司BSA124S-CW高精度分析天平,日本岛津公司高效液相色谱层析系统(包括LC-20AT高压双泵,SIL-20A自动进样器,色谱柱Diamonsil C18(4.6 mm I.D×250 mL,5 μm),RF-20A荧光检测器)。
1.4 试剂配制
1.4.1 标准品储备液配制 称量10 mg新蝶呤(N)和10 mg生物蝶呤(B),分别加入0.1 mol/L NaOH充分溶解并定容到25 mL,分别用EP管每管分装1 mL,置于-20℃冷冻保存。
1.4.2 标准品工作液配制 取标新蝶呤和生物蝶呤准品储备液,加入0.1 mol/L 盐酸分别稀释到80 μg/L并混匀,再加入0.1 mol/L HCL稀释成7个浓度(20.0、10.0、5.0、2.0、1.0、0.1、0.01 μg/L)并上机,每个浓度测定2次,取均值绘制标准曲线。
1.4.3 质控品配制 取标新蝶呤和生物蝶呤准品储备液,加入0.1 mol/L 盐酸分别稀释到80 μg/L并混匀,再加入0.1 mol/L HCL稀释成2.0 μg/L和0.5 μg/L两个水平。
1.4.4 盐酸配制 移液管吸取37%浓盐酸(12 mol/L)并用超纯水分别稀释成9、6、3、1、0.1 mol/L溶液。
1.4.5 碘液(I2-KI)配制 称量15.6 g碘化钾(KI)溶于30 mL超纯水并加入1.95 g碘片(I2)配制成0.5 mol/L I2-KI溶液,再用超纯水分别稀释成0.1、0.05、0.01 mol/L溶液。
1.4.6 抗坏血酸配制 称量2.64 g 抗坏血酸溶于30 mL超纯水配制成0.5 mol/L VitC溶液再用超纯水分别稀释成0.1 mol/L、0.05 mol/L、0.01 mol/L溶液。
1.5 方法
1.5.1 I2氧化法方法 取样本(标准品、质控品及新鲜尿液)0.5 mL,加入6 mol/L盐酸25 μL,0.05 mol/L I2-KI溶液0.5 mL,充分混匀,放置暗处30 min,然后加入0.05 mol/L 抗坏血酸溶液0.5 mL,再加入超纯水定容到2.5 mL,摇匀,用0.45 μm微孔滤器过滤并上机分析。
1.5.2 MnO2氧化法方法 取样本(标准品、质控品及新鲜尿液)并立刻加入抗坏血酸(每mL尿液加入10 mg)混匀,处理前3 000 r/min离心10 min后取上清0.5 mL,依次加入1 mol/L盐酸50 μL、10 mg MnO2,离心过滤,并以0.1 mol/L 盐酸定容到2.5 mL,用0.45 μm微孔滤器过滤并上机分析。
1.5.3 色谱条件参数 流动相92%超纯水和8%HPLC级甲醇,恒定流速0.9 mL/min,色谱柱Diamonsil C18(4.6 mm I.D×250 mmL,5 μm),柱温30℃,激发波长360 nm,检测波长445 nm。
1.6 统计学方法 使用SPSS 17.0软件分析数据。数据通过K-S检验是否符合正态分布,符合正态分布的数据使用配对样本t检验分析,以均值±标准差表示,非正态分布的数据使用2个相关样本Wilcixon秩和检验分析,以中位数(四分位数)表示。
2 结果
2.1 尿蝶呤谱分析在鉴别高苯丙氨酸血症中的应用 选取门诊就诊患儿14份新鲜样本,分别用I2氧化法和MnO2氧化法处理后上机分析新蝶呤(N)、生物蝶呤(B)和生物蝶呤比例(B/(N+B))。可见两种方法辅助诊断PKU和BH4D(PTPS)的符合率均达100%,两种方法均可用于尿蝶呤谱检测。见表1、图1(N保留时间5.6 min,B保留时间10.2 min)。

图1 不同前处理方式处理正常样本、PTPS样本及PKU样本的比较

图2 两种尿喋呤谱前处理的日间重复性试验比较
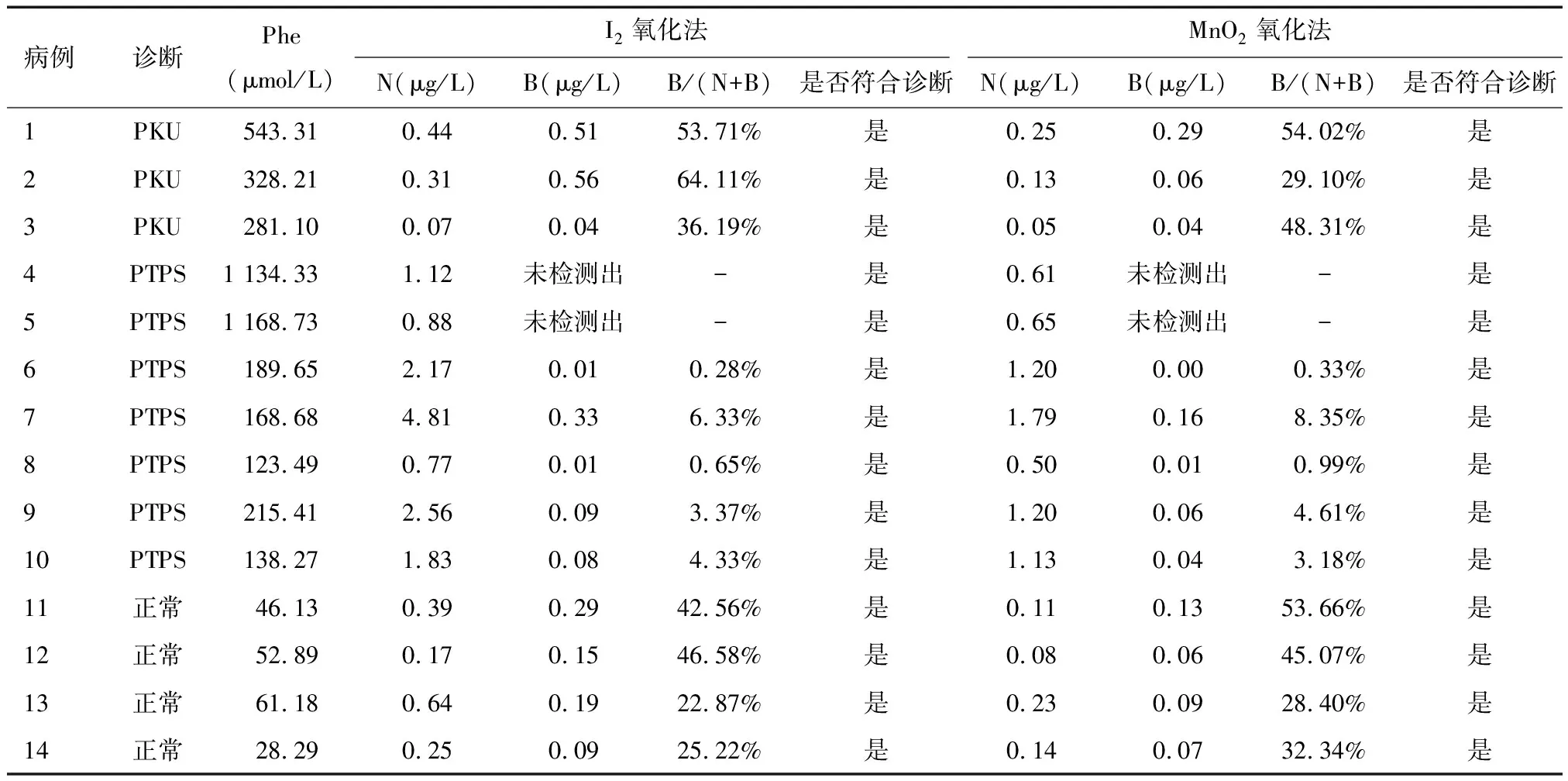
表1 尿蝶呤谱分析在鉴别高苯丙氨酸血症中的应用
2.2 两种方法检测结果及检测限对比 选取新鲜尿液样本,分别用I2氧化法和MnO2氧化法处理后上机分析新蝶呤(N)和生物蝶呤(B),色谱峰面积与浓度成正比,色谱图可见图1~3,每份样本测量两次取均值。I2氧化法处理N和B的检测结果高于MnO2氧化法,差异具有统计学意义(均P<0.05),见表2。I2氧化法和MnO2氧化法处理N的检测限,均取65例中基质空白所产生的仪器信号的3倍值的最低值,见表3。

表2 两种前处理方法结果比较 M(P25,P75)
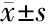
表3 两种前处理方法检测限比较
2.3 两种前处理方法重复性实验对比
2.3.1 批内重复性实验 随机选取3份新鲜样本,分别用I2氧化法和MnO2氧化法处理,每份样本重复测定10次,计算3份样本平均变异系数。两种方法处理新蝶呤(N)和生物蝶呤(B)均有较好的批内精密度(CV<5%),见表4。
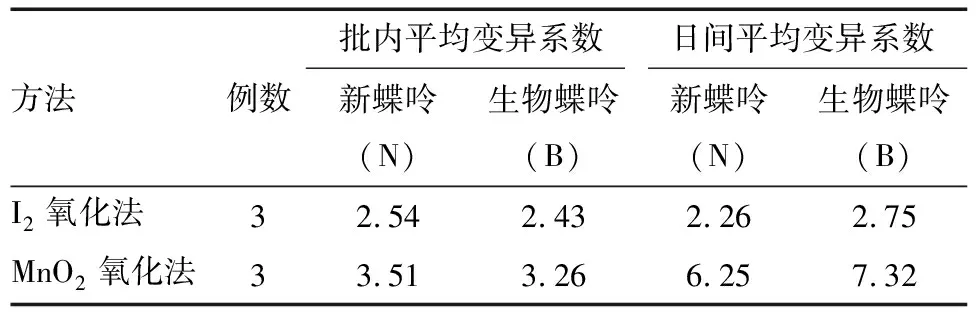
表4 两种方法重复性实验评价 %
2.3.2 日间重复性实验 随机选取3份新鲜尿液样本,I2组样品分装3管,MnO2组样本加入适量抗坏血酸混匀后分装3管,每组各取1份当天处理分析,其余待处理样本置于负20℃冰箱存放,分别在2、3、5、7 d取出后37℃温箱复温30 min后处理分析,每份样品测定2次,计算3份样本平均变异系数。I2氧化法的日间精密度(CV<5%)比MnO2氧化法的日间精密度(5% 2.4 两种前处理方法回收实验对比 随机选取3份新鲜样本各450 μL,分别加50 μL入低、中、高浓度的标准品,混匀后用两种前处理方法分别处理,上机分析,每份重复测量两次取均值,计算平均回收率。可见I2氧化法处低浓度标准品新蝶呤(N)回收率较差(128.19%);MnO2氧化法处理低浓度标准品回较好(N:85.7%,B:87.55%),两种方法中、高浓度回收率均好。见表5。 表5 两种方法回收试验评价 2.5 两种方法线性范围评价对比 选取80 μg/L的新蝶呤、生物蝶呤标准品,两者混匀,加0.1 mol/L 盐酸稀释成20.0、10.0、5.0、2.0、1.0、0.1、0.01 μg/L,然后用I2氧化法和MnO2氧化法分别处理,上机分析,每份重复测量两次取均值,以预测浓度为横坐标,实际浓度为纵坐标,绘制散点图,建立直线回归方程,可见在0.01~20.00 μg/L范围内,两种前处理方法处理的新蝶呤和生物蝶呤均有较好的线性(R2>0.99)。见图3。 图3 不同前处理方法处理新喋呤和生物喋呤线性图 临床上HPA患儿主要苯丙氨酸羟化酶或辅酶四氢生物蝶呤缺乏引起,两者症状相似,但治疗方式不一致,需要鉴别诊断。高效液相色谱法检测尿蝶呤谱、红细胞DHPR活性测定、BH4负荷试验和基因诊断能有效鉴别PKU和BH4D,其中HPLC法检测尿蝶呤谱可快速鉴别PKU、BH4D[6],联合红细胞DHPR活性测定能快速有效鉴别出BH4D的类型,包括PTPS、DHPR、GTPCH三种常见类型[1、7];BH4负荷试验和基因诊断考虑到操作性和时效性,常不作为快速鉴别PKU和BH4D的筛查手段[3,8]。在HPLC法中,国外有研究表明盐酸洗脱干血片也可用于血液中蝶呤类检测[9]。国内常用I2氧化法[5]或者MnO2氧化法[1]处理新鲜尿液标本,这两种方法的标本可选用随机尿,收集方便且无创,实验操作简单,是HPLC法检测尿蝶呤谱前处理的首选方法。 本研究表明,I2氧化法和MnO2氧化法检测尿蝶呤能有效鉴别PKU和BH4D,疾病诊断符合率达到100%,但两种方法检测结果有差异(P<0.05),这可能与两种方法使用不同的盐酸浓度有关(I2氧化法使用6 mol/L,MnO2氧化法使用1 mol/L),有研究表明[10],改变实验环境的酸度会影响蝶呤类物质的检出,这是尿液PH值或离子强度会影响蝶呤类物质荧光基团的结构,从而影响检测;另外,上述两种方法有差异也可能与使用的氧化物类型、浓度或氧化时间有关。氧化物的浓度会对新蝶呤和生物蝶呤有影响,这可能与高浓度氧化物或强氧化性物质会破坏尿液中的新蝶呤和生物蝶呤;低浓度氧化物、弱氧化性物质或氧化时间不足,难以将尿液中的四氢生物蝶呤、二氢生物蝶呤等生物蝶呤衍生物完全氧化成生物蝶呤有关[7]。 在I2氧化法和MnO2氧化法的方法学评价实验中,两种方法N的检测限[I2氧化法:(0.000 63±0.000 27)μg/L;MnO2氧化法:(0.000 76±0.000 32)μg/L],B的检测限[I2氧化法:(0.000 84±0.000 35)μg/L;MnO2氧化法:(0.000 81±0.000 33)μg/L],I2氧化法优于MnO2氧化法。两种方法的批内精密度(CV)均较好(I2氧化法和MnO2氧化法N:2.54%、3.51%,B:2.43%、3.26%);批间CV I2氧化法优于MnO2氧化法(I2氧化法和MnO2氧化法N:2.26%、6.25%,B:2.75%、7.32%)。尿液样本在-20℃冰箱保存,稳定性较好(CV<10%)。在低浓度标准品回收试验中,I2氧化法中N的平均回收率较差,(I2氧化法和MnO2氧化法N:128.19%、85.70%;B:93.49%、87.55%),这可能与低浓度物质在仪器中的响应度低,容易受仪器噪音干扰有关;中、高浓度标准品回收试验N和B的平均回收率均良好(中、高浓度回收率分别是I2氧化法N:109.90%、99.59%,B:97.57%、103.29%;MnO2氧化法N:94.71%、98.41%,B:95.43%、100.50%)。两种方法处理样品在0.01~20.00 μg/L范围内均有良好的线性。上述方法学评价结果可认为I2氧化法优于MnO2氧化法,但两者可基本满足临床上检测尿蝶呤谱的需求。由于两者新蝶呤和生物蝶呤的检测结果、检测限、精密度和回收率有差异,各实验室需要结合实际需要选择合适的方法并制定相应的参考范围[11-12]。 利益相关声明:作者均声明无利益冲突。 作者贡献说明:谢汛杰设计研究方案,实施研究过程,分析数据,论文撰写;江剑辉实验资金支持,论文修改;曾伟宏提出研究思路,设计研究方案,论文修改。

3 讨论

