槲寄生多糖提取工艺优化及抗氧化活性研究
蒋大珍,马佰诚,杨 皎,罗进城,孙雪薇,李佳琳
(佳木斯大学公共卫生学院,黑龙江佳木斯 154007)
槲寄生(Viscum coloratum)作为我国传统中药,历史悠久,2020 年版《中华人民共和国药典》收载并明确槲寄生为桑寄生科植物槲寄生,以冬季至次春采割,除去粗茎,切段,干燥,或蒸后干燥入药,功能主治去风湿、补肝肾、安胎元、用于风湿痹痛[1]。研究表明,槲寄生含有的多糖具有细胞免疫和体液免疫作用,能增强小鼠巨噬细胞TNF-α、IL-1 的分泌[2-3]。目前,植物多糖的提取方法包括热水浸提、酸提取、碱提取、醇提取[4]、酶辅助提取、超声辅助提取、微波辅助提取和超临界萃取等多种方法。热水浸提比较耗时,酸、碱提取容易破坏多糖结构,本试验在热水浸提、乙醇沉淀法基础上辅以超声波,进行了单因素及响应面工艺优化试验的研究,以期减少提取时间、提高提取效率,寻求最优提取工艺条件,并初步探究槲寄生的抗氧化活性。
1 材料和方法
1.1 试验材料
槲寄生茎、叶于2022 年12 月采摘自黑龙江省佳木斯市桦川县横头山镇申家店村(130.652 9°N,46.602 23°E)。2,2-联苯基-1-苦基肼基购自上海麦克林生化科技有限公司,2,2′-联氮基双二铵盐购自上海阿拉丁生化科技股份有限公司,VC 购自天津市凯通化学试剂有限公司,所用试剂均为国产分析纯,所用三蒸水为实验室自制。
试验所用仪器为RE-201D 旋转蒸发仪(郑州生化仪器有限公司)、SHZ-D(Ⅲ)循环水式多用真空泵(郑州生化仪器有限公司)、KQ-500DE 型数控超声波清洗器(昆山市超声仪器有限公司)、YB-FD-1 冷冻干燥机(上海亿倍实业有限公司)、中药粉碎机(长沙步源制药机械设备有限公司)。
1.2 试验方法
1.2.1 槲寄生的预处理
将槲寄生茎、叶剪成小段洗净,70 ℃烘箱烘干,粉碎,过筛(0.45 mm)后得到槲寄生粉末,将粉末浸泡于95%乙醇24 h,除去脂类杂质,抽滤,滤渣烘干后作为提取原料。
1.2.2 槲寄生多糖的提取
称取2 g 槲寄生粉末,每组3 份,按照一定料液比加入蒸馏水浸泡2 h 后放入超声数控清洗机中,设置一定温度、时间、功率进行槲寄生多糖提取,抽滤取滤液,减压浓缩到10 mL,加入4 倍体积的无水乙醇,4 ℃静置过夜,4 500 r/min 离心10 min 收集沉淀,冷冻干燥2 d 得到槲寄生粗多糖[5-6]。
式中,W 表示槲寄生多糖得率(%);m 表示干燥所得槲寄生多糖质量(g);M 表示槲寄生粉末质量(g)。
1.2.3 单因素试验
通过观察多糖得率,探究不同因素(料液比、超声温度、超声时间、超声功率)对槲寄生多糖得率的影响,设计单因素试验。称取2 g 槲寄生多糖粉末,固定料液比[1∶10、1∶20、1∶30、1∶40、1∶50(g∶mL)]、超声温度(40、50、60、70、80 ℃)、超声时间(10、20、30、40、50 min)、超声功率(0、200、300、400、500 W),其余操作同1.2.2。
1.2.4 响应面试验
基于单因素试验的结果,以多糖得率作为响应变量,选择料液比、超声时间、超声温度、超声功率4 个因素作为自变量,使用Design-Expert 13 统计学软件,进行4 因素3 水平试验设计,具体试验因素及水平见表1。

表1 响应面法试验设计因素水平Table 1 Designed factor level of the response surface method
1.2.5 槲寄生粗多糖的分离
将提取工艺优化后所得槲寄生粗多糖用蒸馏水复溶,按照1∶5 的比例加入Sevage 试剂(正丁醇∶氯仿=1∶4),置于分液漏斗中,振荡,去掉中间层变性蛋白和下层有机溶剂,重复多次,取上层多糖溶液,离心,取上清液浓缩至一定体积后装入透析袋(截留3 500 Da)流水透析48 h,浓缩,所得多糖溶液加入无水乙醇至80%,4 ℃醇沉淀12 h,收集醇沉淀结果,分别用乙醚、丙酮润洗3 次,冷冻干燥后得到初步除盐、除蛋白的槲寄生粗多糖。
1.3 槲寄生多糖抗氧化活性测定
精确称取上述方法制备的干燥至恒重的槲寄生多糖粉末200 mg,蒸馏水溶解,定容至100 mL 容量瓶,配制成质量浓度为2 mg/mL 的槲寄生多糖溶液,准备7 支试管,分别稀释成浓度为0.2、0.4、0.6、0.8、1.0、1.5、2.0 mg/mL 的槲寄生多糖溶液备用。阳性对照VC 溶液同上配制。
1.3.1 DPPH 自由基清除率测定
取上述不同浓度样品溶液各2 mL,加入2 mL DPPH 醇(0.2 mmol/L)溶液,室温避光反应30 min。以无水乙醇为空白对照,VC 溶液为阳性对照,重复测定3 次。DPPH 自由基清除率[7-9]计算公式如下
式中,A0为2 mL 无水乙醇+2 mL DPPH 醇溶液的吸光度;A1为2 mL 样品溶液+2 mL DPPH 醇溶液的吸光度;A2为2 mL 样品溶液+2 mL 无水乙醇的吸光度。
1.3.2 ABTS 自由基清除率测定
配制7.4 mmol/L ABTS 溶液,2.6 mmol/L 过硫酸钾溶液,等体积1∶1 混合,定容至100 mL,避光,室温,反应12 h,得到ABTS 储备液,用无水乙醇稀释至A734nm=0.70±0.02,得到ABTS 工作液。取0.1 mL不同浓度槲寄生多糖溶液和阳性对照VC 溶液(0.2、0.4、0.6、0.8、1.0、1.5、2.0 mg/mL)加入3.9 mL ABTS工作液进行反应,常温避光反应10 min,在A734nm下测定混合溶液的吸光值A1,用无水乙醇代替ABTS工作液测定其吸光值,记为A2,等体积无水乙醇重复以上操作,记为A0,ABTS 自由基清除率计算公式[10]如下
1.3.3 三价铁离子总还原力测定
吸取1 mL pH 值为6.6 的磷酸盐缓冲液,加入1 mL 0.03 mol/L 的铁氰化钾,加入不同浓度槲寄生多糖溶液和阳性对照VC 溶液(0.2、0.4、0.6、0.8、1.0、1.5、2.0 mg/mL),50 ℃水浴20 min,加入1 mL 0.6 mol/L 三氯乙酸混匀,随后加入2 mL 0.006 mol/L 的氯化铁溶液,4 500 r/min 离10 min,取上清液于A700nm处测量吸光值,对照组取2 mL水代替氯化铁溶液,空白组取1 mL 水代替样品溶液[11]。重复3 次。
1.4 数据处理
采用Excel 2019 软件分析数据、Design Expert 13 软件进行响应面试验设计及结果分析Origin 8.0软件作图。
2 结果与分析
2.1 单因素对槲寄生多糖得率的影响
由图1 可知,料液比为1∶20~1∶50(g∶mL)时,槲寄生多糖得率呈先上升后缓慢下降的趋势,料液比为1∶30(g∶mL)多糖得率最高,为3.85%;之后缓慢降低,1∶50(g∶mL)时多糖得率下降为3.36%,其原因可能是随着提取溶剂体积的增加,多糖与溶剂面积增加,多糖浸出率也随之增加;但料液比过高,也同时增加了其他物质的溶出,抑制了多糖的浸出[12-13]。

图1 料液比对槲寄生多糖得率的影响Figure 1 Effect of solid-liquid ratio on the yield of mistletoe polysaccharide
由图2 可知,当超声温度为40 ℃时,多糖得率仅为2.28%,当超声温度达70 ℃时,多糖得率为5.59%,但当超声温度达80 ℃时,多糖得率反而降低,这是由于过高的温度可能引起多糖氧化分解,使多糖得率降低[14]。

图2 超声温度对槲寄生多糖得率的影响Figure 2 Effect of ultrasonic temperature on the yield of mistletoe polysaccharide
由图3 可知,当超声时间为10 min 时,多糖得率为7.34%,超声时间为20 min 时,多糖得率达到顶峰,为8.60%,但超声时间为30 min 时,多糖得率开始急剧下降,仅为3.42%,这可能是因为长时间超声对多糖结构造成破坏,影响多糖的溶出[15]。

图3 超声时间对槲寄生多糖得率的影响Figure 3 Effect of ultrasonic time on the yield of mistletoe polysaccharide
由图4 可知,当超声功率达到300 W 时,多糖得率最高,为5.86%,随着超声功率的增加,多糖得率开始持续下降,其原因可能是与在较大功率的超声作用下,糖苷键发生断裂有关[16]。因此,选择最优值附近进行响应面试验。

图4 超声功率对槲寄生多糖得率的影响Figure 4 Effect of ultrasonic power on the yield of mistletoe polysaccharide
2.2 响应面法优化结果
基于响应面数据分析,以料液比(A)、超声时间(B)、超声温度(C)、超声功率(D)作为独立自变量,以槲寄生多糖得率作为因变量,得到以下二次项回归方程
Y=8.300 00+0.055 80A-0.062 58B-0.032 50AD+0.095 75BC+0.095 00BD+0.020 00CD-0.049 74A2-1.100 00B2-1.110 00C2-0.964 90D2
2.2.1 方差分析结果
由表2 可知,多元函数方程模型的F 值为1.16,P 值小于0.000 1,表明回归模型具有统计学差异,而失拟项的P 值为0.698 7,大于0.05,表示模型在统计学上不显著,因此方程是可靠的;该方程的决定系数R2为0.954 9,说明其数据拟合性好,可以用来代替试验数据,描述变量与响应值之间的关系。校正系数R2Adj为0.909 8,表明模型能解释槲寄生多糖得率的90.98%变化,而变异系数为4.930 0%,远低于10%,这表明非试验因素对结果影响较小。根据各项F 值所知,各单因素对多糖得率的影响程度最大的是超声温度(C),其次是超声时间(B)、超声功率(D),最后是料液比(A)。其中,BC、A2、B2、C2、D2对多糖得率的影响极显著(P<0.01),而其余项对指标影响不显著(P>0.05)。

表2 回归模型方差分析Table 2 Regression model analysis of variance
2.2.2 各因素二次项交互作用分析
由图5 可知,在回归模型方差分析结果基础上,创建响应面图及等高线图,以分析选定的各因素对槲寄生多糖得率的影响。响应面图和等高线图可以清晰地展示交互作用对响应值的影响程度。当响应面曲面更为陡峭,等高线更为密集时,说明影响程度更显著。此外,如果等高线图更接近椭圆形,表示两个因素之间的交互作用更强;而如果等高线图趋近圆形,则可以几乎忽略两个变量之间的交互作用[17-18]。由图5 可知,表示超声时间和超声温度对槲寄生多糖得率的交互作用,当超声时间较短时,随着超声温度的增加,槲寄生多糖得率减少;然而,当超声时间较长时,随着超声温度的增加,槲寄生多糖得率增加。响应曲面的倾斜度高且坡度陡峭,表明超声时间和超声温度之间的交互作用呈极显著差异(P<0.01),这与表2 结果一致。由图6 可知,超声温度和超声功率的交互作用接近于圆形,表明两者之间的交互作用几乎可以忽略。

图6 超声温度与超声功率的交互作用对槲寄生多糖得率的影响Figure 6 The effect of interaction between ultrasonic temperature and ultrasonic power on the yield of mistletoe polysaccharid
2.2.3 验证试验
根据响应面试验回归方程模型确定了最佳工艺参数:料液比1∶29.36(g∶mL)、超声时间14.58 min、超声温度64.48 ℃、超声功率271.09 W,在该条件下理论得率为8.74%,根据实际操作及试验条件,将其修正为料液比1∶29、超声时间15 min、超声温度64 ℃、超声功率300 W,在该条件下进行3 次重复试验,求取平均值,槲寄生多糖得率为8.17%,理论值与实际得率仅差0.57%,说明该工艺优化条件稳定合理。
2.3 槲寄生多糖的抗氧化活性试验结果分析
2.3.1 槲寄生多糖对DPPH 自由基清除能力
由图7 可知,槲寄生多糖对DPPH 自由基具有明显的清除效果,此外,随着槲寄生多糖质量浓度的增加,其对DPPH 自由基的清除能力也逐渐增强,呈现出明显的浓度-效应关系,当质量浓度为2 mg/mL时,VC 溶液的清除率已达到95.90%,槲寄生多糖清除率也达到(79.07±0.60)%,其IC50为0.612 mg/mL,表明槲寄生多糖具有较好的抗氧化活性。

图7 槲寄生多糖对DPPH 自由基清除能力Figure 7 Scavenging ability of DPPH free radicals by mistletoe polysaccharides
2.3.2 槲寄生多糖对ABTS 自由基清除能力
由图8 可知,在0.2~2.0 mg/mL 浓度范围内,随着槲寄生多糖质量浓度的增加,其对ABTS 自由基的清除率也增加。当浓度达到2.0 mg/mL 时,其对ABTS 自由基清除率为(51.38±0.29)%,IC50为2.611 mg/mL。由此可知,槲寄生多糖对ABTS 自由基的清除率与其对DPPH 自由基的清除率能力相比相对较弱。

图8 槲寄生多糖对ABTS 自由基清除能力Figure 8 Scavenging ability of ABTS free radicals by mistletoe polysaccharides
2.3.3 槲寄生多糖对三价铁离子总还原力
铁离子总还原力主要基于氧化还原反应,反应过程中,多糖溶液中的活性成分将三价铁离子还原成二价铁离子,吸光度值越大,表明其总还原力越强,相应地,表明该多糖抗氧化能力越好[19]。由图9 可知,槲寄生多糖总还原力弱于VC 溶液,但随着质量浓度的增加,其总还原力呈上升趋势,当浓度为2.0 mg/mL 时,其总还原力为(0.33±0.05),表明槲寄生多糖具有一定的还原能力。
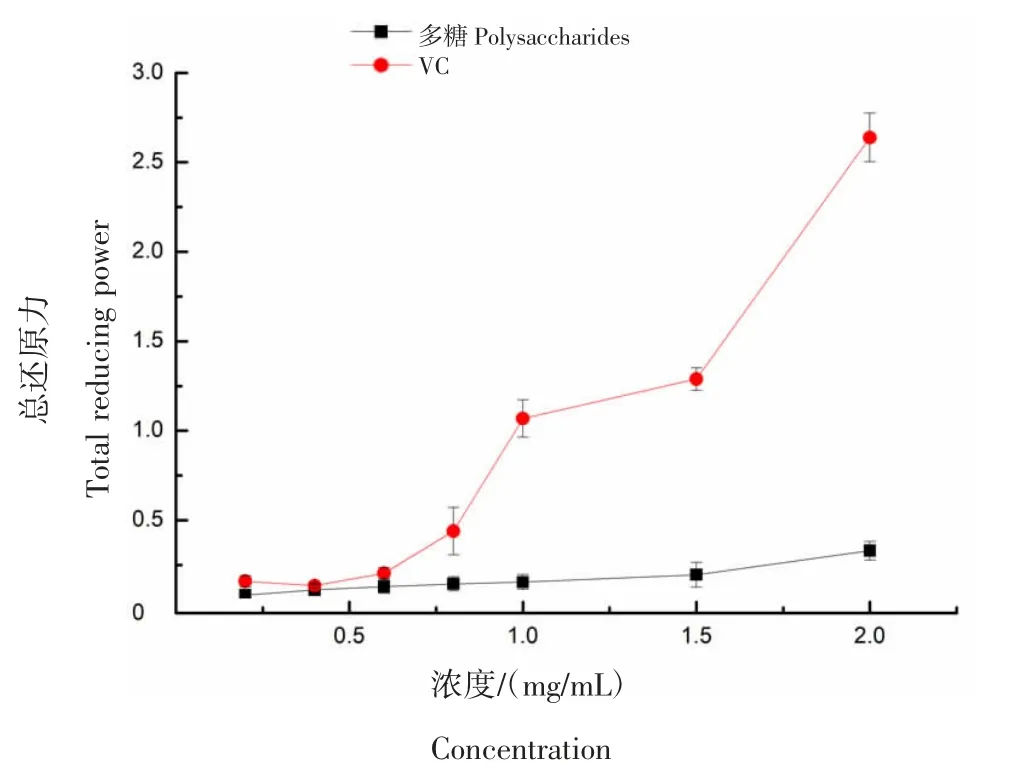
图9 槲寄生多糖对三价铁离子总还原力Figure 9 Total reducing power of mistletoe polysaccharide on trivalent iron ions
综上所述,槲寄生多糖对DPPH 自由基、ABTS自由基均有清除作用,对三价铁离子具有还原作用,但槲寄生多糖对ABTS 自由基的清除率弱于对DPPH 自由基的清除率。
3 讨论与结论
与传统煎煮法相比,超声辅助提取可以破坏细胞壁和细胞膜,释放多糖等成分,多糖提取时间显著缩短,杂质少,超声过程中产生热效应,增加了有效成分的溶解[20]。本试验发现,当温度升高时,分子的平均动能增加,分子之间的碰撞频率和能量也会增加,因此反应速率会加快;同时温度还可以影响反应的平衡常数,即反应物和生成物之间的比例,反应温度升高会使反应的平衡常数向生成物方向移动,因此,促进多糖的生成。在本试验中,只有超声温度和超声时间之间的交互作用对槲寄生多糖的得率有极显著差异(P<0.01),其他因素之间的交互作用对多糖得率无显著影响(P>0.05)。料液比与各因素之间的交互作用均不显著(P>0.05),这可能与试验前浸泡2 h 有关;超声功率本身对试验结果影响显著(P<0.05),但与超声温度之间的交互作用对试验结果影响微小,这可能是由于参数设置的局限性所致。除上述原因外,还可能是与试验未考虑到其他的控制变量或其他试验因素的影响,今后可以进行更大范围的试验,更全面地研究两个因素之间的交互作用。
本试验以槲寄生茎、叶粉末为提取原料,通过采取超声辅助的水提取和醇沉淀方法,经过单因素试验和响应面法的优化,确定了最佳的槲寄生多糖提取工艺条件:料液比1∶29(g∶mL)、超声时间15 min、超声温度64 ℃、超声功率300 W,此条件下槲寄生多糖得率为8.17%,与预测值接近,该方法与热水浸提法相比,缩短了提取时间,能够为槲寄生多糖的量产提供参考。通过初步抗氧化活性分析,2 mg/mL 的槲寄生多糖对DPPH 自由基、ABTS 自由基清除率分别为79.07%和51.38%,IC50分别为0.612、2.611 mg/mL;对三价铁离子总还原力为0.33,表现出较好的抗氧化活性,是一种天然的抗氧化剂,可以为槲寄生多糖的开发利用提供参考依据。未来可以进一步优化超声参数,深入研究槲寄生多糖的生物活性。

