痰热清注射液对9 种肿瘤标志物电化学发光法、光激化学发光法检测结果的干扰情况观察
尹元,张赛,王正印,赵延荣,顾征璟,邢嘉翌,胡昀昭,陆群
1 上海中医药大学附属上海市中西医结合医院检验科,上海 200082;2 复旦大学附属妇产科医院生物样本库
近年来,恶性肿瘤发病率持续上升,肿瘤标志物在肿瘤的早诊断和早治疗发挥重要作用。肿瘤标志物的检测目前主要采用化学发光法,包括直接化学发光法、电化学发光法和光激化学发光法等。研究[1-3]显示,化学发光法检测肿瘤标志物的结果可能受到多种因素的干扰,如部分基于生物素链霉亲和素的化学发光法检测肿瘤标志物、心肌标志物和内分泌检测项目的结果受到了明显干扰[4]。近年来,临床上对药物干扰检测结果给予了很多关注。随着中药在临床上的广泛使用,特别是在中医医院和中西医结合医院,中药对检验结果的干扰日益受到广泛关注。痰热清注射液是一种具有抑菌抗毒、抗炎解热、祛痰镇咳、护胆利肝作用的中药注射液,临床应用广泛[5-6]。在临床工作中,我们偶然发现个别患者的肿瘤标志物检测结果与临床表现不符,经查阅患者病史发现其使用了痰热清注射液。2022年9月—2023年10月,我们观察了痰热清注射液对9 种肿瘤标志物电化学发光法、光激化学发光法检测结果的干扰情况,现将结果报告如下。
1 材料与方法
1.1 痰热清注射液、仪器及试剂 痰热清注射液(20 mL/瓶)购自上海凯宝药业有限公司,批号1609216。Roche Cobas e601全自动电化学发光免疫分析仪和科美Lica500 全自动光激化学发光免疫分析仪均为本实验室正常在用仪器,已按照相关规范进行仪器校准和相关检测项目的分析性能验证。肿瘤标志物检测质控品购自上海市临床检验中心。
1.2 痰热清注射液药物干扰浓度的确定 根据国际临床化学和实验医学联合会(International Federation of Clinical Chemistry and laboratory medicine ,IFCC)的建议,我们将干扰药物浓度设定为该药物治疗浓度的10倍[7]。根据痰热清注射液的药品说明书,该药的治疗用量为1 瓶/日(20 mL/瓶),经计算得到其药物治疗浓度为4 mL/L(血清药物浓度),即本研究中使用的痰热清注射液的药物干扰浓度为40 mL/L。
1.3 检测样本的制备 收集近期未使用痰热清注射液的上海中医药大学附属上海市中西医结合医院肿瘤科患者和健康人新鲜血清(无黄疸、溶血和脂血)混合制备基础样本。将40 μL 痰热清注射液和注射用水分别加入960 μL 基础样本中,分别配制成干扰样本和对照样本,用于后续检测。
1.4 痰热清注射液对9 种肿瘤标志物电化学发光法、光激化学发光法的检测结果干扰情况观察 采用干扰筛选试验。实验前已对检测系统进行仪器校准和检测项目的性能验证,并常规开展室内质量控制,检测系统均符合要求。通过每日的室内质控评估检测系统的稳定性,得到相关检测项目的精密度。将基础样本检测10次,计算批内标准差s,计算dmax/s,然后查dmax/s与重测次数对应表得出各项目重复测定次数,计算得本研究中肿瘤标志物项目重复检测次数为3 次。分别采用电化学发光法、光激化学发光法检测基础样本、干扰样本和对照样本中9种肿瘤标志物(AFP、CEA、CA125、CA15-3、CA19-9、CA72-4、TPSA、FPSA、CYFRA21-1),测定三次并计算均值,计算药物干扰值(dobs)、最大允许干扰值(dc)。药物干扰值(dobs)=干扰样本均值-对照样本均值。参考2022年国家卫生健康委员会临床检验中心临床检验室间质量评价标准中使用的肿瘤标志物的允许总误差(allowable total error,TEa)作为项目的允许总误差(25%),按照临床检验行业标准设定肿瘤标志物的最大允许干扰值(dc)为1/3 Tea(8.33%),即dc=对照样本均值×1/3 Tea(8.33%)。将dobs与dc进行比较,若dobs的绝对值<dc,则不存在干扰;dobs的绝对值>dc且dobs为正,则表明药物对检测结果存在正干扰;若dobs的绝对值>dc且dobs为负,则表明药物对检测结果存在负干扰。
1.5 痰热清注射液的干扰效应及最低干扰浓度测算 采用剂量效应试验。使用干扰样本和对照样本配置药物浓度分别为0 mL/L、10 mL/L、20 mL/L、30 mL/L、40 mL/L 的剂量效应试验样本,使用“1.4”中判定为存在干扰的检测方法检测肿瘤标志物浓度,测定三次并计算均值,计算干扰效应。干扰效应=(各浓度样本均值-0 mL/L 样本均值)/0 mL/L 样本均值×100%。为降低系统漂移影响,第1 次检测按照样本浓度降序检测,第2 次检测按样本浓度升序检测,第3 次检测按样本浓度降序检测。采用多项式回归法建立干扰剂量效应拟合方程,以干扰效应为最大允许干扰值时,计算最低干扰浓度。
2 结果
2.1 痰热清注射液对9 种肿瘤标志物的电化学发光法检测结果干扰情况 电化学发光法检测基础样本中9 种肿瘤标志物的浓度均值分别为AFP 24.45 ng/mL、CEA 25.72 ng/mL、CA125113.80 U/mL、CA15-361.81 U/mL、CA72-428.19 U/mL、TPSA 14.27 ng/mL、FPSA 0.808 ng/mL、CA19-954.28 U/mL、CYFRA2113.01 ng/mL,对照样本浓度均值分别为24.03 ng/mL、23.69 ng/mL、107.00 U/mL、56.20 U/mL、27.35 U/mL、13.08 ng/mL、0.755 ng/mL、50.57 U/mL、12.73 ng/mL,干扰样本浓度均值分别为23.18 ng/mL、23.56 ng/mL、105.86 U/mL、58.23 U/mL、27.33 U/mL、13.08 ng/mL、0.770 ng/mL、34.28 U/mL、12.67 ng/mL,痰热清注射液对电化学发光法检测9种肿瘤标志物的干扰筛选试验结果见表1。由表1可知,痰热清注射液对CA19-9 的电化学发光法检测结果存在负干扰,对AFP、CEA、CA125、CA15-3、CA72-4、TPSA、FPSA、CYFRA21-1 等8 种肿瘤标志物的电化学发光法检测结果均无干扰。
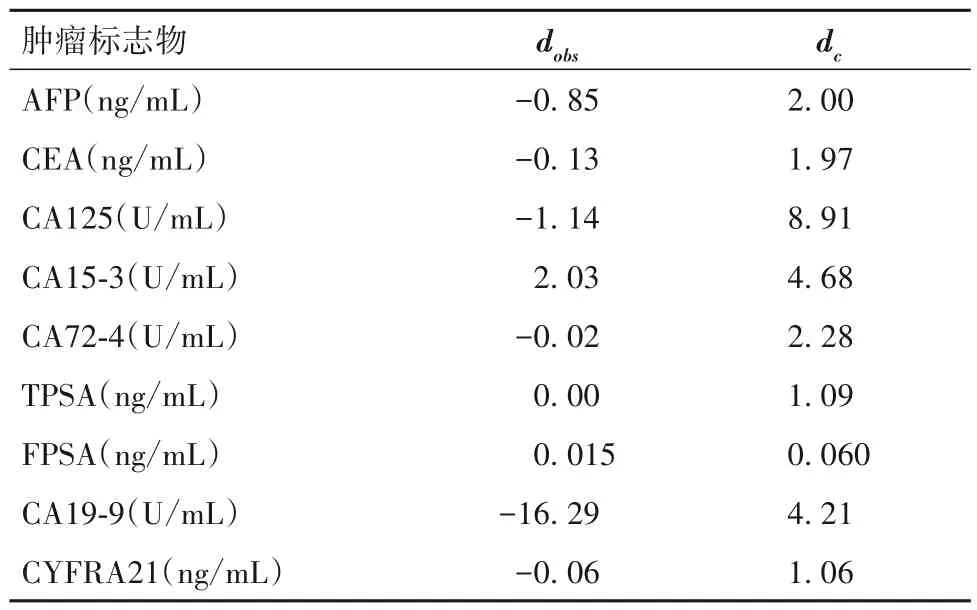
表1 痰热清注射液对电化学发光法检测9种肿瘤标志物的干扰筛选试验结果
2.2 痰热清注射液对9种肿瘤标志物的光激化学发光法检测结果干扰情况 光激化学发光法检测基础样本中9 种肿瘤标志物的浓度均值分别为AFP 24.54 ng/mL、CEA 21.43 ng/mL、CA125120.03 U/mL、CA15-337.20 U/mL、CA72-432.64 U/mL、TPSA 14.20 ng/mL、FPSA 0.97 ng/mL、CA19-955.22 U/mL、CYFRA2110.52 ng/mL,对照样本浓度均值分别为22.81 ng/mL、20.14 ng/mL、121.62 U/mL、34.50 U/mL、36.82 U/mL、14.94 ng/mL、0.92 ng/mL、60.40 U/mL、11.36 ng/mL,干扰样本浓度均值分别为23.53 ng/mL、19.78 ng/mL、120.86 U/mL、34.23 U/mL、37.41 U/mL、14.36 ng/mL、0.92 ng/mL、58.37 U/mL、11.05 ng/mL,痰热清注射液对光激化学发光法检测9 种肿瘤标志物的干扰筛选试验结果见表2。由表2可知,痰热清注射液对9 种肿瘤标志物的光激化学发光法检测结果均无干扰。
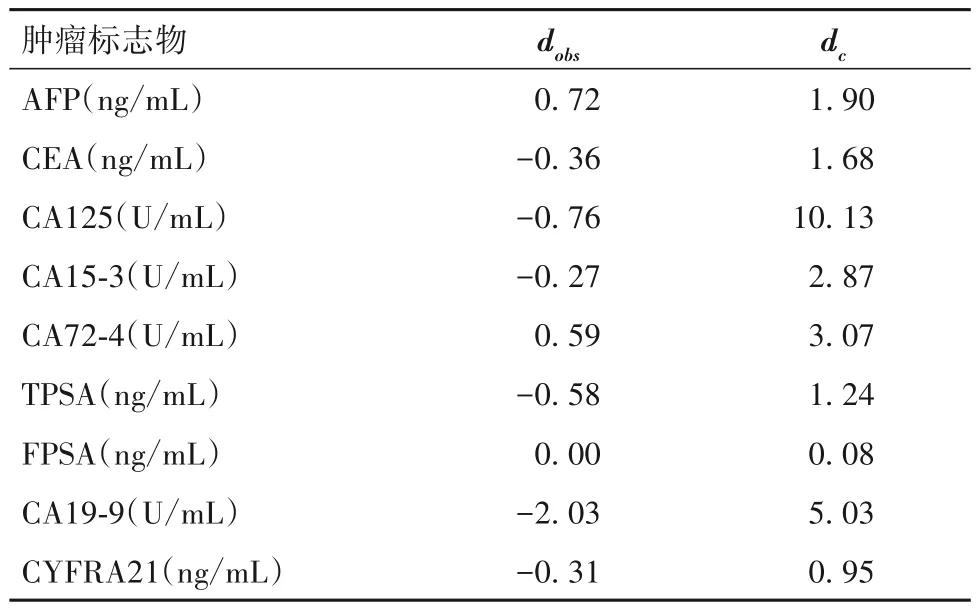
表2 痰热清注射液对光激化学发光法检测9种肿瘤标志物的干扰筛选试验结果
2.3 痰热清注射液的干扰效应及最低干扰浓度痰热清注射液对CA19-9 干扰的剂量效应试验结果见表3。由表3 可知,当药物浓度为40 mL/L 时,痰热清注射液对电化学发光法检测CA19-9 的干扰效应为-29.28%。建立的干扰剂量效应拟合方程为:Y=-0.7231X-1.938(R2=0.9784)。其中Y 为干扰效应值,X 为干扰药物浓度,R2为相关系数。当Y=-8.33 时,X 为8.84 mL/L,即痰热清注射液对电化学发光法检测CA19-9 产生干扰的最低干扰浓度为8.84 mL/L。
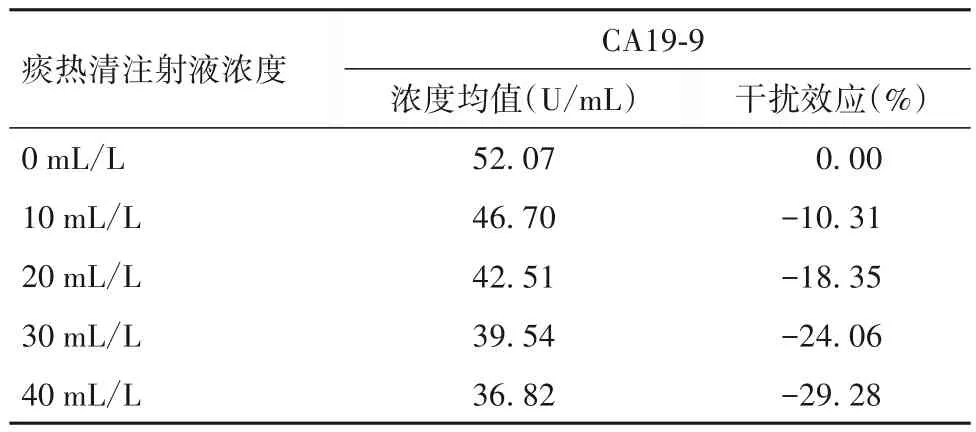
表3 痰热清注射液对CA19-9干扰的剂量效应试验结果
3 讨论
药物干扰在对临床检验结果的干扰中普遍存在[8]。齐志宏等[9]研究发现,羟苯磺酸钙能够对酶法检测血肌酐产生明显的负干扰。在前期研究[10-11]中,我们也发现痰热清注射液和红花注射液对部分临床生化检验项目也存在明显干扰。在临床免疫学检测中,有很多物质会造成干扰,如异嗜性抗体(heterophile antibody,HAb)、类风湿因子(rheumatoid factor,RF)、人抗动物抗体(human anti-animal antibody,HAAb)、自身抗体等,这些物质主要是与被测物化学结构存在差异但活性类似的物质[12]。一些治疗性药物抗体也可以通过与检测试剂中的抗体竞争抗原,对检测结果产生干扰,如使用地高辛抗体Fab片段[13]。罗氏电化学发光法检测CA19-9是将样本、生物素化的CA19-9 单克隆抗体和钌(Ru)a 标记的CA19-9特异性单抗一起孵育,形成抗原抗体夹心复合物。随后添加包被链霉亲合素的磁珠微粒进行孵育,复合体与磁珠通过生物素和链霉亲合素的作用结合。随后将反应液吸入测量池中,通过电磁作用将磁珠吸附在电极表面,未与磁珠结合的物质通过清洗液被去除,给电极加以一定的电压,使复合体化学发光,并通过光电倍增器测量发光强度以确定含量。电化学发光法因其特异性好、灵敏度高、检测范围宽等优点已广泛应用于临床免疫学检测[14]。罗氏CA19-9试剂说明书指出,厂商已经对可能的干扰因素进行了验证,并指出CA19-9的检测结果不受黄疸(胆红素<1129 μmol/L或<66 mg/dL)、溶血(血红蛋白<1.4 mmol/L 或<2.2 g/dL)、脂血(脂肪乳剂<1500 mg/dL)和生物素(<100 ng/mL 或<409 nmol/L)的影响。同时也不受27 种常用药物和类风湿因子(rheumatoid factor,RF<1500 IU/mL)的干扰,但并未指出具体药物名称。但对于接受高剂量生物素治疗的患者(>5 mg/d),必须在末次生物素治疗8 h 后再进行采血检测。
痰热清注射液是一种由黄芩、连翘、金银花、山羊角、熊胆粉等组成的中成药,具有清热解毒、镇咳平喘、抗炎等作用,在临床使用中表现出确切疗效,使用广泛[15]。本研究中,我们发现痰热清注射液对罗氏Cobas e601 电化学发光法检测CA19-9 产生了明显负干扰,但干扰的具体机制尚不清楚。由于药物的种类繁多,特别是中药的复杂性,因此药物对临床检验结果的干扰通常比较隐匿[16]。本研究也存在一定的局限性,如本研究是在体外进行的干扰研究,药物在体内的代谢和存在形式和体外可能存在差异。此外不同厂家生产的痰热清注射液可能由于成分的差异也对结果的干扰存在差异。
综上所述,痰热清注射液对CA19-9的电化学发光法检测结果存在负干扰,干扰效应为-29.28%,最低干扰浓度为8.84 mL/L。痰热清注射液对光激化学发光法检测9种肿瘤标志物没有干扰。因此我们建议临床医生和检验人员都需对该项目的检测中的干扰因素给予足够的重视。同时体外诊断试剂厂商应该对药物干扰引起高度重视,在产品验证阶段应对可能的干扰药物进行充分验证并在试剂盒说明书中告知用户。为了尽可能减少药物的使用对检测结果的干扰,检验人员当发现检测结果和临床不符时,可以采取样品稀释、更换检测系统或联系临床重新采样等方式来消除干扰以得到正确结果指导临床的诊疗。

