基于FAERS 数据库的布罗索尤单抗安全信号挖掘与分析
黄敏仪,胡润凯,韩伟超,谢保城*
1.东莞东华医院 药学部,广东 东莞 523000
2.东莞市人民医院 药学部,广东 东莞 523000
X 连锁低磷性佝偻病是以磷代谢失衡的骨矿化障碍性罕见疾病,发病率为(3.9~5.0)/10 万[1]。2018 年5 月,低磷性佝偻病被纳入《第一批罕见病目录》第51 号罕见病[2],X 连锁低磷性佝偻病是低磷性佝偻病最常见的一种,约占遗传性低磷性佝偻病80%,其主要累及骨骼系统、肌肉系统、牙齿发育等方面,且致残率高[3]。传统的治疗方案主要为补充磷酸盐制剂和活性维生素D 等对症治疗,国内1 项调查分析显示,使用传统疗法的患者中治疗效果不理想率达76.42%[4]。
布罗索尤单抗作为治疗X 连锁低磷性佝偻病的最新代替疗法,是一种全人源性抗FGF23 单克隆抗体,该药与FGF23 结合并抑制其生物活性,通过增加肾脏对磷酸盐的吸收并升高血清1,25-二羟基维生素D 的浓度,改善患者的骨骼矿化和减少相关的骨骼疾病[5]。布罗索尤单抗用于成人和1 岁及以上儿童患者X 连锁低磷性佝偻病的治疗,于2018年在美国获批上市[6],2019 年被列入中国《第二批临床急需境外新药名单》,并于2021 年1 月在中国获批上市。多项研究显示,布罗索尤单抗疗效明显优于传统治疗[7],但由于其上市的时间较短,目前对该药的相关安全性研究报道较少,有必要加强对其的用药安全性研究。因此,本研究通过以访问美国食品药品管理局不良事件报告系统(FDA adverse events reporting system,FAERS)数据库为基础[8],收集布罗索尤单抗上市后的可疑药品不良事件(adverse drug events,ADE)数据并对其进行整理与分析,挖掘该药在真实世界中的药物警戒信号,从而为临床用药的安全性提供参考依据。
1 资料与方法
1.1 数据来源与整理
本研究收集的数据来源于美国食品药品管理局公共数据开放项目(openFDA),其原始数据由FAERS 数据库导入。所收集的药品ADE 均采用MedDRA 25.1 中不良反应术语集进行编码。
研究数据收集于FAERS 收到的自2004 年1 月1 日—2023 年6 月30 日布罗索尤单抗ADE 上报数据,利用Open Vigil FDA 分析工具提取数据[9]。为确保数据完整性,限定检索词为目标药物的通用名“burosumab”及商品名“crysvita”,将获得的数据导入Microsoft Office Excel 2019 进行筛选、整理及分析等,排除药物说明书适应证、操作或产品管理错误等ADE 信号的报告,以减少偏倚。
1.2 方法
在本研究中,基于比例失衡测量法(表1),通过采用报告比值比(reporting odds ratio,ROR)、比例报告比值比(proportional reporting ratio,PRR)和贝叶斯置信区间神经网络传播法(bayesian confidence propagation neural network,BCPNN)等方法对布罗索尤单抗进行ADE 信号挖掘[10-11]。BCPNN 法计算信息成分(information component,IC)值。当ROR、PRR 和BCPNN 的计算结果均符合标准时,则代表生成了1 个信号,且计算值越大代表目标药物与可疑ADE 之间的相关性越强。各信号挖掘方法的计算与标准见表2。
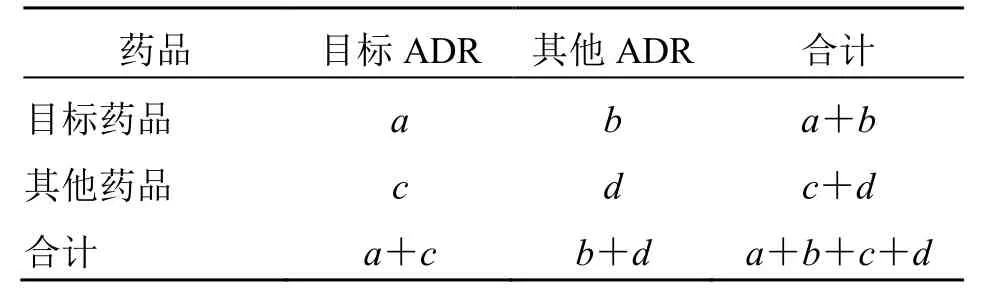
表1 信号检测列联表Table 1 Combination table of signal detection
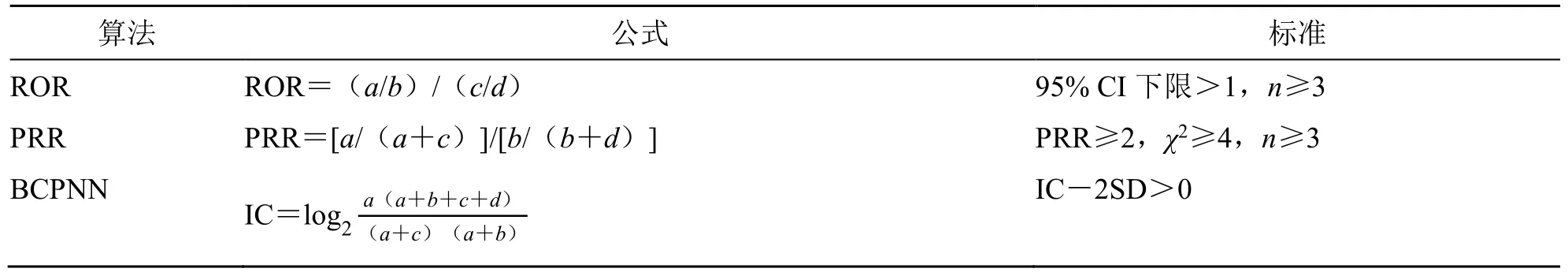
表2 信号检测的主要算法Table 2 Main algorithms of signal detection
2 结果
2.1 ADE 报告的基本情况
数据结果显示,从2004 年1 月1 日—2023 年6 月30 日FAERS 共收到ADE 报告16 697 425 份,其中与布罗索尤单抗相关的ADE 报告有4 852 份,占总ADE 报告数量的0.029 1%。其中严重ADE 报告(死亡、危及生命、住院、致残及先天畸形等)共996 份,约占布罗索尤单抗报告总数的20.53%;布罗索尤单抗上市第1 年(2018 年)的ADE 报告数有117 份,并呈逐年上升的趋势;上报人职业主要为卫生专业人员(包括医生和药剂师),占总数的89.26%;报告主要呈报国家为美国、英国及德国等发达国家,占总数的96.74%;用于治疗遗传性低磷性佝偻病的报告占75.91%,见表3。

表3 布罗索尤单抗相关ADE 报告的基本情况Table 3 Basic information about ADE reports associated with burosumab
2.2 各SOC 的ADE 报告及信号情况
根据ROR 法、PRR 法和BCPNN 法等方法的信号检测标准,共获得与布罗索尤单抗相关的信号110 个,其中说明书未提及的有28 个,较为常见的有甲亢、骨畸形、骨折、感染等。将筛选出的信号按照SOC 进行分类统计后,发现共涉及8 个系统器官,主要累及的系统器官有肌肉骨骼系统疾病(1 220 份报告)、给药部位各种反应(834 份报告)、神经系统疾病(311 份报告)和各类检查(281 份报告)等,见表4。
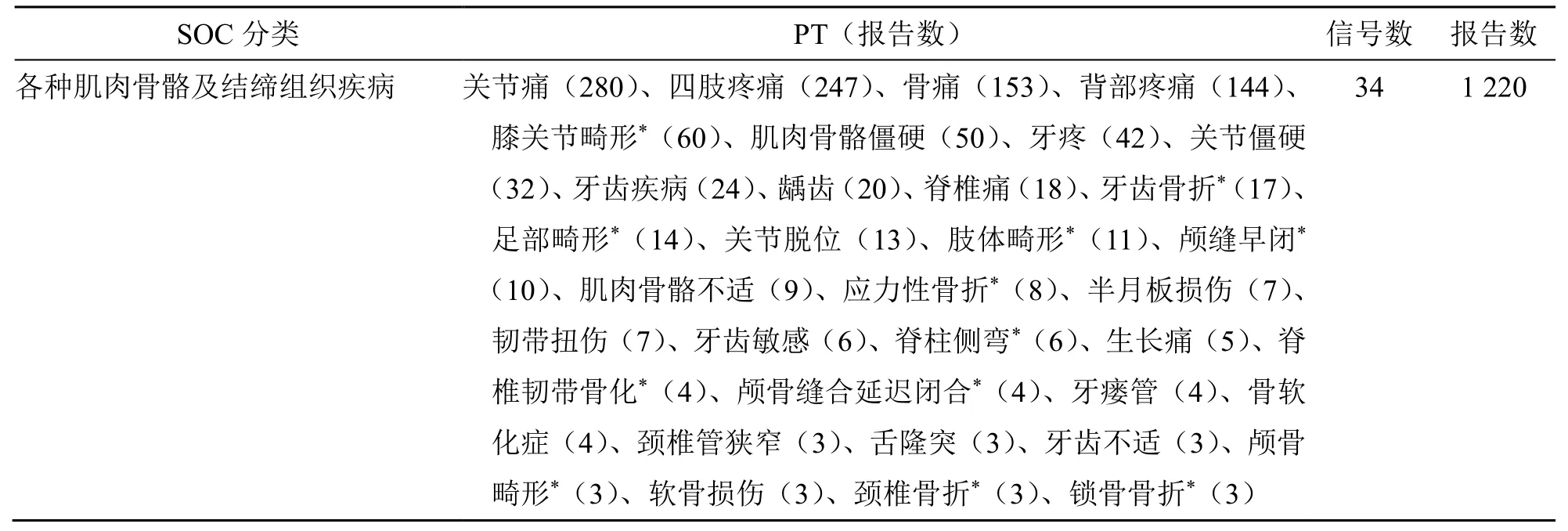
表4 布罗索尤单抗警戒信号累及系统/器官Table 4 Burosumab safety signal involvement system/organ
2.3 警戒信号排名情况
根据ADE 发生频次(a值)和信号强度(IC-2SD)分别对前20 个PT 进行排序,见表5、6。在警戒信号中,较常见的ADR 为肌肉骨骼痛、不宁腿综合征、注射液部位反应等,均为说明书提及的;而在相关性较高中,说明书未提及的有颅骨缝合延迟闭合、三发性甲状旁腺功能亢进和不安手综合征等,而发生频次较多的ADE 有不宁腿综合征、牙脓肿、维生素D 减少、膝关节畸形和血磷升高。

表5 布罗索尤单抗报告频数排名前20 位的ADE 信号Table 5 Top 20 ADE signals with the highest reported frequency of burosumab
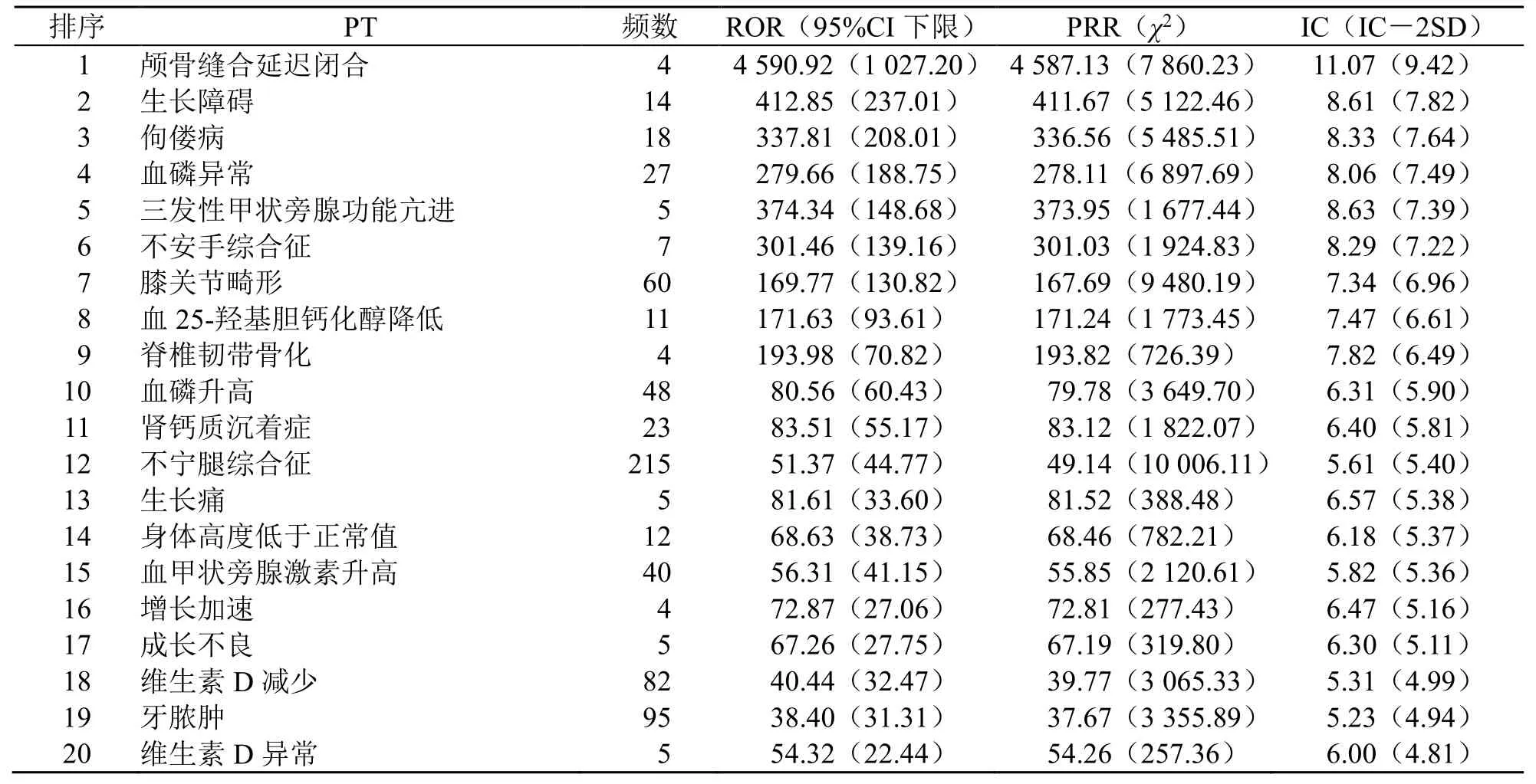
表6 布罗索尤单抗报告强度排名前20 位的ADE 信号Table 6 The top 20 ADE signals of burosumab reported strength
3 讨论
3.1 ADE 报告基本情况分析
本研究通过检索FARES 数据库自2004 年1 月1 日—2023 年6 月30 日收集的数据,发现布罗索尤单抗相关的ADE 报告最早出现在2018 年,符合该药上市的时间相关性。ADE 数量呈逐年增长的趋势,且上报人群主要为卫生专业技术人员,而FAERS 数据库中所有药物的ADE 报告上报人总体情况是以非卫生专业人员为主,可能原因是本品的使用环境导致,由于布罗索尤单抗只有注射剂型,需由卫生专业人员操作对患者进行注射。而报告中严重ADE 占20.53%,美国安全用药规范研究院(ISMP)将布罗索尤单抗定为高警示药物,提示使用不当会造成严重危害[12],因此,对于布罗索尤单抗的临床使用应加强对不良反应的监测。
报告中最主要的适应证为遗传性低磷性佝偻病,这与说明书适应证相符;上报国家主要为美国(4 522 份报告),而中国的报告只有3 份,可能与FAERS 的ADE 报告上报要求有关。目前,国内对于布罗索尤单抗的安全性研究报道较少,其ADE 风险可能在不同人种会存在差异,对中国人群的安全性仍需更多临床数据证明。
3.2 警戒信号分析
为避免单一算法导致结果偏倚或假阳性,本研究同时采用了比例失衡法中的频数法(ROR、PRR)和贝叶斯法(BCPNN)对布罗索尤单抗的安全警戒信号进行挖掘,其中,BCPNN 法相比ROR 法和PRR 法灵敏度一般,但是特异度高,且结果随着报告数量的增加而稳定[13],因此采用BCPNN 信号对报告信号强度进行排序。而通过本研究获得的布罗索尤单抗警戒信号主要分布在肌肉骨骼系统、给药部位各种反应、神经系统疾病和相关的检查指标等方面,这与药品说明书中的不良反应种类大致相同,证实了本研究方法的可信度。
本研究挖掘到的说明书未记载警戒信号有28个,涉及较多的是甲状旁腺功能亢进、骨畸形、骨折等。相关研究报道[14],X 连锁低磷性佝偻病患者在不同时期会呈现出稍不同的症状,如儿童时期会引发骨骼畸形,成年期则出现骨折等表现,并且传统治疗药物中的磷酸盐制剂如剂量过高会引起继发性甲状旁腺功能亢进[15]。另外,本研究还发现1个较罕见的警戒信号不安手综合征(a=7;ROR 的95% CI 下限=139.16;PRR=301.03、χ2=1 924.83;IC-2SD=7.22),目前并无相关研究报道布罗索尤单抗会引起该ADE,其与不安腿综合症的发病机制一样,可以出现双手麻木等症状[16],与布罗索尤单抗的相关性还需进一步的临床研究验证,但其警戒信号强度较高,在临床上应加以关注。
不宁腿综合征、牙脓肿、维生素D 减少、膝关节畸形和血磷升高等警戒信号无论在报告数还是信号强度均排在前列,除膝关节畸形可能由于原疾病进展造成的,其余均为说明书提及的不良反应,国外相关研究报道[17],上述不良反应均可能发生在成人,但对于儿童并无发生不宁腿综合征的报道。另外,在布罗索尤单抗ADE 报告频数排名前20 位的PT 中,出现频率最多的PT 为注射部位反应。1项来自美国关于成人的研究结果显示[18],布罗索尤单抗治疗组中11.8%患者出现注射部位疼痛、瘙痒、红斑、皮疹、淤伤和血肿等反应;另外1 项关于儿童的研究结果显示[19],布罗索尤单抗治疗组出现注射液部位反应的发生率为52%,2 项研究均为严重程度较轻,多在数天内基本痊愈。由于布罗索尤单抗为注射剂型,需皮下注射,如操作不当容易发生不良反应。因此,应注意加强对医务人员和患者的药物注射知识教育和宣讲,且该药的使用应由医务人员进行操作,保证患者用药安全。
3.3 局限性
本研究是基于FAERS 布罗索尤单抗上市后的警戒信号研究,其数据样本量大,但也存在一定的局限性[20]:FAERS 属于自发呈报数据库,是由不同人员进行上报,容易出现漏报、错报和重复上报等问题;此外患者可能出现基础疾病进展、合并用药等情况,会导致结果出现一定的偏倚;尽管本次采用了ROR、PRR 和BCPNN 3 种方法同时检测警戒信号,但只能说明在统计学上存在相关性,无法确定因果关系;另外,本研究的ADE 报告数据主要来自欧美等国家,而我国的相关报告数据少,对于研究结果是否符合我国人群实际情况,有待进一步临床研究加以验证。
4 结论
本研究基于FAERS 信号挖掘方法,首次对布罗索尤单抗的警戒信号进行较为全面的分析,结果显示,共挖掘出28 个布罗索尤单抗说明书未收录的警戒信号,其中发现不安手综合征等罕见信号。因此,在临床上使用布罗索尤单抗时,除该药说明书收录的不良反应外,还需密切关注患者原有疾病进展情况以及说明书未收录的警戒信号,保证患者用药安全。
利益冲突所有作者均声明不存在利益冲突

