白内障术后确诊PAX6杂合子突变致Peters异常1例
韩新红 刘福义 张敏 姜雅琴 黄旭东 王继兵
作者单位:1潍坊眼科医院,潍坊 261041;2潍坊内分泌及代谢病医院,潍坊 262699
患儿,女,7 岁,因“双眼视力下降”于2020 年6 月8日就诊于潍坊眼科医院。家属诉患儿自幼双眼视力差。患儿4 年前于外地医院行“双眼白内障摘除联合一期人工晶状体(IOL)植入术”;3年前无明显诱因下出现双眼眼压高,外地医院就诊,给予酒石酸溴莫尼定滴眼液、布林佐胺滴眼液、布林佐胺噻吗洛尔滴眼液、贝美前列素滴眼液滴眼治疗3个月后眼压控制正常。患儿足月剖宫产,智力正常,父母非近亲结婚。患儿父亲自幼视力差,有“双眼先天性白内障”病史,其父亲2020年7月27日来院时眼部检查:右眼视力无光感,右眼眼压60 mmHg(1 mmHg=0.133 kPa)。左眼外伤后眼球摘除,义眼片在位;右眼眼部检查见图1。患儿曾祖父有青光眼病史。否认家族内其余成员眼部及其他遗传病史、类似病史。
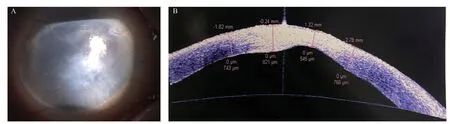
图1.Perters异常患儿父亲右眼眼部检查A:眼前节照片;B:眼前节OCT。Figure 1.Eye examination of Peters abnormal's fatherA: Anterior segment photography; B: Anterior segment optical coherence tomography.
患儿于2020年6月8日入院眼科检查示:右眼裸眼视力(UCVA)0.05 ,矫正0.16(+10.00 DS/-2.00 DC×135°);左眼UCVA 0.05,矫正0.10(+7.50 DS/-5.00 DC×10°)。眼压:右眼15 mmHg,左眼20 mmHg。裂隙灯显微镜检查:双眼眼球轻度水平震颤,角膜下方见大小2 mm×3 mm角膜白斑,可见细小血管长入,角膜形态欠规则,前房中深,房水清,无虹膜,IOL位正,IOL前可见白色增殖膜,晶状体后囊膜混浊(图2);双眼玻璃体、眼底窥不清;双眼固视可,不稳定,右眼注视,左眼外斜约5°。右眼眼轴长度20.17 mm,左眼眼轴长度20.60 mm。双眼B超检查未见明显异常。角膜内皮镜检查:右眼内皮细胞数量测不出,左眼约1 854个/mm2。眼前节OCT示双眼线状增强信号与角膜内皮相贴,右眼中央角膜厚度(CCT)为535 μm,左眼CCT为734 μm(图3A-B)。患儿心脏彩超未见明显异常。基因检测结果:PAX6基因有1个杂合突变,变异来源于该位点杂合变异的父亲,其母亲该位点无变异(图4)。诊断:双眼Peters异常、双眼后发性白内障、双眼IOL前膜、双眼IOL植入术后。考虑患儿左眼视轴区白色增殖膜明显,于2020年6月9日行左眼晶状体后囊膜切除术+前部玻璃体切割术(术中清除视轴区白色增殖膜)。术后眼底照相:左眼视网膜血管迂曲,走形欠规则,未见黄斑中心凹反光。左眼眼底OCT线状扫描均未见黄斑中心凹结构,视网膜各层结构存在(图3C)。术后多次复诊,左眼UCVA 0.06,矫正0.16(+6.75 DS/-5.50 DC×10°)。患儿自诉术后视物较前清晰,且其家属诉患儿日常活动更自如。术后2个月内双眼眼压药物控制尚可。但自2020年8月中旬起在持续联合应用3种降眼压药物情况下,左眼眼压多次复测仍大于25 mmHg,最高达39 mmHg,持续3周。于2020年9月9日予左眼硅管置入术。术后1年内复诊,在应用降眼压药物前提下左眼眼压控制在18~23 mmHg范围内。

图2.Perters异常患儿双眼眼前节照片A:右眼;B:左眼。Figure 2.Binocular anterior segment photography of Peters abnormalA: Right eye; B: Left eye.
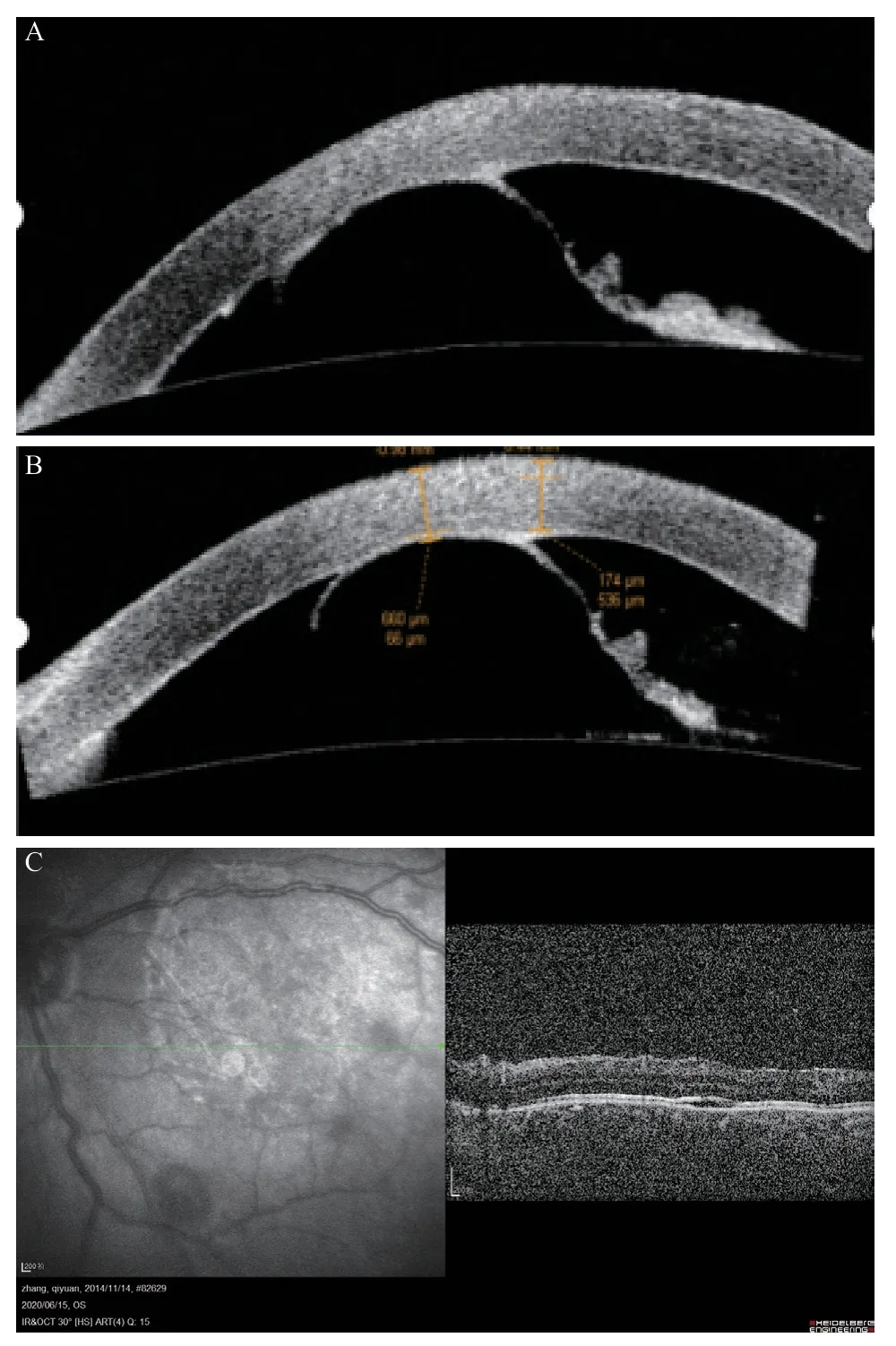
图3.Perters异常患儿双眼眼前节OCT和眼底OCTA、B:分别为右眼、左眼眼前节OCT;C:左眼眼底OCT。Figure 3.Binocular anterior segment OCT and fundus OCT of Peters abnormalA, B: Anterior segment OCT of right eye and left eye respectively; C: Fundus OCT of left eye.OCT, optical coherence tomography.

图4.Perters异常患儿及其父母的基因检测结果Figure 4.Gene test results of Peters abnormal and her parents
讨论
Peters异常是一种眼前段发育异常的罕见的致盲性眼病[1],少数患者可合并眼底先天发育异常。其发病年龄小,表型多样,多以散发的形式出现,但也可以为常染色体显性或隐性的方式发病[2]。本病例临床特点:①先天起病;②角膜变性,白色混浊;③无虹膜;④先天性青光眼;⑤眼底黄斑及视网膜血管发育异常;⑥眼球震颤;⑦基因检测示PAX6基因有 1个来源于父亲的杂合突变,且其父亲眼部表现与患儿相似。以上临床特点均符合Peters异常的临床诊断[3]。目前关于Peters异常的治疗,如角膜混浊致密,阻碍光线进入眼内,可早期行角膜移植术,但角膜移植术后免疫排斥风险高。本例患儿双眼部分周边角膜尚透明,且全周虹膜缺损,暂不需角膜移植手术。如合并严重白内障,可行白内障手术治疗以防止形觉剥夺性弱视。本例患儿已行双眼白内障摘除术,但双眼IOL前白色增殖膜及后囊膜混浊,且左眼视轴区增殖膜致密,因此给予手术切除增殖膜,尽可能提高视力,刺激视觉发育。如引起青光眼,在药物控制欠佳时,需联合抗青光眼手术治疗,且多数患者需多次抗青光眼手术。有研究表明,引流阀置入术成功率要高于单纯小梁切开术[4]。本例Peters患儿为IOL植入术后,且全周虹膜缺损,前房深度适中,置入硅管后损伤角膜内皮概率小,且后期无虹膜异常增殖或脱色素阻塞硅管的风险,结合本例患儿病情及患儿父母意愿,此次手术行硅管置入术,手术成功率高且术后并发症少。此外,对于此类合并眼部其他异常的白内障患者,建议先完善检查,确诊之后再制定比较全面的治疗方案,更有利于患者获得长期治疗效果。
PAX6突变与多种先天性眼部畸形有关。PAX6的突变主要导致无虹膜[5]。此外,在极少数情况下,PAX6突变会导致其他眼部异常,如先天性白内障、Peters异常、中央凹发育不良、小眼症和视神经发育不良等[6]。本例患儿PAX6基因序列分析发现1个突变c.718C>T(p.R240X),该突变在clinvar数据库中有收录,提示为致病突变。本例致病位点明确,符合遗传伦理,虽然目前尚无有效治疗方式,但通过产前基因诊断或者胚胎植入前遗传学诊断技术,阻断该病在家族中继续传递有重要意义。
利益冲突申明本研究无任何利益冲突
作者贡献声明韩新红:收集数据;参与选题、设计及资料的分析和解释;撰写论文;对编辑部的修改意见进行修改。刘福义:参与资料收集及整理。张敏:参与选题、设计和修改论文的结果、结论。姜雅琴:参与选题、设计、资料的分析和解释,修改论文中关键性结果、结论,根据编辑部的修改意见进行核修。黄旭东、王继兵:行手术操作

