下调硫酸乙酰肝素酶减轻大鼠心肌缺血再灌注损伤的机制
李招兵 刘雨露 黄云辉
南华大学衡阳医学院附属南华医院心血管内科(湖南衡阳 421002)
心肌缺血再灌注损伤(myocardial ischemiareperfusion,MI/R),因其多种复杂的机制参与心肌细胞死亡,使得I/R损伤的防治变得更加棘手[1-2]。文献报道,I/R损伤的机制包括ROS富集、钙超载、线粒体功能障碍、氧化应激和炎症反应等[3-5]。通过探讨其调控的病理过程的关键靶标分子,为临床筛选潜在的心脏保护药物提供依据。
硫酸乙酰肝素酶(Heparanase,HPSE)是能降解细胞表面和细胞外基质中的硫酸肝素的内切葡萄糖醛酸酶,调控细胞黏附、增殖和迁移[6-7]。NODA等[8]研究发现,低表达HPSE介导NF-κB信号途径,从而抵抗肺I/R。也有文献报道,HPSE抑制剂可以减轻胰岛细胞未折叠蛋白反应及氧化应激,减轻细胞的凋亡[9]。因此,笔者推测下调HPSE基因可以保护心肌缺血再灌注大鼠心肌细胞的损伤。本研究旨在探讨下调HPSE抑制UPRmt信号通路对缺血再灌注心肌细胞的影响,为MI/R的治疗提供理论依据。
1 材料与方法
1.1 MI/R动物模型及分组60只健康成年SD雄性大鼠,10~12周龄,280~320 g,购自江苏集萃药康生物科技股份有限公司,使用许可证号SYXK(湘)2020-0002,本实验经过南华大学动物伦理委员会批准同意。饲养于温度为25~28 ℃,湿度为40%~50%的SPF级环境。
大鼠适应性喂养1周后,利用随机数字表将大鼠分为对照组、I/R组、I/R+shRNA-NC组和I/R+Heparanase-shRNA组,每组15只。对照组开胸后仅穿线但不结扎,其他各组大鼠均采用结扎冠脉左前降支的手术方式制备MI/R模型[10],大鼠腹腔注射戊巴比妥钠溶液(50 mg/kg)麻醉,并用动物呼吸器通气,潮气量(6~8 mL/kg),呼吸机频率(80次/min)。夹趾无退缩后于左心耳根部下方2 mm进针,肺动脉圆锥旁出针结扎左前降支,当心尖处变苍白、心脏搏动减弱,完全结扎时于针线上方垫一直径为1.0 mm适当长度的棉线并打活结,30 min后解开结扎线,然后再灌注3 h,逐层缝合后关胸,术后注意保温。动脉结扎后使用心电图检测结果显示ST段上抬0.1 mV以上,持续30 min后打开结扎线,恢复血流灌注,心电图显示结扎后ST段下降1/2以上视为造模成功。
1.2 药物与试剂白细胞介素-6(interleukin-6,IL-6)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α) ELISA试剂盒均购自武汉菲恩生物科技有限公司;肌红蛋白(myohemoglobin,Mb)试剂盒子、肌酸激酶同工酶(creatine kinase MB,CK-MB)和心肌肌钙蛋白I(cardiac troponin,cTnI)试剂盒均购自上海基免实业有限公司;Caspase-3/鼠抗(美国CST公司)、Bax/鼠抗(上海碧云天生物科技有限公司)、Bcl-2/鼠抗(Proteintech Technology,Inc)、Heparanase/兔抗(GeneTex,Inc)、HSP70/兔抗(武汉华美生物工程有限公司)、LonP1/兔抗(Proteintech Technology,Inc)和ACTIN/兔抗(Proteintech Technology,Inc);苏木素、伊红(购自北京索莱宝科技有限公司);中性甲醛、乙醇、二甲苯(上海联迈生物工程有限公司);丙二醛(Malondialdehyde,MDA)、超氧化物歧化酶(superoxidedismutase,SOD)检测试剂盒均购自普利莱基因技术有限公司;二抗抗鼠和抗兔(Proteintech Technology,Inc)。
1.3 主要仪器超速离心机(美国Beckman Optima公司,型号:MAX-130K)、-20 ℃冰箱(德国Siemens公司)、-80 ℃超低温冰箱(美国Thermo Scientific公司,型号:Forma 900)、Synergy™ HT多功能酶标仪(USA Bio-Tek Instruments,Inc.,型号:iMark)、微型垂直电泳槽及转膜系统(上海天能科技有限公司,型号:VE 180)、凝胶成像分析系统(上海天能科技有限公司,型号:2500R,1600R)。
1.4 构建Heparanase-shRNA的载体本实验中使用的Heparanase-shRNA和NC-shRNA均购自上海吉凯基因生物有限公司。设计靶向硫酸乙酰肝素酶RNA干扰序列,合成靶序列的双链DNA,接入pGCL-GFP载体,PCR筛选阳性克隆,测序鉴定。包装产生具备感染能力的慢病毒:(1)293T细胞购于中国科学院细胞库,细胞用含10% 胎牛血清的DMEM培养,将细胞放于37 ℃(含5℅CO2)细胞培养箱中培养,隔24 h给细胞换1次培养基,每当细胞密度为70%~80%时,将细胞传代,分瓶培养。(2)用pHelper1.0和pHelper2.0质粒与相应体积的转染试剂混匀,室温下静置15 min。293T细胞用PBS洗3遍,加入含10%血清的DMEM培养基15 mL。将转染复合物缓慢加入到细胞培养液中,充分混匀后,将细胞放于细胞培养箱中培养6~12 h后,给细胞换液,加入含10%胎牛血清的DMEM培养基,置入培养箱内继续培养48 h。(3)检测病毒的滴度(1 × 108TU/mL)后,I/R+Heparanase-shRNA组大鼠通过尾静脉注射含50 μg Heparanase-shRNA的生理盐水0.2 mL,I/R+shRNA-NC组大鼠尾静脉注射含50 μg NC-shRNA的生理盐水0.2 mL,其余两组大鼠经尾静脉注射等量生理盐水。
1.5 Western blot检测蛋白表达水平取上述处死的大鼠心肌组织,剪取0.025 g组织,用冰预冷PBS洗组织,加入300 μL RIPA裂解液于生物样品均质仪中反复研磨组织直至看不见组织块;冰上,裂解10 min;4 ℃,12 000 r/min离心 15 min;将离心后的上清转至1.5 mL的离心管中;取200 μL蛋白上清,加入50 μL 5×loading buffer混匀,沸水煮5 min,放入冰盒中速冷备用。用10% SDS-聚丙烯酰胺凝胶电泳提取总蛋白,用1×TBST将PVDF膜置摇床上洗净丽春红,随后将放入5%的脱脂牛奶中,使PVDF膜全部浸入牛奶中,在常温下封闭2 h,按照蛋白抗体说明书稀释一抗,将膜置于4 ℃冰箱孵育过夜。次日用TBST洗涤PVDF膜3~5次。洗完后室温下孵育相应种属的二抗1 h,TBST洗涤4~5次,每次20 min。打开全自动凝胶成像系统,将PVDF膜置于成像板上,滴加适量的超敏ECL化学发光试剂,检测蛋白含量。用AlphaImager2200-灰度扫描软件统计灰度值,以ACTIN为内参蛋白,对目的蛋白进行半定量分析。
1.6 大鼠心脏功能及心肌损伤标记物检测使用DW-T6彩色多普勒超声仪连接小动物Medlab生物信号采集系统检测各组大鼠心率(heart rate,HR)、左心室射血分数(left ventricular ejection fraction,LVEF)、左室壁厚度(left ventricular wall thickness,LVWT)及再灌注末经腹主动脉取血100 μL,静置后以3 000 r/min离心15 min,分离血清,ELISA检测血清MB、CK-MB和cTnI水平。
1.7 氧化应激物质检测完成大鼠心脏功能检测后从颈总动脉插管接取0.5 mL 大鼠血液,离心(1 000 ×g,20 min),取上清液留存在-20 ℃冰箱。以ELISA法检测血清SOD、MDA的含量(具体操作依据该使用说明书)。
1.8 大鼠心肌病理情况观察完成大鼠心肌损伤标记物检测后断脖法处死大鼠,取大鼠心肌组织,使用二甲苯浸泡后使用梯度乙醇脱水,苏木精浸泡后盐酸乙醇分化、氨水冲洗,分别使HE染色和TUNEL染色中性树胶封片,在400倍镜观察大鼠心肌细胞状态,并随机选取5个视野统计心肌细胞凋亡率。
1.9 炎症因子检测取上述大鼠外周血,在低温离心机中以 3 000 r/min离心15 min,取上清液严格按照ELISA试剂盒说明书检测IL-6和TNF-α含量水平。
1.10 统计学方法本研究数据分析采用软件为SPSS 22.0,本研究作图采用软件为GraphPad Prism5,多组间比较使用单因素方差分析,组间两两比较采用独立样本t检验。检验水平α=0.05。
2 结果
2.1 大鼠Heparanase蛋白相对表达的检测Western blot检测结果发现,与对照组比较,I/R组大鼠Heparanase蛋白相对表达显著升高(t=24.03,P<0.01);与I/R+shRNA-NC组比较,I/R+HeparanaseshRNA组Heparanase蛋白相对表达显著降低(t=13.18,P<0.01),见图1。
2.2 大鼠心脏功能和心肌损伤标记物的检测检测大鼠心脏功能以及心肌损伤标记物,结果发现,与Control组比较,I/R组大鼠HR、LVEF、LVWT均显著降低,CK-Mb、cTnI、Mb水平均显著升高(P<0.05);与I/R+shRNA-NC组比较,I/R+HeparanaseshRNA组HR、LVEF、LVWT均显著升高,CK-Mb、cTnl、Mb水平均显著降低(P<0.05),见图2。

图2 大鼠心脏功能以及心肌损伤标记物的检测Fig.2 Detection results of cardiac function and myocardial injury markers in rat myocardium
2.3 TUNEL及HE染色观察大鼠心肌病理改变TUNEL染色观察大鼠心肌组织发现,与Control组比较,I/R组大鼠心肌细胞凋亡率显著升高(t=55.51,P<0.01);与I/R+shRNA-NC组比较,I/R+Heparanase-shRNA组大鼠心肌细胞凋亡率显著降低(t=32.66,P<0.01),见图3A。由HE染色观察大鼠心肌组织可以看出,Control组大鼠心肌组织、肌外膜、心肌纤维均正常且完整;I/R组大鼠和I/R+shRNA-NC组大鼠心肌纤维弯曲,肌红蛋白溶解,同时心肌肌细胞核固缩、溶解,肌束膜破裂;I/R+Heparanase-shRNA组大鼠心肌组肌外膜较为完整、心肌纤维弯曲显著改善,见图3B。

图3 TUNEL及HE染色观察大鼠心肌病理改变(400 ×)Fig.3 Observation the pathological changes of rat myocardium by TUNEL and HE staining in rat myocardium(400 ×)
2.4 大鼠心肌组织凋亡相关蛋白的检测据Western blot方法检测各组凋亡蛋白表达发现,与Control组比较,I/R组大鼠Caspase-3蛋白相对表达水平显著升高(t=8.61,P<0.01)、Bax蛋白相对表达水平显著升高(t=9.04,P<0.01),Bcl-2蛋白相对表达水平显著降低(t=14.51,P<0.01);与I/R+shRNA-NC组比较,I/R+Heparanase-shRNA组Caspase-3蛋白相对表达水平显著降低(t=7.27,P<0.01)、Bax蛋白相对表达水平显著降低(t=15.85,P<0.01),而Bcl-2蛋白相对表达水平显著升高(t=11.86,P<0.01),见图4。

图4 大鼠心肌组织凋亡相关蛋白检测Fig.4 Detection of apoptosis-related proteins in rat myocardium
2.5 大鼠血清氧化应激标记物及炎症因子检测检测大鼠氧化应激标记物及炎症因子,结果发现,与Control组比较,I/R组大鼠MDA、IL-6、TNF-α水平显著升高,SOD水平显著降低(P<0.05);与I/R+shRNA-NC组比较,I/R+Heparanase-shRNA组MDA、IL-6、TNF-α水平显著降低,SOD水平显著升高(P<0.05),见图5。

图5 大鼠血清氧化应激标记物及炎症因子检测Fig.5 Detection the serum oxidative stress markers and inflammatory factors in rat myocardium
2.6 大鼠心肌组织UPRmt标志蛋白检测据Western blot方法检测凋亡蛋白发现,与Control组比较,I/R组大鼠HSP70蛋白相对表达水平显著上升(P<0.05);LonP1蛋白相对表达水平显著下降(P<0.05);与I/R+shRNA-NC组比较,I/R+Heparanase-shRNA组大鼠HSP70、LonP1蛋白相对表达水平显著上升(P<0.01),见图6。
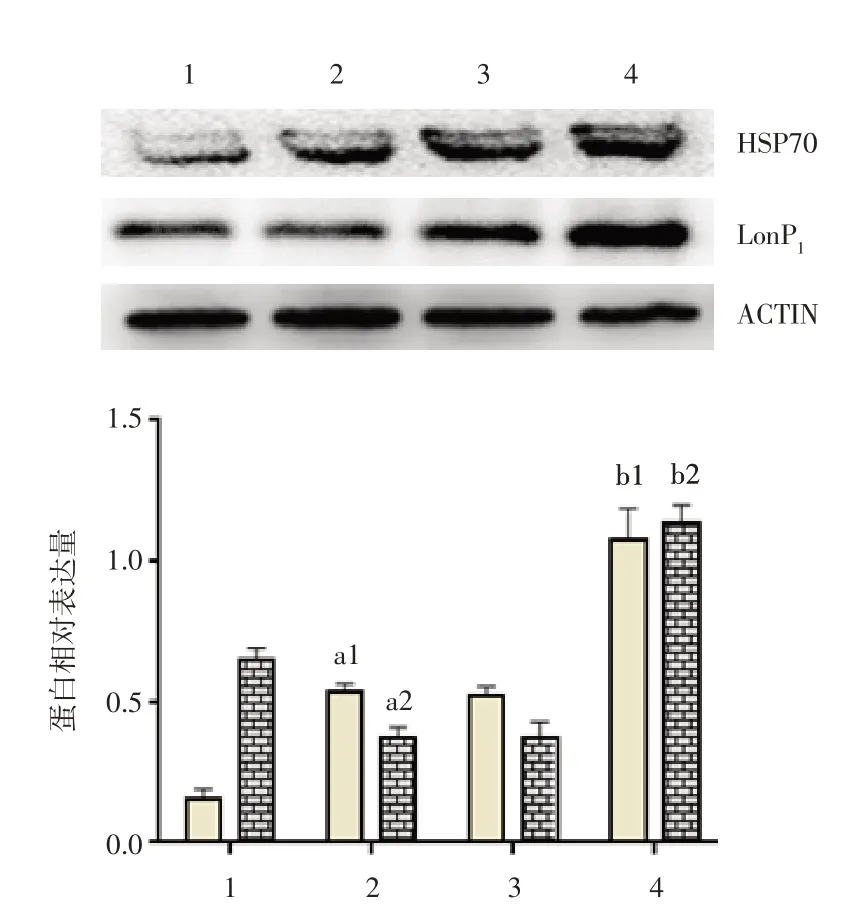
图6 大鼠心肌组织UPRmt标志蛋白检测Fig.6 Detection the UPRmt marker proteins in rat myocardium
3 讨论
及时恢复堵塞冠脉的血流是实现挽救缺血心肌细胞的最有效方法[11-13]。然而,再灌注是一把“双刃剑”,除了挽救缺血心肌外,还会引起新的心肌细胞死亡,即再灌注损伤[14-16]。到目前为止,临床上较好的预防或治疗再灌注损伤的方法和药物还亟待解决。
心肌缺血再灌注发生前会导致氧自由基及炎症因子的大量释放,从而引起心肌僵硬和损伤,心脏功能障碍[17-19]。因此,早期精准清除氧自由基和炎症因子能够有效缓解心肌损伤和心脏功能障碍。崔勤涛等[20]研究发现心肌缺血再灌注大鼠血清Mb、CK-MB和cTnI水平明显升高,SOD和GSH含量降低,MDA含量升高,经下调的长链非编码RNA核内富集转录物1预处理后,其心肌损伤明显好转,氧化应激和炎症水平显著降低。本研究结果发现,下调Heparanase的表达后,心肌缺血再灌注大鼠心脏功能明显好转,心肌病理损伤得到改善,心肌氧化应激水平降低。同时与I/R+shRNA-NC组比较,I/R+Heparanase-shRNA组大鼠MDA、IL-6、TNF-α表达水平显著下降,而SOD水平显著升高,说明下调HPSE基因的表达后,炎症因子水平显著降低,提示大鼠体内的炎症和氧化应激水平得到有效的抑制,与WANG等[21]研究结果相一致。因此,下调Heparanase可降低心肌缺血再灌注损伤大鼠心肌氧化应激和炎性反应,从而缓解大鼠心肌损伤。
前期研究结果显示:心肌缺血再灌注损伤组大鼠心肌病理损伤程度、心肌损伤标记物、氧化应激和炎症因子含量水平明显升高,而大鼠EF、LVSP、FS明显低下,心肌病理损伤严重,CK-MB、Mb和cTnI升高明显[22]。通过检测大鼠心肌血流动力学情况发现:与I/R+shRNA-NC组比较,I/R+Heparanase-shRNA组大鼠HR、LVEF、LVWT均显著升高,而CK-Mb、cTnI、Mb表达水平均显著降低,说明下调HPSE后,大鼠心脏跳动能力增强同时心脏收缩能力增强,表明大鼠心脏功能明显改善;也表明了下调HPSE后,大鼠心肌细胞得到了有效的保护,细胞破裂显著减少,使得细胞中的相关酶进入血液减少,缓解心肌组织受损,与PEI等[23]研究结果一致。
氧化应激与炎症因子之间的恶性循环直接攻击损伤的心肌细胞导致膜通透性显著增加,最终破坏促凋亡与抑凋亡之间的稳态,进一步加重心肌缺血再灌注大鼠心肌损伤。本研究发现,与I/R+shRNA-NC组比较,I/R+Heparanase-shRNA组大鼠Caspase-3、Bax蛋白相对表达水平显著降低,Bcl-2蛋白相对表达水平显著升高。说明下调HPSE基因的表达后,心肌细胞中凋亡基因受到抑制,抗凋亡基因受到了促进,心肌细胞凋亡得到了明显的改善,保护MI/R,与NGUYUEN等[24]研究结果一致。
众所周知,不良应激刺激可诱发线粒体未折叠蛋白反应(UPRmt),UPRmt的分子伴侣蛋白HSP70水平不足则可促进未折叠蛋白过度富集诱导线粒体损伤,而UPRmt的标志蛋白LonP1不足则不能很好地介导蛋白降解途径识别、降解未折叠蛋白,从而导致线粒体内膜显著畸形、超极化及凋亡[25]。文献[26]报道,HSP70与LonP1之间的稳态遭到破坏则导致未折叠蛋白过度富集,造成未折叠蛋白反应信号系统不能对抗氧化应激和炎症反应诱导的线粒体损伤。本研究发现,与Control组比较,I/R组大鼠HSP70蛋白相对表达显著上升,而LonP1蛋白相对表达下降;与I/R+shRNA-NC组比较,I/R+Heparanase-shRNA组大鼠HSP70、LonP1蛋白相对表达显著上升,表明下调Heparanase促线粒体折叠系统和识别降解功能的恢复。
本研究仅对大鼠心肌缺血再灌注损失模型作了较多探索,但小动物生理学结构及功能与人体差异较大,应该更进一步寻找临床证据和结合与之对应的体外细胞实验,提升该研究的实际应用价值。
综上所述,下调HPSE通过介导UPRmt信号途径抑制氧化应激、炎症反应和细胞凋亡从而减轻缺血再灌注大鼠心肌细胞的损伤。最近研究发现,HPSE抑制剂抑制人类胶质母细胞瘤细胞自噬发生[27],是否下调HPSE减轻大鼠心肌缺血再灌注损伤是通过抑制自噬途径也值得我们进一步探讨。

